湖南省十三市州2024年中考模拟训练化学试卷
试卷更新日期:2024-04-25 类型:中考模拟
一、单选题
-
1. 2024年中央电视台春节联欢晚会上,唐代著名诗人李白的诗歌再次成为万众瞩目的焦点。下列李白的诗歌中涉及化学变化的是( )A、白酒新熟山中归 B、轻舟已过万重山 C、黄河之水天上来 D、欲上青天揽明月2. 中国生态环境部确定2023年六五环境日的主题为“建设人与自然和谐共生的现代化”。为了倡导这一主题,我们应该做到( )A、兴建牧场养殖 B、进行垃圾焚烧 C、鼓励植树造林 D、提倡燃煤发电3. 奶茶是非常受欢迎的一种饮品。下列制作奶茶的原料中富含蛋白质的是( )A、茶叶 B、牛奶 C、白糖 D、冰块4. 下列有关硬水性质实验的操作,正确的是( )A、
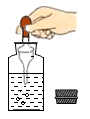 取样品
B、
取样品
B、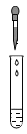 滴加肥皂水
C、
滴加肥皂水
C、 振荡
D、
振荡
D、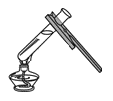 加热水样
5. 学习科学知识可以用来辨别“真”、“伪”。下列叙述属于“真”的是( )A、红磷在空气中燃烧产生大量白色烟雾 B、冬天的早晨看到窗户的玻璃上有“冰花”,说明空气中含有水蒸气 C、用量筒量取一定体积的稀盐酸时,若仰视读数,则量取的液体偏少 D、制取气体时,先装药品,然后检查装置的气密性6. 下列做法符合安全要求的是()A、油锅着火,用菜扑灭 B、燃气泄漏,点火检查 C、室内起火,开窗通风 D、电器着火,用水浇灭7. 在化学王国里,数字被赋予了丰富的内涵。下列化学用语中数字“2”的说法正确的是( )
加热水样
5. 学习科学知识可以用来辨别“真”、“伪”。下列叙述属于“真”的是( )A、红磷在空气中燃烧产生大量白色烟雾 B、冬天的早晨看到窗户的玻璃上有“冰花”,说明空气中含有水蒸气 C、用量筒量取一定体积的稀盐酸时,若仰视读数,则量取的液体偏少 D、制取气体时,先装药品,然后检查装置的气密性6. 下列做法符合安全要求的是()A、油锅着火,用菜扑灭 B、燃气泄漏,点火检查 C、室内起火,开窗通风 D、电器着火,用水浇灭7. 在化学王国里,数字被赋予了丰富的内涵。下列化学用语中数字“2”的说法正确的是( )①
②2NH3
③H2SO4
④
⑤
⑥
⑦H2O2
A、表示离子个数的是⑤⑥ B、表示离子所带电荷数的是④⑤ C、表示分子中原子个数的是③⑦ D、表示分子个数的是①②8. 某科技团队设想利用物质溶解时的降温效果,打造无电力冷却系统,他们选择的这种物质可能是( )A、NH4NO3 B、NaOH C、NaCl D、MnO29. 目前大多新能源电动汽车使用锂电池驱动。如图是锂元素在周期表中的部分信息及原子结构示意图。下列说法正确的是( )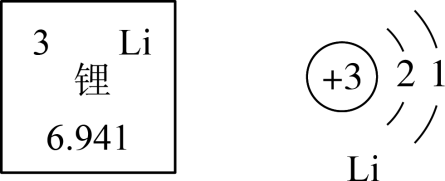 A、锂原子在化学反应中容易失去一个电子 B、锂离子核外有3个电子 C、锂元素的相对原子质量为6.941g D、锂原子的核电荷数为110. 科学思维是化学核心素养的重要组成部分,下列示例说法正确的是( )A、比较:一氧化碳和二氧化碳的组成元素相同,所以两者的性质完全相同 B、推理:单质由同种元素组成,所以同种元素组成的物质一定是单质 C、分析:金刚石与石墨物理性质差异很大是由于碳原子排列方式不同 D、归纳:氧分子是由氧原子构成的,所以氨分子是由氨原子构成的11. 在趣味实验“点水成冰”中用到了过饱和醋酸钠溶液。如图是醋酸钠的溶解度曲线,下列说法正确的是( )
A、锂原子在化学反应中容易失去一个电子 B、锂离子核外有3个电子 C、锂元素的相对原子质量为6.941g D、锂原子的核电荷数为110. 科学思维是化学核心素养的重要组成部分,下列示例说法正确的是( )A、比较:一氧化碳和二氧化碳的组成元素相同,所以两者的性质完全相同 B、推理:单质由同种元素组成,所以同种元素组成的物质一定是单质 C、分析:金刚石与石墨物理性质差异很大是由于碳原子排列方式不同 D、归纳:氧分子是由氧原子构成的,所以氨分子是由氨原子构成的11. 在趣味实验“点水成冰”中用到了过饱和醋酸钠溶液。如图是醋酸钠的溶解度曲线,下列说法正确的是( ) A、常温下,醋酸钠属于微溶物质 B、40℃时,将60g醋酸钠放入100g水中形成饱和溶液 C、40℃时,醋酸钠饱和溶液的溶质质量分数是39.6% D、将40℃时醋酸钠饱和溶液升温至60℃,溶质质量分数增大12. 下列关于酸、碱、盐用途的说法中,错误的是( )A、盐酸在工业上可用于除铁锈 B、氢氧化钠可用于改良酸性土壤 C、氯化钠在医疗上可用于配制生理盐水 D、小苏打可用于治疗胃酸过多症13. 表中酸性强弱情况揭示出复分解反应的一条规律,即较强酸发生类似反应可以生成较弱酸。下列反应均能发生,其中不符合该规律的是( )
A、常温下,醋酸钠属于微溶物质 B、40℃时,将60g醋酸钠放入100g水中形成饱和溶液 C、40℃时,醋酸钠饱和溶液的溶质质量分数是39.6% D、将40℃时醋酸钠饱和溶液升温至60℃,溶质质量分数增大12. 下列关于酸、碱、盐用途的说法中,错误的是( )A、盐酸在工业上可用于除铁锈 B、氢氧化钠可用于改良酸性土壤 C、氯化钠在医疗上可用于配制生理盐水 D、小苏打可用于治疗胃酸过多症13. 表中酸性强弱情况揭示出复分解反应的一条规律,即较强酸发生类似反应可以生成较弱酸。下列反应均能发生,其中不符合该规律的是( )溶质
H2SO4
HCl
H2S
H2CO3
HClO
酸性
大→小
A、H2SO4+2NaHCO3=Na2SO4+2H2O+2CO2↑ B、2HCl+CaS=CaCl2+H2S↑ C、CO2+H2O+Ca(ClO)2=CaCO3↓+2HClO D、H2S+CuSO4=H2SO4+CuS↓14. 区别熟石灰与烧碱的水溶液,可选择( )A、CO2 B、稀盐酸 C、CuSO4溶液 D、NaCl溶液15. 小颖同学为比较Mg、Fe、Cu三种金属的活动性顺序进行了如图甲所示的实验,实验后把两试管中的物质倒入烧杯中(如图乙),发现烧杯内的红色固体明显增多,充分反应后过滤,再向滤渣中加入适量稀盐酸, 产生无色气泡。根据上述信息,判断下列说法正确的是( ) A、原a、b试管中溶液都一定呈浅绿色 B、滤液中一定含有Mg2+、Fe2+ , 可能含有Cu2+ C、滤渣质量一定大于所加铁粉的总质量 D、滤渣含有三种固体物质
A、原a、b试管中溶液都一定呈浅绿色 B、滤液中一定含有Mg2+、Fe2+ , 可能含有Cu2+ C、滤渣质量一定大于所加铁粉的总质量 D、滤渣含有三种固体物质二、填空题
-
16. 水是宝贵的自然资源,在日常生活中有着极其广泛的运用。下表为我国生活饮用水的标准:
感官指标
化学指标
细菌学指标
水质无色无味,
且澄清透明
pH6.5~8.5;总硬度<
250mg/L(以碳酸钙计);
铜<1.0mg/L……等
细菌总数<100个/mL。等
 (1)、将不符合感官指标的浑浊坑水用如图所示的简易净水器进行净化,其中活性炭的作用是。(2)、如果地下水硬度过大,或者坑水中病原微生物过多,家庭通常都采取的方法来降低硬度和杀灭病原微生物。在化学指标一栏中,水中铜要小于1.0mg/L,这里的铜是指(填“分子”、“原子”、“元素”或“铜单质”)。17. 化学与人类生活、科技发展密切相关,回答下列问题。(1)、长沙地铁发展迅速,在建设过程中使用的大量钢材属于(填“金属材料”或“合成材料”)。(2)、黑火药是中国古代四大发明之一,由硝酸钾、硫磺和木炭按照一定的比例混合而成。黑火药着火时,发生如下化学反应:2KNO3+3C+S=K2S+X↑+3CO2↑,其中X的化学式是。(3)、湖南博物馆中珍藏着许多古代名人字画,用墨汁所作的书画能保存至今的原因是。(4)、湖南美食,全国闻名。例如:毛氏红烧肉、东安鸡、枸杞煲猪手等,这些食物被端上桌后香味扑面而来,从微观角度解释其原因是。18. 请根据如图回答问题:
(1)、将不符合感官指标的浑浊坑水用如图所示的简易净水器进行净化,其中活性炭的作用是。(2)、如果地下水硬度过大,或者坑水中病原微生物过多,家庭通常都采取的方法来降低硬度和杀灭病原微生物。在化学指标一栏中,水中铜要小于1.0mg/L,这里的铜是指(填“分子”、“原子”、“元素”或“铜单质”)。17. 化学与人类生活、科技发展密切相关,回答下列问题。(1)、长沙地铁发展迅速,在建设过程中使用的大量钢材属于(填“金属材料”或“合成材料”)。(2)、黑火药是中国古代四大发明之一,由硝酸钾、硫磺和木炭按照一定的比例混合而成。黑火药着火时,发生如下化学反应:2KNO3+3C+S=K2S+X↑+3CO2↑,其中X的化学式是。(3)、湖南博物馆中珍藏着许多古代名人字画,用墨汁所作的书画能保存至今的原因是。(4)、湖南美食,全国闻名。例如:毛氏红烧肉、东安鸡、枸杞煲猪手等,这些食物被端上桌后香味扑面而来,从微观角度解释其原因是。18. 请根据如图回答问题: (1)、实验A为验证质量守恒定律。实验时若取用红磷的量不足,对实验的结果(选填“有”或“没有”)影响。(2)、实验B反应停止后溶液中的溶质一定有氯化钙,可能还有(填化学式),反应后从溶液中要得到氯化钙固体需要用到上述装置(填编号)。19. 第19届亚运会在杭州市举行。本届亚运会不仅采用氢气作为火炬燃料,还使用了大量氢燃料电池车。高纯度、低成本的大量制取和储存氢气已成为氢能源利用领域的研究热点。如图就是一种比较经济的制取氢气的新工艺流程。
(1)、实验A为验证质量守恒定律。实验时若取用红磷的量不足,对实验的结果(选填“有”或“没有”)影响。(2)、实验B反应停止后溶液中的溶质一定有氯化钙,可能还有(填化学式),反应后从溶液中要得到氯化钙固体需要用到上述装置(填编号)。19. 第19届亚运会在杭州市举行。本届亚运会不仅采用氢气作为火炬燃料,还使用了大量氢燃料电池车。高纯度、低成本的大量制取和储存氢气已成为氢能源利用领域的研究热点。如图就是一种比较经济的制取氢气的新工艺流程。 (1)、在制得氢气和氧化铝(Al2O3)的反应中,金属镓的作用可能是。(2)、氢气是理想燃料的原因是写出1点即可)。(3)、氧化铝可以借助太阳能重新变成氧气与金属铝,该反应的化学方程式为。(4)、该生产流程中,可循环利用的物质是。(5)、镁铝合金(MgnAl12)是一种潜在的储氢材料,该合金在一定条件下完全吸收氢气得到MgH2和Al,该合金通常选择真空熔炼而非空气中熔炼的原因是。20. 如图是初中化学常见的实验或改进实验。请按要求回答问题。
(1)、在制得氢气和氧化铝(Al2O3)的反应中,金属镓的作用可能是。(2)、氢气是理想燃料的原因是写出1点即可)。(3)、氧化铝可以借助太阳能重新变成氧气与金属铝,该反应的化学方程式为。(4)、该生产流程中,可循环利用的物质是。(5)、镁铝合金(MgnAl12)是一种潜在的储氢材料,该合金在一定条件下完全吸收氢气得到MgH2和Al,该合金通常选择真空熔炼而非空气中熔炼的原因是。20. 如图是初中化学常见的实验或改进实验。请按要求回答问题。 (1)、装置C中仪器a的名称是。(2)、用过氧化氢溶液制氧气时反应速率非常快,因此制气装置应该选用图中的(填字母);用该装置制取氧气发生反应的化学方程式是。(3)、用收集的氧气进行D实验时,观察到的现象是,铁丝剧烈燃烧,放出大量的热,。(4)、E实验能够验证二氧化碳的性质是(答一点)。
(1)、装置C中仪器a的名称是。(2)、用过氧化氢溶液制氧气时反应速率非常快,因此制气装置应该选用图中的(填字母);用该装置制取氧气发生反应的化学方程式是。(3)、用收集的氧气进行D实验时,观察到的现象是,铁丝剧烈燃烧,放出大量的热,。(4)、E实验能够验证二氧化碳的性质是(答一点)。三、实验题
-
21. 氢氧化钠溶液和稀盐酸混合没有明显现象,它们是否发生了反应呢?某化学兴趣小组的同学设计如图甲所示实验进行探究。他们在盛有一定量X溶液的烧杯中放置pH传感器和温度传感器,然后开启电磁搅拌器,从滴定管中逐滴加入Y溶液;计算机显示两种传感器所得的数据曲线如图乙和图丙。
 (1)、【实验分析】写出稀盐酸和氢氧化钠溶液反应的化学方程式。(2)、由图乙可知,图甲滴定管中的Y溶液是(选填“NaOH溶液”或“稀盐酸”)。(3)、关于图乙、图丙的说法正确的是____(填字母)。A、图乙中c点表示的溶液中Na+和Cl-微粒数目相同 B、取图丙中d点的溶液,加入碳酸钠溶液,会产生气泡 C、取图乙a点的溶液,进行蒸发结晶,再将所得固体溶于水,测得溶液的pH=7,可以得出稀盐酸和NaOH溶液发生了反应(4)、图丁是图甲中NaOH溶液和稀盐酸反应的微观示意图(水分子略去),则反应前的“b”表示的微粒是(填微粒符号)。
(1)、【实验分析】写出稀盐酸和氢氧化钠溶液反应的化学方程式。(2)、由图乙可知,图甲滴定管中的Y溶液是(选填“NaOH溶液”或“稀盐酸”)。(3)、关于图乙、图丙的说法正确的是____(填字母)。A、图乙中c点表示的溶液中Na+和Cl-微粒数目相同 B、取图丙中d点的溶液,加入碳酸钠溶液,会产生气泡 C、取图乙a点的溶液,进行蒸发结晶,再将所得固体溶于水,测得溶液的pH=7,可以得出稀盐酸和NaOH溶液发生了反应(4)、图丁是图甲中NaOH溶液和稀盐酸反应的微观示意图(水分子略去),则反应前的“b”表示的微粒是(填微粒符号)。 (5)、【拓展迁移】
(5)、【拓展迁移】将40g、10%的NaOH溶液与40g、10%的稀盐酸混合,充分反应后,滴入紫色石蕊溶液显色。
四、计算题
-
22. 生铁和钢都是铁和碳的合金,生铁含碳量为2%~4.3%,钢含碳量为0.03%~2%,化学兴趣小组的同学为确定该铁合金是生铁还是钢,他们取11.5g铁合金样品盛放到锥形瓶中,将100g稀盐酸分成5等份,分5次加入锥形瓶,每次待充分反应后记录实验数据。实验数据整理如下表所示:
次数
加盐酸前
第1次
第2次
第3次
第4次
第5次
加入稀盐酸的质量(g)
0
20
20
20
20
20
锥形瓶内物质的总质量(g)
11.5
31.4
m
71.2
91.1
111.1
【查阅资料】碳不与稀盐酸反应。
请回答下列问题:
(1)、根据质量守恒定律,该反应中生成气体的总质量为。(2)、实验数据表中m的值为。(3)、请通过计算确定该铁合金是生铁还是钢(写出计算过程,计算结果保留到0.1%)。
-