广东省肇庆市封开县2024年中考一模化学试题
试卷更新日期:2024-04-25 类型:中考模拟
一、选择题:本大题共15小题,每小题3分,共45分。在每小题列出的四个选项中,只有一个是符合题目要求的。
-
1. 下列不属于化学变化的是( )A、植物的光合作用 B、金刚石加工成钻石 C、汽油的燃烧 D、铁片生锈2. 下列做法中正确的是( )A、为节约药品,应将做NaOH固体溶解实验得到的溶液倒回装有NaOH溶液的试剂瓶 B、为提高水的利用率,将工业污水用于农业浇灌 C、为减少白色污染,购物时尽量少用塑料袋 D、为增加节日气氛,大量燃放烟花爆竹3. 下列化学用语表示正确的是( )A、两个水分子:2H2O B、三个氧原子:O3 C、一个钙离子:Ca+2 D、氮元素:N24. 下列说法中,不正确的是( )A、我国制碱工业的先驱是侯德榜 B、门捷列夫提出了近代原子学说 C、屠呦呦因研究青蒿素获诺贝尔奖 D、中国科学家张青莲在测定锌、铟等元素的相对原子质量方面做出卓越贡献5. 下列实验操作正确的是( )A、连接玻璃管与胶皮管
 B、检查装置气密性
B、检查装置气密性  C、塞橡胶塞
C、塞橡胶塞  D、闻药品气味
D、闻药品气味  6. 为了解水稻选种、种植、生长、收割的全过程,项目学习小组开展了《水稻的一生》实践活动。请根据题意回答下列小题。(1)、实验室配制溶质质量分数为16%的NaCl溶液进行选种,不需要用到的仪器是( )A、托盘天平 B、玻璃棒 C、试管 D、烧杯(2)、有关《水稻的一生》项目实践活动的说法正确的是( )A、古代“舂米”去稻壳的过程属于物理变化 B、水稻生长过程中应大量使用农药除去虫害 C、收割稻谷使用的不锈钢镰刀硬度比纯铁小 D、水稻生长过程中,需喷洒(NH4)2HPO4水溶液以促生长,(NH4)2HPO4属于混合物7. 铈(Ce)是一种常见的稀土元素。如图是元素周期表中铈元素的相关信息,下列说法不正确的是( )
6. 为了解水稻选种、种植、生长、收割的全过程,项目学习小组开展了《水稻的一生》实践活动。请根据题意回答下列小题。(1)、实验室配制溶质质量分数为16%的NaCl溶液进行选种,不需要用到的仪器是( )A、托盘天平 B、玻璃棒 C、试管 D、烧杯(2)、有关《水稻的一生》项目实践活动的说法正确的是( )A、古代“舂米”去稻壳的过程属于物理变化 B、水稻生长过程中应大量使用农药除去虫害 C、收割稻谷使用的不锈钢镰刀硬度比纯铁小 D、水稻生长过程中,需喷洒(NH4)2HPO4水溶液以促生长,(NH4)2HPO4属于混合物7. 铈(Ce)是一种常见的稀土元素。如图是元素周期表中铈元素的相关信息,下列说法不正确的是( )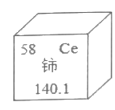 A、铈的相对原子质量是140.1 B、铈的原子序数为58 C、铈原子的核电荷数为58 D、铈属于非金属元素8. 酚酞是常见的酸碱指示剂,化学式为C20H14O4 , 下列有关酚酞的叙述正确的是( )A、酚酞的相对分子质量为38 B、酚酞由20个碳原子、14个氢原子和4个氧原子构成 C、酚酞中碳、氧元素的质量比为20:4 D、酚酞是由碳元素、氢元素和氧元素组成9. 按氧化物、酸、碱、盐的顺序排列的一组物质是( )
A、铈的相对原子质量是140.1 B、铈的原子序数为58 C、铈原子的核电荷数为58 D、铈属于非金属元素8. 酚酞是常见的酸碱指示剂,化学式为C20H14O4 , 下列有关酚酞的叙述正确的是( )A、酚酞的相对分子质量为38 B、酚酞由20个碳原子、14个氢原子和4个氧原子构成 C、酚酞中碳、氧元素的质量比为20:4 D、酚酞是由碳元素、氢元素和氧元素组成9. 按氧化物、酸、碱、盐的顺序排列的一组物质是( )氧化物
酸
碱
盐
A.
CuO
HNO3
Na2CO3
NaCl
B.
Na2SO4
H2O
NaOH
HCl
C.
CO2
NaOH
H2CO3
NH4Cl
D.
Fe2O3
H2SO4
Ca(OH)2
Na2CO3
A、A B、B C、C D、D10. 二氧化碳灭火器(如图)使用广泛,生产时将二氧化碳气体加压液化后装入小钢瓶中,使用时将其喷出灭火。下列有关该型灭火器的说法错误的是( ) A、加压液化时,二氧化碳分子间间隔缩小 B、电线老化短路起火,先切断电源,再用二氧化碳灭火器灭火 C、灭火时,二氧化碳起到降低着火点和隔绝空气的作用 D、适用于扑灭图书馆内图书失火11. 学习化学课程的主题内容,下列说法有错误的一组是( )
A、加压液化时,二氧化碳分子间间隔缩小 B、电线老化短路起火,先切断电源,再用二氧化碳灭火器灭火 C、灭火时,二氧化碳起到降低着火点和隔绝空气的作用 D、适用于扑灭图书馆内图书失火11. 学习化学课程的主题内容,下列说法有错误的一组是( )A.物质的性质与应用
B.物质的组成与结松
①医疗上可在液氮冷冻麻醉条件下做手术
②小苏打是焙制糕点发酵粉的主要成分之一
①蛋壳、贝壳和石灰石的主要成分都是碳酸钙
②稀有气体原子的最外层都有8个电子
C.科学探究与化学实验
D.化学与社会实践
①用酒精浸泡花瓣的汁液自制酸碱指示剂
②食用醋、厨房洗洁精两溶液的pH逐渐增大
①青铜比纯铜熔点低、硬度大,古代用青铜铸剑
②干冰可用在舞台上制造“云雾”
A、A B、B C、C D、D12. 下列化学方程式与事实相符且正确的是( )A、治疗胃酸过多:Mg(OH)2+H2SO4=MgSO4+2H2O B、氧化汞加热分解2HgO2Hg+O2↑ C、用氯酸钾与二氧化锰制氧气:KClO3KCl+O3 D、硫在氧气中燃烧S+O2SO2↑13. 下列是部分化学知识的归纳,其中完全正确的一组是( )A.物质的分类
B.资源的利用和保护
①氧化物中含有氧元素
②混合物中一定含有多种元素
①保护空气要减少有害气体和烟尘的排放
②爱护水资源要节约用水和防止水体污染
③保护金属资源只能通过防止金属腐蚀实现
C.“低碳经济”的措施
D.用“化学”眼光分析
①改造或淘汰高能耗、高污染产业
②研制和开发新能源替代传统能源
③教科书循环使用
①洗涤剂去油污是因为起乳化作用
②湿衣服晾干是因为分子之间有间隔
③用适量的熟石灰改良酸性土壤
A、A B、B C、C D、D14. 如图为Na2CO3和NH4HCO3的溶解度曲线。下列说法正确的是( )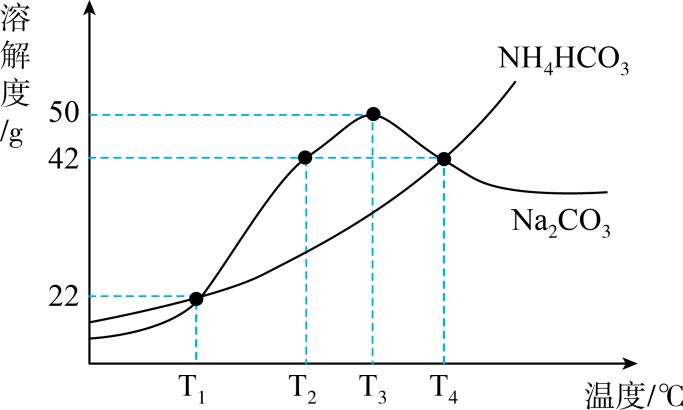 A、T1℃时,将30gNH4HCO3加到50g水中,NH4HCO3完全溶解 B、T2℃的Na2CO3饱和溶液升温到T3℃,溶质质量分数不变 C、将100gNa2CO3溶液从T4℃降温到T1℃,一定析出Na2CO3晶体 D、将T1℃的两物质饱和溶液升温到T4℃,为使溶液恰好饱和,加入两固体质量一定相等
A、T1℃时,将30gNH4HCO3加到50g水中,NH4HCO3完全溶解 B、T2℃的Na2CO3饱和溶液升温到T3℃,溶质质量分数不变 C、将100gNa2CO3溶液从T4℃降温到T1℃,一定析出Na2CO3晶体 D、将T1℃的两物质饱和溶液升温到T4℃,为使溶液恰好饱和,加入两固体质量一定相等二、非选择题:本大题共6小题,第16小题7分,第17小题8分,第18~21小题各10分,共55分。
-
15. 我国劳动人民很早就会通过“凿井”获得干净的水源。明代徐光启的《泰西水法》记载:“凿井者……既作底,更加细石子厚一二尺,能令水清而味美……取清水,置净器煮熟倾入白磁器中,候澄清,下有沙土者,此水质恶。”(1)、凿井:用生铁做成的铁凿和铁锤为挖凿工具,生铁属于(填“单质”或“合金”),它和钢的区别是。铁在等物质存在的条件下,易腐蚀生锈。(2)、澄水:用鹅卵石、碎瓦砾、木炭、沙子有序叠放在水眼之上,其中木炭的主要作用是。(3)、煮试:“置净器煮熟……下有沙土者”中的“沙土”(主要成分为碳酸钙)。若井水中含较多的Ca(HCO3)2 , 加热时则会形成“沙土”和两种氧化物,该反应化学方程式为。实验室常用来检验井水属于硬水还是软水。16. 化学研究物质。试从科学家认识物质的视角认识二氧化碳。(1)、【组成】
二氧化碳是由(填元素名称或符号)两种元素组成的。(2)、【结构】二氧化碳是由(填粒子名称)构成的。
(3)、【来源】工业上,煅烧石灰石(主要成分是CaCO3)来制取二氧化碳,该反应的化学方程式为。
(4)、【性质】根据图回答问题。向充满CO2的软矿泉水瓶中倒入澄清石灰水,旋紧瓶塞后充分振荡,能观察到的现象是软矿泉水瓶收缩变瘪和 , 该反应的化学方程式为。
 (5)、【用途】
(5)、【用途】液态二氧化碳灭火的原理是。
17. 【基础实验与跨学科实践】回答下列问题:
(1)、实验室制取CO2及其性质检验。
i.图中仪器a的名称是。
ii.实验室制取CO2 , 应选择图中的发生装置(填字母),化学方程式为。
iii.实验室加热高锰酸钾制取O2 , 应选择图中的发生装置(填字母),化学方程式为。
(2)、下面是某品牌的“便携式制氧机”的反应原理:用A剂、B剂产生氧气,其中A剂为白色颗粒(2Na2CO3•3H2O2),B剂为MnO2。
制氧机工作时发生了两步反应。
第一步:2Na2CO3•3H2O2=2Na2CO3+3H2O2
第二步:产生氧气的化学方程式为。
(3)、2Na2CO3•3H2O2属于(填“纯净物”或“混合物”)。18. “学化学,爱化学,用好化学”兴趣小组的同学围绕“酸碱中和反应”开展实验探究活动,请你参与下列活动。【实验探究】将氢氧化钾溶液与稀硫酸混合,观察不到明显现象,为证明氢氧化钾溶液与稀硫酸发生了反应,三位同学进行了以下实验。
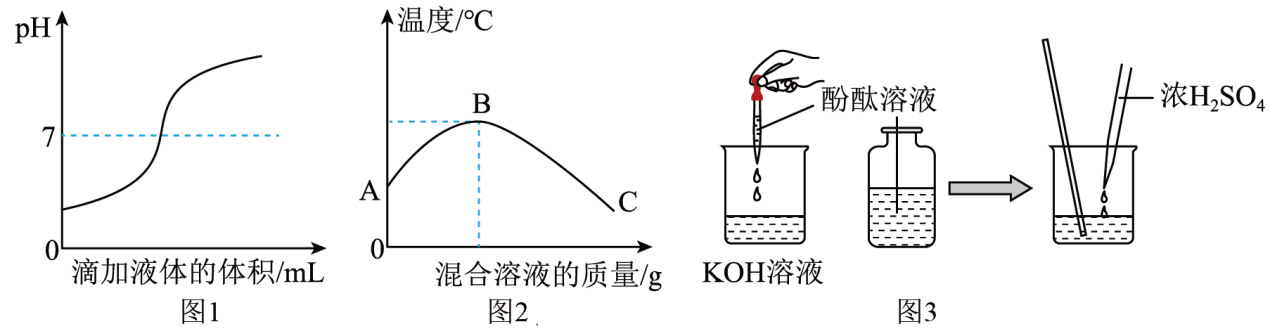 (1)、测定溶液pH变化的方法。
(1)、测定溶液pH变化的方法。甲同学在实验过程中测得pH变化如图1所示,则该同学是将(填字母序号)。
a.氢氧化钾溶液滴入稀硫酸中
b.稀硫酸滴入氢氧化钾溶液中
(2)、测混合过程中的温度变化。乙同学在实验过程中测得反应混合溶液的温度变化如图2所示,说明稀硫酸与氢氧化钾溶液发生的反应是(填“放热”或“吸热”)反应。图2中B点表示的含义是。
(3)、借助于酸碱指示剂丙同学通过图3所示实验,他观察到溶液由红色变成无色,也证明氢氧化钾溶液与稀硫酸发生了化学反应,反应的化学方程式为。
(4)、【提出问题】针对反应后溶液中溶质的成分,大家纷纷提出了猜想。【猜想与假设】
猜想一:只有K2SO4;猜想二:有K2SO4和H2SO4;猜想三:有K2SO4和KOH
【进行实验】
为了验证猜想,学习小组选用Fe2O3粉末、BaCl2溶液,进行如下探究:
实验方案
实验操作
实验现象
实验结论
方案一
取少量反应后的溶液于试管中,加入Fe2O3粉末
、
溶液中有H2SO4猜想二正确
方案二
取少量反应后的溶液于试管中,滴加BaCl2溶液
产生白色沉淀
溶液中有H2SO4 , 猜想二正确
(5)、【实验结论】通过探究,同学们一致确定猜想二是正确的。【评价与反思】
丁同学针对上述方案提出疑问,认为方案二是不合理的,理由是。
(6)、同学们经过反思与讨论,最后认为方案一中的Fe2O3粉末可以用某些物质代替,也能得到同样的实验结论,请你选出下列的不可用来代替Fe2O3药品的字母序号____。A、Mg B、CuO C、KCl D、Na2CO319. 铜是人类最先发现和使用的金属之一。(1)、湿法炼铜《梦溪笔谈》记载:“熬胆矾(硫酸铜)铁釜,久之亦化为铜”,其涉及的化学方程式为 , 该反应体现铁的活动性比铜(填“强”或“弱”)。
(2)、火法炼铜目前世界上80%的原生铜是使用火法冶炼生产。以辉铜矿(主要成分为Cu2S)为原料,炼铜的主要流程如图所示。

i.粉碎辉铜矿的目的是。
ii.吹炼炉中反应的化学方程式为 , 该反应属于(填基本反应类型)。
iii.火法炼铜工艺的烟气制酸系统能减缓的环境问题是。
(3)、生物炼铜i.随着技术的发展及环境保护意识的提升,“生物炼铜技术逐渐兴起。其中反应之一为 , X的化学式为。
ii.火法炼铜和生物炼铜环境负荷对比数据如表所示,由表中信息可知,“生物炼铜”的优点有(写1条即可)。
冶炼方法
能耗
温室效应CO2/kg
酸化效应SO2/kg
电力/kW·h
煤/kg
火法炼铜
8706.90
3656.24
10909.29
79.04
生物炼铜
3915.14
1402.22
4090.57
11.93
20. 为测定实验室制取二氧化碳后液体中氯化钙的溶质质量分数,取溶液100g,逐滴加入碳酸钠溶液,生成沉淀的质量与加入碳酸钠溶液的质量关系如图。 (1)、与氯化钙反应的碳酸钠溶液的质量为g。(2)、计算制取二氧化碳后液体中氯化钙的溶质质量分数。
(1)、与氯化钙反应的碳酸钠溶液的质量为g。(2)、计算制取二氧化碳后液体中氯化钙的溶质质量分数。