吉林省通化市梅河口市2024年高考第一次模拟考试化学试题
试卷更新日期:2024-04-19 类型:高考模拟
一、选择题:本题共15小题,每小题3分,共45分。在每小题给出的四个选项中,只有一项是符合题目要求的。
-
1. 化学与生活密切相关,下列不涉及化学变化的是( )A、植物油制作奶油 B、太阳能电池发电 C、土豆片遇碘变蓝 D、鸡蛋加热后凝固2. 下列叙述正确的是( )A、熟石膏的化学式:CaSO4·2H2O B、过氧化钠的电子式:
 C、基态氧原子的电子排布图:
C、基态氧原子的电子排布图: D、Ba(OH)2溶液中滴入少量稀硫酸发生反应的离子方程式:
3. 科学家利用FOX-7合成有机物T的反应历程如图所示(部分物质省略),T可用作固体火箭的新型推进剂,下列叙述正确的是( )
D、Ba(OH)2溶液中滴入少量稀硫酸发生反应的离子方程式:
3. 科学家利用FOX-7合成有机物T的反应历程如图所示(部分物质省略),T可用作固体火箭的新型推进剂,下列叙述正确的是( )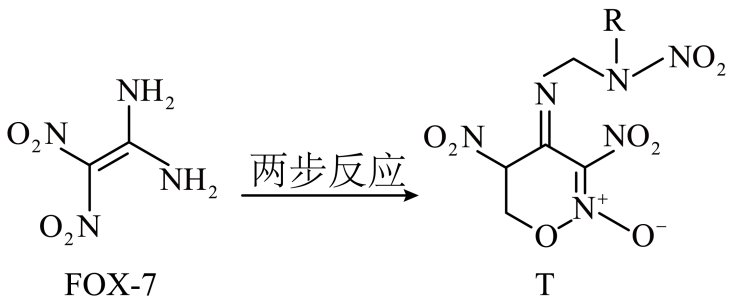 A、FOX-7不能发生加成反应 B、FOX-7不能使酸性KMnO4溶液褪色 C、T属于芳香族化合物 D、已知T中R为乙基,则T含1个手性碳原子4. 下列说法正确的是( )
A、FOX-7不能发生加成反应 B、FOX-7不能使酸性KMnO4溶液褪色 C、T属于芳香族化合物 D、已知T中R为乙基,则T含1个手性碳原子4. 下列说法正确的是( ) A、图甲用
A、图甲用 (杯酚)识别C60和C70 , 操作①②为过滤,操作③为蒸馏
B、图乙装置可用于收集NH3并验满
C、图丙装置可用于干燥MnCl2·4H2O
D、图丁装置可用于探究铁的析氢腐蚀
5. 短周期主族元素X、Y、Z、R的原子序数依次增大,某种性质递变规律如图所示,下列元素性质与元素对应正确的是( )
(杯酚)识别C60和C70 , 操作①②为过滤,操作③为蒸馏
B、图乙装置可用于收集NH3并验满
C、图丙装置可用于干燥MnCl2·4H2O
D、图丁装置可用于探究铁的析氢腐蚀
5. 短周期主族元素X、Y、Z、R的原子序数依次增大,某种性质递变规律如图所示,下列元素性质与元素对应正确的是( ) A、原子半径:F、Cl、Br、I B、电负性:Si、P、S、Cl C、第一电离能:Si、P、S、Cl D、最高化合价:C、N、O、F6. 天然气因含有少量等气体开采应用受限,菌在酸性溶液中可实现天然气的催化脱硫,其原理如下图所示。下列说法错误的是( )
A、原子半径:F、Cl、Br、I B、电负性:Si、P、S、Cl C、第一电离能:Si、P、S、Cl D、最高化合价:C、N、O、F6. 天然气因含有少量等气体开采应用受限,菌在酸性溶液中可实现天然气的催化脱硫,其原理如下图所示。下列说法错误的是( ) A、自然界游离态的硫广泛存在于各种矿石中 B、基态的价层电子轨道表示式为
A、自然界游离态的硫广泛存在于各种矿石中 B、基态的价层电子轨道表示式为 C、该反应I的离子方程式为
D、在此过程中,每脱去时,需消耗
7. 某储氢材料前驱体结构如下图,M、W、X、Y、Z五种元素原子序数依次增大,基态Z原子的电子填充了3个能级,其中有2个未成对电子。下列说法错误的是( )
C、该反应I的离子方程式为
D、在此过程中,每脱去时,需消耗
7. 某储氢材料前驱体结构如下图,M、W、X、Y、Z五种元素原子序数依次增大,基态Z原子的电子填充了3个能级,其中有2个未成对电子。下列说法错误的是( ) A、简单氢化物沸点高低: B、Y和W位于同一主族 C、第一电离能大小: D、阴、阳离子中均有配位键8. 次磷酸()是一元中强酸,次磷酸钠()广泛应用于化学镀镍,次磷酸钠的生产与镀镍过程如图所示。下列有关说法正确的是( )
A、简单氢化物沸点高低: B、Y和W位于同一主族 C、第一电离能大小: D、阴、阳离子中均有配位键8. 次磷酸()是一元中强酸,次磷酸钠()广泛应用于化学镀镍,次磷酸钠的生产与镀镍过程如图所示。下列有关说法正确的是( ) A、的核外电子有26种空间运动状态 B、“碱溶”时氧化剂与还原剂的物质的量之比为 C、(正四面体结构)中的键角: D、次磷酸铵与足量氢氧化钠共热:9. 生物体内多巴胺的合成是以酪氨酸为起始原料,在多种复杂的生物酶共同作用下完成的,其过程如下图所示。下列相关说法错误的是( )
A、的核外电子有26种空间运动状态 B、“碱溶”时氧化剂与还原剂的物质的量之比为 C、(正四面体结构)中的键角: D、次磷酸铵与足量氢氧化钠共热:9. 生物体内多巴胺的合成是以酪氨酸为起始原料,在多种复杂的生物酶共同作用下完成的,其过程如下图所示。下列相关说法错误的是( )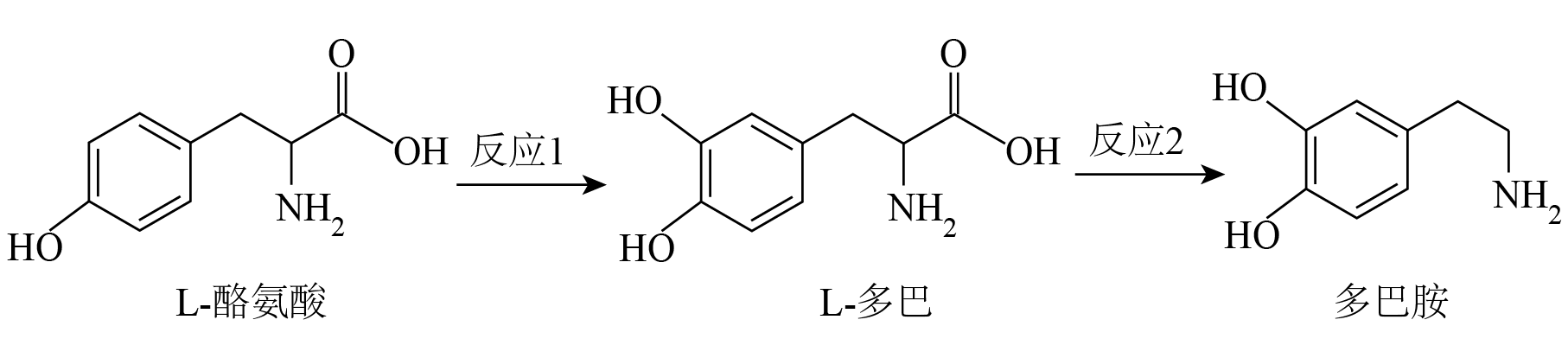 A、多巴胺分子中所有碳原子可能同平面 B、多巴与浓溴水反应最多可以消耗 C、酪氨酸与多巴混合发生缩合反应可生成3种二肽 D、上图中三种有机物均可与溶液发生显色反应10. 下列实验操作、现象和涉及的离子方程式均正确的是( )
A、多巴胺分子中所有碳原子可能同平面 B、多巴与浓溴水反应最多可以消耗 C、酪氨酸与多巴混合发生缩合反应可生成3种二肽 D、上图中三种有机物均可与溶液发生显色反应10. 下列实验操作、现象和涉及的离子方程式均正确的是( )选项
操作
现象
离子方程式
A
向明矾溶液中加入过量氨水
最后得无色溶液
B
将少量通入到溶液中
产生白色沉淀
C
向溶液中加入少量溶液
产生白色沉淀
D
向溶液中滴加5滴溶液,然后再滴加5滴溶液
先产生白色沉淀,后变成黄色沉淀
A、A B、B C、C D、D11. Aun纳米团簇能催化水煤气变换反应,其微观反应机理如图1所示,反应过程中相对能量的变化如图2所示。已知图2中TS表示过渡态,FS表示稳定的共吸附。下列说法错误的是( ) A、水煤气变换反应为H2O + COCO2 + H2 B、稳定性:FSe2大于FSe1 C、水煤气变换反应的H<0 D、制约总反应速率的反应为CO*+OH*=COOH*12. 利用化工厂产生的烟灰(ZnO的质量分数为ω,还含有少量CuO、MnO2、FeO等杂质)制备活性ZnO的工艺流程如图。下列说法错误的是( )
A、水煤气变换反应为H2O + COCO2 + H2 B、稳定性:FSe2大于FSe1 C、水煤气变换反应的H<0 D、制约总反应速率的反应为CO*+OH*=COOH*12. 利用化工厂产生的烟灰(ZnO的质量分数为ω,还含有少量CuO、MnO2、FeO等杂质)制备活性ZnO的工艺流程如图。下列说法错误的是( ) A、由滤液1中的阳离子主要含有[Zn(NH3)4]2+、[Cu(NH3)4]2+、NH4+可知,滤渣1中含有FeO 和MnO2 B、“除杂”工序反应的离子方程式:Zn+[Cu(NH3)4]2+ =Cu + [Zn(NH3)4]2+ C、“蒸氨沉锌”、“煅烧”时产生的气体可返回到“浸取”工序中循环使用 D、从m kg烟灰中得到活性ZnO a kg,则ZnO 的回收率%13. 用锂硫电池处理含有氯化铵的废水装置如图,锂硫电池工作原理:16Li + S8 8Li2S。下列说法正确的( )
A、由滤液1中的阳离子主要含有[Zn(NH3)4]2+、[Cu(NH3)4]2+、NH4+可知,滤渣1中含有FeO 和MnO2 B、“除杂”工序反应的离子方程式:Zn+[Cu(NH3)4]2+ =Cu + [Zn(NH3)4]2+ C、“蒸氨沉锌”、“煅烧”时产生的气体可返回到“浸取”工序中循环使用 D、从m kg烟灰中得到活性ZnO a kg,则ZnO 的回收率%13. 用锂硫电池处理含有氯化铵的废水装置如图,锂硫电池工作原理:16Li + S8 8Li2S。下列说法正确的( ) A、a 电极与锂硫电池的正极相连 B、c、e为阴离子交换膜,d为阳离子交换膜 C、当锂硫电池中消耗32g硫时,N室增加的离子总物质的量为4 mol D、出口一和出口二物质分别为H3PO4浓溶液、Na2SO4浓溶液14. 现有一种由正离子An+、Bm+和负离子X—组成的无机固体电解质,该物质在高温相为无序结构,低温相为有序结构,两者的结构如图,下列说法错误的是( )
A、a 电极与锂硫电池的正极相连 B、c、e为阴离子交换膜,d为阳离子交换膜 C、当锂硫电池中消耗32g硫时,N室增加的离子总物质的量为4 mol D、出口一和出口二物质分别为H3PO4浓溶液、Na2SO4浓溶液14. 现有一种由正离子An+、Bm+和负离子X—组成的无机固体电解质,该物质在高温相为无序结构,低温相为有序结构,两者的结构如图,下列说法错误的是( ) A、n=2,m=1 B、高温相中X—的堆积方式和氯化钠中Cl—的堆积方式相同 C、低温相中An+的配位数为4 D、高温相的良好导电性与其结构中存在大量的空位有关15. 常温下,Ka(CH3COOH)=1.0×10-5 , 向某含有ZnSO4酸性废液加入一定量CH3COONa后,再通入H2S生成ZnS沉淀,始终保持H2S饱和,即c(H2S)=0.1mol/L,体系中pX[pX=—1gX,X为、或c(Zn2+), 单位为 mol/L]与关系如图。下列说法错误的是( )
A、n=2,m=1 B、高温相中X—的堆积方式和氯化钠中Cl—的堆积方式相同 C、低温相中An+的配位数为4 D、高温相的良好导电性与其结构中存在大量的空位有关15. 常温下,Ka(CH3COOH)=1.0×10-5 , 向某含有ZnSO4酸性废液加入一定量CH3COONa后,再通入H2S生成ZnS沉淀,始终保持H2S饱和,即c(H2S)=0.1mol/L,体系中pX[pX=—1gX,X为、或c(Zn2+), 单位为 mol/L]与关系如图。下列说法错误的是( ) A、②中X为 B、A 点溶液的pH为4 C、Ka1(H2S) 的数量级为10-7 D、Ksp(ZnS)=10-21.7
A、②中X为 B、A 点溶液的pH为4 C、Ka1(H2S) 的数量级为10-7 D、Ksp(ZnS)=10-21.7二、非选择题:本题共4小题,共58分。
-
16. 作为电极材料,具有价格低,电位高、环境友好、安全性能高等优点,受到广泛关注。由菱锰矿(主要成分为 , 含有少量Fe、Ni、Al等元素)制备的流程如图。

已知常温下部分物质的如表。
物质
回答下列问题:
(1)、基态Mn原子的价电子轨道表示式为。(2)、常温下,若溶矿反应完成后,反应器中溶液pH=5,可沉淀完全的金属离子是;若测得溶液中浓度为0.1 , 浓度为0.01 , 为防止、发生沉淀,反应器中溶液用石灰乳调节的pH应小于。(已知:离子浓度小于等于 , 即可认为该离子沉淀完全)(3)、加入少量BaS溶液除去 , 生成的沉淀有(填化学式)。(4)、具有强氧化性的过一硫酸()可代替电解槽反应将氧化为 , 该反应的离子方程式为(已知:的电离第一步完全,第二步微弱)。(5)、煅烧窑中,生成反应的化学方程式是。(6)、中锰元素的平均价态为+3.5。在不同温度下,合成的中、和的含量与温度的关系见下表。T/℃
/%
/%
/%
700
5.56
44.58
49.86
750
2.56
44.87
52.57
800
5.50
44.17
50.33
850
6.22
4440
49.38
由此可以确定,在上述温度范围内,锰元素的平均价态的变化情况是。
17. 对叔丁基邻苯二酚是一种无色晶体,有毒,是工业上常用的一种阻聚剂,实验室可用邻苯二酚和甲基叔丁基醚在硫酸的催化下反应制备,反应原理及实验过程如下。
相关物质的物理性质如下:
物质
熔点(℃)
沸点(℃)
溶解性
邻苯二酚
103
245
溶于水、乙醇等,易溶于丙酮、吡啶、碱溶液
甲基叔丁基醚
-110
55.2
易溶于乙醇、乙醚等,不溶于水
对叔丁基邻苯二酚
57
285
溶于甲醇、乙醚、四氯化碳等,难溶于冷水,微溶于热水
已知:实验过程中会生成3,5—二叔丁基邻苯二酚、磺化产物等副产物
请回答:
(1)、操作1主要在如图装置中进行,仪器A的名称是 , 使用仪器B的优点是。 (2)、反应中浓硫酸不宜过多的原因是。(3)、向混合液A中加入溶液的目的主要是除去混合液中的硫酸,调节pH,操作2的名称是 , 操作3的目的是。(4)、①将混合液B进行减压蒸馏的目的是。
(2)、反应中浓硫酸不宜过多的原因是。(3)、向混合液A中加入溶液的目的主要是除去混合液中的硫酸,调节pH,操作2的名称是 , 操作3的目的是。(4)、①将混合液B进行减压蒸馏的目的是。②用重结晶法提纯对叔丁基邻苯二酚的操作顺序是(填序号)。
a.向粗产品中加入石油醚 b.用蒸馏水洗涤 c.加热充分溶解
d.加入活性炭脱色 e.冷却结晶f减压过滤 g.趁热过滤 h.干燥
18. 氮及其化合物在生产、环保研究等方面用途非常广泛,回答下列问题:(1)、用浓氨水除去Fe(OH)3样品中少量的Cu(OH)2 , 生成[Cu(NH3)4]2+ , 1mol[Cu(NH3)4]2+含molσ键。(2)、硝酸厂尾气可以回收制备硝酸。已知:①
②
, 。
(3)、在隔绝空气的密闭容器中发生反应:FeSO4(aq)+NO(g)Fe(NO)SO4(aq)(棕黄色),下列叙述正确的是____。(填标号)A、溶液颜色不变,反应达到平衡状态 B、其他条件不变,充入少量O2 , 平衡不移动 C、其他条件不变,加少量FeSO4 , 溶液颜色加深 D、其他条件不变,微热,溶液颜色加深(4)、向一恒容密闭容器中充入适量NH3和O2 , 在一定条件下发生反应,氧化产物是N2、NO、NO2、N2O中的一种,达到平衡时改变温度,反应物和生成物的浓度与温度关系如图所示: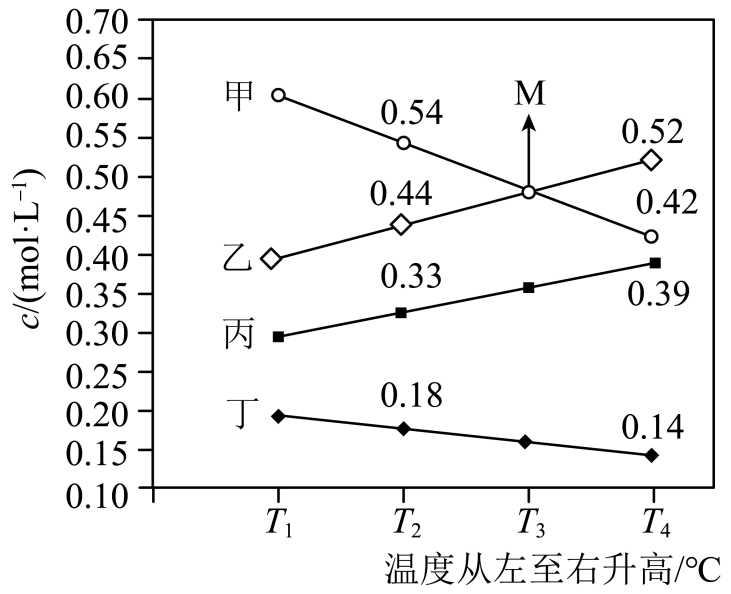
①甲是(填化学式),写出该反应的化学方程式:。
②正反应(填“>”“<”或“=”)0,判断依据是
③T3℃时NH3的平衡转化率为。
19. 氯霉素是广普抑菌抗生素。下图是以化合物A为原料合成氯霉素的一种路线:
请回答下列问题:
(1)、A的化学名称是。(2)、E→F的有机反应类型为。(3)、C的结构简式为。(4)、A→B 的反应分为两步,第一步形成碳氮双键,第二步形成碳碳单键,第二步反应的化学方程式为。(5)、F中N原子的杂化类型为。(6)、M 是 A 的同系物且相对分子质量比A 大14,符合条件的M 有种(不考虑立体异构)(7)、根据合成氯霉素的信息,设计以 (酪氨酸)为原料合成
(酪氨酸)为原料合成 (D- 型酪氨醇)的路线(无机试剂任选) 。
(D- 型酪氨醇)的路线(无机试剂任选) 。