2024年中考化学二轮专题复习-实验室制取气体的原理探究
试卷更新日期:2024-04-17 类型:二轮复习
一、选择题
-
1. 下列各组物质加热时能迅速放出氧气的是( )A、氯酸钾 B、锰酸钾 C、二氧化锰 D、氯酸钾和高锰酸钾的混合物2. 将混有高锰酸钾的氯酸钾固体放入试管中加热,完全反应后,试管中剩余的固体共有( )A、2种 B、3种 C、4种 D、5种3. 实验室制取气体的原理与装置省略反应试剂与夹持装置都正确的是( )A、
 B、
B、 C、
C、 D、
D、 4. 小明设计了趣味实验装置(见图),其气密性良好。若要使B中尖嘴导管有“喷泉”产生,则A中加入的固体和液体可能是
4. 小明设计了趣味实验装置(见图),其气密性良好。若要使B中尖嘴导管有“喷泉”产生,则A中加入的固体和液体可能是
①NaOH固体和水 ②硝酸铵固体和水 ③锌和稀硫酸 ④碳酸钠粉末和稀盐酸 ⑤生石灰和水 ⑥二氧化锰和过氧化氢溶液
A、②③④⑥ B、①③④⑤⑥ C、①③⑤⑥ D、①②③⑤⑥5. 要使下图装置中的小气球鼓起来,则使用的固体和液体可以是( )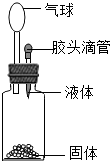
①硝酸铵和水;②铁和稀硫酸;③固体氢氧化钠和水;④二氧化锰和双氧水;⑤石灰石和稀盐酸
A、①②③④⑤ B、②③④⑤ C、②③⑤ D、②④⑤6. 下图是初中化学常用的实验装置,下列说法正确的是( ) A、B和E组合可以用来实验室制取并收集CO2 B、实验室里用装置A制备氧气,反应的化学方程式为 C、图F中集气瓶内盛少里水的作用是吸收二氧化硫,减少污染 D、若用图G装置收集H2 , 无论排空法还是排水法,H2都从c端进入7. 现有下列反应:①:② ;③。其中适用于实验室制取二氧化碳的是( )A、①② B、③ C、①②③ D、②③8. 用如图装置进行实验,将装置倾斜,使管①、②中药品接触,观察到气球鼓起,一段时间后又恢复原状。下列药品符合该实验现象的是( )
A、B和E组合可以用来实验室制取并收集CO2 B、实验室里用装置A制备氧气,反应的化学方程式为 C、图F中集气瓶内盛少里水的作用是吸收二氧化硫,减少污染 D、若用图G装置收集H2 , 无论排空法还是排水法,H2都从c端进入7. 现有下列反应:①:② ;③。其中适用于实验室制取二氧化碳的是( )A、①② B、③ C、①②③ D、②③8. 用如图装置进行实验,将装置倾斜,使管①、②中药品接触,观察到气球鼓起,一段时间后又恢复原状。下列药品符合该实验现象的是( )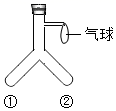 A、镁条和稀盐酸 B、大理石和稀盐酸 C、二氧化锰和过氧化氢溶液 D、生石灰和水9. 实验室制取氧气时,必须满足的条件是()A、必须使用催化剂 B、必须用含氧元素的物质作反应物 C、必须加热 D、必须用排水法收集10. 工业上可用二氧化硫制取氢气,流程如下图。下列有关说法错误的是( )
A、镁条和稀盐酸 B、大理石和稀盐酸 C、二氧化锰和过氧化氢溶液 D、生石灰和水9. 实验室制取氧气时,必须满足的条件是()A、必须使用催化剂 B、必须用含氧元素的物质作反应物 C、必须加热 D、必须用排水法收集10. 工业上可用二氧化硫制取氢气,流程如下图。下列有关说法错误的是( ) A、采用该流程可减少二氧化硫对大气的污染 B、膜反应器中反应为:2HI=H2+I2 C、分离器中分离出的副产品是硫酸 D、生产流程中能被循环利用的物质是I211. 已知草酸(H2C2O4)晶体与浓硫酸共热发生化学反应: 。某化学兴趣小组同学利用如图所示的装置,符合题意连接装置,进行实验,可以验证m g某混合气体的成分是CO2、H2O和CO,并粗略测出每种气体的质量(每套装置限用一次,无水硫酸铜遇水分变蓝)。连接装置后先通一段时间氮气,再继续实验。下列说法正确是:( )
A、采用该流程可减少二氧化硫对大气的污染 B、膜反应器中反应为:2HI=H2+I2 C、分离器中分离出的副产品是硫酸 D、生产流程中能被循环利用的物质是I211. 已知草酸(H2C2O4)晶体与浓硫酸共热发生化学反应: 。某化学兴趣小组同学利用如图所示的装置,符合题意连接装置,进行实验,可以验证m g某混合气体的成分是CO2、H2O和CO,并粗略测出每种气体的质量(每套装置限用一次,无水硫酸铜遇水分变蓝)。连接装置后先通一段时间氮气,再继续实验。下列说法正确是:( ) A、装置的连接顺序依次为混合气体→E→C→B→D →A→尾气处理 B、实验时应先通混合气体后点燃酒精喷灯 C、计算CO的质量时,既能根据A中燃烧管内固体减少的质量计算,也可根据A中澄清石灰水增加的质量计算,二种方法均准确 D、通过装置B、C、D在反应前后增加的总质量可以得出CO2的质量12. 过氧化钠(Na2O2)能与二氧化碳反应生成氧气,可作为呼吸面具中氧气的来源。潜水艇遇到紧急情况时,也使用过氧化钠来供氧,反应的化学方程式为:2Na2O2+2CO2=2Na2CO3+O2。以下从该反应获取的信息中,正确的是( )
A、装置的连接顺序依次为混合气体→E→C→B→D →A→尾气处理 B、实验时应先通混合气体后点燃酒精喷灯 C、计算CO的质量时,既能根据A中燃烧管内固体减少的质量计算,也可根据A中澄清石灰水增加的质量计算,二种方法均准确 D、通过装置B、C、D在反应前后增加的总质量可以得出CO2的质量12. 过氧化钠(Na2O2)能与二氧化碳反应生成氧气,可作为呼吸面具中氧气的来源。潜水艇遇到紧急情况时,也使用过氧化钠来供氧,反应的化学方程式为:2Na2O2+2CO2=2Na2CO3+O2。以下从该反应获取的信息中,正确的是( )①过氧化钠属于氧化物 ②该反应属于置换反应 ③反应前后部分氧元素化合价发生了变化 ④实验室可利用这一原理制取纯净的氧气。
A、①③④ B、①③ C、①④ D、①②③13.利用下图所示装置,能完成实验室制取气体的是( )
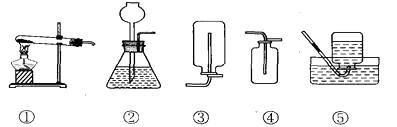 A、用①③制取氧气 B、用②③制取二氧化碳 C、用②④制取氧气 D、用①⑤制取二氧化碳14. 下列各反应中最适合潜水艇里供给氧气的反应是( )A、2KClO3
A、用①③制取氧气 B、用②③制取二氧化碳 C、用②④制取氧气 D、用①⑤制取二氧化碳14. 下列各反应中最适合潜水艇里供给氧气的反应是( )A、2KClO3 2KCl+3O2↑
B、2H2O22H2O+O2↑
C、2Na2O2+2CO2═2Na2CO3+O2
D、2H2O
2KCl+3O2↑
B、2H2O22H2O+O2↑
C、2Na2O2+2CO2═2Na2CO3+O2
D、2H2O 2H2↑+O2↑
15. 长途运输鱼苗的容器内必须满足下列条件才能保持鱼苗的存活:充足的氧气、鱼苗呼出的二氧化碳要及时除去、防止细菌繁殖、水的pH在8左右.现有以下3种具有杀菌能力的物质供选择使用:双氧水、过氧化钙(CaO2)、过氧化钠(Na2O2),它们在容器内可发生如下反应:
2H2↑+O2↑
15. 长途运输鱼苗的容器内必须满足下列条件才能保持鱼苗的存活:充足的氧气、鱼苗呼出的二氧化碳要及时除去、防止细菌繁殖、水的pH在8左右.现有以下3种具有杀菌能力的物质供选择使用:双氧水、过氧化钙(CaO2)、过氧化钠(Na2O2),它们在容器内可发生如下反应:(1)2H2O2═2H2O+O2↑
(2)2Na2O2+2H2O═4NaOH+O2↑
(3)2Na2O2+2CO2═2Na2CO3+O2
(4)2CaO2+2H2O═2Ca(OH)2+O2↑
(5)2CaO2+2CO2═2CaCO3+O2
你认为最合适的物质是( )
A、双氧水 B、过氧化钙 C、过氧化钠 D、双氧水与过氧化钠组合高温16. 实验室制备二氧化硫气体,下列方法最适合的是( )A、Na2SO3(固)+H2SO4(浓)=Na2SO4+SO2↑+H2O B、4FeS2(固)+11O2 2Fe2O3+8SO2
C、C+2H2SO4(浓)CO2↑+2SO2↑+2H2O
D、2CuSO4
2Fe2O3+8SO2
C、C+2H2SO4(浓)CO2↑+2SO2↑+2H2O
D、2CuSO4 2CuO+2SO2↑+O2↑
17. 下列反应都可产生氧气,其中最适宜潜水艇做供给氧气的反应的是( )A、2KClO32KCl+3O2↑ B、2H2O
2CuO+2SO2↑+O2↑
17. 下列反应都可产生氧气,其中最适宜潜水艇做供给氧气的反应的是( )A、2KClO32KCl+3O2↑ B、2H2O 2H2↑+O2↑
C、2Na2O2+2CO2→2Na2CO3+O2↑
D、4HNO32H2O+4NO2↑+O2↑
18.
2H2↑+O2↑
C、2Na2O2+2CO2→2Na2CO3+O2↑
D、4HNO32H2O+4NO2↑+O2↑
18.为测定气球内的气体成分,有学生用超薄材料制成的气球按如图装置进行实验.开始时气球沉于烧杯底部,打开开关后,过一会儿气球从烧杯底部慢慢浮起,最后悬于烧杯口.气球内可能的气体是( )
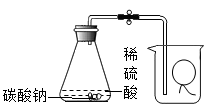 A、甲烷 B、氧气 C、二氧化硫 D、氢气19.
A、甲烷 B、氧气 C、二氧化硫 D、氢气19.我国科学家在CO低温氧化的研究上取得了突破性进展。即使四氧化三钴(Co3O4)纳米棒的催化,使汽车尾气中的CO在低温时与O2反应生成CO2。下列关于该反应的说法中,不正确的是()
 A、反应类型为化合反应 B、可降低汽车尾气对大气的污染 C、反应前后Co3O4质量改变 D、反应前后碳元素的化合价改变20. 鱼苗在长途运输中,通常将鱼苗养在相对密闭的容器内,加入某种药品,使容器内满足下列条件才能保持鱼苗的存活:充足的氧气、及时除去鱼苗呼出的CO2水的pH调节在8左右,碱性不能太强.现有以下四种物质供选择:双氧水、过氧化钙(CaO2).过氧化钠(Na2O2)、氯酸钾.它们的有关化学性质如下:
A、反应类型为化合反应 B、可降低汽车尾气对大气的污染 C、反应前后Co3O4质量改变 D、反应前后碳元素的化合价改变20. 鱼苗在长途运输中,通常将鱼苗养在相对密闭的容器内,加入某种药品,使容器内满足下列条件才能保持鱼苗的存活:充足的氧气、及时除去鱼苗呼出的CO2水的pH调节在8左右,碱性不能太强.现有以下四种物质供选择:双氧水、过氧化钙(CaO2).过氧化钠(Na2O2)、氯酸钾.它们的有关化学性质如下:
(1)2H2O=2H2O+O2↑
(2)2Na2O2+2HO =4NaOH十O2↑
(3)2Na2 O2+2CO2= 2Na2CO3+O2
(4)2CaO2+2H2O=2Ca(OH)2+O2↑
(5)2CaO2+2CO2 =2CaCO3↓+O2
(6)KClO3不与H2O、CO2反应
在鱼苗长途运输中你认为最适合加入的物质是( )A、双氧水 B、过氧化钙 C、过氧化钠 D、氯酸钾二、填空题
-
21. 在军事术语上把核潜艇在海里的连续航行叫长行。为了保证长时间潜行,在潜艇里要配备氧气的化学再生装置。制氧气方法有以下几种:①加热高锰酸钾 ②电解水 ③在常温下使过氧化钠(Na2O2)与二氧化碳反应生成碳酸钠和氧气 ④加热氧化汞。其中最适宜在潜艇里制氧气的方法是(填标号) , 反应的化学方程式为 , 与其他几种方法相比该方法具有的优点之一是:。22. 氢气是一种极其理想的新能源,它燃烧后只产生 , 对环境没有污染,实验室我们常用和反应来制取氢气,化学方程式 .23. 潜水艇要配备氧气的再生装置,以保证长时间潜航.有以下几种制氧气的方法:①加热高锰酸钾;②电解水;③常温下过氧化钠( Na2O2)固体与二氧化碳反应生成碳酸钠和氧气.
你认为最合适在潜水艇里制氧气的方法是(填序号) . 与其他两种方法相比,这种方法的两条优点是、 .
24.请根据下图所示实验,回答问题。

(1)A中仪器a的名称是 。玻璃管中的现象是 ,反应的化学方程式为 。
(2)B装置可用于高锰酸钾制氧气,反应的化学方程式为 。
(3)实验室用C装置制取CO2 , 反应的化学方程式为 。
(4)二氧化碳的收集方法与氧气不完全相同,原因是 。25.实验室既可用KMnO4(或KClO3和MnO2的混合物)在加热条件下使其分解制取氧气,也可用下图装置,通过分解过氧化氢(H2O2)来制取氧气。请你根据已学化学知识和经验回答下列问题:
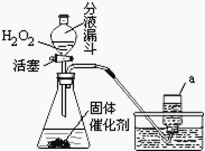
(1)写出过氧化氢分解的化学方程式: 。
(2)写出上图装置中仪器a的名称:。
(3)与高锰酸钾(或氯酸钾和二氧化锰的混合物)制取氧气相比,用过氧化氢制取氧气的优点是: 。
(4)收集氧气的方法还可用 法,你选择此方法的理由是: 。
(5)上图发生装置还可以用于制取的气体有 ,并写出制取该气体的化学方程式 。三、综合题
-
26. 某化学实验小组在老师的指导下从如图中选择装置在实验室进行气体的制备实验。
 (1)、写出有标号仪器的名称① , ②。(2)、在实验室里一般不能制得氧气的是(填序号)。
(1)、写出有标号仪器的名称① , ②。(2)、在实验室里一般不能制得氧气的是(填序号)。A.高锰酸钾(KMnO4) B.氯酸钾(KClO3)
C.过氧化氢(H2O2) D.氯化钠(NaCl)
依据是:要选择制取氧气的反应物,该反应物中必须含。
(3)、该小组同学首先用加热高锰酸钾的方法制取氧气。①应选择的气体发生装置为(填字母序号)。
②若用装置F收集氧气,收集完毕,将集气瓶移出水面,(填“正放”或“倒放”)在桌面上。若收集到的气体不纯,则可能的原因是。
(4)、该小组同学然后用过氧化氢和二氧化锰制取氧气。①写出该反应的化学方程式。
②若要获得平稳的氧气流,应选择的发生装置是(填字母序号)。
③若用装置D收集氧气,则验满的操作方法为。
④为节省药品,我们可以通过(填某实验操作)的方法从反应后的混合物中分离回收MnO2。
(5)、实验室常用大理与稀盐酸接触即可制取二氧化碳。①可选择的发生装置为(填字母序号),选择气体发生装置时,必须考虑的是和。
②已知二氧化碳密度比空气大,能溶于水,那么收集二氧化碳的装置是(填字母序号)。
③该小组同学用图中的M装置收集二氧化碳,那么用从端(填“a”或“b”)通入二氧化碳将瓶内空气排出。
 (6)、该小组同学用图中的N装置收集一定体积的氧气,装置接口连接的顺序为(填字母序号)。27. 为探究影响氯酸钾分解速率的因素,小明把实验温度恒定在330 ℃或380 ℃(其他实验条件如表),并设计了如下实验。
(6)、该小组同学用图中的N装置收集一定体积的氧气,装置接口连接的顺序为(填字母序号)。27. 为探究影响氯酸钾分解速率的因素,小明把实验温度恒定在330 ℃或380 ℃(其他实验条件如表),并设计了如下实验。实验编号
氯酸钾的质量
催化剂及其质量∕g
温度∕℃
反应的时间/s
氧气体积/mL
①
2.0
无
330
100
V1
②
2.0
氧化铁0.5
330
100
V2
③
2.0
二氧化锰0.5
330
100
V3
④
2.0
二氧化锰0.5
380
100
V4
请回答:
(1)、若想证明氧化铁是氯酸钾分解制取氧气的催化剂,除测定结果V1<V2外,还需要证明氧化铁在化学反应前后的不变。(2)、探究氧化铁对氯酸钾分解速率的影响,要选用实验进行对比。(填写实验编号)(3)、若V3<V4 , 则得到的实验结论是;实验③反应的化学方程式是。(4)、如图所示,在KClO3和Fe2O3质量比为5:4之前,氧化铁质量越多,反应速率越快,可能的原因是。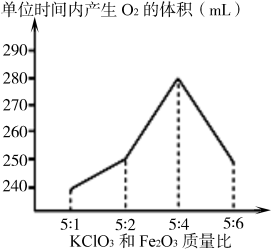
四、实验探究题
-
28. 实验室现有药品:高锰酸钾、氯酸钾、过氧化氢溶液、二氧化锰粉末、块状石灰石、稀盐酸、稀硫酸。使用装置C反应物须块状固体和液体,反应条件是常温,优点是可控制反应的发生和停止。请根据实验室现有药品和下列装置回答问题。
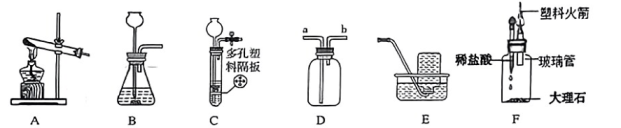 (1)、反应原理:实验室加热混合物制取O2的化学方程式为 。(2)、仪器选用:用过氧化氢溶液制取较纯净的O2时,则发生装置和收集装置选用(填写字母)。(3)、药品选用:用C装置来制取某气体,选用的药品为 (填写药品名称)。(4)、收集气体:收集CO2用装置D,则气体应从 口进 (填“a”或“b”)。(5)、趣味实验:小圳同学在社团活动中利用F装置“发射火箭”,先挤压胶头滴管,套在玻璃管上的塑料火箭向上冲出,完成发射:则F装置中发生反应的化学方程式为 。29. 化学是一门以实验为基础的科学,根据下列实验装置回答问题。
(1)、反应原理:实验室加热混合物制取O2的化学方程式为 。(2)、仪器选用:用过氧化氢溶液制取较纯净的O2时,则发生装置和收集装置选用(填写字母)。(3)、药品选用:用C装置来制取某气体,选用的药品为 (填写药品名称)。(4)、收集气体:收集CO2用装置D,则气体应从 口进 (填“a”或“b”)。(5)、趣味实验:小圳同学在社团活动中利用F装置“发射火箭”,先挤压胶头滴管,套在玻璃管上的塑料火箭向上冲出,完成发射:则F装置中发生反应的化学方程式为 。29. 化学是一门以实验为基础的科学,根据下列实验装置回答问题。 (1)、写出仪器的名称: 。(2)、写出装置制取氧气的化学方程式: 。从燃烧的条件考虑,棉花团没有燃烧的原因是 。(3)、若用过氧化氢溶液制取干燥的氧气,导管的接口顺序正确的是 ____ 。A、 B、 C、 D、(4)、实验室制取二氧化碳,若要控制反应的发生和停止,可选择的发生装置是 ,该装置有一处错误,请改正: 。(5)、若用装置收集二氧化碳,二氧化碳收集满的现象是 。(6)、图中的装置可以制造“化学喷泉”。将胶头滴管中的溶液挤进圆底烧瓶时,二氧化碳与氢氧化钠溶液反应,瓶内压强减小,很快看到长导管顶端产生“喷泉”现象。若将烧瓶内的换成下列四种气体中的 ____ 仍可产生“喷泉”现象填字母序号。A、 B、 C、 D、
(1)、写出仪器的名称: 。(2)、写出装置制取氧气的化学方程式: 。从燃烧的条件考虑,棉花团没有燃烧的原因是 。(3)、若用过氧化氢溶液制取干燥的氧气,导管的接口顺序正确的是 ____ 。A、 B、 C、 D、(4)、实验室制取二氧化碳,若要控制反应的发生和停止,可选择的发生装置是 ,该装置有一处错误,请改正: 。(5)、若用装置收集二氧化碳,二氧化碳收集满的现象是 。(6)、图中的装置可以制造“化学喷泉”。将胶头滴管中的溶液挤进圆底烧瓶时,二氧化碳与氢氧化钠溶液反应,瓶内压强减小,很快看到长导管顶端产生“喷泉”现象。若将烧瓶内的换成下列四种气体中的 ____ 仍可产生“喷泉”现象填字母序号。A、 B、 C、 D、五、计算题
-
30. 某小组利用如图所示装置对KClO3制氧气进行了探究:
(资料卡片):
①KClO3的熔点约为356℃,MnO2在加热条件下不分解。
②KClO3分解时,传感器得到氧气浓度随温度的变化示意图及使用不同催化剂时的固体残留率示意图如下:
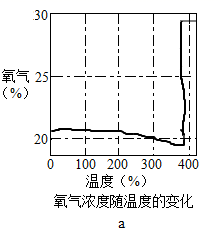
 (1)、将2.45gKClO3和一定质量的MnO2混合物后,加热至完全反应,可得氧气的质量为多少?(写出计算过程)(2)、由图a可知KClO3分解温度(填“高于”、“等于”或“低于”)其熔点。(3)、图a中,在KClO3分解前,传感器测得氧气浓度降低的原因可能是。(4)、分析图b,对KClO3分解催化效果更好的催化剂是。
(1)、将2.45gKClO3和一定质量的MnO2混合物后,加热至完全反应,可得氧气的质量为多少?(写出计算过程)(2)、由图a可知KClO3分解温度(填“高于”、“等于”或“低于”)其熔点。(3)、图a中,在KClO3分解前,传感器测得氧气浓度降低的原因可能是。(4)、分析图b,对KClO3分解催化效果更好的催化剂是。