2024年广东省深圳市中考模拟卷 03
试卷更新日期:2024-04-17 类型:中考模拟
一、单选题
-
1. 健康生活离不开化学。下列做法错误的是( )A、合理选择保健药剂和有添加剂的食品 B、霉变的大米高温蒸煮后食用 C、喝高钙牛奶可预防佝偻病和骨质疏松 D、合理摄入油脂有益身体健康2. 掌握化学用语是学好化学的关键。下列化学用语与所表述的意义相符合的是( )
①Fe2+——铁离子;②2Ca2+——2个钙离子;③O2——2个氧原子;④ ——钠离子;⑤2H2O——2个水分子;⑥2H——2个氢元素;⑦ ——氮气中氮元素的化合价为零
A、①⑤⑦ B、②③④⑥ C、①②⑤⑦ D、②⑤⑦3. 下列各组物质的名称或俗称和化学式表示的是同一种物质的是 ( )
A、熟石灰、消石灰、CaO B、铁锈、氢氧化铁、Fe(OH)3 C、生石灰、消石灰、Ca(OH)2 D、烧碱、火碱、NaOH4. 神舟十三号载人飞船使用的是目前世界上最先进的砷化镓太阳能电池。砷、镓的原子结构示意图和镓元素在元素周期表中的信息如图所示,下列说法不正确的是 ( ) A、镓属于金属元素 B、砷化镓的化学式为 C、镓的相对原子质量为 D、砷和镓元素位于同一周期5. 下列关于水和溶液的说法正确的是( )A、升高温度,可以增大固体物质的溶解度 B、均一、稳定的液体都是溶液 C、用活性炭净水既能吸附水中的色素和异味,又能降低水的硬度 D、电解水时正极产生的气体能使带火星的木条复燃6. 我国科学家发现了新冠治疗新药千金藤素(C37H38N2O6),下列说法正确的是 ( )A、千金藤素属于氧化物 B、千金藤素由碳、氢、氮、氧四种元素组成 C、千金藤素中氢元素的质量分数最大 D、千金藤素中氮、氧元素的质量比为1∶37. 下列对化学知识的归纳不完全正确的一组是( )
A、镓属于金属元素 B、砷化镓的化学式为 C、镓的相对原子质量为 D、砷和镓元素位于同一周期5. 下列关于水和溶液的说法正确的是( )A、升高温度,可以增大固体物质的溶解度 B、均一、稳定的液体都是溶液 C、用活性炭净水既能吸附水中的色素和异味,又能降低水的硬度 D、电解水时正极产生的气体能使带火星的木条复燃6. 我国科学家发现了新冠治疗新药千金藤素(C37H38N2O6),下列说法正确的是 ( )A、千金藤素属于氧化物 B、千金藤素由碳、氢、氮、氧四种元素组成 C、千金藤素中氢元素的质量分数最大 D、千金藤素中氮、氧元素的质量比为1∶37. 下列对化学知识的归纳不完全正确的一组是( )A.安全常识
B.辨清物质
油着火——用水浇灭
燃气泄漏——严禁火种
水银不是银——是汞单质
干冰不是冰——固体是
C.元素与人体健康
D.初中化学中常见的“三”
缺锌——易食欲不振
缺钙——易患佝偻病
地壳中含量前三位的元素——氧、硅、铝
最主要的化学肥料——氮肥、磷肥、钾肥
A、A B、B C、C D、D8. 下列物质间的转化,只加稀盐酸不能一步完成的是( )A、MgO→MgCl2 B、Fe→FeCl3 C、Cu(OH)2→CuCl2 D、Na2CO3→NaCl9. 氨气可转化为尿素,其反应前后分子种类变化的微观示意图如下。下列说法错误的是( ) A、乙是CO2 B、反应前后原子种类和个数都不变 C、甲、丁中都含有氢元素 D、参加反应的甲与生成的丙分子个数比为1:110. 如图是甲、乙、丙(析出晶体不含结晶水)三种物质的 溶解度曲线,从图中获得的信 息错误的是( )
A、乙是CO2 B、反应前后原子种类和个数都不变 C、甲、丁中都含有氢元素 D、参加反应的甲与生成的丙分子个数比为1:110. 如图是甲、乙、丙(析出晶体不含结晶水)三种物质的 溶解度曲线,从图中获得的信 息错误的是( )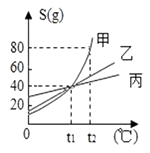 A、t1℃时甲、乙、 丙三者的溶解度相等 B、将等质量的甲乙丙三种物质分别配成t2℃的饱和溶液,所需水最多的是甲 C、t2℃时,90g 甲的饱和溶 液降温至t1℃时,析出甲的晶体 20g D、t2℃时甲的质量分数为 40%的溶液降温至t1℃会有晶体析11. 对一瓶已变质的NaOH溶液进行如下实验,其中实验方案能达到实验目的是( )
A、t1℃时甲、乙、 丙三者的溶解度相等 B、将等质量的甲乙丙三种物质分别配成t2℃的饱和溶液,所需水最多的是甲 C、t2℃时,90g 甲的饱和溶 液降温至t1℃时,析出甲的晶体 20g D、t2℃时甲的质量分数为 40%的溶液降温至t1℃会有晶体析11. 对一瓶已变质的NaOH溶液进行如下实验,其中实验方案能达到实验目的是( )选项
实验目的
实验方案
A
证明溶液中存在Na2CO3
取样,滴加无色酚酞溶液
B
除去溶液中的Na2CO3
加入一定量的CaCl2溶液,然后过滤
C
证明溶液部分变质
取样,加入过量呈中性的BaCl2溶液,振荡后滴加无色酚酞溶液
D
测溶液的pH
用玻璃棒蘸取少许溶液涂在湿润的pH试纸上,与标准比色卡对比
A、A B、B C、C D、D12. 归纳整理是一种很好的学习方法。下面是同学们在复习中梳理得到的一组图像,其中图像与实验表述一致的是( )A、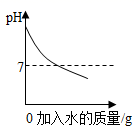 加水稀释NaOH溶液
B、
加水稀释NaOH溶液
B、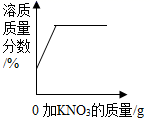 一定温度下,向不饱和KNO3溶液中加入KNO3固体
C、
一定温度下,向不饱和KNO3溶液中加入KNO3固体
C、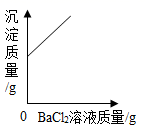 向一定量的稀硫酸中滴加BaCl2溶液,
D、
向一定量的稀硫酸中滴加BaCl2溶液,
D、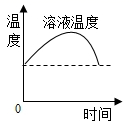 硝酸铵溶于水后温度的变化
硝酸铵溶于水后温度的变化
二、实验题
-
13. 下图中A~E为常见的实验装置,请根据要求填空。
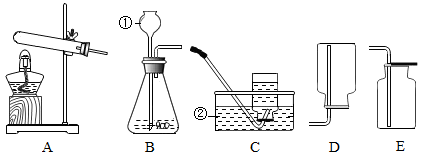 (1)、写出标号仪器的名称:① , ②。(2)、实验室用氯酸钾和二氧化锰的混合物制取氧气,反应的符号表达式为;基本反应类型是 , 应选用的发生装置是(填字母)。若选择该装置用高锰酸钾制取氧气,则试管口缺少 , 用高锰酸钾制取氧气的符号表达式为。(3)、用E装置收集氧气时,检验氧气是否集满的方法是。(4)、小李同学想用过氧化氢溶液和二氧化锰混合来制取较纯净的氧气,则他应选用的制取装置组合是、(填字母),反应的文字表达式为 , 二氧化锰起作用。
(1)、写出标号仪器的名称:① , ②。(2)、实验室用氯酸钾和二氧化锰的混合物制取氧气,反应的符号表达式为;基本反应类型是 , 应选用的发生装置是(填字母)。若选择该装置用高锰酸钾制取氧气,则试管口缺少 , 用高锰酸钾制取氧气的符号表达式为。(3)、用E装置收集氧气时,检验氧气是否集满的方法是。(4)、小李同学想用过氧化氢溶液和二氧化锰混合来制取较纯净的氧气,则他应选用的制取装置组合是、(填字母),反应的文字表达式为 , 二氧化锰起作用。三、科学探究题
-
14. 硫酸亚铁晶体是一种重要的化工原料,用途十分广泛。某化学兴趣小组欲制备硫酸亚铁晶体并探究其分解产物。(1)、【探究一】制备铜同时制得硫酸亚铁晶体(FeSO4·xH2O)
以黄铜矿(CuFeS2)为原料,采用生物炼铜是现代炼铜的新工艺,原理为:。向上述反应后的溶液中加入Fe粉,发生两个主要反应,得到FeSO4溶液和Cu,
CuFeS2为二硫化亚铁铜,也可以表示为CuS·FeS,其中S元素的化合价为。
(2)、发生主要反应的两个化学方程式为:①;②。(3)、FeSO4溶液经蒸发浓缩、降温结晶、过滤等操作得到硫酸亚铁晶体(FeSO4·xH2O)。【探究二】探究硫酸亚铁晶体受热分解的产物
硫酸亚铁晶体(FeSO4·xH2O)是一种重要的食品和饲料添加剂,对其进行热分解研究。
查阅资料:①硫酸铜粉末为白色,吸水后变成蓝色晶体。
②二氧化硫能使高锰酸钾溶液褪色。
③硫酸亚铁晶体加热会先失去结晶水,高温会继续分解产生一种金属氧化物和两种非金属氧化物。
称取ag硫酸亚铁晶体样品按图1高温加热,使其完全分解,对所得产物进行探究,并通过称量装置B的质量测出x的值。
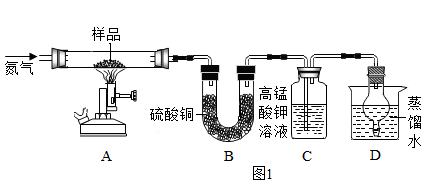
装置B中硫酸铜粉末变蓝,质量增加12.6g,说明产物中有 , 装置C中高锰酸钾溶液褪色,说明产物中还有;实验前后都要通入氮气。实验后要持续通入氮气,否则测出的x会(填“偏大”“偏小”或“不变”)。
(4)、硫酸亚铁晶体完全分解后,装置A中残留红棕色固体。已知硫酸亚铁分解还生成另一物质SO3(高温下为气态),写出FeSO4分解的化学方程式。(5)、利用热分析仪对此硫酸亚铁晶体(FeSO4·xH2O)进行热分解,获得相关数据,绘制成固体质量一分解温度的关系图如图2,结合实验并根据图2中有关数据,可计算出FeSO4·xH2O中的x=。
四、流程题
-
15. 年春节联欢晚会中只此青绿呈现了宋代千里江山图 , 让我们仿佛置身于宋代的青山绿水之中。千里江山图里的绿色来自孔雀石,其主要成分为 , 含有、杂质。工业上以孔雀石为原料制备重要化工原料胆矾的流程如图。
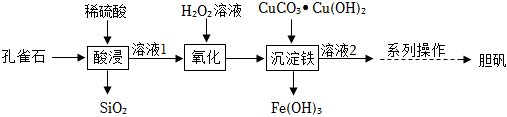
回答相关问题:
(1)、《千里江山图色彩依旧,说明常温下绿色颜料孔雀石的性质 。(2)、“酸浸”发生的反应属于四大基本反应类型中的 ,溶液中含的金属阳离子有 。(3)、“氧化”过程中发生反应的化学方程式为: 请补充完该方程式。(4)、“沉淀铁”不能将替换为 , 其原因是 任答点。(5)、系列操作有蒸发、结晶、 、洗涤、干燥。(6)、加热胆矾至全部变成白色无水 , 固体质量减轻了 不需要写出计算过程。五、综合应用题
-
16. 垃圾袋焚烧促进了垃圾处置的减量化、资源化和无害化。化学兴趣小组的同学们对垃圾焚烧产生了兴趣,他们走进垃圾焚烧厂,展开了项目式学习之旅。(1)、项目一:了解垃圾焚烧工艺系统
【实地参观】垃圾焚烧工艺系统由垃圾储存系统、焚烧系统、余热锅炉系统、烟气净化系统、汽轮发电系统、灰渣处理系统、给排水系统、渗沥液处理系统组成。
【表达交流】
垃圾进入焚烧系统前,需要将垃圾进行分类,下列垃圾属于可回收物的是____(填字母序号)。A、废旧金属 B、快递纸箱 C、食物残渣(2)、为了使垃圾在焚烧系统的充分燃烧,可进行的操作是。(3)、项目二:检验垃圾渗沥液的成分【进行实验】
实验操作
实验现象
实验结论
步骤1
取少量黑色的垃圾渗沥液于烧杯中,加入足量的 , 静置
上层溶液变为无色,异味消除
步骤2
取少量上层溶液于试管中,向其中滴加紫色石蕊溶液
。
渗沥液中含有H+
步骤3
另取少量上层溶液于试管中,向其中滴加。
产生白色沉淀
渗沥液中含有Cl-
(4)、【得出结论】垃圾渗沥液中含有H+和Cl- ,【分析解释】
步骤3中发生反应的化学方程式是。
(5)、项目三:讨论垃圾焚烧的意义【讨论交流】
垃圾焚烧的意义是(写一种即可)。
-
-
-