初中科学浙教版 八年级下册 第二章 微粒的模型与符号同步练习
试卷更新日期:2024-04-14 类型:单元试卷
一、单选题
-
1. 有3种不同的原子,甲原子核内有6个质子和6个中子,乙原子核内有6个质子和8个中子,丙原子核内有7个质子和7个中子.下列说法正确的是( )A、甲和乙是同一种元素 B、甲和乙的核电荷数不同 C、乙和丙核外电子数相等 D、乙和丙互为同位素原子2. 质子和中子都是由u夸克和d夸克组成的,u夸克带电量为e,d夸克带电量为为为基础电荷。下列论断可能正确的是( )A、质子由1个u夸克和1个d夸克组成,中子由1个u夸克和2个d夸克组成 B、质子由1个u夸克和2个d夸克组成,中子由2个u夸克和1个d夸克组成 C、质子由2个u夸克和1个d夸克组成,中子由1个u夸克和2个d夸克组成 D、质子由2个u夸克和1个d夸克组成,中子由1个u夸克和1个d夸克组成3. R、X两种元素间能形成多种化合物,已知其中一种化合物RX中 R元素的质量分数为46.7%,则下列化合物中,R元素的质量分数大于46.7%的是( )A、RX2 B、R2X3 C、R2X D、R2X54. 某金属元素只有一种化合价。 已知它的氯化物的相对分子质量为M,它的氢氧化物的相对分子质量为N,则该金属的化合价为( )A、 B、 C、 D、5. 硫隔绝空气加热后的蒸气中有一种物质的化学式为S8 , 关于S8的叙述不正确的有( )A、它是一种新型的化合物 B、它是一种单质 C、它的一个分子中有8个硫原子 D、相对分子质量为2566. 下列关于Na、Na+两种粒子的判断正确的是( )
①核电荷数相同②核外电子数相等
③Na+比Na稳定④质量几乎相等
⑤质子数相等
A、①②⑤ B、②④ C、①③④⑤ D、①②③④⑤7. 达菲的主要制作原料是八角、茴香中的莽草酸(C7H10O5)。下列关于莽草酸的说法中,正确的是( )A、莽草酸中碳元素的质量分数约为 48.28% B、莽草酸由7个碳原子、10个氢原子、5个氧原子构成 C、莽草酸的相对分子质量为 174g D、莽草酸中碳、氢、氧三种元素的质量比为7:10:58. 有三种不同的原子,A原子核内有6个质子和6个中子,B原子核内有7个质子和7个中子,C原子核内有6个质子和8个中子。下列说法正确的是( )A、A和C的核电荷数不同 B、B和C的核外电子数相同 C、A和C是同一种元素 D、B和C互为同位素原子9. 元素周期表是学习和研究化学的重要工具。下表是元素周期表的一部分,A~F代表六种不同短周期元素。下列说法不正确的是( )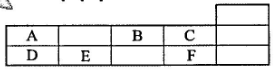 A、原子序数 E<C B、A、D同族 C、A、B同周期 D、C、F化学性质相似10. 电子数相同、质子数不同的两种粒子,它们可能是( )A、两种不同元素的原子 B、两种不同元素的离子 C、两种不同的分子 D、同种元素的原子和离子11. 根据元素化合价高低的顺序,在NH4Cl、N2、N2O、X、N2O3 , N2O4、KNO3的排列中,X应是( )A、KNO2 B、(NH4)2SO4 C、NO D、N2O312. 下列叙述错误的是( )A、分子、原子和离子都能直接构成物质 B、原子中原子核与核外电子的电量相等,电性相反,所以整个原子不显电性 C、决定原子质量大小的主要是质子和电子 D、原子如果得到或失去电子就变成离子13. 锆(Zr)的一种氧化物是耐高温的新型陶瓷材料,经测定,锆原子核内有51个中子,核外有40个电子,其氯化物的相对分子质量为233,若锆的氯化物和氧化物中锆元素的化合价相同,则其氧化物的化学式为( )A、Zr2O B、ZrO C、Zr2O3 D、ZrO214. 空气中部分氧气在遇到闪电时可转化为臭氧(O3)。下列说法中,正确的是( )A、O2转化为O3是物理变化 B、O2和O3的化学性质相同 C、O2和O3混合得到的物质是纯净物 D、等质量的 O2和O3含有的氧原子的个数之比是1:115. 下列物质的化学式,书写错误的是 ( )A、氯化亚铁FeCl2 B、氢氧化钠 NaOH C、氧化镁 MgO D、碳酸钠 NaCO316. 元素周期表是学习和研究化学的重要工具。根据图示,判断错误的是 ( )
A、原子序数 E<C B、A、D同族 C、A、B同周期 D、C、F化学性质相似10. 电子数相同、质子数不同的两种粒子,它们可能是( )A、两种不同元素的原子 B、两种不同元素的离子 C、两种不同的分子 D、同种元素的原子和离子11. 根据元素化合价高低的顺序,在NH4Cl、N2、N2O、X、N2O3 , N2O4、KNO3的排列中,X应是( )A、KNO2 B、(NH4)2SO4 C、NO D、N2O312. 下列叙述错误的是( )A、分子、原子和离子都能直接构成物质 B、原子中原子核与核外电子的电量相等,电性相反,所以整个原子不显电性 C、决定原子质量大小的主要是质子和电子 D、原子如果得到或失去电子就变成离子13. 锆(Zr)的一种氧化物是耐高温的新型陶瓷材料,经测定,锆原子核内有51个中子,核外有40个电子,其氯化物的相对分子质量为233,若锆的氯化物和氧化物中锆元素的化合价相同,则其氧化物的化学式为( )A、Zr2O B、ZrO C、Zr2O3 D、ZrO214. 空气中部分氧气在遇到闪电时可转化为臭氧(O3)。下列说法中,正确的是( )A、O2转化为O3是物理变化 B、O2和O3的化学性质相同 C、O2和O3混合得到的物质是纯净物 D、等质量的 O2和O3含有的氧原子的个数之比是1:115. 下列物质的化学式,书写错误的是 ( )A、氯化亚铁FeCl2 B、氢氧化钠 NaOH C、氧化镁 MgO D、碳酸钠 NaCO316. 元素周期表是学习和研究化学的重要工具。根据图示,判断错误的是 ( )H
He
X
Y
Z
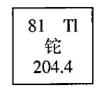 A、铊元素属于金属元素 B、铊元素的核内质子数为81 C、Z的原子序数大于Y D、X和Y处于同一周期17. 下列对分子、原子、离子的认识,正确的是 ( )A、原子是最小的粒子,不可再分 B、温度越高,分子运动速率越快 C、分子是保持物质性质的一种粒子 D、铝原子与铝离子的化学性质相同18. 建立模型是学习科学的重要方法,在理解化学反应的本质时往往引入模型。下图是某反应的微观模型,有关该模型的叙述中,正确的是( )
A、铊元素属于金属元素 B、铊元素的核内质子数为81 C、Z的原子序数大于Y D、X和Y处于同一周期17. 下列对分子、原子、离子的认识,正确的是 ( )A、原子是最小的粒子,不可再分 B、温度越高,分子运动速率越快 C、分子是保持物质性质的一种粒子 D、铝原子与铝离子的化学性质相同18. 建立模型是学习科学的重要方法,在理解化学反应的本质时往往引入模型。下图是某反应的微观模型,有关该模型的叙述中,正确的是( ) A、反应前后分子数目不变 B、反应前后原子种类发生改变 C、
A、反应前后分子数目不变 B、反应前后原子种类发生改变 C、 和
和 化学性质相似
D、
化学性质相似
D、 是保持氧气化学性质的微粒
是保持氧气化学性质的微粒
二、填空题
-
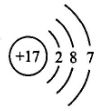
19. 已知某元素 R(相对原子质量为32)的氧化物中,R 元素的质量分数为 50%,则 R元素的化合价为。20. 某种牙膏中含有抗牙腐蚀药物,它的化学式为Na2FPO3。 已知F在化合物中的化合价为-1,钠的相对原子质量是23,氧的相对原子质量是16,磷的相对原子质量是31。则 Na2FPO3属于(填“单质”或“化合物”),其中磷的化合价为 , Na2FPO3的相对分子质量是144,则氟的相对原子质量为。21. 如图是氯元素原子结构示意图,该原子核外有个电子层,与氯元素在同一纵行的氟元素,其原子结构与氯原子相似。 试推测,氟原子在化学反应中形成的离子符号是。
 22. 某物质化学式为 HnRO2n-1 , 相对分子质量为 M,则 R 的化合价为 , R的相对原子质量为。23.(1)、某三价金属氧化物中氧元素的质量分数为30%,则该金属元素的相对原子质量为。(2)、A、B两元素的相对原子质量之比为2:1,仅由这两种元素组成的化合物里,A、B两元素的质量比为2:3,则该化合物的化学式为 ;若其中B元素为-n价,则此化合物中 A元素的化合价为。(3)、元素 R 有多种氧化物,其中 RO 中含氧53.33%,那么相对分子质量为 76,含氧为63.15%的 R的氧化物的化学式是 。24. 不同的分子(1)、不同种类、不同数目的原子能构成不同的分子。构成分子的原子可以是同种原子,也可以是不同种原子。如1个氧分子由2个氧原子构成,1个臭氧分子由3个氧原子构成,1个水分子由2个氢原子和1个氧原子构成。
22. 某物质化学式为 HnRO2n-1 , 相对分子质量为 M,则 R 的化合价为 , R的相对原子质量为。23.(1)、某三价金属氧化物中氧元素的质量分数为30%,则该金属元素的相对原子质量为。(2)、A、B两元素的相对原子质量之比为2:1,仅由这两种元素组成的化合物里,A、B两元素的质量比为2:3,则该化合物的化学式为 ;若其中B元素为-n价,则此化合物中 A元素的化合价为。(3)、元素 R 有多种氧化物,其中 RO 中含氧53.33%,那么相对分子质量为 76,含氧为63.15%的 R的氧化物的化学式是 。24. 不同的分子(1)、不同种类、不同数目的原子能构成不同的分子。构成分子的原子可以是同种原子,也可以是不同种原子。如1个氧分子由2个氧原子构成,1个臭氧分子由3个氧原子构成,1个水分子由2个氢原子和1个氧原子构成。不同的分子能构成不同的物质。如水由水分子构成,二氧化碳由构成,氢气由氢气分子构成。
(2)、同种原子在直接构成物质时,如果原子的不同,所形成的物质结构就不同。如金刚石和石墨都是由碳原子直接构成的,但碳原子的排列方式不同,所以金刚石和石墨的结构也就不同。25. 原子核的构成(1)、原子核是由更小的两种粒子和中子构成的。(2)、一个质子带一个单位的正电荷,中子 , 一个电子带一个单位的负电荷。26. 2013 年5月,某市自来水有股奇怪的味道,经专家多轮综合检测,基本认定引起此次异味的主要物质是邻叔丁基苯酚。将30克邻叔丁基苯酚完全燃烧,生成88克 CO2和25.2克 H2O(无其他产物)。已知邻叔丁基苯酚的相对分子质量为 150,则:(1)、30克邻叔丁基苯酚中含碳元素 克,氢元素克。(2)、邻叔丁基苯酚的化学式为。三、实验探究题
-
27. 氨气与氧气的反应如图所示:
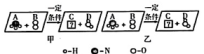 (1)、如图甲所示,若C是空气中的主要成分,则反应的化学方程式为 , 生成的C与D的质量比是。(2)、如图乙所示,若C是氧化物,且 A 与B 的分子个数比为4:5时,该反应的化学方程式为28. 如图所示,下列A~E 容器中,分别盛有不同的物质。
(1)、如图甲所示,若C是空气中的主要成分,则反应的化学方程式为 , 生成的C与D的质量比是。(2)、如图乙所示,若C是氧化物,且 A 与B 的分子个数比为4:5时,该反应的化学方程式为28. 如图所示,下列A~E 容器中,分别盛有不同的物质。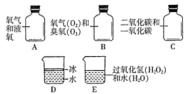 (1)、其中所盛物质属于混合物的是(填字母,下同),属于单质的是 , 属于纯净物的是。(2)、图中“o”和“●”分别表示质子数不同的两种原子,则下列各图示表示化合物的是 (填字母)。A、
(1)、其中所盛物质属于混合物的是(填字母,下同),属于单质的是 , 属于纯净物的是。(2)、图中“o”和“●”分别表示质子数不同的两种原子,则下列各图示表示化合物的是 (填字母)。A、 B、
B、 C、
C、 D、
D、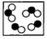 29. 如图是元素周期表的一部分,请回答相关问题:
29. 如图是元素周期表的一部分,请回答相关问题:第一周期
1H
2He
第二周期
3Li
4Be
5B
6C
7N
8O
9F
10Ne
第三周期
11Na
12Mg
13A1
14Si
15P
16S
17C1
18Ar
(1)、锂元素与钠元素位于同一纵行的原因是相同,它们在化学反应中都是失去电子,铝元素与氧元素形成化合物的化学式是。(2)、M2-与Ar核外电子排布相同,则M元素的名称为元素。30. 元素周期表将已知元素科学有序地排列起来,便于我们研究它们的性质和用途。右表表示元素周期表的一部分,请回答下列问题。H
He
①
N
②
Ne
③
Ar
(1)、元素在周期表中的分布是有规律的,表中①②③所代表的三种元素中,属于非金属的是。(2)、表中氮元素的化合价有多种,请写出化合价为+1价的氮的氧化物(用化学式表示)。(3)、氦气的化学式为。(4)、随着新元素的不断发现,元素周期表还将逐渐完善。最近,科学家用大量高速钙原子轰击锫原子,形成了117号元素的原子,该元素原子核中一定含有117个。31. 19 世纪以前,人们一直认为原子是不可分的。1897年汤姆生发现了带负电的电子,并提出类似“葡萄干面包”的原子模型。为进一步探究原子的结构,1911年英国科学家卢瑟福进行了著名的α粒子轰击金箔实验。
【收集证据】绝大多数α粒子穿过金箔后仍沿原来的方向前进,只有少数α粒子发生了较大的偏转,并且有极少数α粒子的偏转超过90°,有的甚至几乎达到180°,像是被金箔弹了回来。
【猜想与假设】α粒子遇到电子后,就像飞行的子弹碰到灰尘一样运动方向不会发生明显的改变,而结果却出乎意料,除非原子的大部分质量集中到了一个很小的结构上,否则大角度的散射是不可能的。
【解释与结论】
(1)、卢瑟福所说的“除非原子的大部分质量集中到了一个很小的结构上”中的“很小的结构”指的是;(2)、当α粒子轰击金箔时,下图能正确表示运动轨迹的是; (3)、实验中能说明原子内部绝大部分是空的证据是;32. 隔夜菜是否能吃,主要在于烧熟后的隔夜菜中亚硝酸盐含量的变化是否符合食品安全要求。蔬菜中的硝酸盐来自生长过程中所施氮肥,空气中微生物(如硝酸盐还原菌),会产生一种还原酶,使蔬菜中的部分硝酸盐还原成亚硝酸盐。烧熟后的菜在食用和保存阶段都会有一些细菌进入:做熟的蔬菜更适合细菌生长。
(3)、实验中能说明原子内部绝大部分是空的证据是;32. 隔夜菜是否能吃,主要在于烧熟后的隔夜菜中亚硝酸盐含量的变化是否符合食品安全要求。蔬菜中的硝酸盐来自生长过程中所施氮肥,空气中微生物(如硝酸盐还原菌),会产生一种还原酶,使蔬菜中的部分硝酸盐还原成亚硝酸盐。烧熟后的菜在食用和保存阶段都会有一些细菌进入:做熟的蔬菜更适合细菌生长。某研究小组对烧熟的菜中亚硫酸盐含量做了测试,数据如下表:盖有保鲜膜的菜肴在4℃的冰箱中放置不同时间的亚硝酸盐含量(单位:mg/kg)
菜肴
半小时
6小时
18小时
24小时
炒青菜
0.6861
0.7982
4.3333
5.3624
韭菜炒蛋
1.8153
1.9249
2.8390
5.6306
红烧肉
2.4956
4.2558
4.0668
5.5188
红烧鲫鱼
/
2.0948
3.2300
7.2397
将一份红烧鲫鱼样本(不盖保鲜膜)在常温下放置4小时,测定其亚硝酸盐含量为8.9483mg/g。
请根据以上材料,回答下列问题:
(1)、亚硝酸盐中含有亚硝酸根离子NO2﹣ , 其中氮元素的化合价是价。(2)、根据表中的数据,菜中的亚硝酸盐含量变化的共同规律是:。(3)、要使烧熟后的隔夜菜中亚硝酸盐含量尽可能低,保存的条件应该是。(4)、用多种菜做实验的目的是。33. 碘是一种由碘分子构成的非金属单质,某同学利用碘进行了如下的实验:①把少量的固体碘放在湿润的馒头上,发现馒头会变蓝色(提示:碘分子能使馒头中的淀粉变蓝色);
②再取少量的碘溶解在水中,用馒头去蘸取碘液,发现馒头也会变蓝色。则:
(1)、取少量的碘放入烧杯中,用酒精灯加热,碘升华变成碘蒸气,把湿润的馒头放在碘蒸气中,馒头 (填会或不会)变蓝色。(2)、由上述三个实验可知,分子是。(3)、现在市场上买来的食盐都是加碘盐(含有KIO3 , ),用馒头沾取少量的食盐水(填会或不会)变蓝色。四、解答题
-
34. 如图是市售某品牌牙膏包装盒上的部分说明。其主要活性成分单氟磷酸钠(Na2FPO3),是牙膏常用添加剂之一,实验表明牙膏中单氟磷酸钠的质量分数达到0.76%~0.80%时,防龋齿效果较好。
 (1)、求单氟磷酸钠中氟元素的质量分数(计算结果精确到0.01%)。(2)、通过计算判断,该牙膏是否有较好的防龋齿效果。35. 化学是研究物质的,而物质是由肉眼看不到的分子、原子和离子等微观粒子构成的,让我们从五彩缤纷的宏观世界步入充满神奇色彩的微观世界。(1)、金秋十月,丹桂飘香,从分子的角度分析其原因是。(2)、元素周期表是我们学习化学的重要工具。 下表是小科同学绘制的元素周期表的局部,依据此表回答问题。
(1)、求单氟磷酸钠中氟元素的质量分数(计算结果精确到0.01%)。(2)、通过计算判断,该牙膏是否有较好的防龋齿效果。35. 化学是研究物质的,而物质是由肉眼看不到的分子、原子和离子等微观粒子构成的,让我们从五彩缤纷的宏观世界步入充满神奇色彩的微观世界。(1)、金秋十月,丹桂飘香,从分子的角度分析其原因是。(2)、元素周期表是我们学习化学的重要工具。 下表是小科同学绘制的元素周期表的局部,依据此表回答问题。
①其中有一处元素符号不正确,应改为。
②地壳中含量最多的元素的原子的质子数是 , 在化学反应中它易(填“得到”或“失去”)电子。
36. 如图所示为电解水(水通雪氢气+氧气)的模型图,据图填空。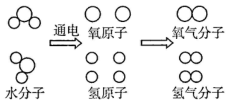 (1)、 在这个过程中,水分子最终变成了 和 ,这说明发生了(填“物理”或“化学”)变化。(2)、 在这一过程中,分子的种类发生了变化,水分子已经变成了其他分子,已经不能再保持水的 (填“物理”或“化学”)性质。(3)、在这个模型图中,可以看到一种比分子更小的微粒,这种微粒在这一变化中保持不变,它是化学变化中的基本单位,也是化学变化中的最小微粒,这种微粒的名称是。
(1)、 在这个过程中,水分子最终变成了 和 ,这说明发生了(填“物理”或“化学”)变化。(2)、 在这一过程中,分子的种类发生了变化,水分子已经变成了其他分子,已经不能再保持水的 (填“物理”或“化学”)性质。(3)、在这个模型图中,可以看到一种比分子更小的微粒,这种微粒在这一变化中保持不变,它是化学变化中的基本单位,也是化学变化中的最小微粒,这种微粒的名称是。