四川省宜宾市2024年中考化学模拟试卷
试卷更新日期:2024-04-12 类型:中考模拟
一、选择题:本大题共14小题,共42分。
-
1. 化学与我们的衣、食、住、行以及能源、信息、材料、国防、环境保护、医药卫生、资源利用等方面都有密切的联系,它是一门社会迫切需要的实用学科。化学的迅猛发展离不开一代又一代科学家前赴后继的研究与探索。下列科学家中发现元素周期律并编制元素周期表的是( )A、张青莲 B、屠呦呦 C、拉瓦锡 D、门捷列夫2. 化学源于生活,同时又服务于生活。下列说法错误的是( )A、用甲醛水溶液浸泡食用海鲜 B、炒菜时油锅不慎着火,迅速用锅盖盖灭 C、消毒酒精存放应远离火源 D、纸袋代替塑料袋可缓解“白色污染”3. 年月日至月日,第十九届亚运会在杭州举办,秉承“绿色、智能、节俭、文明”的办会理念,下列措施不可行的是( )A、积极推进新能源汽车的使用,逐步淘汰燃油汽车 B、垃圾分类存放、处理 C、将路边散落的塑料袋、树叶集中焚烧,保持整洁的环境 D、积极推广共享单车4. 用氯化钠固体和水配制溶质质量分数的氯化钠溶液,下列说法正确的是( )A、移动游码使其右侧对其标尺的刻度线,再将氯化钠加到左盘 B、如果量筒读数时仰视,所配制的溶液溶质质量分数将偏大 C、配制溶液需要经过计算、称量、量取、溶解、转液、贴标签等步骤 D、溶解时用玻璃棒搅拌可以增大氯化钠的溶解度5. 用“”形玻璃管进行微型实验,将注射器中的过氧化氢溶液推入管中与二氧化锰接触。下列有关说法错误的是( )
 A、二氧化锰可以增加生成氧气的质量 B、若处粉末是木炭粉,能看到有白光产生 C、若处粉末是硫粉,处产生的气体会污染空气 D、用“”形玻璃管进行实验可以节约药品、减少污染6. 2022年,首届完全实现“碳中和”的绿色冬季奥运会在北京举办。除了可再生能源、材料的使用,现代绿色制冷技术的应用。其中各种“黑科技”也大放异彩。其中速滑竞赛服使用了蜂窝样式的聚氨酯材料,以求最大限度提高运动员的成绩。下列有关聚氨酯(C16H22N2O5)n说法正确的是( )A、氢元素与氧元素的质量比为22:5 B、属于有机高分子化合物 C、聚氨酯由45个原子构成 D、完全燃烧后的产物只有CO2和H2O7. 在火箭的制造中使用了钛合金,钛元素在元素周期表中的相关信息如图所示,从图中获得信息错误的是( )
A、二氧化锰可以增加生成氧气的质量 B、若处粉末是木炭粉,能看到有白光产生 C、若处粉末是硫粉,处产生的气体会污染空气 D、用“”形玻璃管进行实验可以节约药品、减少污染6. 2022年,首届完全实现“碳中和”的绿色冬季奥运会在北京举办。除了可再生能源、材料的使用,现代绿色制冷技术的应用。其中各种“黑科技”也大放异彩。其中速滑竞赛服使用了蜂窝样式的聚氨酯材料,以求最大限度提高运动员的成绩。下列有关聚氨酯(C16H22N2O5)n说法正确的是( )A、氢元素与氧元素的质量比为22:5 B、属于有机高分子化合物 C、聚氨酯由45个原子构成 D、完全燃烧后的产物只有CO2和H2O7. 在火箭的制造中使用了钛合金,钛元素在元素周期表中的相关信息如图所示,从图中获得信息错误的是( )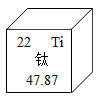 A、钛的原子序数是22 B、钛原子的核电荷数是22 C、钛元素属于金属元素 D、钛元素的相对原子质量是47.87g8. 下列有关化学用语表示正确的是( )A、纤维素: B、钠原子结构示意图:
A、钛的原子序数是22 B、钛原子的核电荷数是22 C、钛元素属于金属元素 D、钛元素的相对原子质量是47.87g8. 下列有关化学用语表示正确的是( )A、纤维素: B、钠原子结构示意图: C、个锌离子:
D、个碳原子:
9. 推理是一种重要的学习方法,下列推理正确的是( )A、氧化钙溶于水生成氢氧化钙温度会升高,活泼金属与酸反应温度会升高,两者都是化学反应,所以温度会升高的反应都是化学反应 B、CO2能使澄清石灰水变浑浊,所以澄清石灰水变浑浊的变化一定是化学变化 C、无色酚酞溶液遇碱溶液变红,所以使无色酚酞溶液变红色的溶液一定是碱溶液 D、化合物是由不同种元素组成的纯净物,所以由不同种元素组成的纯净物一定是化合物10. 关于如图实验的说法正确的是( )
C、个锌离子:
D、个碳原子:
9. 推理是一种重要的学习方法,下列推理正确的是( )A、氧化钙溶于水生成氢氧化钙温度会升高,活泼金属与酸反应温度会升高,两者都是化学反应,所以温度会升高的反应都是化学反应 B、CO2能使澄清石灰水变浑浊,所以澄清石灰水变浑浊的变化一定是化学变化 C、无色酚酞溶液遇碱溶液变红,所以使无色酚酞溶液变红色的溶液一定是碱溶液 D、化合物是由不同种元素组成的纯净物,所以由不同种元素组成的纯净物一定是化合物10. 关于如图实验的说法正确的是( ) A、实验进行一段时间后玻璃瓶中的溶液变红 B、对比实验中两支试管内液面的高低,不能说明二氧化碳与氢氧化钠发生了反应 C、实验中型管内液面左高右低 D、实验可探究催化剂的种类对反应速率的影响11. 如图是硝酸钾和氯化钠的溶解度曲线图。时,分别将硝酸钾和氯化钠放入水中,充分溶解。在该温度下,下列说法不正确的是( )
A、实验进行一段时间后玻璃瓶中的溶液变红 B、对比实验中两支试管内液面的高低,不能说明二氧化碳与氢氧化钠发生了反应 C、实验中型管内液面左高右低 D、实验可探究催化剂的种类对反应速率的影响11. 如图是硝酸钾和氯化钠的溶解度曲线图。时,分别将硝酸钾和氯化钠放入水中,充分溶解。在该温度下,下列说法不正确的是( ) A、两种溶液中溶质的质量分数相等 B、若将该硝酸钾溶液降温到 , 溶液中溶质和溶液的质量比为: C、硝酸钾中含有少量氯化钠,可通过降温结晶的方法提纯 D、若将该硝酸钾溶液变为时的饱和溶液,溶质的质量分数一定减小12. 在给定条件下,下列物质间的转化能实现的是( )A、 B、 C、 D、13. 归纳是学习化学的重要方法,小丽总结出如图所示不同类别的物质之间的反应关系图中“”连接的物质表示能相互反应 , 除指示剂外图①中的物质可能是( )
A、两种溶液中溶质的质量分数相等 B、若将该硝酸钾溶液降温到 , 溶液中溶质和溶液的质量比为: C、硝酸钾中含有少量氯化钠,可通过降温结晶的方法提纯 D、若将该硝酸钾溶液变为时的饱和溶液,溶质的质量分数一定减小12. 在给定条件下,下列物质间的转化能实现的是( )A、 B、 C、 D、13. 归纳是学习化学的重要方法,小丽总结出如图所示不同类别的物质之间的反应关系图中“”连接的物质表示能相互反应 , 除指示剂外图①中的物质可能是( ) A、 B、 C、 D、14. 如图实验不能达到实验目的的是 ( )
A、 B、 C、 D、14. 如图实验不能达到实验目的的是 ( ) A、图 , 区分硬水和软水 B、图 , 探究与水的反应 C、图 , 探究接触面积对反应速率的影响 D、图 , 比较空气与人体呼出的气体中含量
A、图 , 区分硬水和软水 B、图 , 探究与水的反应 C、图 , 探究接触面积对反应速率的影响 D、图 , 比较空气与人体呼出的气体中含量二、填空题:本大题共1小题,共10分。
-
15. 在“宏观微观符号”之间建立联系,是化学学科特有的思维方式。
 (1)、如图所示,该反应中涉及种氧化物。
(1)、如图所示,该反应中涉及种氧化物。该反应的化学方程式为 , 反应前后涉及化合价改变的元素有种。
(2)、如图所示,从微观的角度分析,甲处应填入的离子符号为。从微观的角度说明该反应的实质是。若想证明两种物质是否恰好完全反应,可在反应后的溶液中加入适量的试剂,该试剂是填字母。
溶液
酚酞溶液
石蕊溶液
溶液
三、流程题:本大题共1小题,共10分。
-
16. 以粉煤灰主要成分为、及少量等为原料制取纯净的部分工艺流程如图:

【资料】溶液中滴入溶液会呈血红色。
(1)、“酸浸”时温度不宜过高的原因是。滤渣的主要成分是。(2)、“除铁”时,发生反应的化学方程式为;检验溶液中铁元素已除尽的方法是。(3)、“结晶”是向浓溶液中通入气体,从而获得晶体的过程。溶液中和盐酸的浓度随通气时间的变化如图所示图中物质的浓度数值为另一种浓度表示法。由此可得出的结论是。(4)、“煅烧”时发生反应的化学方程式为。其中可以循环利用的物质是。(5)、高温烧结的氧化铝,又称人造刚玉或人造宝石,可用于制机械轴承、钟表中的钻石、坩埚、高强度陶瓷等。由此可推知氧化铝的性质有____填序号。A、硬度大 B、熔点高 C、性质稳定四、科普短文题:本大题共1小题,共10分。
-
17. 阅读下面科普短文.
肼又称联氨,有类似于氨的刺鼻气味,贮存时用氮气保护并密封,用途广泛.肼燃烧放热量大且燃烧产物对环境无污染,常用作火箭燃料,点燃时与助燃物质液态发生反应,生成和高压锅炉水处理时用于脱除氧气以防止锅炉的腐蚀,也可以把锅炉内表面锈蚀后的氧化铁还原为结构紧密的四氧化三铁保护层,减缓锅炉锈蚀.用于烟草、土豆、玉米的贮藏,用于食用盐酸的制造等.熔点 , 沸点;有强烈的吸水性,形成水合肼 , 可以用固体烧碱进行脱水;能吸收空气中的二氧化碳;易溶于水;与液氧接触能自燃;长期暴露在空气中或短时间受热时易发生分解.对眼睛有刺激作用,能引起延迟性发炎,对皮肤和粘膜也有强烈的腐蚀作用.
依据短文内容,回答下列问题:
(1)、肼的下列性质中,属于物理性质的是____填字母序号,下同 .A、与氧化铁作用 B、易溶于水 C、易分解 D、有刺鼻的气味(2)、肼在常温下为填“固态”“液态”或“气态” .(3)、肼作为火箭燃料燃烧时反应的化学方程式为 .(4)、水合肼的相对分子质量是(5)、使用水合肼时应注意以下____防护措施.A、戴橡胶手套 B、皮肤接触后立即用流动清水冲洗 C、戴防毒面具 D、工作后沐浴更衣五、实验题:本大题共2小题,共20分。
-
18. 如图为初中化学常见的仪器装置,请回答下列问题。
 (1)、写出仪器名称:为。(2)、实验室用加热混有的固体制取 , 发生装置应选用填字母序号,下同 , 反应前后在固体混合物中的质量分数选填“有”或“无”改变。(3)、实验室制取 , 发生反应的化学方程式为 , 装置中盛放浓硫酸可用来干燥 , 气体从填长管或短管通入。(4)、实验室制取可选用装置收集,点燃前必须进行的操作是。19. 化学是以实验为基础的科学,请按照要求回答下列问题。
(1)、写出仪器名称:为。(2)、实验室用加热混有的固体制取 , 发生装置应选用填字母序号,下同 , 反应前后在固体混合物中的质量分数选填“有”或“无”改变。(3)、实验室制取 , 发生反应的化学方程式为 , 装置中盛放浓硫酸可用来干燥 , 气体从填长管或短管通入。(4)、实验室制取可选用装置收集,点燃前必须进行的操作是。19. 化学是以实验为基础的科学,请按照要求回答下列问题。 (1)、如图甲,同学们制作的简易净水器中小卵石、石英砂和蓬松棉的作用是。(2)、如图乙,将浓氨水加入左侧试管,分钟后观察到的现象是;使用气球目的是为了氨气密度小于空气。(3)、如图丙,左侧试管中发生反应的化学方程式。
(1)、如图甲,同学们制作的简易净水器中小卵石、石英砂和蓬松棉的作用是。(2)、如图乙,将浓氨水加入左侧试管,分钟后观察到的现象是;使用气球目的是为了氨气密度小于空气。(3)、如图丙,左侧试管中发生反应的化学方程式。六、计算题:本大题共1小题,共8分。
-
20. 某兴趣小组用镁条与一定溶质质量分数的稀硫酸反应。测得产生氢气的质量与稀硫酸的质量关系如下表假设镁条中除表面有氧化镁外,没有其它杂质。
加入稀硫酸质量
产生气体质量
 (1)、用化学方程式说明当稀硫酸的质量为时,不产生氢气的原因是。(2)、计算镁条中金属镁的质量分数写出计算过程。(3)、在图中画出产生气体与加入稀硫酸的质量的关系图,标出有关物质的量。
(1)、用化学方程式说明当稀硫酸的质量为时,不产生氢气的原因是。(2)、计算镁条中金属镁的质量分数写出计算过程。(3)、在图中画出产生气体与加入稀硫酸的质量的关系图,标出有关物质的量。
-
-
-