湖北省随州市曾都区、随县多校联考2024年中考一模化学试题
试卷更新日期:2024-04-12 类型:中考模拟
一、单选题(共15题,每题1分)
-
1. 根据物质组成种类的多少可以把物质分为纯净物和混合物,下列属于纯净物的是( )A、稀有气体 B、盐酸 C、冰水混合物 D、石油2. 高“钙”奶、富“硒”茶、补“铁”酱油,这里的“钙、硒、铁”指的是( )A、原子 B、元素 C、分子 D、离子3. 钼是组成眼睛虹膜的元素之一,虹膜可调节瞳孔大小,控制进入眼球内的光线。Na2MoO4是Mo元素的重要化合物,其中Mo元素的化合价是( )A、+4 B、+5 C、+6 D、+74. 2023年3月22日世界水日的主题是“加速变革”,“中国水周”的活动主题为“强化依法治水携手共护母亲河”。下列说法不正确的是( )A、水源保护地附近禁止建设化工企业 B、农业灌溉采用滴灌或喷淋代替水浇地 C、建设海绵城市,增加雨水渗透,可有效留下淡水,改善环境 D、为减少环境污染,将污水深注入地下5. 下列实验操作正确的是( )A、倾倒液体
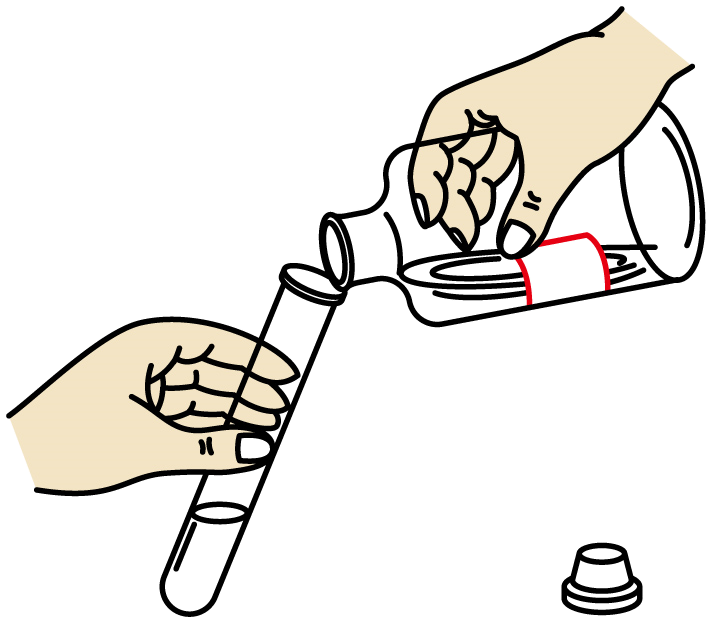 B、称取固体
B、称取固体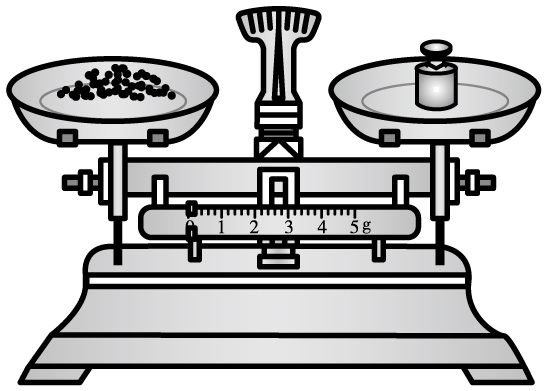 C、量取液体
C、量取液体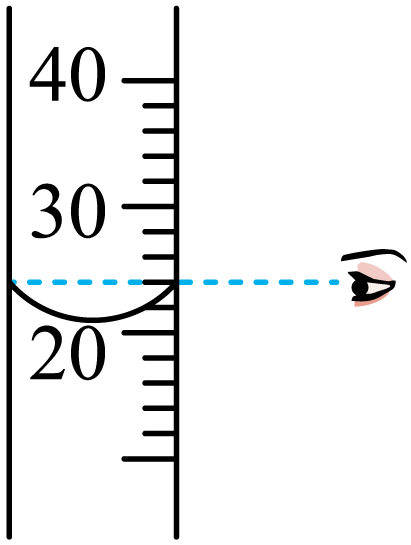 D、滴加液体
D、滴加液体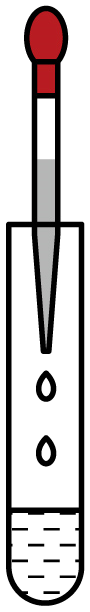 6. 下列生活中的常见物质能使紫色石蕊试液变红的是( )A、碳酸饮料 B、植物油 C、食盐水 D、白酒7. 为强化安全意识,提升安全素养,某校举行了消防安全知识竞赛。下列做法正确的是( )A、室内起火,打开所有门窗通风 B、炒菜时油锅着火,立即盖上锅盖 C、家中燃气泄漏,立即打开排气扇通风 D、在煤炉上放一壶水能防止CO中毒8. 氯在元素周期表中的信息如图所示。下列有关说法正确的是( )
6. 下列生活中的常见物质能使紫色石蕊试液变红的是( )A、碳酸饮料 B、植物油 C、食盐水 D、白酒7. 为强化安全意识,提升安全素养,某校举行了消防安全知识竞赛。下列做法正确的是( )A、室内起火,打开所有门窗通风 B、炒菜时油锅着火,立即盖上锅盖 C、家中燃气泄漏,立即打开排气扇通风 D、在煤炉上放一壶水能防止CO中毒8. 氯在元素周期表中的信息如图所示。下列有关说法正确的是( )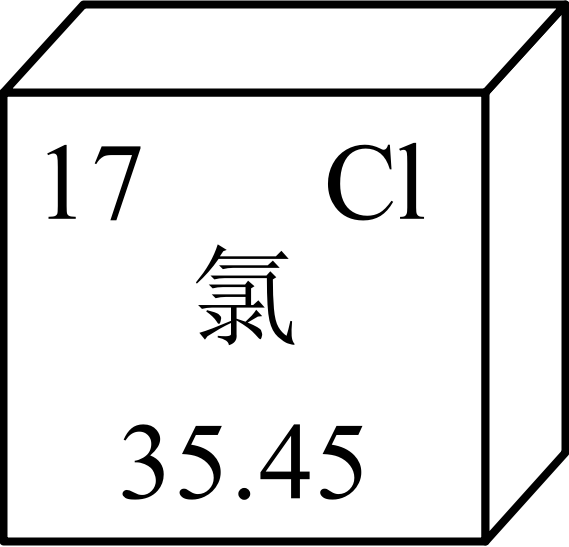 A、氯属于金属元素 B、氯的元素符号是Cl C、氯的相对原子质量是35.45g D、Cl-有17个电子9. 下列物质的用途体现其化学性质的是( )A、干冰升华会吸热——作食品制冷剂 B、石墨具有导电性——作干电池的电极 C、焦炭具有可燃性——用作燃料 D、铅锑合金的熔点低——用于制作保险丝10. 下列描述的变化中,不能用质量守恒定律解释的是( )A、蜡烛燃烧后质量减小 B、将3g食盐放入3g水中完全溶解后得6g溶液 C、铁生锈后质量增加 D、硫粉在空气中充分燃烧后固体质量减小到0g11. 下列做法与目的不符的是( )A、鉴别空气与呼出气体——倒入澄清石灰水 B、鉴别水和酚酞——倒入氨水 C、鉴别二氧化锰与胆矾——看颜色 D、鉴别N2和CO2——闻气味12. 某兴趣小组对KClO3分解反应的催化剂进行研究,在相同的加热条件下,用如图所示的装置完成表中的实验。结合数据分析,下列有关说法错误的是( )
A、氯属于金属元素 B、氯的元素符号是Cl C、氯的相对原子质量是35.45g D、Cl-有17个电子9. 下列物质的用途体现其化学性质的是( )A、干冰升华会吸热——作食品制冷剂 B、石墨具有导电性——作干电池的电极 C、焦炭具有可燃性——用作燃料 D、铅锑合金的熔点低——用于制作保险丝10. 下列描述的变化中,不能用质量守恒定律解释的是( )A、蜡烛燃烧后质量减小 B、将3g食盐放入3g水中完全溶解后得6g溶液 C、铁生锈后质量增加 D、硫粉在空气中充分燃烧后固体质量减小到0g11. 下列做法与目的不符的是( )A、鉴别空气与呼出气体——倒入澄清石灰水 B、鉴别水和酚酞——倒入氨水 C、鉴别二氧化锰与胆矾——看颜色 D、鉴别N2和CO2——闻气味12. 某兴趣小组对KClO3分解反应的催化剂进行研究,在相同的加热条件下,用如图所示的装置完成表中的实验。结合数据分析,下列有关说法错误的是( )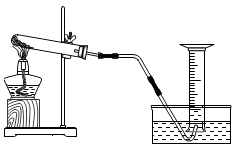
编号
KClO3质量/g
催化剂
催化剂质量/g
收集50mLO2所需时间/s
实验1
5
一
一
171
实验2
5
MnO2
0.5
49
实验3
5
KCl
0.5
154
A、实验1的目的是作对照实验 B、由实验1和实验3,可知KCl在该反应中具有催化作用 C、MnO2在该反应中的催化效果比KCl的好 D、用MnO2作催化剂能够增加氧气的产量13. 下列实验设计不能达到实验目的的是( )选项
A
B
C
D
实验设计
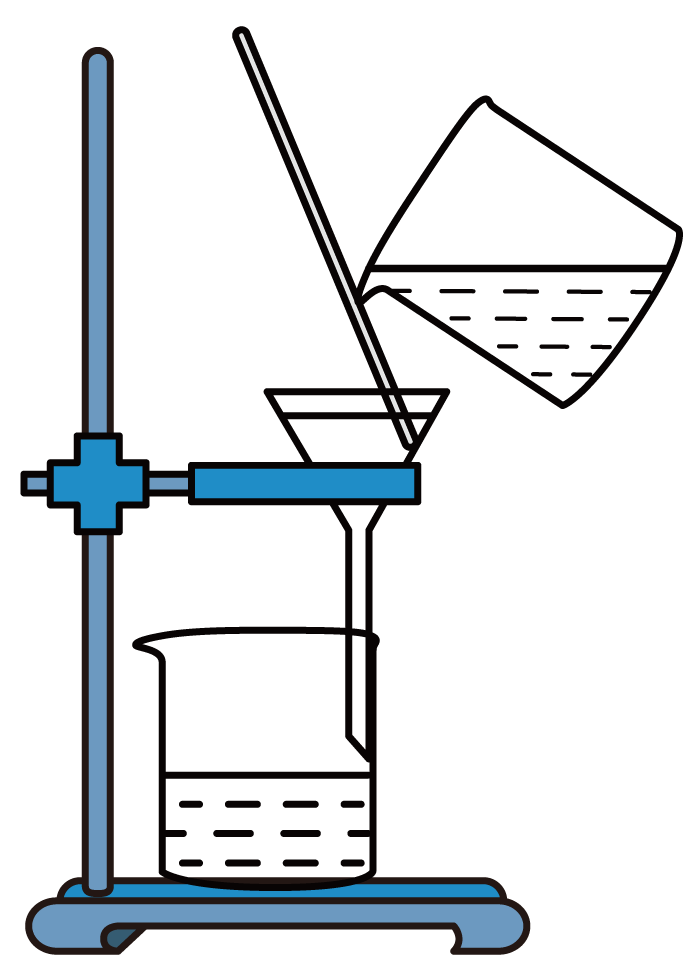
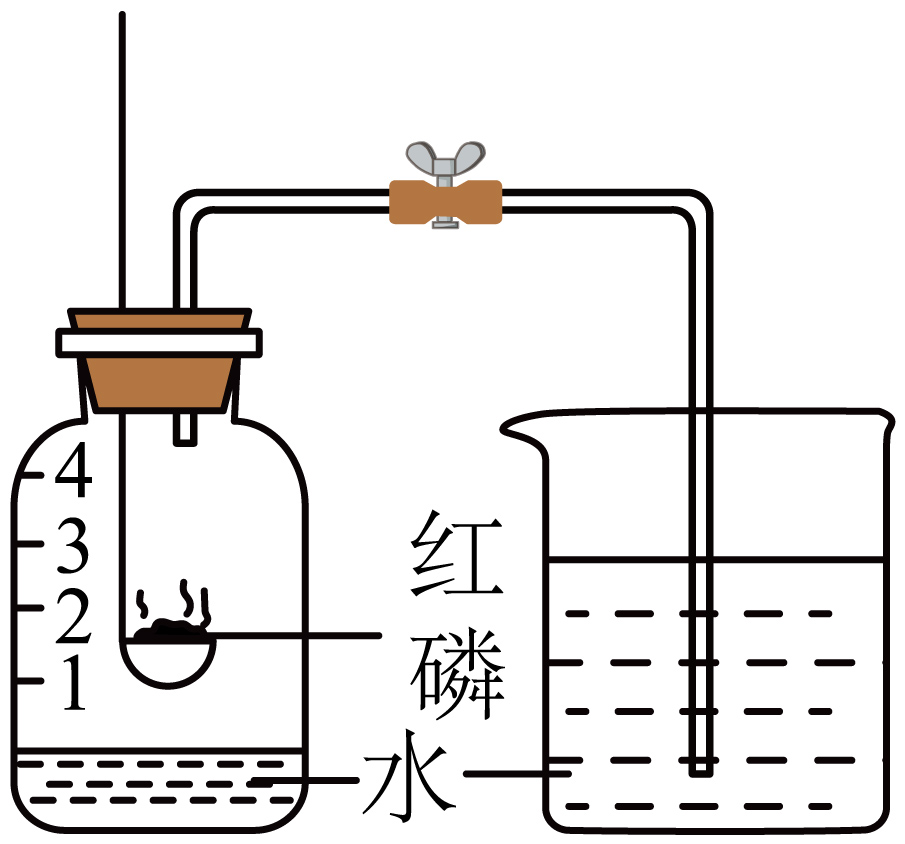

实验目的
降低水的硬度
测定空气中氧气含量
检查装置的气密性
比较呼出气体和空气中水蒸气的含量
A、A B、B C、C D、D14. 如图是某化学反应的微观示意图,其中不同的圆球代表不同原子。下列说法中正确的是( )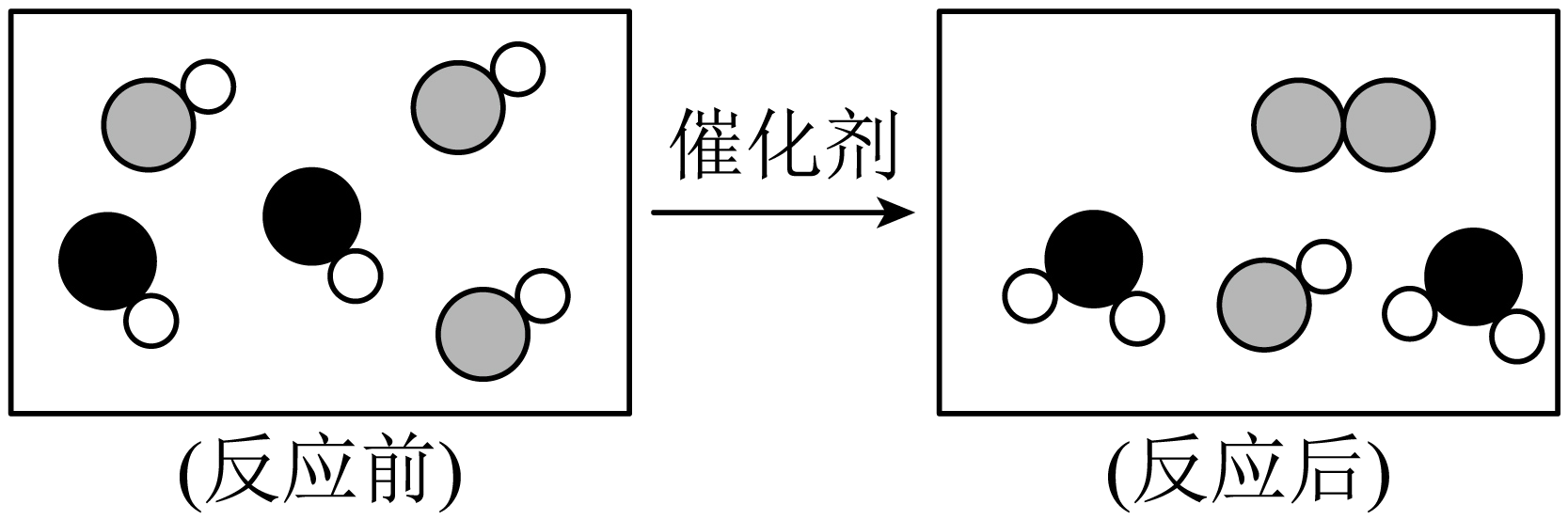 A、该反应中参加反应的反应物分子个数比为2:3 B、图中反应前是混合物,反应后是纯净物 C、该反应是化合反应 D、反应前后,原子的种类和数目不变15. 甲、乙、丙是初中化学常见的物质,它们之间存在如图所示的转化关系(图中“→”表示一种物质一步转化成另一种物质,部分反应、生成物及反应条件已省略)。下列说法与图示关系不相符的是( )
A、该反应中参加反应的反应物分子个数比为2:3 B、图中反应前是混合物,反应后是纯净物 C、该反应是化合反应 D、反应前后,原子的种类和数目不变15. 甲、乙、丙是初中化学常见的物质,它们之间存在如图所示的转化关系(图中“→”表示一种物质一步转化成另一种物质,部分反应、生成物及反应条件已省略)。下列说法与图示关系不相符的是( )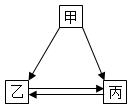 A、若丙是H2O,甲可以是H2O2 B、若乙是CO2 , 甲可以是C C、若甲是O2 , 乙可以是CO D、若甲是CO,乙可以是Fe,丙可以是Cu
A、若丙是H2O,甲可以是H2O2 B、若乙是CO2 , 甲可以是C C、若甲是O2 , 乙可以是CO D、若甲是CO,乙可以是Fe,丙可以是Cu二、填空题(本大题共5题,化学方程式每个1分,其余每空0.5分,共 19分)
-
16. 用化学用语填空:(1)、2个氮原子;(2)、钙元素;(3)、碳酸根离子;(4)、保持一氧化碳化学性质的最小粒子是;(5)、铝制品有较好抗腐蚀性,其原因用化学方程式是;(6)、实验室常用酒精灯加热,酒精燃烧的化学方程式是。17. 化学与人类生活息息相关,是造福于人类的科学。请利用所学知识回答下列问题。(1)、I、化学与生活
用石墨作干电池的电极是利用了石墨的性;(2)、做饭时,有时燃气灶或煤炉的火焰呈现黄色或橙色,锅底出现黑色,此时应将灶具或炉具的进风口 (填“变大”或“变小”)。(3)、Ⅱ、化学与环境倡导“低碳”生活,主要是为了减少(填化学式)的排放量。
(4)、“提高防火意识,预防森林火灾”。到林区活动时,下列做法错误的是____。A、禁带火种 B、严禁吸烟 C、野外生火 D、文明祭祀(5)、目前未计入空气污染指数检测项目的是____(填字母)。A、一氧化碳 B、可吸入颗粒物 C、二氧化氮 D、二氧化碳(6)、Ⅲ、化学与新能源神舟十六号载人飞船于今年5月30日成功发射。液氢是运载火箭常用的燃料之一,氢气作为燃料的优点是____。
A、制取成本高 B、产物无污染 C、燃烧热值高 D、贮存困难(7)、新能源汽车越来越受到人们的青睐,某新能源汽车定位系统应用了一种新型材料氮化铝(AlN)工业上在氮气流中用氧化铝与焦炭在高温条件下制得氮化铝,并生成一种可燃性气体,该反应的化学方程式为。18. 元素的化合价和物质的类别是学习物质性质的两个重要方面,如图是氮元素的价类二维图。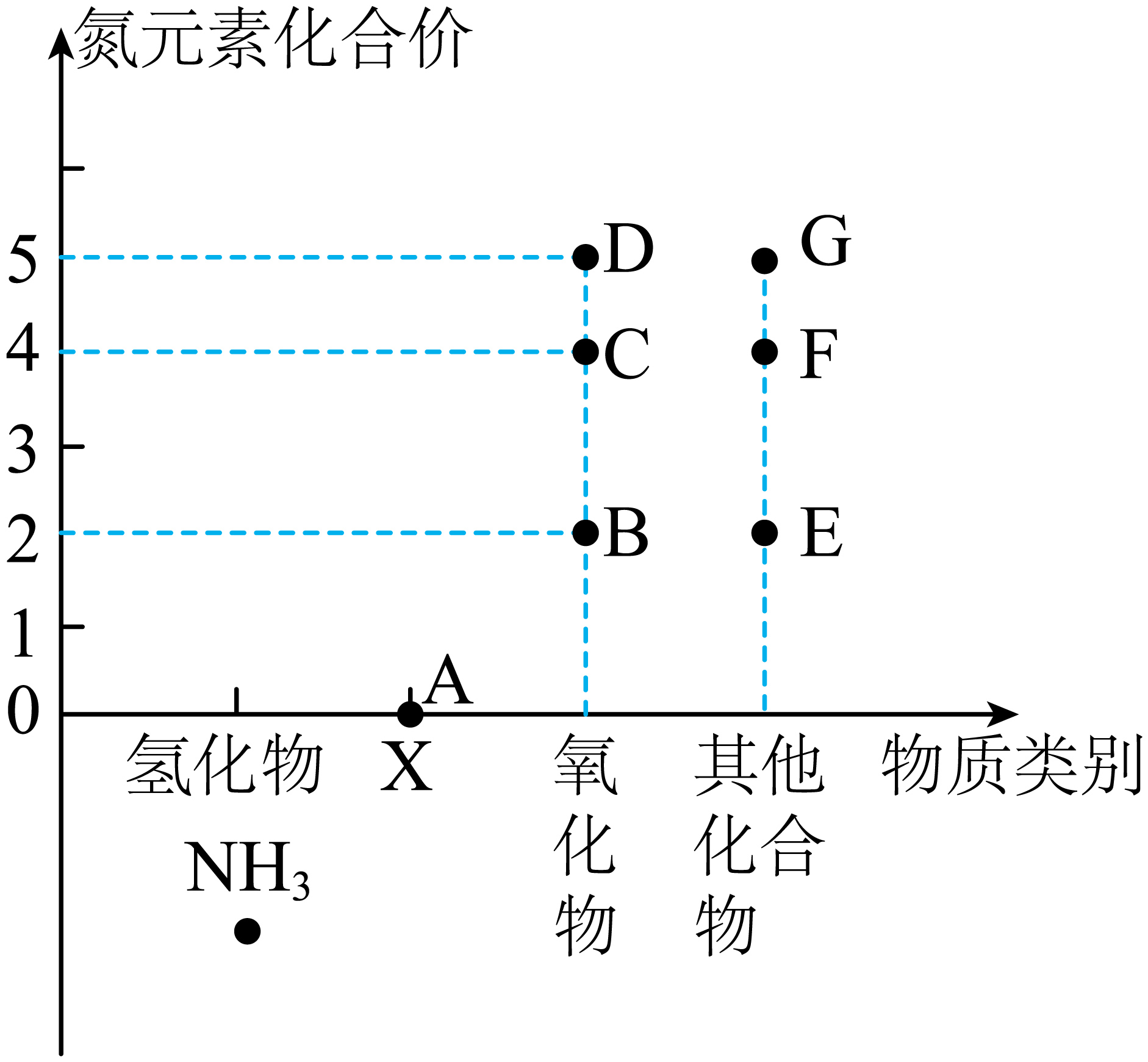 (1)、图中A点对应的物质的化学式为 , 它对应的物质类别X是。(2)、NH3中有种元素,其中N:H的元素质量比为。(3)、图中C点对应的物质为大气污染物之一,写出其对应的化学式为 , 它是汽车在行驶时氧气和氮气反应所生成的,该反应过程中氮元素的化合价(填“升高”“降低”或“不变”)。(4)、KNO3是一种对提高农作物的产量具有重要作用的肥料,它对应图中的 (填字母)点,其名称是。19. 探秘燃烧(1)、
(1)、图中A点对应的物质的化学式为 , 它对应的物质类别X是。(2)、NH3中有种元素,其中N:H的元素质量比为。(3)、图中C点对应的物质为大气污染物之一,写出其对应的化学式为 , 它是汽车在行驶时氧气和氮气反应所生成的,该反应过程中氮元素的化合价(填“升高”“降低”或“不变”)。(4)、KNO3是一种对提高农作物的产量具有重要作用的肥料,它对应图中的 (填字母)点,其名称是。19. 探秘燃烧(1)、I、探究燃烧条件
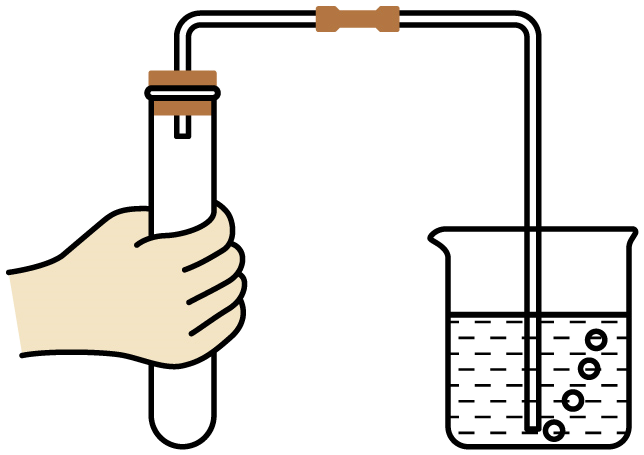
实验一:加热片刻,观察到 A中棉球燃烧产生蓝色火焰,B中棉球不燃烧,由此得出燃烧的条件之一是。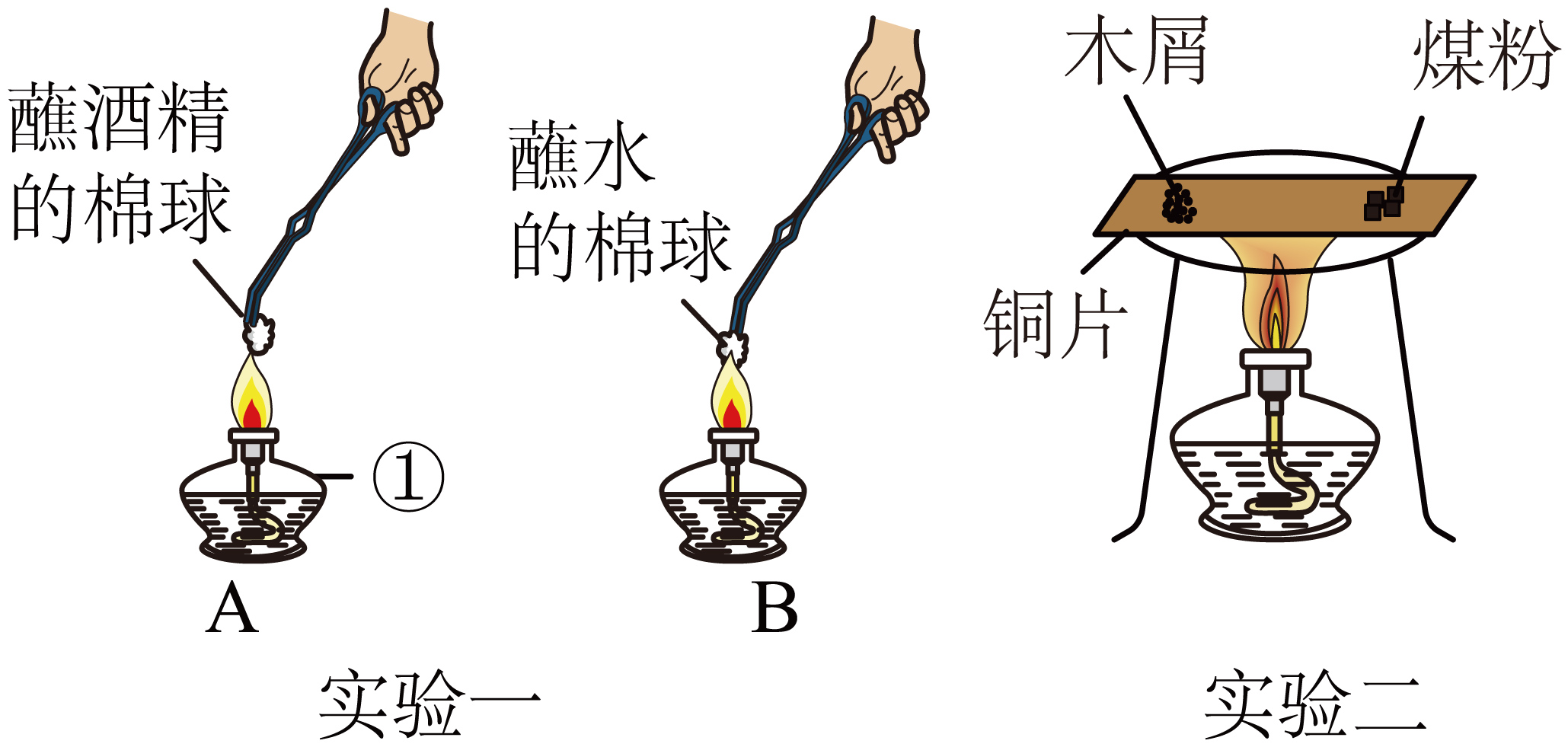 (2)、实验二:装置中木屑燃烧,煤粉没有燃烧,说明燃烧的条件之一是。(3)、Ⅱ、探究“影响燃烧剧烈程度的因素”
(2)、实验二:装置中木屑燃烧,煤粉没有燃烧,说明燃烧的条件之一是。(3)、Ⅱ、探究“影响燃烧剧烈程度的因素”实验编号
可燃物
集气瓶中气体
反应现象
甲
细铁丝
氧气
剧烈燃烧、大量放热
乙
细铁丝
空气
不燃烧
丙
铁粉
空气
剧烈燃烧、并发出大量火星
实验甲的现象还有、;比较实验甲与乙,产生不同现象的原因是。
(4)、实验丙的产物与甲相同,写出反应的化学方程式。(5)、上述实验中,能说明“反应物与氧气接触的面积不同,现象不同”的是。(填编号)20. 空气是宝贵的自然资源,如图是以空气等为原料合成尿素[CO(NH2)2的流程。请按要求回答相关问题: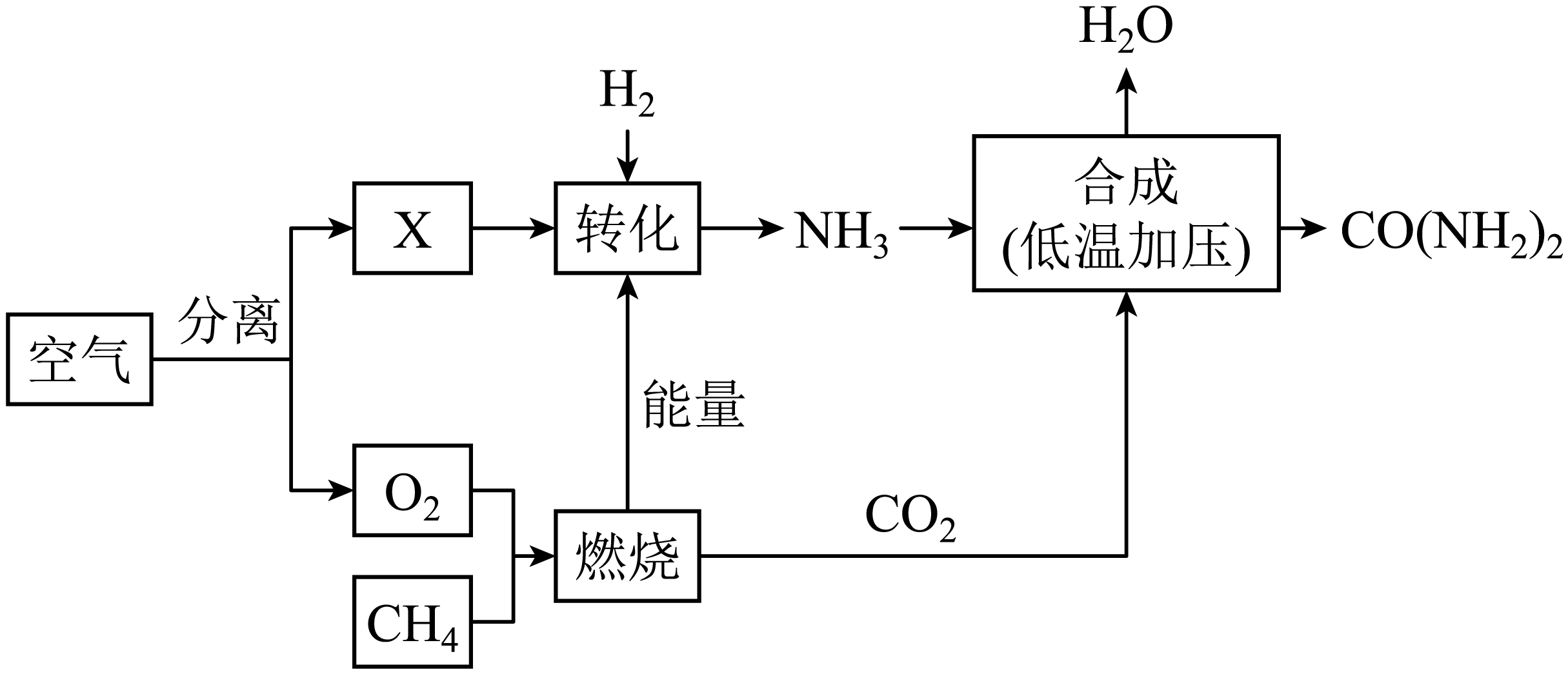 (1)、分离液态空气属于变化 (填“物理”或“化学”)(2)、X转化为NH3的基本反应类型属于;(3)、该流程中,利用甲烷燃烧提供合成尿素的反应物,其燃烧的化学方程式为;(4)、根据流程,写出利用NH3制备尿素的化学方程式。
(1)、分离液态空气属于变化 (填“物理”或“化学”)(2)、X转化为NH3的基本反应类型属于;(3)、该流程中,利用甲烷燃烧提供合成尿素的反应物,其燃烧的化学方程式为;(4)、根据流程,写出利用NH3制备尿素的化学方程式。三、实验题(本大题共2题,化学方程式每个1分,其余每空0.5分,共12分)
-
21. 某化学兴趣小组的同学利用双氧水、二氧化锰、高锰酸钾,开展氧气的实验室制取的研究。请结合下列实验装置, 回答有关问题。
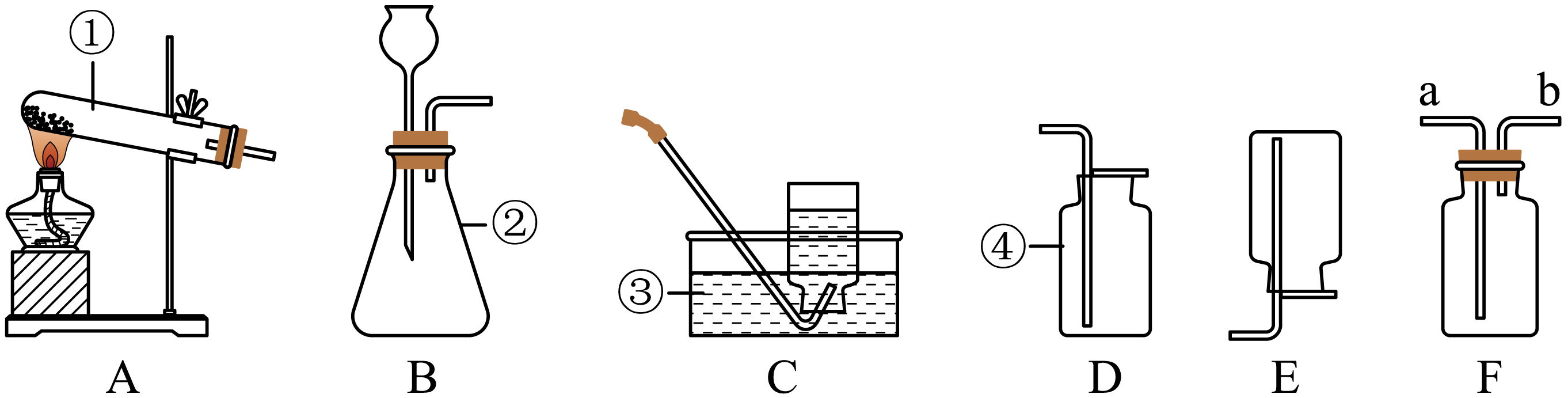 (1)、写出图中标有序号的仪器名称:②。(2)、若实验室用高锰酸钾制取氧气, 该反应的化学方程式为:。(3)、若用C装置收集氧气,正确的操作顺序为____(填序号)。
(1)、写出图中标有序号的仪器名称:②。(2)、若实验室用高锰酸钾制取氧气, 该反应的化学方程式为:。(3)、若用C装置收集氧气,正确的操作顺序为____(填序号)。a.将导管伸入集气瓶口,让气体进入瓶中
b.将装满水的集气瓶倒置在水槽中
c.当气体收集满时,用毛玻璃片盖住瓶口,将集气瓶移出水面正放置于桌面
A、bac B、abc C、acb(4)、若用F装置收集 瓶干燥的氧气,如何验满:。(5)、选用B 装置来制取氧气时,该反应的化学方程式为。实验结束后,若要分离出二氧化锰,可将残留物经过滤、洗涤、干燥。过滤操作时,需将圆形滤纸折叠。下列滤纸折叠过程图示中,正确的是 (选填“甲”或“乙”)。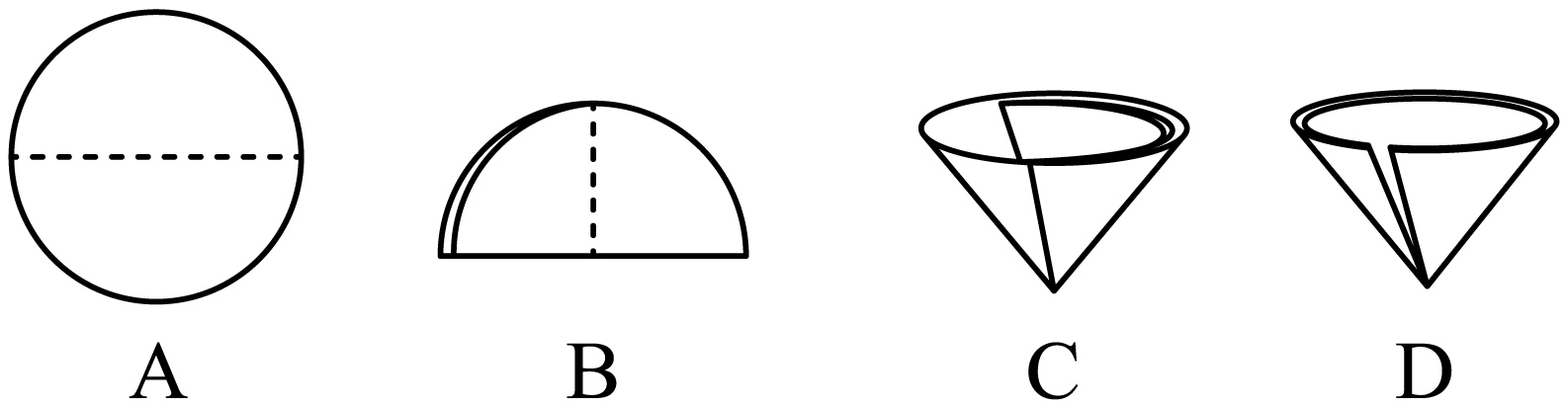
甲: A→B→C 乙: A→B→D
(6)、在过滤操作中玻璃棒的作用是。若滤液仍浑浊,下列可能的原因有。(写一条即可)22. 金属材料的使用见证了人类文明发展的过程,我们可以从多角度了解。(1)、随州市博物馆的镇馆之宝“曾侯乙编钟”是战国时期的青铜器,青铜硬度比纯铜硬度(填“大”或“小”)。(2)、春秋战国时期铁器已开始使用,赭石(主要成分为 Fe2O3)是一种铁矿石,写出用 一氧化碳与赭石炼铁的反应的化学方程式。(3)、活动一:探究铁生锈的条件某学习小组用相同的光亮铁钉探究铁生锈与哪些因素有关,设计的实验如图所示。
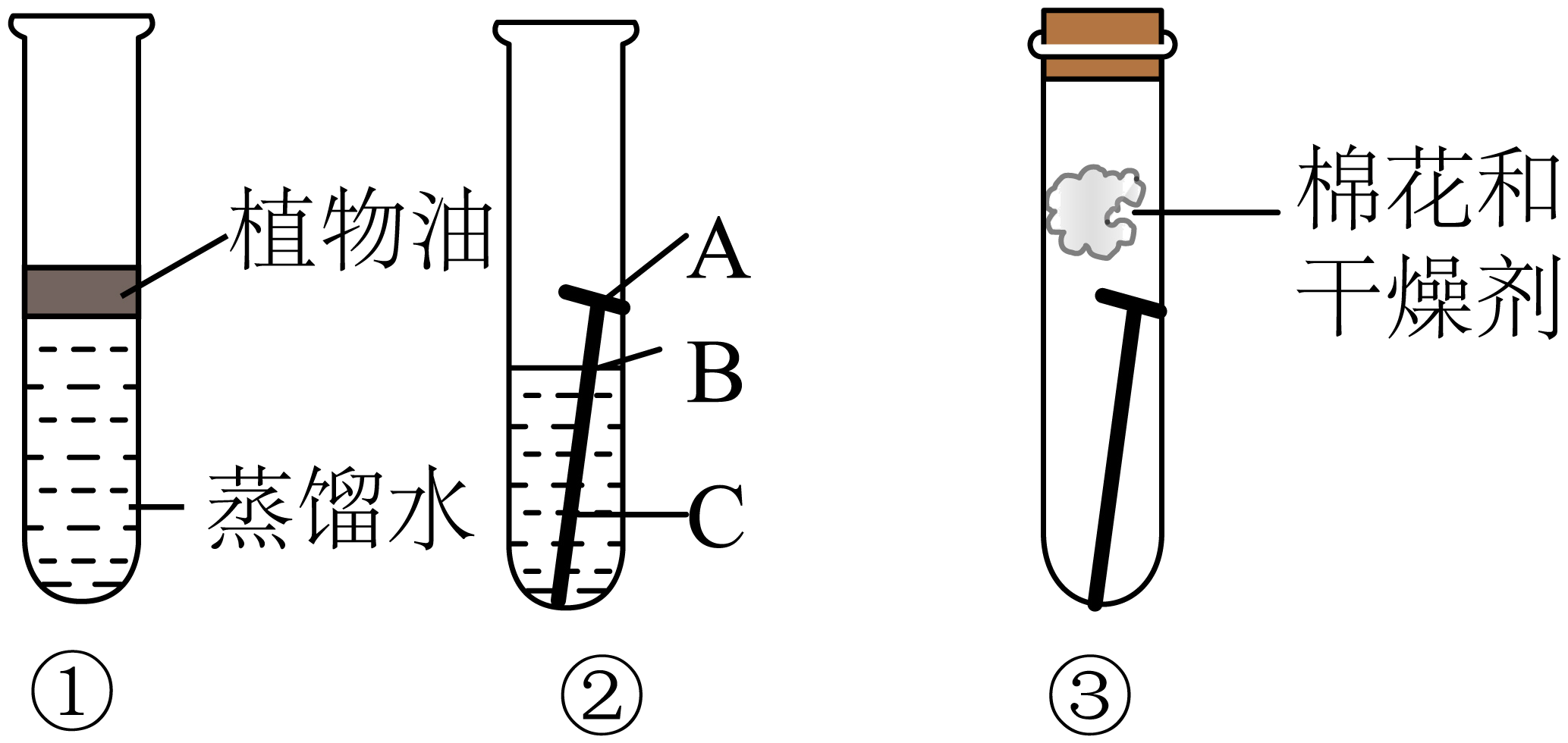
一周后观察,试管①和③中的铁钉无明显变化,试管②中的铁钉明显生锈。探究发现铁生锈的主要条件是铁与直接接触。②中铁钉的A、B、C三处中处锈蚀最严重。
(4)、试管①中加入的蒸馏水要事先煮沸,其目的是。蒸馏水的上面加入一层植物油的作用是。(5)、【能力发展】保护金属资源的有效途径(写一条)。
(6)、活动二 探究金属的化学性质如图所示为化学小组探究金属的化学性质所做的四个实验。 回答下列问题:
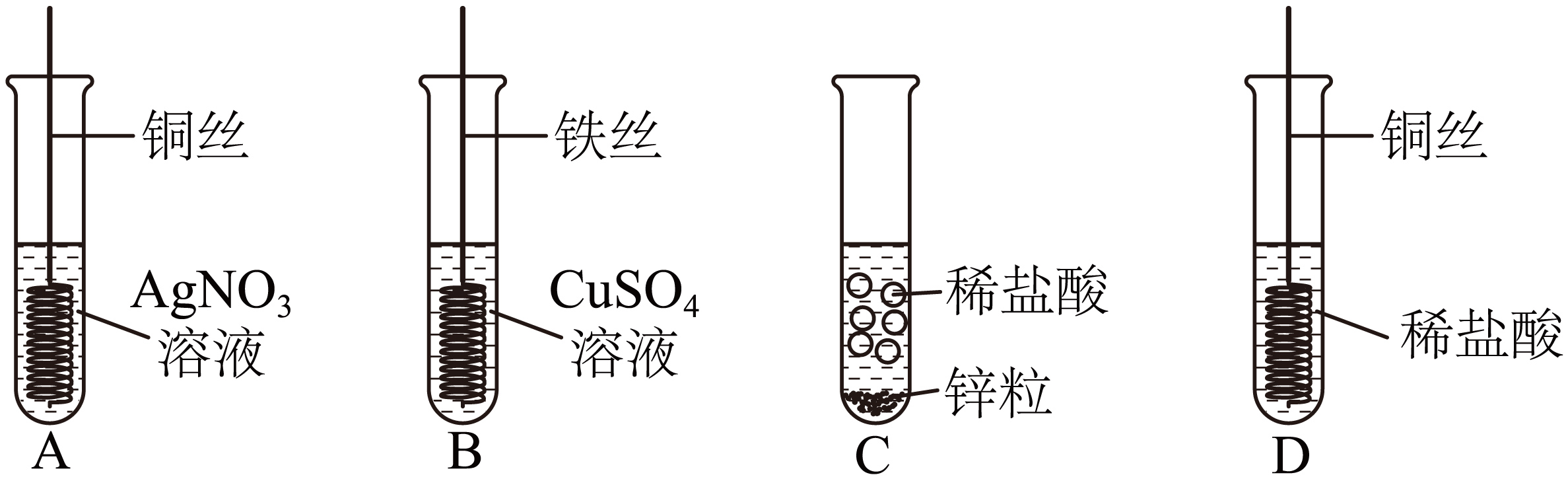
①写出溶液变蓝的反应的化学方程式。
②由上述实验能得出金属的活动性顺序是。
(7)、该化学小组进一步对含有Fe(NO3)3、X(NO3)3的混合溶液进行探究,流程如下 (X、Y各表示一种金属):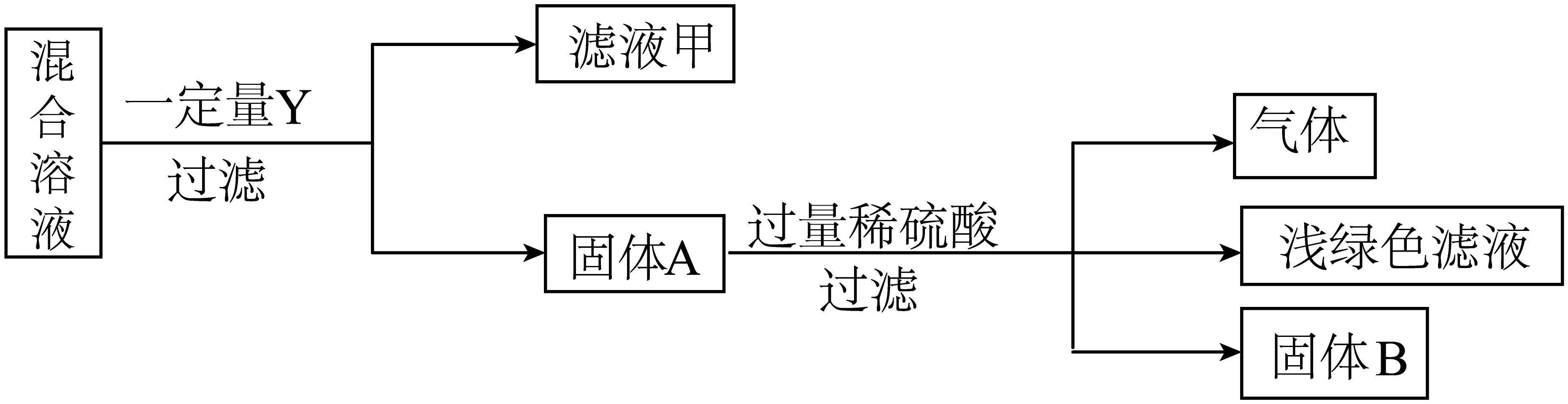
根据实验探究流程,回答下列问题:
①金属Fe、X、Y的活动性由强到弱的顺序是。
②固体A中所含成分可能有种情况。
③浅绿色滤液中 定含有的阳离子是。
四、计算题(本大题共1题,共4分)
-
23. 鸡蛋壳的主要成分为碳酸钙, 为测定鸡蛋壳中碳酸钙的含量,化学兴趣小组做了如下实验(假设鸡蛋壳中除碳酸钙外的其他成分都不溶于水,且不与稀盐酸反应)。
 (1)、产生二氧化碳的质量为;(2)、试计算鸡蛋壳中碳酸钙的质量分数(结果保留一位小数)。
(1)、产生二氧化碳的质量为;(2)、试计算鸡蛋壳中碳酸钙的质量分数(结果保留一位小数)。