贵州省铜仁市四校联考2023-2024学年九年级下学期3月月考化学试卷
试卷更新日期:2024-04-12 类型:月考试卷
一、选择题(本大题包括7个小题,每小题2分,共14分。每小题只有一个答案符合题目要求。)
-
1. 目前铜仁市正在积极创建全国文明城市。下列做法与助推文明城市建设不相符的是( )A、发展高耗能产业 B、积极植树造林 C、减少使用一次性塑料用品 D、分类回收垃圾2. 在配制稀硫酸并制备氢气的实验中,下列装置和实验操作正确并规范的是( )A、量取浓硫酸
 B、稀释浓硫酸
B、稀释浓硫酸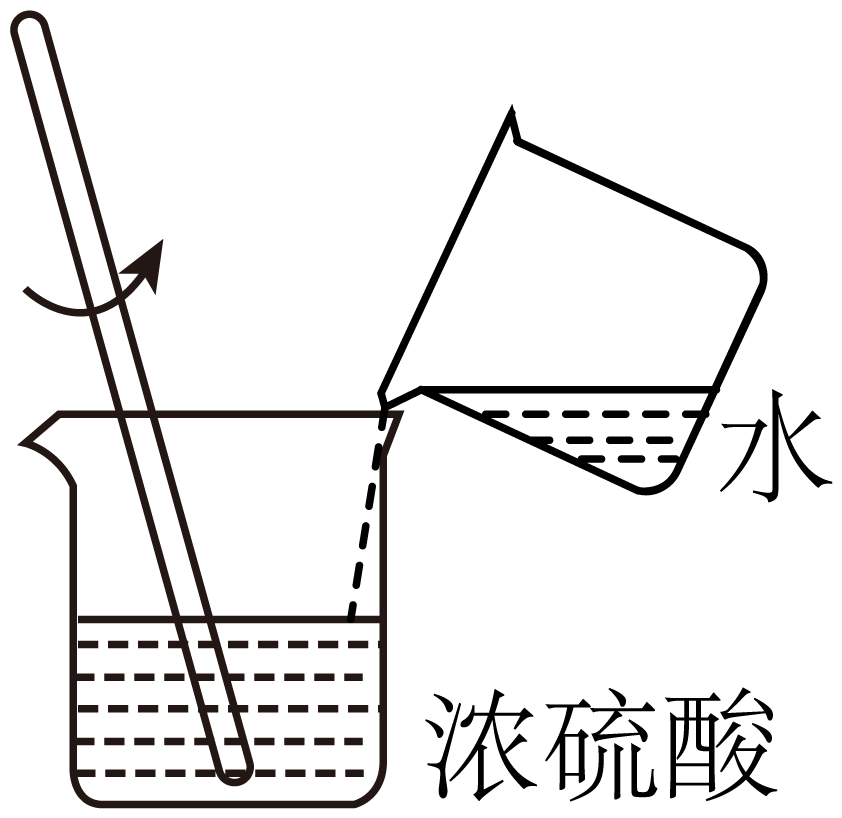 C、制取氢气
C、制取氢气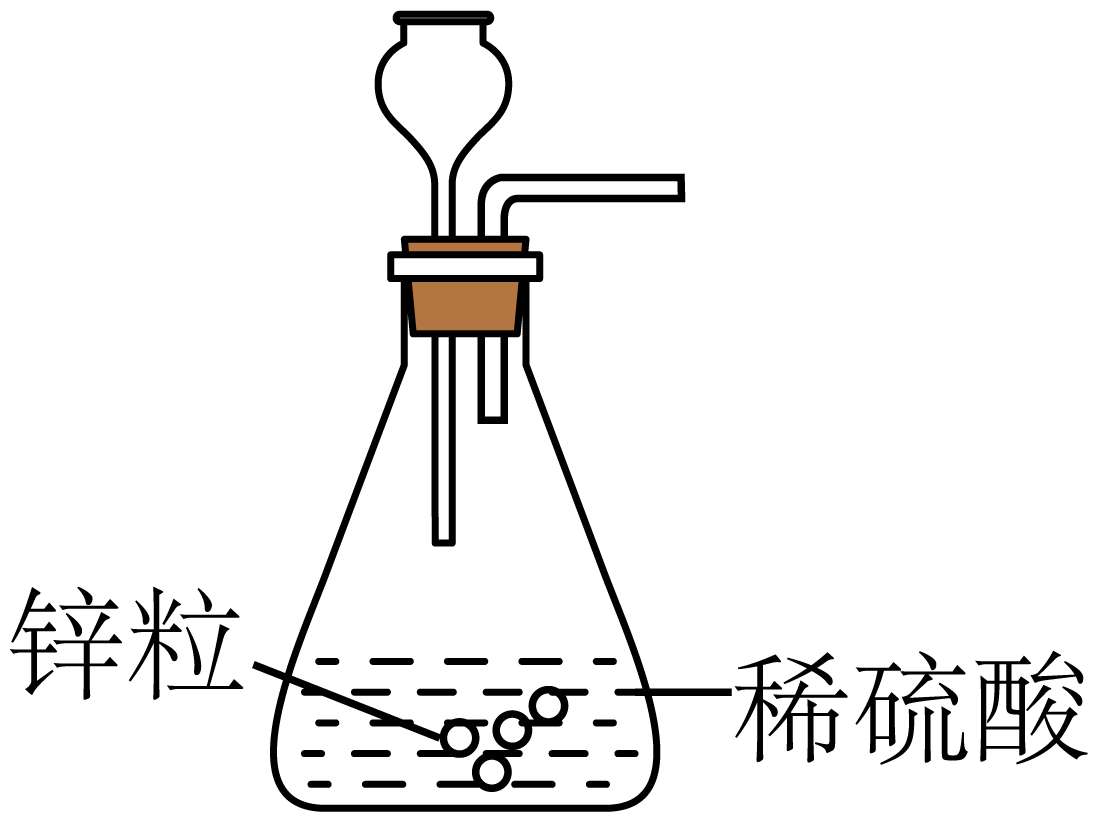 D、干燥氢气
D、干燥氢气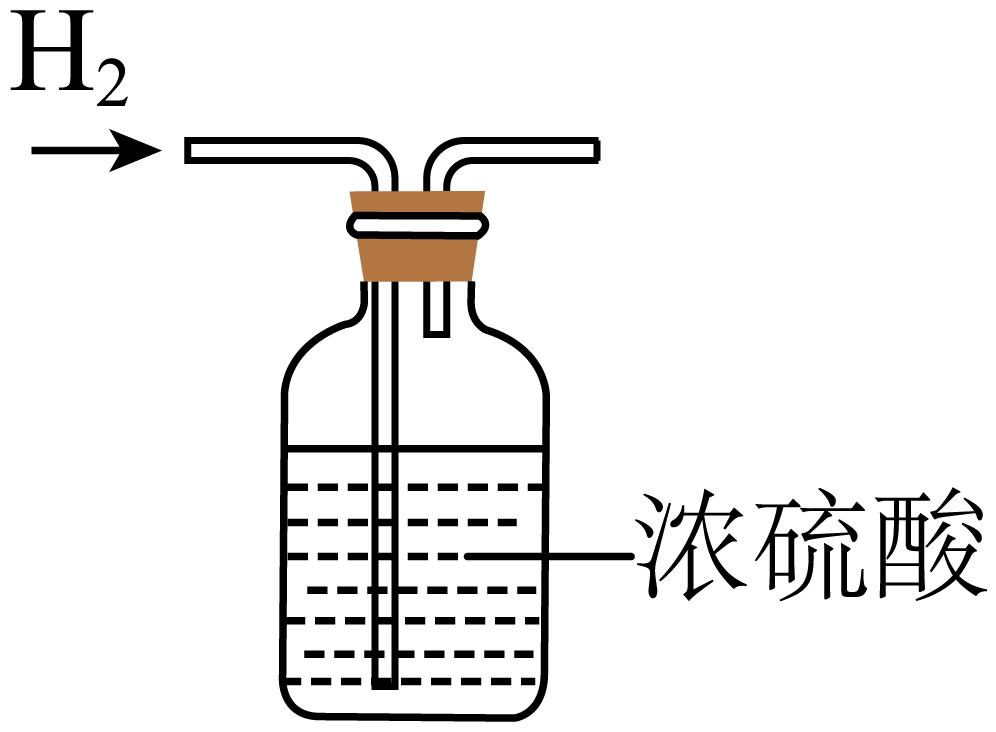 3. 分类是化学学习中常用的思维方法,下列有关物质分类正确的是( )A、单质:氧气、空气、食醋 B、碱:氢氧化钾、氢氧化钙、氢氧化铜 C、混合物:合金、冰水混合物、高锰酸钾 D、氧化物:二氧化碳、氧化铁、过氧化氢溶液4. 某管道疏通剂标签上的部分文字如图所示。下列说法正确的是( )
3. 分类是化学学习中常用的思维方法,下列有关物质分类正确的是( )A、单质:氧气、空气、食醋 B、碱:氢氧化钾、氢氧化钙、氢氧化铜 C、混合物:合金、冰水混合物、高锰酸钾 D、氧化物:二氧化碳、氧化铁、过氧化氢溶液4. 某管道疏通剂标签上的部分文字如图所示。下列说法正确的是( )品名:管道疏通剂
成分:氢氧化钠、铝粉、硝酸钠
注意事项:使用时要防明火
保存方法:密封
适用范围:毛发、残渣等淤积物
A、氢氧化钠中阴离子的符号为OH-2 B、氢氧化钠中含有一种金属元素 C、铝原子的结构示意图为 D、硝酸钠的化学式为NO3Na
5. 你经常做家庭小实验吗?根据你的经验,下列家庭小实验不能成功的是( )A、用食盐去除烧水壶中的水垢 B、用洗涤剂去除油污 C、用漏勺捞起饺子 D、把一只冷碟子放在蜡烛火焰上方,以获得少量炭黑6. N2是重要的化工原料,N2和H2反应的微观示意图如下,下列说法正确的是
D、硝酸钠的化学式为NO3Na
5. 你经常做家庭小实验吗?根据你的经验,下列家庭小实验不能成功的是( )A、用食盐去除烧水壶中的水垢 B、用洗涤剂去除油污 C、用漏勺捞起饺子 D、把一只冷碟子放在蜡烛火焰上方,以获得少量炭黑6. N2是重要的化工原料,N2和H2反应的微观示意图如下,下列说法正确的是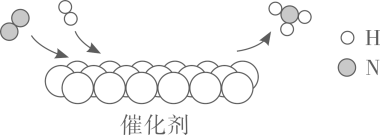 A、常温下N2的化学性质很活泼 B、
A、常温下N2的化学性质很活泼 B、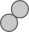 和
和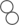 按个数比1:1进行该反应
C、
按个数比1:1进行该反应
C、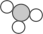 中N、H元素的质量比为1:3
D、反应前后分子种类和数目发生变化
7. 某同学对下列四个实验都分别设计了两种方案,其中两种方案均能达到实验目的的是( )
中N、H元素的质量比为1:3
D、反应前后分子种类和数目发生变化
7. 某同学对下列四个实验都分别设计了两种方案,其中两种方案均能达到实验目的的是( )序号
实验
方案一
方案二
A
除去CO2中的CO
点燃
通过灼热的炭层
B
除去CaO中的CaCO3
高温煅烧
加足量的稀盐酸
C
鉴别NaCl和NaOH固体
取等量的固体,加入等量同温的水,溶解,测温度变化
取等量固体于表面皿上,一段时间后观察固体表面是否潮解
D
鉴别CuO粉末和木炭粉
取样,观察颜色
取样,加入足量稀硫酸
A、A B、B C、C D、D二、非选择题:本题包括7个小题,共46分。
-
8. 2023年贵州铜仁●梵净山冬季马拉松充满着“化学元素”。(1)、此次比赛是一场绿色的运动盛会。比赛期间广泛使用氢能源车辆,氢气作为燃料的优点是(答一点即可);骑共享自行车(如图)属于低碳生活新时尚。下列做法不利于自行车防锈的是。

A.金属部件镀金属铬 B.链条涂防锈油
C.雨淋后自然晾干链条 D.车架喷油漆
(2)、铜仁市为马拉松选手及游客们准备了米豆腐、牛肉干、卷粉等特色小吃。餐后的食物残渣应投入印有标识的垃圾箱。____A、 B、
B、 C、
C、 D、
D、 (3)、比赛期间主办方还在各补给点提供了高品质安全直饮水和氧气瓶。该直饮水经过二氧化氯消毒,标出二氧化氯中氯元素的化合价;氧气可以用于急救是利用它的性质。(4)、赛道实现了5G网络的全覆盖。制造5G芯片的氮化镓(GaN)材料可由氯化镓(GaCl3)制取,镓离子的符号为。9. 构建宏观与微观意识,是学习化学的重要思想。(1)、水的组成:
(3)、比赛期间主办方还在各补给点提供了高品质安全直饮水和氧气瓶。该直饮水经过二氧化氯消毒,标出二氧化氯中氯元素的化合价;氧气可以用于急救是利用它的性质。(4)、赛道实现了5G网络的全覆盖。制造5G芯片的氮化镓(GaN)材料可由氯化镓(GaCl3)制取,镓离子的符号为。9. 构建宏观与微观意识,是学习化学的重要思想。(1)、水的组成:①如图1为电解水装置:b管气体是 。电解水的化学方程式为 。
②下列实验也能证明水是由氢元素和氧元素组成的是 (填字母)。
A.水的净化
B.氢气在氧气中燃烧
C.氢气与氧化铜反应
D.水的蒸发
(2)、未来“水能源”:科学家认为“氢能源将成为未来主要的能源”,由水获得氢被认为是未来制氢的方向。

①如图2中“光电转换”过程中,光能最终转化为能。
②请在如图3方框内补充相应的微粒。根据该示意图可知,化学反应的实质为。
10. 溶液与人类的生产、生活密切相关。(1)、厨房中的下列物质分别放入水中,能形成溶液的是 (填序号)。A、白糖 B、花生油 C、面粉(2)、如图为硝酸钾和氯化钠的溶解度曲线示意图。
①t1℃时,将40g硝酸钾加到100g水中,充分搅拌,形成溶液(填“饱和”或“不饱和”)。
②P点表示t1℃时,硝酸钾的溶解度氯化钠的溶解度(填“大于”、“等于”或“小于”)。
(3)、李红同学在实验室配制一定溶质质量分数的氯化钠溶液,在称量氯化钠时发现天平指针偏向左侧,此时她应该进行的操作是;想要让氯化钠固体快速溶解,你的办法是。(4)、20℃时,向40g溶质质量分数为20%的氯化钠溶液中加入68g水,若要得到该温度下氯化钠的饱和溶液,至少还需要再加入g氯化钠固体。(20℃时,氯化钠的溶解度为36g。)11. 金属材料的使用与生产、生活和社会发展密切相关。(1)、金属材料的冶炼。工业炼铁:首先是将焦炭变成一氧化碳,再利用一氧化碳的性和铁矿石反应,最终得到铁。焦炭也具有还原性,你认为工业上没有直接利用焦炭炼铁的原因是。
(2)、金属材料的使用和保护。铝制品具有良好耐腐蚀性的原因是(用化学方程式表示)。(3)、金属的化学性质。①乐在化中社团的同学想比较Mg、Fe、Cu的金属活动性,请你帮他们一起完成以下探究:
实验操作
实验现象
实验结论
镁表面产生大量气泡;铁表面;铜表面无明显变化
活动性:Mg>Fe>Cu
任写一个上述实验中发生的化学反应方程式
②将上述实验结束后的溶液倒入烧杯中,得到溶液A,取m克溶液A于烧杯中,加入一定量的镁粉充分反应后得到溶液B。若溶液B质量仍为m克,则溶液B中的溶质组合可能有。
12. 制备物质和探究物质的性质是初中学习化学的重要实验内容。如图是实验室制取气体的有关仪器和装置。 (1)、仪器①的名称是。(2)、用A装置制取氧气的化学方程式 , 基本反应类型是。用C装置收集氧气,验满时应将带火星的木条放在(填“a”或“b”)端。(3)、实验室制取二氧化碳的化学方程式 , 应选的发生装置是(填序号),将产生的气体从D装置的c端进入,观察到的现象是。(4)、用图E所示装置(夹持仪器已省略)完成了燃烧条件的探究。
(1)、仪器①的名称是。(2)、用A装置制取氧气的化学方程式 , 基本反应类型是。用C装置收集氧气,验满时应将带火星的木条放在(填“a”或“b”)端。(3)、实验室制取二氧化碳的化学方程式 , 应选的发生装置是(填序号),将产生的气体从D装置的c端进入,观察到的现象是。(4)、用图E所示装置(夹持仪器已省略)完成了燃烧条件的探究。已知:红磷着火点为240℃,白磷着火点为40℃。
①燃烧条件的探究:说明可燃物燃烧需要温度达到可燃物的着火点的现象是。
②空气中氧气含量的粗略测定:待火焰熄灭后,打开活塞,烧杯中的水进入封闭的W形玻璃管。若该实验测定的空气中氧气含量偏低,则可能的原因是(写一条)。
13. 为深入了解酸这类重要的物质,某化学小组以“研究硝酸(HNO3)的性质”为主题开展了以下项目式学习,请你和他们一起完成探究。(1)、【任务一】硝酸的物理性质
同学们通过查阅资料可知,纯硝酸为无色透明液体,有刺激性气味。浓硝酸中溶质质量分数通常为68%左右,无色透明,易挥发,在空气中产生白雾(与浓盐酸相同),浓硝酸敞口放置一段时间后,其溶质质量分数会(填“变大”、“不变”或“变小”),因此要保存。(2)、【任务二】硝酸的化学性质①不稳定性:浓、稀硝酸性质相差很大,如稀硝酸相对稳定,但浓硝酸不稳定,在光照或遇热会分解而放出二氧化氮、水和某助燃单质。请写出浓硝酸受热发生反应的化学方程式:。
②强酸性:稀硝酸和稀硫酸都具有酸的通性,是因为两种酸中都存在(写符号)。
③强氧化性:小组同学将紫色石蕊溶液滴到装有浓硝酸的试管中,发现石蕊溶液先变红后褪色。
(3)、【提出问题】石蕊溶液褪色的原因是什么呢?【猜想假设】
甲同学猜想:石蕊变质,你的猜想:。
(4)、【讨论与交流】同学们认为甲同学猜测不合理,理由是。
(5)、【实验设计与验证】为了验证自己的猜想是否正确,请你设计实验方案进行探究。
(6)、【反思评价】通过本次探究你对酸的新认识是。