广东省梅州市2024年中考模拟化学试题
试卷更新日期:2024-04-11 类型:中考模拟
一、选择题(15小题,45分)
-
1. 下列过程中只发生物理变化的是( )A、石灰石与稀盐酸
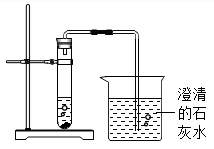 B、点燃蜡烛熄灭的白烟
B、点燃蜡烛熄灭的白烟 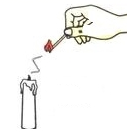 C、肥皂遇到硬水起浮渣
C、肥皂遇到硬水起浮渣  D、稀有气体通电发光
D、稀有气体通电发光  2. 日常生活中,用得最多的材料是有机合成材料。下列不属于有机合成材料的是( )A、合金 B、塑料 C、合成橡胶 D、合成纤维3. 下列图标中属于“回收标志”的是A、
2. 日常生活中,用得最多的材料是有机合成材料。下列不属于有机合成材料的是( )A、合金 B、塑料 C、合成橡胶 D、合成纤维3. 下列图标中属于“回收标志”的是A、 B、
B、 C、
C、 D、
D、 4. 进行化学实验必须注意安全,下列做法符合实际的是 ( )A、不慎将浓硫酸沾到皮肤上,应立即用水冲洗,再涂上硼酸溶液 B、氢氧化钠有强烈的腐蚀性,实验使用时,最好戴上防护眼镜 C、在实验室里可用品尝的办法区别食盐和蔗糖晶体 D、配制稀硫酸时,先在量筒中加入一定量的浓硫酸,再慢慢注入水搅拌5. 某科研团队发布消息洛匹那韦(化学式为C37H48N4O5)能对病毒有抑制效果,下列对于该物质的说法正确的是( )A、洛匹那韦属于混合物 B、洛匹那韦分子由碳、氢、氮、氧四种元素组成 C、洛匹那韦中氮、氧元素的质量比为7:10 D、洛匹那韦由碳原子、氢原子、氮原子和氧原子构成6. 关于实验现象的描述,不正确的是( )A、葡萄糖溶液与新制氢氧化铜混合加热至沸腾,会出现红色沉淀 B、打开浓盐酸的试剂瓶,瓶口会出现白烟 C、硫在氧气中燃烧,产生明亮的蓝紫色火焰 D、鸡蛋清溶液中加入浓硝酸,微热后出现黄色沉淀7. 下列对于宏观现象的微观解释中,错误的是( )A、金刚石和石墨物理性质差异很大,是因为原子排列方式不同 B、“酒香不怕巷子深”,说明了分子在不断运动 C、一氧化碳和二氧化碳具有不同的化学性质,是因为构成它们的分子不同 D、20mL水与20mL酒精混合后体积小于40mL,是因为分子数目减少8. 下图所示的四个实验中只发生物理变化是( )A、
4. 进行化学实验必须注意安全,下列做法符合实际的是 ( )A、不慎将浓硫酸沾到皮肤上,应立即用水冲洗,再涂上硼酸溶液 B、氢氧化钠有强烈的腐蚀性,实验使用时,最好戴上防护眼镜 C、在实验室里可用品尝的办法区别食盐和蔗糖晶体 D、配制稀硫酸时,先在量筒中加入一定量的浓硫酸,再慢慢注入水搅拌5. 某科研团队发布消息洛匹那韦(化学式为C37H48N4O5)能对病毒有抑制效果,下列对于该物质的说法正确的是( )A、洛匹那韦属于混合物 B、洛匹那韦分子由碳、氢、氮、氧四种元素组成 C、洛匹那韦中氮、氧元素的质量比为7:10 D、洛匹那韦由碳原子、氢原子、氮原子和氧原子构成6. 关于实验现象的描述,不正确的是( )A、葡萄糖溶液与新制氢氧化铜混合加热至沸腾,会出现红色沉淀 B、打开浓盐酸的试剂瓶,瓶口会出现白烟 C、硫在氧气中燃烧,产生明亮的蓝紫色火焰 D、鸡蛋清溶液中加入浓硝酸,微热后出现黄色沉淀7. 下列对于宏观现象的微观解释中,错误的是( )A、金刚石和石墨物理性质差异很大,是因为原子排列方式不同 B、“酒香不怕巷子深”,说明了分子在不断运动 C、一氧化碳和二氧化碳具有不同的化学性质,是因为构成它们的分子不同 D、20mL水与20mL酒精混合后体积小于40mL,是因为分子数目减少8. 下图所示的四个实验中只发生物理变化是( )A、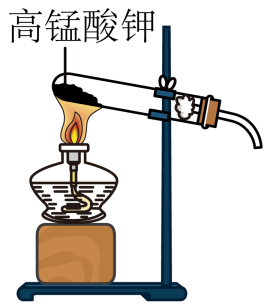 实验室制取氧气
B、
实验室制取氧气
B、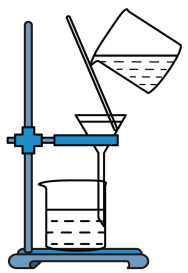 过滤液体
C、
过滤液体
C、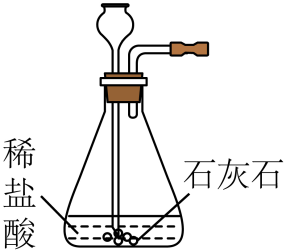 实验室制取二氧化碳
D、
实验室制取二氧化碳
D、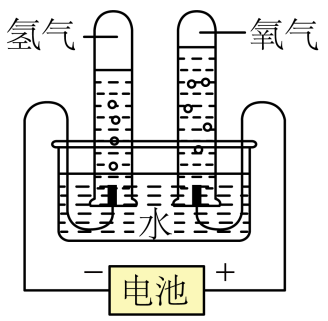 水的电解
9. 硒是人体必需的微量元素,严重缺硒有可能诱发皮肤疾病。已知硒的核电荷数为34,质子数与中子数之和为79。下列有关硒原子的说法中,不正确的是( )A、质子数为34 B、核外电子数为34 C、相对原子质量为79g D、中子数为4510. 下列图示实验操作中,正确的是( )A、
水的电解
9. 硒是人体必需的微量元素,严重缺硒有可能诱发皮肤疾病。已知硒的核电荷数为34,质子数与中子数之和为79。下列有关硒原子的说法中,不正确的是( )A、质子数为34 B、核外电子数为34 C、相对原子质量为79g D、中子数为4510. 下列图示实验操作中,正确的是( )A、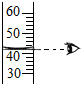 B、
B、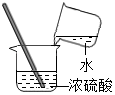 C、
C、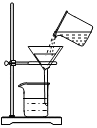 D、
D、 11. CCTV-2有一档节目《是真的吗?》。下列哪个选项是真的( )A、催化剂在化学反应中只能加快化学反应速率 B、所有原子的原子核内都有质子和中子 C、aL水和bL酒精混合后体积小于(a+b)L D、一种元素在同一种物质中表现出的化合价是唯一的12. 下图广口瓶里分别装入下列各组中的气体,滴管分别滴入各组中的液体时,玻璃管下端所系的气球能够鼓起来的是( )
11. CCTV-2有一档节目《是真的吗?》。下列哪个选项是真的( )A、催化剂在化学反应中只能加快化学反应速率 B、所有原子的原子核内都有质子和中子 C、aL水和bL酒精混合后体积小于(a+b)L D、一种元素在同一种物质中表现出的化合价是唯一的12. 下图广口瓶里分别装入下列各组中的气体,滴管分别滴入各组中的液体时,玻璃管下端所系的气球能够鼓起来的是( )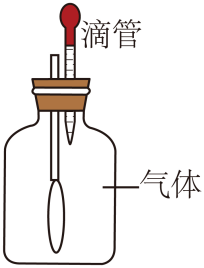 A、氢气、浓硫酸 B、氮气、苛性钠溶液 C、O2、水 D、CO2、烧碱溶液13. 溶液是一种重要的混合物,下列有关溶液的说法正确的是( )A、将食盐加入水中,所得溶液的质量与加入的食盐和水的总质量一定相等 B、洗涤剂能够洗涤油污是因为洗涤剂能够溶解油污 C、不饱和溶液通过降低温度一定能变成饱和溶液 D、25℃时,将某KNO3溶液蒸发10克水析出a克晶体,再蒸发10克水析出b克晶体,a与b的质量不一定相等14. 下列实验方案中,能达到实验目的的是( )
A、氢气、浓硫酸 B、氮气、苛性钠溶液 C、O2、水 D、CO2、烧碱溶液13. 溶液是一种重要的混合物,下列有关溶液的说法正确的是( )A、将食盐加入水中,所得溶液的质量与加入的食盐和水的总质量一定相等 B、洗涤剂能够洗涤油污是因为洗涤剂能够溶解油污 C、不饱和溶液通过降低温度一定能变成饱和溶液 D、25℃时,将某KNO3溶液蒸发10克水析出a克晶体,再蒸发10克水析出b克晶体,a与b的质量不一定相等14. 下列实验方案中,能达到实验目的的是( )选项
实验目的
实验方案
A
检验二氧化碳气体中含有少量的一氧化碳
用燃着的木条点燃
B
分离碳酸钠和氢氧化钠的固体混合物
加入适量氢氧化钙溶液,过滤
C
除去氯化钠固体中的少量碳酸钠
加入适量稀盐酸,充分反应后,蒸发
D
鉴别氯化钠溶液、氢氧化钠溶液和稀盐酸
各取少量溶液于试管中,分别滴加无色酚酞溶液,观察溶液颜色的变化
A、A B、B C、C D、D15. 下列实验不能达到实验目的是( )A、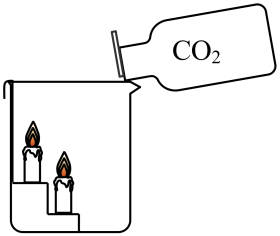 CO2的性质实验
B、
CO2的性质实验
B、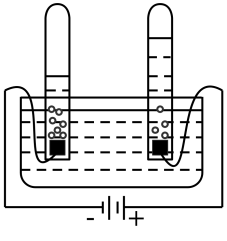 电解水实验
C、
电解水实验
C、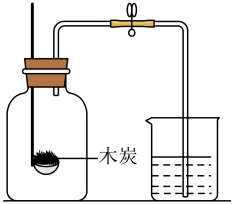 测定空气中氧气的含量
D、
测定空气中氧气的含量
D、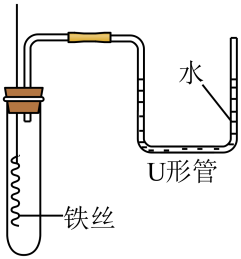 铁丝在空气中的变化
铁丝在空气中的变化
二、综合题(6小题,55分)
-
16. 稀土金属因其独特的性能而被誉为“新材料之母”。下图是钪在元素周期表的信息及其离子结构示意图。回答下列问题:
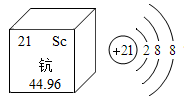 (1)、钪元素位于元素周期表的第周期,钪土(氧化钪)的相对分子质量为。(2)、钪的化学性质与铝相似,能与热水反应生成氢氧化钪和氢气,写出化学方程式。(3)、工业上用钪土与酸反应制备钪盐。请写出钪土与盐酸反应的化学方程式。17. 图1是KNO3和NaCl的溶解度曲线。回答下列问题:
(1)、钪元素位于元素周期表的第周期,钪土(氧化钪)的相对分子质量为。(2)、钪的化学性质与铝相似,能与热水反应生成氢氧化钪和氢气,写出化学方程式。(3)、工业上用钪土与酸反应制备钪盐。请写出钪土与盐酸反应的化学方程式。17. 图1是KNO3和NaCl的溶解度曲线。回答下列问题: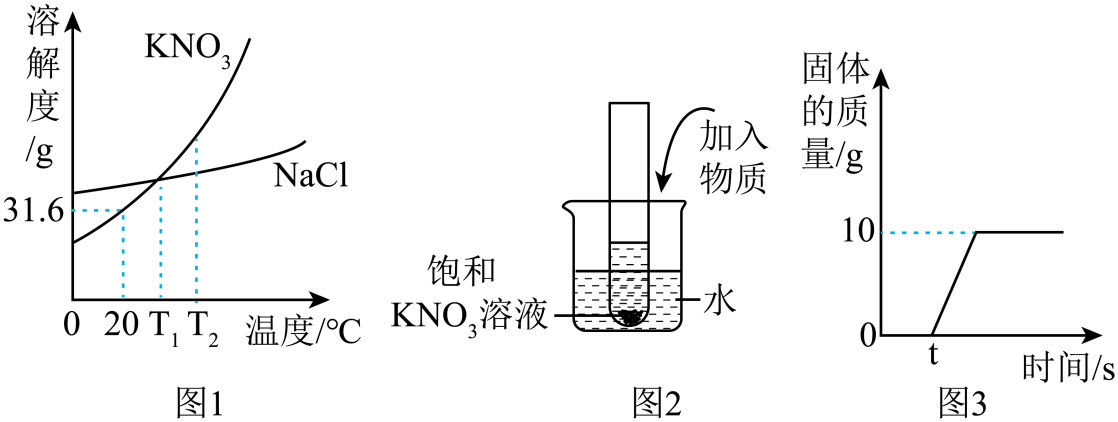 (1)、将T2℃时KNO3和NaCl的饱和溶液各100g,降温至T1℃,所得溶液的溶质质量分数:KNO3(填“>”、“<”或“=”)NaCl。(2)、图2试管底部有未溶解的KNO3固体,向烧杯的水中加入物质M后,试管中的固体增加,则加入的物质M可能是____(填字母)。A、氯化钠固体 B、氢氧化钠固体 C、冰块 D、生石灰(3)、60℃时,向装有100g水的烧杯中加入一定量KNO3形成溶液,再降温至20℃,析出固体的质量变化如图3。
(1)、将T2℃时KNO3和NaCl的饱和溶液各100g,降温至T1℃,所得溶液的溶质质量分数:KNO3(填“>”、“<”或“=”)NaCl。(2)、图2试管底部有未溶解的KNO3固体,向烧杯的水中加入物质M后,试管中的固体增加,则加入的物质M可能是____(填字母)。A、氯化钠固体 B、氢氧化钠固体 C、冰块 D、生石灰(3)、60℃时,向装有100g水的烧杯中加入一定量KNO3形成溶液,再降温至20℃,析出固体的质量变化如图3。①ts时,烧杯中的溶液为(填“饱和”或“不饱和”)溶液。
②60℃时,烧杯中溶液的质量为g。
18. 合理利用能源和保护环境是全世界所关注的问题。请回答下列相关问题。(1)、化石燃料造福人类的同时,也对环境造成了不良影响,如煤燃烧时排放出的(填一种即可)等污染物会导致酸雨。(2)、氢气是清洁燃料,氢气在空气中燃烧的化学方程式为。(3)、从“低碳经济”的角度分析,化石燃料、太阳能、风能等能源中,应尽量减少的使用。(4)、目前,很多家庭都已经使用了天然气作为燃料。为防止燃气泄漏造成危险,使用天然气的家庭报警器应安装在燃气灶附近墙壁的(填“上”或“下”)方。19. 【基础实验与跨学科实践】 (1)、实验室制氧气
(1)、实验室制氧气ⅰ.写出仪器a的名称:。
ⅱ.用高锰酸钾制取O2 , 应选择的发生装置为(填字母),该反应的化学方程式为。
ⅲ.如装置C所示,点燃沾有酒精的棉条,将其缓慢放入集满CO2的烧杯中,看到棉条上的火焰熄灭,再将其提起,棉条由上到下复燃。根据实验现象,说明燃烧的条件之一是。
(2)、电解水制氧气设计并制作电解水简易装置,如装置D所示,将铅笔芯作为电极是利用铅笔芯中石墨的性,接通电源后水中的两支铅笔芯电极附近的现象是。
(3)、光合作用制氧气向装置E的水中通入适量CO2 , 放在阳光下一段时间后,观察到水草表面有气泡产生,利用法收集到少量氧气(如装置E图所示),此时试管内的气体压强比外界大气压(填“大”“小”或“相等”)。
20. 请回忆你和老师共同完成的酸和碱反应的实验探究,并下列要求进行实验的设计与分析:(1)、请你依据下图设计一个酸和碱反应的探究实验:
实验步骤
实验现象
结论
①向烧杯中加入10mL氢氧化钠溶液,并滴入几滴酚酞溶液;
②再用滴管慢慢滴入稀硫酸,并不断搅拌溶液。
①溶液颜色;
②不断搅拌溶液至溶液颜色恰好变成色为止。
酸和碱发生了中和反应,该反应属四种基本反应类型中的反应。
(2)、我选取BaCl2、酚酞、紫色石蕊三种溶液设计实验,分别探究上述酸、碱反应后烧杯中的硫酸是否过量,请你根据下表帮我判断正确的实验方案及分析方案错误的原因:实验方案
实验步骤
实验现象
实验结论
方案一
取样,滴入适量的氯化钡溶液
出现白色沉淀
硫酸过量
方案二
取样,滴入几滴无色酚酞溶液
酚酞溶液不变色
酸、碱恰好反应
方案三
取样,滴入几滴紫色石蕊溶液
溶液变红
硫酸过量
①设计的三个方案中,有一个正确的方案是:方案。
②请分析另外两个方案,错误的原因:
一个方案错误的原因是:;
另一个方案错误的原因是:。
21. 用下列实验探究镁的性质。(1)、实验一:将打磨后的镁条插入装有空气的集气瓶中做燃烧的实验时,生成的白色固体中有少许淡黄色固体。
生成白色固体的反应符号表达式为。(2)、针对淡黄色固体,提出猜想:镁能与N2反应生成淡黄色的氮化镁固体。将1.44g镁在N2中充分燃烧,生成淡黄色固体2.00g。氮化镁的化学式为。但在空气中燃烧镁条时很难观察到生成物中有淡黄色固体,原因是。
(3)、实验二:2.4g镁条与足量稀盐酸的反应,充分反应后,将所得溶液蒸发,实验装置如下图所示。
实验甲中看见大量气泡迅速冒出,用燃着的木条检验听到尖锐的爆鸣声,则该气体为。
(4)、将实验甲得到的溶液进行实验乙,若得到固体为MgCl2 , 该固体质量是g , 实验甲中反应的符号表达式为。(5)、拓展延伸:在实验乙将溶液蒸干的过程中MgCl2会转变为MgO,蒸干后得到固体为MgCl2和MgO的混合物6.75g,该混合物中MgCl2和MgO的质量之比为。