2024年中考化学二轮专题复习-燃料及其利用
试卷更新日期:2024-04-06 类型:二轮复习
一、选择题
-
1. 下列处理事故的方法中正确的是( )A、发现煤气泄漏,立即拨打电话119 B、档案材料着火,用液体二氧化碳扑灭 C、室内起火,迅速打开所有门窗通风 D、高层楼房失火时,要乘电梯迅速撤离2. 6月5日是“世界环境日”。有关能源的开发和利用不合理的是( )A、氢能是理想的新型能源,它有资源丰富、燃烧放热多、产物不污染环境等优点 B、开采出来的石油应该经过加工后再综合利用 C、开发和利用太阳能、水能、风能等能源 D、煤、石油、天然气等化石燃料为不可再生能源,应禁止使用3. 纳米铁粉在空气中稍加热即可剧烈燃烧并生成黑色固体,如图是纳米铁粉在锥形瓶中燃烧的实验。下列说法不正确的是( )
 A、纳米铁粉燃烧的产物可能是Fe3O4 B、激光手电照射为反应提供热量而达到纳米铁粉的着火点 C、实验过程中气球先膨胀后不变 D、水的作用是避免高温熔化物溅落炸裂瓶底4. 劳动教育贯穿义务教育阶段,以下劳动项目与所涉及的化学知识不相符的是( )
A、纳米铁粉燃烧的产物可能是Fe3O4 B、激光手电照射为反应提供热量而达到纳米铁粉的着火点 C、实验过程中气球先膨胀后不变 D、水的作用是避免高温熔化物溅落炸裂瓶底4. 劳动教育贯穿义务教育阶段,以下劳动项目与所涉及的化学知识不相符的是( )选项
劳动项目
涉及到的化学知识
A
使用煤炉时,用扇子往炉中扇风
空气流通,提供充足的氧气
B
用布擦干淋湿的自行车
铁在潮湿空气中容易生锈
C
用铅笔芯作简易电池的电极材料
铅笔芯具有导电性
D
用明矾处理浑浊的天然水
明矾主要起杀菌消毒的作用
A、A B、B C、C D、D5. 为了达到相应的实验目的,下列实验设计不合理的是( )A
B
C
D




探究不同催化剂对H2O2分解的催化效果
探究铁、镁金属活动性强弱
除去 CO中混有的少量CO2
探究可燃物燃烧与着火点的关系
A、A B、B C、C D、D6. 根据下列实验方案进行实验,不能达到相应实验目的的是( )A、比较Al、Cu、Ag的金属活动性强弱 B、测定空气里氧气的含量
B、测定空气里氧气的含量 C、探究铁钉锈蚀的条件
C、探究铁钉锈蚀的条件 D、探究物质燃烧的三个条件
D、探究物质燃烧的三个条件 7. 通过下列图示实验得出的结论中,正确的是( )
7. 通过下列图示实验得出的结论中,正确的是( )①
 ②
② 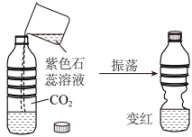 ③
③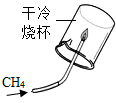 ④
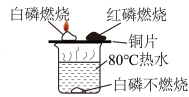
④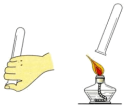 A、实验①条件下红磷不燃烧,说明红磷不是可燃物 B、实验②说明二氧化碳能使石蕊溶液变红 C、实验③实验后干冷烧杯壁出现水珠,可证明甲烷由氢元素和碳元素组成 D、实验④可用于检验氢气的纯度8. 魅力化学,魅力实验。下列实验现象描述正确的是( )
A、实验①条件下红磷不燃烧,说明红磷不是可燃物 B、实验②说明二氧化碳能使石蕊溶液变红 C、实验③实验后干冷烧杯壁出现水珠,可证明甲烷由氢元素和碳元素组成 D、实验④可用于检验氢气的纯度8. 魅力化学,魅力实验。下列实验现象描述正确的是( )


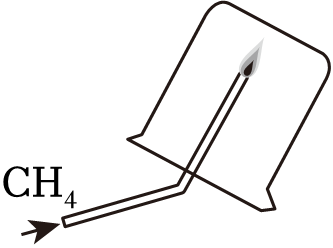
A.硫在空气中燃烧:发出蓝紫色火焰,放热
B.加热通入足量二氧化碳后的石蕊溶液:溶液由红色变为紫色
C.镁带在空气中燃烧:发出耀眼白光,产生白色烟雾
D.甲烷在空气中燃烧:发出淡蓝色火焰
A、A B、B C、C D、D9. 化学教科书上有8个“基础实验”,以下叙述正确的是( )A、“一定溶质质量分数的氯化钠溶液的配制”实验中,称量时氯化钠放在托盘天平的右盘 B、“氧气的制取与性质”实验中,做铁丝燃烧实验的集气瓶内要预留少量水 C、“燃烧的条件”实验中,一小片乒乓器碎片酒精灯火焰上加热,发现不能燃烧 D、“金属的物理性质和某些化学性质”实验中,铜片在酒精灯火焰上加热,表面变黄色10. 为了预防火灾发生,我们应当了解燃烧与灭火的相关知识,下列说法错误的是( )A、增大氧气浓度可以促进可燃物燃烧 B、酒精灯不慎打翻起火可用湿抹布扑灭 C、在加油站使用手机可能引发燃烧、爆炸 D、电线着火用水扑灭11. 对铁生锈与燃烧条件的实验探究如图所示。下列说法正确的是( ) A、对比①②可探究:接触氧气是否为铁生锈的条件之一 B、对比②③可探究:接触水是否为铁生锈的条件之一 C、对比①④可探究:温度达到着火点是否为铁燃烧的条件之一 D、对比③④可探究:接触氧气是否为铁燃烧的条件之一12. 如图所示,加热烧瓶中的水使之沸腾。水蒸气从铜管喷出,此时将火柴靠近管口处,再迅速移开火柴,火柴立即燃烧。下列说法错误的是( )
A、对比①②可探究:接触氧气是否为铁生锈的条件之一 B、对比②③可探究:接触水是否为铁生锈的条件之一 C、对比①④可探究:温度达到着火点是否为铁燃烧的条件之一 D、对比③④可探究:接触氧气是否为铁燃烧的条件之一12. 如图所示,加热烧瓶中的水使之沸腾。水蒸气从铜管喷出,此时将火柴靠近管口处,再迅速移开火柴,火柴立即燃烧。下列说法错误的是( )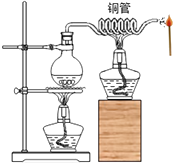 A、水沸腾时,水分子质量和体积都增大 B、管口处水蒸气的作用是使火柴温度达到着火点 C、火柴移离水蒸气,与氧气充分接触,从而燃烧 D、火柴完全燃烧的产物含有二氧化碳和水等13. 用如图所示装置探究燃烧的条件。有关该实验的说法正确的是( )
A、水沸腾时,水分子质量和体积都增大 B、管口处水蒸气的作用是使火柴温度达到着火点 C、火柴移离水蒸气,与氧气充分接触,从而燃烧 D、火柴完全燃烧的产物含有二氧化碳和水等13. 用如图所示装置探究燃烧的条件。有关该实验的说法正确的是( )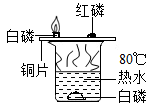 A、热水的作用只是提供热量 B、温度达到可燃物的着火点,可燃物就会燃烧 C、铜片上的红磷燃烧,产生大量的白烟 D、向水中白磷通氧气,白磷会燃烧14. 推理是化学学习中常用的思维方法。下列推理正确的是( )A、分子可以构成物质,所以物质都由分子构成 B、燃烧过程中伴随着发光放热,所以有发光放热现象的变化都是燃烧 C、催化剂在化学反应前后质量不变,所以反应前后质量不变的物质都是催化剂 D、单质只含一种元素,所以只含一种元素的纯净物都是单质15. 一种新型绿色电池——燃料电池,是把H2、CO、CH4和空气不断输入,直接氧化,使化学能转变成电能,被称为21世纪的“绿色”发电站。这三种气体可以作为燃料的原因是( )A、都是无毒无害的气体 B、都可以燃烧并放出大量的热 C、燃烧产物均为二氧化碳和水 D、均在自然界大量存在16. 机制炭(如图)常用作烧烤燃料,引燃它可以使用固体酒精,盖灭炭火可以使用燃烧后产生的炭灰。下列说法错误的是( )
A、热水的作用只是提供热量 B、温度达到可燃物的着火点,可燃物就会燃烧 C、铜片上的红磷燃烧,产生大量的白烟 D、向水中白磷通氧气,白磷会燃烧14. 推理是化学学习中常用的思维方法。下列推理正确的是( )A、分子可以构成物质,所以物质都由分子构成 B、燃烧过程中伴随着发光放热,所以有发光放热现象的变化都是燃烧 C、催化剂在化学反应前后质量不变,所以反应前后质量不变的物质都是催化剂 D、单质只含一种元素,所以只含一种元素的纯净物都是单质15. 一种新型绿色电池——燃料电池,是把H2、CO、CH4和空气不断输入,直接氧化,使化学能转变成电能,被称为21世纪的“绿色”发电站。这三种气体可以作为燃料的原因是( )A、都是无毒无害的气体 B、都可以燃烧并放出大量的热 C、燃烧产物均为二氧化碳和水 D、均在自然界大量存在16. 机制炭(如图)常用作烧烤燃料,引燃它可以使用固体酒精,盖灭炭火可以使用燃烧后产生的炭灰。下列说法错误的是( ) A、机制炭做成空心增大了与空气的接触面积 B、炭灰可以盖灭炭火是因为隔绝了空气 C、烧烤应该在空气流通的地方进行 D、酒精的燃烧是为了升高机制炭的着火点17. 以科学原理和事实为依据进行推理是学习化学的一种重要方法。下列推理合理的是( )A、催化剂的质量在化学反应前后不变,则在化学反应前后质量不变的物质一定是催化剂 B、某物质在氧气中燃烧生成二氧化碳和水,则该物质一定含有碳、氢、氧元素 C、中和反应生成了盐和水,所以能生成盐和水的反应一定是中和反应 D、点燃氢气之前需要验纯,所以点燃甲烷之前也同样需要验纯18. 如图所示,实验方案设计能达到实验目的的是A、探究MnO2可以做H2O2溶液反应的催化剂
A、机制炭做成空心增大了与空气的接触面积 B、炭灰可以盖灭炭火是因为隔绝了空气 C、烧烤应该在空气流通的地方进行 D、酒精的燃烧是为了升高机制炭的着火点17. 以科学原理和事实为依据进行推理是学习化学的一种重要方法。下列推理合理的是( )A、催化剂的质量在化学反应前后不变,则在化学反应前后质量不变的物质一定是催化剂 B、某物质在氧气中燃烧生成二氧化碳和水,则该物质一定含有碳、氢、氧元素 C、中和反应生成了盐和水,所以能生成盐和水的反应一定是中和反应 D、点燃氢气之前需要验纯,所以点燃甲烷之前也同样需要验纯18. 如图所示,实验方案设计能达到实验目的的是A、探究MnO2可以做H2O2溶液反应的催化剂 B、探究面粉在一定条件下能爆炸
B、探究面粉在一定条件下能爆炸 C、探究质量守恒定律
C、探究质量守恒定律 D、探究用锌粒和稀盐酸制取氢气
D、探究用锌粒和稀盐酸制取氢气 19. 小明将纸条分别紧紧卷在木棒和铁棒上,加热纸条(如图),木棒上的纸条立即燃烧,而铁棒上的纸条不会立即燃烧。据此推测木棒和铁棒具有不同的( )
19. 小明将纸条分别紧紧卷在木棒和铁棒上,加热纸条(如图),木棒上的纸条立即燃烧,而铁棒上的纸条不会立即燃烧。据此推测木棒和铁棒具有不同的( ) A、密度 B、导热性 C、硬度 D、延展性20. 蜡烛(足量)在如图甲所示盛有空气的密闭装置内燃烧至熄灭,用仪器测出这一过程中瓶内氧气含量的变化,如图乙所示。下列判断不正确的是( )
A、密度 B、导热性 C、硬度 D、延展性20. 蜡烛(足量)在如图甲所示盛有空气的密闭装置内燃烧至熄灭,用仪器测出这一过程中瓶内氧气含量的变化,如图乙所示。下列判断不正确的是( ) A、蜡烛燃烧火焰分三层其中外焰温度最高 B、氧气浓度小于一定值时,蜡烛无法燃烧 C、实验后向装置内倒入澄清石灰水,澄清石灰水变浑浊 D、蜡烛熄灭后,瓶内二氧化碳气体的体积分数为84.04%
A、蜡烛燃烧火焰分三层其中外焰温度最高 B、氧气浓度小于一定值时,蜡烛无法燃烧 C、实验后向装置内倒入澄清石灰水,澄清石灰水变浑浊 D、蜡烛熄灭后,瓶内二氧化碳气体的体积分数为84.04%二、填空题
-
21. 化学源于生活,生活中处处存在着化学知识,请回答下列问题。(1)、中国馆屋顶采用了暴露在阳光下便会产生电的光伏板,产生的电能可以供给馆内运营使用,光伏板将能转化为电能。生产光伏板需用高纯硅,构成硅的粒子是填粒子名称。屋顶还设置了雨水收集系统,请你从爱护水资源方面说说这样做的目的是。(2)、市场上常用的净水器中一般含有活性炭,其作用是。(3)、下列生活现象中属于缓慢氧化的是____填字母序号A、动植物呼吸 B、点燃鞭炮 C、木材燃烧 D、大白菜腐烂22. 诗人陆游的笔记中记载“书灯勿用铜盏,想瓷盏最省油,蜀中有夹瓷盏…可省油之半”“一端作小窍,注清冷水于其中,每夕一易之”,夹瓷盏被称为省油灯,用棉绳做炷(灯芯),上层盏盛油,下层盏盛水。其结构示意图如图。
 (1)、图中属于可燃物的是和 , 这是燃烧的个条件之一。(2)、省油灯的原理是:油燃烧 , 上层内盏油温 , 下层盏内水吸热,减少油的 , 以达到省油的目的。(3)、“注清冷水于其中,每夕一易之”说明下层盏中的水不断减少。对该现象的微观解释正确的是(多选,填字母序号)。
(1)、图中属于可燃物的是和 , 这是燃烧的个条件之一。(2)、省油灯的原理是:油燃烧 , 上层内盏油温 , 下层盏内水吸热,减少油的 , 以达到省油的目的。(3)、“注清冷水于其中,每夕一易之”说明下层盏中的水不断减少。对该现象的微观解释正确的是(多选,填字母序号)。a.水分子受热分解 b.水分子不断运动
c.水分子间隔变大 d.水分子数目减少
23. 同学们学习了燃烧与灭火后,在实验室设计并完成了如下实验,以探究灭火的原理。实验方法:点燃3 支蜡烛,在其中一支蜡烛上扣一个烧杯如图Ⅰ; 将另两支蜡烛分别放在两个烧杯中,然后向一个烧杯中加入适量碳酸钠和盐酸如图Ⅲ。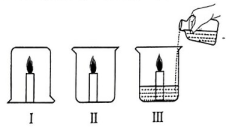 (1)、 实验原理:Ⅲ中反应的化学方程式为。(2)、实验现象:Ⅱ中蜡烛正常燃烧,Ⅰ和Ⅲ中蜡烛熄灭,Ⅲ中的现象还有。(3)、 实验后,接下来必须要做的事情是 , 完善实验报告,离开实验室。(4)、 问题与交流:Ⅲ中的操作,可能造成的结果是。24. 用如图所示装置可以完成以下实验一和实验二。
(1)、 实验原理:Ⅲ中反应的化学方程式为。(2)、实验现象:Ⅱ中蜡烛正常燃烧,Ⅰ和Ⅲ中蜡烛熄灭,Ⅲ中的现象还有。(3)、 实验后,接下来必须要做的事情是 , 完善实验报告,离开实验室。(4)、 问题与交流:Ⅲ中的操作,可能造成的结果是。24. 用如图所示装置可以完成以下实验一和实验二。
实验一:探究燃烧条件,B处盛放木炭,实验步骤如下:
步骤Ⅰ.先在A处通入N2一段时间后,点燃酒精灯,观察现象;
步骤Ⅱ. .
步骤Ⅲ.在A处通入O2一段时间,观察现象;
步骤Ⅳ.在A处继续通入O2 , 点燃酒精灯,观察现象。
实验二:探究CO的性质,B处盛放氧化铜粉末。从A处通人CO一段时间后,点燃酒精灯。下列说法中正确的是
①实验一中,步骤Ⅱ的操作是熄灭酒精灯,待B冷却至室温;
②实验一中,步骤Ⅰ与Ⅲ对比,说明燃烧需要可燃物与氧气接触;
③实验二中,步骤Ⅳ观察到的现象是:木炭燃烧放热、发红光,C中澄清石灰水变浑浊;
④实验二中,玻璃管中固体减少的质量等于C中增加的质量;
⑤实验二中,实验结束时需要先熄灭酒精灯再继续通CO,以防止氧气进人使灼热的铜再次被氧化;
⑥实验二中,观察到C中澄清石灰水变浑浊即可证明CO与CuO发生了反应。
25. 3月25日国家重点研发项目固态氢能发电并网率先在广州和昆明同时实现,这也是我国首次将光伏发电制成固态氢能应用于电力系统。(1)、将光伏,风力发出的电用于电解水制氢。电解水的化学方程式为。(2)、氢能使用受到制约的困难之一是储存难,氢化钙(CaH2)是一种固态储氢材料.氢化钙中钙元素为+2价,则氢元素的化合价为。(3)、氢能源与煤炭等能源相比,具有的显著优势是(任写一点)。三、综合题
-
26. 氢能作为一种高效、清洁的可再生能源具有良好的发展前景。根据制备方式及制备过程中碳排放量的不同,氢能分为“灰氢”“蓝氢”和“绿氢”。图1是炼厂制氢技术碳排放及制氢成本关系图(CNY:Chinese Yuanf的缩写,即人民币),图2是在光照条件下,使用C3N4/CQDS复合催化剂可水转化为氢气的微观示意图。
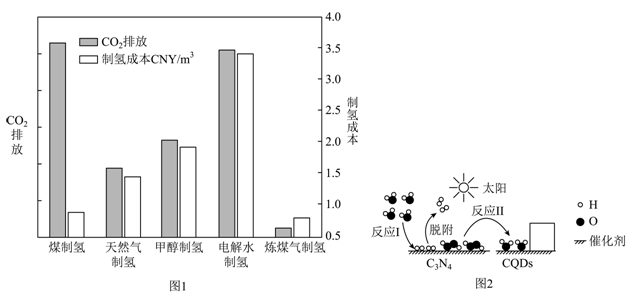 (1)、“灰氢”:由化石能源制取氢气,制氢过程排放二氧化碳等温室气体。
(1)、“灰氢”:由化石能源制取氢气,制氢过程排放二氧化碳等温室气体。①“灰氢”制取过程中,会导致的环境问题是。
②结合图1分析,电解水制氢尚未普及的主要原因是。
(2)、“蓝氢”:由化石能源制氢气,用碳捕获与封存技术减少二氧化碳排放。工业上碳捕获通常利用一定的CaO吸附CO2。①使用纳米CaO的吸附效果优于微米CaO的原因是。
②碳捕获所得高浓度的二氧化碳可用于(举一例用途)。
(3)、“绿氢”:由核能、可再生能源分解水获得氢气,制氢过程没有排放温室气体。①反应1、II前后没有改变的粒子是(写化学符号)。写出图中方框内粒子的化学式:。
②反应Ⅱ的化学方程式为。
27. 随着工业生产的高速发展和人们生活水平的提高,排入大气中的CO2越来越多,导致温室效应增强。碳替代、碳减排、碳封存、碳循环是实现碳中和的4种主要途径。科学家预测,到2050年,4种途径对全球碳中和的贡献率如图1。CO2的吸收是碳封存的首要环节,常选用NaOH、氨水、一乙醇胺等作吸收剂。在研究膜吸收法吸收CO2时,研究人员通过实验比较了一乙醇胺、二乙醇胺、氨基乙酸钾3种吸收剂对烟气中CO2的脱除效果,其结果如图2。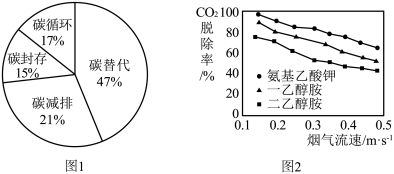
依据上文,回答下列问题:
(1)、排入大气中的CO2越来越多,导致效应增强。自然界吸收CO2的主要途径是作用。(2)、由图1可知,到2050年,对全球碳中和贡献率最大的途径是 。(3)、碳封存时常用NaOH溶液吸收二氧化碳,反应生成碳酸钠和水,该反应的化学方程式为 。(4)、碳替代指用新能源代替化石能源,目前人类可开发和利用的新能源有(写一种即可)。(5)、对比图2中三条曲线可知当烟气流速相同时,对烟气中CO2的脱除效果最好的是。(6)、下列做法不符合低碳生活理念的是____。(填序号)A、乘坐公共交通替代私家车出行 B、双面打印纸质资料 C、关注个人卫生,使用一次性筷子 D、夏季空调温度不低于26℃四、实验探究题
-
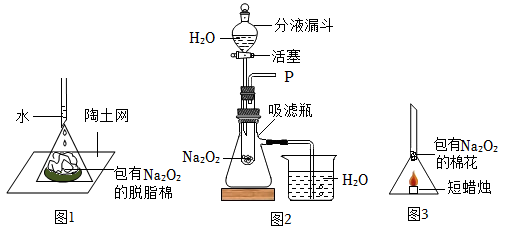
28. 元旦联欢会上,化学老师给同学们表演了一个“水能生火”的魔术(如图1所示),他将包有过氧化钠(Na2O2)粉末的棉花放在陶土网上,向棉花上滴了几滴水,棉花立刻燃烧了起来,同学们产生了浓厚的兴趣,为什么棉花会燃烧起来呢?
【提出猜想】
(1)、a.小明认为过氧化钠(Na2O2)与水反应时放出了热量。b.小刚又根据燃烧的条件,对小明的猜想进行了补充:。
(2)、【实验与分析】同学们设计了图2的实验装置。打开分液漏斗的活塞,控制水滴加的速度,看到试管中有气泡产生,将带火星的木条靠近P出口,观察到带火星的木条复燃,证明小刚的猜想正确。
实验中还观察到烧杯中的现象是。
(3)、完成了以上实验,老师介绍该反应的产物一共有两种,于是同学们又展开了进一步的探究,继续探究反应后生成的另一种物质。请你回答:另一种产物必含的元素是(写元素符号)。(4)、【老师介绍】过氧化钠不仅可以和水发生反应,也可以和二氧化碳反应生成碳酸钠固体和氧气,写出与二氧化碳反应的化学方程式:。因此,过氧化钠经常被用于潜水艇和防毒面具中提供氧气。
(5)、【补充实验】明确了以上性质,小芳又设计了一个实验(如图3)。
将一团包有过氧化钠的棉花塞到漏斗的管中,漏斗下方点燃一支短蜡烛(蜡烛火焰与棉花不接触)。一段时间后棉花能燃烧。这主要是因为蜡烛燃烧生成能与过氧化钠(Na2O2)反应的物质 , 同时反应放热。
(6)、【实验反思】①结合上述实验事实,你对于保存过氧化钠固体提出的安全建议是。
②若Na2O2着火,(填“能”或“不能”)用CO2灭火。
29. 秆用于制沼气可以解决农村的燃料短缺问题,助力美丽乡村建设。沼气的主要成分是CH4 , 可能含有CO2、CO。小涵与小明采集了某沼气池中的气体样品,探究该沼气中是否含有CO2和CO。【查阅资料】 ①CH4+4CuO4Cu+CO2+2H2O;CuO+COCu+CO2
②氢氧化钠溶液能够吸收CO2,浓硫酸能够吸收水。
【设计实验】小明与小涵设计并进行了如图所示实验(装置气密性良好,忽略装置内空气中的水蒸气)。

【实验分析】
(1)、 实验前要先通一会儿气体样品,然后再点燃D处的酒精灯,其目的是排尽装置内的空气,从安全角度看可以。(2)、 【定性分析】观察到装置 A 中的澄清石灰水变浑浊,小明认为沼气中含有 , 请写出装置A 中发生的化学方程式:。
(3)、 观察到装置 D 中的黑色固体变红,小涵认为沼气中含有 CO,小明经分析认为小涵的结论不严谨,理由是。(4)、【定量分析】小涵想通过装置D中固体减少的质量(即参加反应的CuO中氧元素的质量)和装置E增加的质量来判断混合气体中是否含有CO。反应结束后,测得装置D中固体减少的质量是a,装置E增加的质量是b。经分析沼气中含有CO,则a与b之间满足数学关系为 。
(5)、【问题解决】上述装置中气球的作用是。
五、计算题
-
30. 凤凰县家用化石燃料的使用,经历了如下图所示的过程,括号中的物质是对应燃料的主要成分。
 (1)、我国的“西气东输”工程中的“气”指的是(2)、天然气、沼气的主要成分均为甲烷(CH4),完全燃烧16kg的甲烷,可产生多少二氧化碳?(温馨提示:CH4+2O2CO2+2H2O)
(1)、我国的“西气东输”工程中的“气”指的是(2)、天然气、沼气的主要成分均为甲烷(CH4),完全燃烧16kg的甲烷,可产生多少二氧化碳?(温馨提示:CH4+2O2CO2+2H2O)