2024年中考化学二轮专题复习-水与常见的溶液
试卷更新日期:2024-04-01 类型:二轮复习
一、选择题
-
1. 2023年3月22日是第三十一届“世界水日”,主题为“ 加速发展”下列关于水的说法正确的是( )A、活性炭能使海水转化为淡水 B、硬水和软水可用食盐水来区分 C、农业上大力普及喷灌、滴灌等节水灌溉技术 D、将喷头洗浴改为浴缸泡浴2. 下列关于水的说法中,正确的是( )A、自然界的淡水资源很丰富,不需要节约用水 B、水变成水蒸气的过程中水分子体积变大 C、电解水实验中得到的氧气和氢气的体积比约为1:2 D、氢气燃烧生成水的实验,说明水是由氢气、氧气组成的3. 水对于生命活动、工农业生产具有重要意义。下列有关水的说法错误的是( )A、尽量缩短用水时间,随手关闭水龙头 B、为节约经济成本,工厂将污水直接排到河的下游 C、组织志愿者进行爱水护河环保活动,及时清理河道垃圾 D、农业上采用喷灌和滴灌可以节约用水4. 下列属于乳化现象的是( )A、碘溶于酒精中 B、用汽油洗去机器上的油污 C、用洗洁精洗去碗上的油污 D、用水洗去衣服上的污渍5. 不同温度下KNO3的溶解度如下表所示。下列说法正确的是( )
温度/℃
20
30
40
溶解度/g
31.6
45.8
63.9
A、20 ℃时,100 g KNO3饱和溶液中溶质质量为31.6 g B、30 ℃时,100 g KNO3饱和溶液的溶质质量分数为45.8% C、30 ℃时,将50 g KNO3放入100 g水中得到150 g溶液 D、40 ℃时,100 g水中最多溶解63.9 g KNO36. 下列有关水与溶液的说法错误的是( )A、电解水时,负极产生的气体是氢气 B、饱和溶液就是不能再溶解任何物质的溶液 C、溶液是均一、稳定的混合物 D、天然淡水生产自来水需要经过沉淀、过滤、杀菌消毒等净化过程7. 下图为电解水实验的改进装置,反应前注射器活塞均在 0 刻度处,实验结束后,注射器Ⅰ的活塞移动至 8mL 刻度处。下列有关说法正确的是( )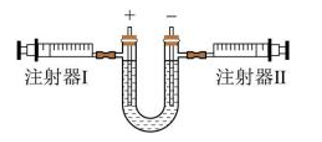 A、注射器Ⅰ中产生的气体为氢气 B、实验结束后注射器Ⅱ的活塞移动至 16mL 刻度处 C、注射器Ⅱ中产生的气体能使带火星的木条复燃 D、电解水实验说明水中含有氢气和氧气8. 下列操作方法或解释不合理的是( )
A、注射器Ⅰ中产生的气体为氢气 B、实验结束后注射器Ⅱ的活塞移动至 16mL 刻度处 C、注射器Ⅱ中产生的气体能使带火星的木条复燃 D、电解水实验说明水中含有氢气和氧气8. 下列操作方法或解释不合理的是( )实验
操作方法或解释
A
用量筒量取液体
视线与液体凹液面的最低处齐平
B
软化硬水
煮沸或蒸馏
C
除去 MnO2 中少量 KCl
溶解→过滤→洗涤→干燥
D
将 3000L 氧气压缩到 20L 的钢瓶中
因为分子变小了
A、A B、B C、C D、D9. 如图是A、B两种固体物质的溶解度曲线,下列分析正确的是( ) A、物质A的溶解度大于物质B的溶解度 B、物质A中混有少量的B,可采用降温结晶的方法提纯A C、t1℃时,把15gA放入50g水中充分溶解,可得到65g溶液 D、将A、B两物质的饱和溶液从t2℃升温至t3℃时,溶质质量分数A>B10. 下列实验设计能达到实验目的的是( )
A、物质A的溶解度大于物质B的溶解度 B、物质A中混有少量的B,可采用降温结晶的方法提纯A C、t1℃时,把15gA放入50g水中充分溶解,可得到65g溶液 D、将A、B两物质的饱和溶液从t2℃升温至t3℃时,溶质质量分数A>B10. 下列实验设计能达到实验目的的是( )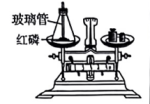
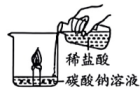
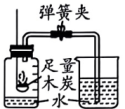
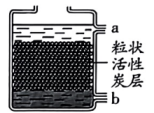
A.验证质量守恒定律
B.探究灭火的原理之一
C.用于测定空气中O2的含量
D.海水从b口进入净化后可得纯净水
A、A B、B C、C D、D11. 对影响溶质在水中溶解速率的实验探究如下图所示。下列说法正确的是( )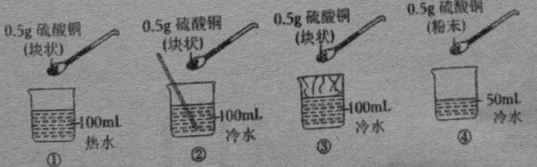 A、对比实验①和②,可探究水的温度对溶质在水中溶解速率的影响 B、对比实验②和③,可探究搅拌对溶质在水中溶解速率的影响 C、对比实验③和④,可探究固体溶质的颗粒大小对溶质在水中溶解速率的影响 D、对比实验①和④,可探究水的体积对溶质在水中溶解速率的影响12. 如图是甲、乙两种物质的溶解度曲线。下列说法正确的是( )
A、对比实验①和②,可探究水的温度对溶质在水中溶解速率的影响 B、对比实验②和③,可探究搅拌对溶质在水中溶解速率的影响 C、对比实验③和④,可探究固体溶质的颗粒大小对溶质在水中溶解速率的影响 D、对比实验①和④,可探究水的体积对溶质在水中溶解速率的影响12. 如图是甲、乙两种物质的溶解度曲线。下列说法正确的是( )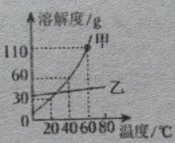 A、乙的溶解度一定大于甲 B、20℃时,甲的饱和溶液的溶质质量分数为30% C、将60℃时甲的饱和溶液降温至40℃,析出50g晶体 D、当甲中混有少量乙时,可采用降温结晶的方法提纯甲13. 在“配制50g溶质质量分数为15%的氯化钠溶液”实验中,下列操作正确的是( )
A、乙的溶解度一定大于甲 B、20℃时,甲的饱和溶液的溶质质量分数为30% C、将60℃时甲的饱和溶液降温至40℃,析出50g晶体 D、当甲中混有少量乙时,可采用降温结晶的方法提纯甲13. 在“配制50g溶质质量分数为15%的氯化钠溶液”实验中,下列操作正确的是( )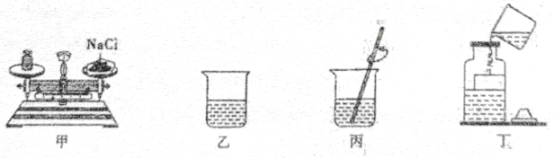 A、甲图表示称取7.5g氯化钠 B、乙图表示量取42.5mL水 C、丙图表示溶解氯化钠 D、丁图表示向试剂瓶中转移溶液14. 中国第35次南极科考队在中山站南冰盏发现“蓝冰区”。蓝冰是致密的冰,可作未来大型飞机冰上起降的永久机场。有关蓝冰的说法正确的是( )
A、甲图表示称取7.5g氯化钠 B、乙图表示量取42.5mL水 C、丙图表示溶解氯化钠 D、丁图表示向试剂瓶中转移溶液14. 中国第35次南极科考队在中山站南冰盏发现“蓝冰区”。蓝冰是致密的冰,可作未来大型飞机冰上起降的永久机场。有关蓝冰的说法正确的是( ) A、它的化学性质与水相同 B、它是干冰可升华成气体 C、里边存有蓝色的物质 D、可做机场是因其表面光滑15. 下列有关溶液的说法错误的是 ( )A、饱和溶液不一定是浓溶液,不饱和溶液一定是稀溶液 B、不饱和溶液转化为饱和溶液,溶液中溶质的质量分数可能不变 C、将5g氯化钠加入到95g水中,完全溶解后,所得溶液中溶质的质量分数是 5% D、将一定质量某物质的饱和溶液降温析出晶体后,溶液中溶质的质量一定减小16. “生命吸管”是一种户外净水装置,能对天然水进行处理。下列说法错误的是( )
A、它的化学性质与水相同 B、它是干冰可升华成气体 C、里边存有蓝色的物质 D、可做机场是因其表面光滑15. 下列有关溶液的说法错误的是 ( )A、饱和溶液不一定是浓溶液,不饱和溶液一定是稀溶液 B、不饱和溶液转化为饱和溶液,溶液中溶质的质量分数可能不变 C、将5g氯化钠加入到95g水中,完全溶解后,所得溶液中溶质的质量分数是 5% D、将一定质量某物质的饱和溶液降温析出晶体后,溶液中溶质的质量一定减小16. “生命吸管”是一种户外净水装置,能对天然水进行处理。下列说法错误的是( ) A、超滤膜可以除去难溶性杂质 B、利用椰壳活性炭的吸附性可以消除异味 C、抗菌颗粒可以消灭细菌 D、通过“生命吸管”得到的水是纯净物17. 在生产、生活和实验中经常用到水。如图中甲为活性炭净水器示意图,乙是制取蒸馏水简易装置图,下列说法正确的是( )
A、超滤膜可以除去难溶性杂质 B、利用椰壳活性炭的吸附性可以消除异味 C、抗菌颗粒可以消灭细菌 D、通过“生命吸管”得到的水是纯净物17. 在生产、生活和实验中经常用到水。如图中甲为活性炭净水器示意图,乙是制取蒸馏水简易装置图,下列说法正确的是( ) A、图2甲中活性炭的作用是杀菌消毒 B、图2甲中水流下进上出是为了提高水的净化效果 C、图2乙中烧杯内水的作用是密封 D、图2乙经过蒸馏后的水仍然是硬水18. 如图是一个气密性良好的装置,当胶头滴管中的液体滴入时,小气球明显鼓起来,4个小时后,气球无法恢复原状,则使用的固体和液体可以是( )
A、图2甲中活性炭的作用是杀菌消毒 B、图2甲中水流下进上出是为了提高水的净化效果 C、图2乙中烧杯内水的作用是密封 D、图2乙经过蒸馏后的水仍然是硬水18. 如图是一个气密性良好的装置,当胶头滴管中的液体滴入时,小气球明显鼓起来,4个小时后,气球无法恢复原状,则使用的固体和液体可以是( ) A、硝酸铵和水 B、铁和稀硫酸 C、固体氢氧化钠和水 D、氯化钠和稀盐酸19. 下列说法正确的是( )
A、硝酸铵和水 B、铁和稀硫酸 C、固体氢氧化钠和水 D、氯化钠和稀盐酸19. 下列说法正确的是( )①由同种元素组成的物质可能是混合物
②由一种反应物生成其他物质的反应叫分解反应
③电解水时正极和负极所得气体质量比为8: 1
④化合反应和氧化反应是包含关系
⑤等质量的H2O和HO2所含氢原子数目相同
⑥木炭和活性炭都具有吸附性,木炭比活性炭的吸附性更强
⑦一种元素可能在同一种物质中显示不同的化合价
⑧铁原子、水分子、氯化钠离子.都是保持对应物质化学性质的最小粒子
A、①②③④⑦⑧ B、②④⑤⑥ C、①③④⑦ D、①③⑦20. 某温度下,甲、乙两个烧杯中各盛有100g相同浓度的KCl溶液.现将甲烧杯中的溶液蒸发掉35g水.析出晶体5g;乙烧杯中的溶液蒸发掉45g水,析出晶体10g。则原溶液的质量分数为( )A、10% B、15% C、20% D、25%二、填空题
-
21. “水煮活鱼”是湖南特色菜之一,要想做好这道菜需要注意以下两点:(1)、一定要用铁锅,用铁锅烹饪主要是利用铁的(填物理性质)。(2)、一定要用山泉水,山泉水是硬水,请问生活中将硬水软化的方法:。(3)、刘奶奶在做菜过程中油锅不小心起火了,请问灭火方法是,灭火原理是:。22. 小英同学从水库中取出浑浊水样进行实验。
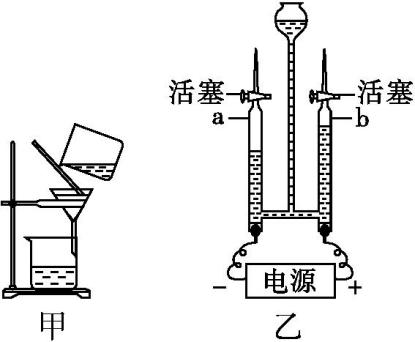 (1)、将水样静置,用如图甲装置进行过滤,其操作规范的是(填字母)。
(1)、将水样静置,用如图甲装置进行过滤,其操作规范的是(填字母)。a.用玻璃棒引流 b.滤纸边缘高出漏斗
c.漏斗末端未紧靠烧杯内壁
d.将滤纸用水润湿,使其紧贴漏斗内壁
(2)、在处理后的水样中加入一定量肥皂水,振荡,观察到泡沫较少,浮渣较多,说明该水样属于(填“硬水”或“软水”)。(3)、生活中常用的方法降低水的硬度,并起到消毒杀菌的作用。
(4)、为了人类的生存和发展,人类必须爱惜水。下列做法不利于保护水资源的是____(填字母)。A、生活污水直接排放 B、提倡使用节水器具 C、工业上冷却水重复利用 D、园林浇灌用滴灌、喷灌(5)、写出如图乙装置中发生反应的化学方程式: , a管和b管中最终产生的气体体积比约为。23. 如图是a、b、c三种固体物质的溶解度曲线。请结合图示回答下列问题: (1)、P点的含义是。(2)、t1℃时,a、b、c三种物质的溶解度由大到小的关系是(用“>”“<”或“=”表示)。(3)、t2℃时,把50 g a放入50 g水中,充分溶解后,得到的a的溶液的质量为g。(4)、t1 ℃时,a的饱和溶液的溶质质量分数为(保留小数点后一位),将该饱和溶液变为不饱和溶液,可采取的措施有(写一种)。(5)、a的固体中混有了少量的c物质,分离提纯a的操作:配成高温下的a的饱和溶液、、过滤、洗涤、干燥。24. 水是一种宝贵的自然资源。(1)、如图1所示是常用的电解水装置。电解水的化学方程式是;检验b中产生的气体的方法是。从微观角度分析,当有2个氧原子结合成1个氧分子时,就有个水分子破裂。(2)、如图2所示是自来水厂净水过程示意图。
(1)、P点的含义是。(2)、t1℃时,a、b、c三种物质的溶解度由大到小的关系是(用“>”“<”或“=”表示)。(3)、t2℃时,把50 g a放入50 g水中,充分溶解后,得到的a的溶液的质量为g。(4)、t1 ℃时,a的饱和溶液的溶质质量分数为(保留小数点后一位),将该饱和溶液变为不饱和溶液,可采取的措施有(写一种)。(5)、a的固体中混有了少量的c物质,分离提纯a的操作:配成高温下的a的饱和溶液、、过滤、洗涤、干燥。24. 水是一种宝贵的自然资源。(1)、如图1所示是常用的电解水装置。电解水的化学方程式是;检验b中产生的气体的方法是。从微观角度分析,当有2个氧原子结合成1个氧分子时,就有个水分子破裂。(2)、如图2所示是自来水厂净水过程示意图。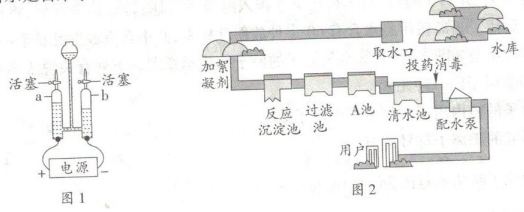
①图中A池需要除去色素和异味,加入的物质是 , 利用其性。
②硬水会对我们的生产生活造成危害,生活中常用的方法来降低水的硬度。
③水是一切生命体生存所必需的物质,为了人类的生存和发展,人类必须爱护水资源,一方面要节约用水,另一方面要。
25. 某实践小组参观本地矿泉水厂,该厂矿泉水含钙、钾等矿物质,其生产流程示意图如图。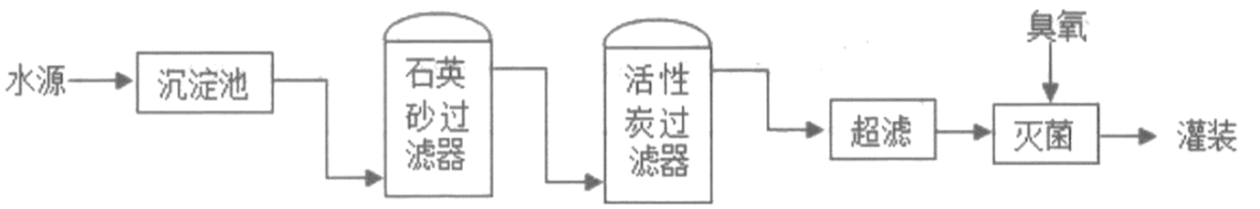 (1)、该矿泉水是(填“混合物”或“纯净物”);矿泉水中的钙、钾指的是填“元素”或“单质”)。(2)、活性炭过滤器中活性炭的作用是。(3)、超滤是利用薄膜(仅允许小分子和离子通过)进行物质分离的技术。若水源中含有下列物质,推测该流程中“超滤”的主要作用是除去(填字母序号)。
(1)、该矿泉水是(填“混合物”或“纯净物”);矿泉水中的钙、钾指的是填“元素”或“单质”)。(2)、活性炭过滤器中活性炭的作用是。(3)、超滤是利用薄膜(仅允许小分子和离子通过)进行物质分离的技术。若水源中含有下列物质,推测该流程中“超滤”的主要作用是除去(填字母序号)。①难溶性大颗粒 ②可溶性金属离子 ③可溶性大分子和大分子团
(4)、臭氧的化学式O3的微观意义是(写出一点即可)。三、综合题
-
26. 氢能作为一种高效、清洁的可再生能源具有良好的发展前景。根据制备方式及制备过程中碳排放量的不同,氢能分为“灰氢”“蓝氢”和“绿氢”。图1是炼厂制氢技术碳排放及制氢成本关系图(CNY:Chinese Yuanf的缩写,即人民币),图2是在光照条件下,使用C3N4/CQDS复合催化剂可水转化为氢气的微观示意图。
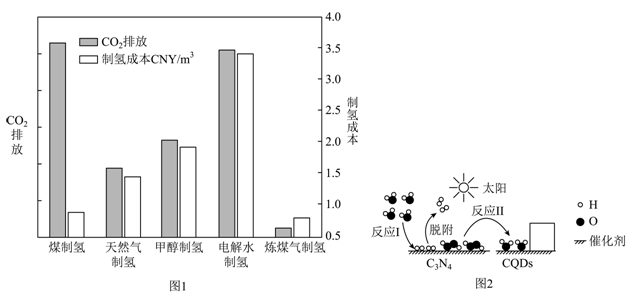 (1)、“灰氢”:由化石能源制取氢气,制氢过程排放二氧化碳等温室气体。
(1)、“灰氢”:由化石能源制取氢气,制氢过程排放二氧化碳等温室气体。①“灰氢”制取过程中,会导致的环境问题是。
②结合图1分析,电解水制氢尚未普及的主要原因是。
(2)、“蓝氢”:由化石能源制氢气,用碳捕获与封存技术减少二氧化碳排放。工业上碳捕获通常利用一定的CaO吸附CO2。①使用纳米CaO的吸附效果优于微米CaO的原因是。
②碳捕获所得高浓度的二氧化碳可用于(举一例用途)。
(3)、“绿氢”:由核能、可再生能源分解水获得氢气,制氢过程没有排放温室气体。①反应1、II前后没有改变的粒子是(写化学符号)。写出图中方框内粒子的化学式:。
②反应Ⅱ的化学方程式为。
27. 根据如图所示的溶解度曲线,回答下列问题.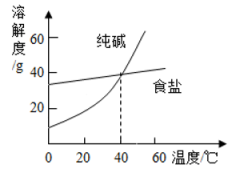 (1)、写出两种物质的化学式:纯碱 , 食盐 , 这两种物质均属于填物质类别 .(2)、我国某些盐湖里出产天然碱主要成分为纯碱晶体,并含有少量食盐杂质 , 实验室里从天然碱中分离出较纯的纯碱晶体应采用的方法.(3)、具体的实验操作步骤为加热溶解;;;洗涤晾于.(4)、完成中操作的必备的实验仪器有、、、和 .
(1)、写出两种物质的化学式:纯碱 , 食盐 , 这两种物质均属于填物质类别 .(2)、我国某些盐湖里出产天然碱主要成分为纯碱晶体,并含有少量食盐杂质 , 实验室里从天然碱中分离出较纯的纯碱晶体应采用的方法.(3)、具体的实验操作步骤为加热溶解;;;洗涤晾于.(4)、完成中操作的必备的实验仪器有、、、和 .四、实验探究题
-
28. 实验室有一包久置的生石灰干燥剂,同学们对其是否变质以及变质的程度感到好奇,于是开展了如下探究:
[提出问题] 该干燥剂的成分有哪些?
[查阅资料] ①碳酸钙在900 ℃以上时会分解生成氧化钙和二氧化碳;②氢氧化钙在500 ℃以上会分解生成氧化钙和水。
(1)、[实验验证]实验步骤
实验现象
实验结论
①取少量该干燥剂样品于试管中,加入一定量的水
该干燥剂样品中一定有氧化钙
②取①中上层清液于试管中,滴加酚酞溶液
溶液变红
该干燥剂样品中一定有
③另取少量干燥剂样品于试管中,滴加足量稀盐酸
该干燥剂样品中一定有碳酸钙
(2)、[分析讨论] 小明同学认为步骤②不能得到结论正确,原因是。(3)、步骤③发生反应的化学方程式为。(4)、[拓展探究]为了进一步探究干燥剂中是否有氢氧化钙,小红称取该干燥剂m1 g,加热至固体质量不再变化,称量反应后固体质量为m2 g,加热温度应控制的范围是 , 若m1(填“>”“<”或“=”)m2 , 说明该干燥剂中含有氢氧化钙。
(5)、根据上述数据,请你计算小红称取的固体物质中氢氧化钙的质量是(用含m1、m2的式子表示)g。(6)、[实验反思] 结合固体的成分,你认为生石灰干燥剂除了能吸收空气中的水分外,还能吸收空气中的。29. 小王同学在学习完酸、碱、盐的化学性质后,对复分解反应的条件产生了兴趣,于是和同学们进行了探究实验。
[查阅资料]
①在溶液中发生的复分解反应大多是在酸、碱、盐之间进行的,而酸、碱、盐都是电解质,在溶液中都能电离出离子。
②复分解反应的实质是电解质在溶液中发生离子间的互换后,使某些离子的浓度迅速减小,反应向减小离子浓度的方向进行。如果离子混合后,离子浓度不发生变化,那就没有发生反应。
[提出问题]复分解反应发生的条件是什么?
[探究过程]同学们进行了如图甲所示的实验。
(1)、B试管中产生的现象是(2)、C试管的溶液中减少的离子是(3)、A试管中没有现象,为了验证发生了反应,同学们又进行了如图乙所示的实验,由此现象可得到的结论是;还可以加入进行验证。(4)、D试管中也没有现象,同学们结合两种物质的溶解度曲线(如图丙所示),采用的方法得到了硝酸锌晶体,从而说明这两种物质的混合属于变化。(5)、[得出结论]结合资料,同学们得出了结论:复分解反应发生的条件是。
(6)、[总结提升]从上面的探究过程中,同学们也可以得出“证明化学反应能发生的思路是证明有新物质生成或的结论。
五、计算题
-
30. 向盛有稀硫酸的烧杯中加入一定量的镁粉,固体完全溶解后,再向所得溶液中加入溶液,所得沉淀质量与加入溶液的质量关系如图所示。
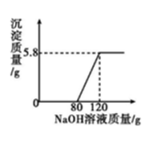 (1)、是由种元素组成。(2)、中、、的质量比为。(3)、的相对分子质量为。(4)、所用氢氧化钠溶液的溶质质量分数为。(5)、求恰好完全反应时所得溶液的溶质质量分数。要求写出计算过程,精确到
(1)、是由种元素组成。(2)、中、、的质量比为。(3)、的相对分子质量为。(4)、所用氢氧化钠溶液的溶质质量分数为。(5)、求恰好完全反应时所得溶液的溶质质量分数。要求写出计算过程,精确到