专题四 物质的鉴别--【高效二轮复习】2023-2024学年中考科学二轮复习(浙教版)
试卷更新日期:2024-03-27 类型:二轮复习
一、选择题
-
1. 某混合气体可能含有H2、CO、CO2、HCl中的一种或几种,某同学采取实验进行检验:将混合气体先通入澄清石灰水时无明显现象产生,导出的气体通过浓硫酸后再通入放有炽热氧化铜粉末的试管,发现试管中有红色物质出现.最后将试管中导出的气体通入放有白色硫酸铜粉末的U形管,未见有明显现象产生。根据上述实验,可以判定该混合气体中一定没有( )A、H2 B、H2和CO2 C、CO D、H2、CO2和HCl2. 某固体可能含有CaCl₂、Na₂SO₄、CuSO₄、KNO₃、Na₂CO₃中的一种或几种,现对其进行如下实验:
①取少量固体于试管中,加适量蒸馏水,固体完全溶解得无色透明溶液;
②在①所得溶液中,滴加足量的BaCl₂溶液,产生白色沉淀,过滤后,在白色沉淀中加过量稀盐酸,沉淀部分溶解,且有气泡产生。
下列对原固体成分的说法正确的是( )
A、一定有Na₂CO₃和Na₂SO₄,可能含有KNO₃、CuSO₄、CaCl₂ B、一定有Na₂CO₃,Na₂SO₄和CuSO₄两种物质中至少有一种 C、一定有Na₂CO₃和Na₂SO₄,不含CaCl₂,可能有KNO₃、CuSO₄ D、一定有Na₂CO₃和Na₂SO₄,不含CuSO₄和CaCl₂,可能有KNO₃3. 用下列试剂中的一种就能将BaCl2、NaCO3和NaCl这三种无色溶液一一区别开来,这种试剂是( )A、稀H2SO4 B、NaOH溶液 C、AgNO3溶液 D、KNO3溶液4. 某固体粉末可能含有离子中的若干种,取一定量的该固体粉末溶于水中得澄清透明溶液,分成两等份。取其中一份溶液加入一定量的Fe粉完全溶解,溶液中没有固体析出,经测定该溶液恰好是加入Fe粉后溶液质量增加的最大限度,增加的质量为0.56g。取另一份溶液加入过量的NaOH溶液,过滤,取洗涤干燥后的滤渣充分灼烧得固体2.4g,在滤液中滴入过量的溶液,过滤,洗涤干燥得9.32g固体。下列说法不正确的是( )A、该固体中一定没有 B、该固体中一定没有 C、该固体中不能确定是否含有 D、该固体中一定含有5. 实验废液中可能含有离子K+、Mg2+、Cl-、Ba2+、SO42-、CO32-中的几种,为确定可能含有的离子,兴趣小组进行了下面的实验:①取一份废液,加入氯化钡溶液有白色沉淀产生,再加入足量稀盐酸,沉淀无变化;
②另取一份废液,加入氢氧化钾溶液出现白色沉淀,再加入足量稀盐酸,沉淀全部溶解,
分析上面实验得出的结论中,正确的是( )
A、只含有Mg2+、SO42- B、一定含有K+、Mg2+、Cl-、SO42- C、一定含有Mg2+、SO42- , 可能含有Cl-、K+ D、一定含有Cl-、K+ , 可能含有Mg2+、SO42-6. 向Cu(NO3)2、Al(NO3)3和AgNO3的混合溶液中加入铁粉,充分反应后过滤,向滤渣中滴加稀硫酸时有气泡产生。下列推断下列推断正确的是( )A、滤渣中一定有铁、铜、银,可能有铝 B、滤液中的溶质只有Al(NO3)3和Fe(NO3)2 C、滤液中一定有Fe(NO3)2 , 可能有Al(NO3)3 D、滤液中一定有Al(NO3)3和Fe(NO3)2 , 可能有Cu(NO3)27. 向一定量的AgNO3和Cu(NO3)2的混合溶液中加入Zn,溶液质量与加入Zn的质量关系如下图所示,下列说法正确的是( )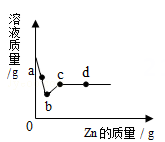 A、a点溶液中有2种阳离子 B、c点溶液中溶质为Zn(NO3)2 C、若取b~c段溶液,滴加稀盐酸,会产生白色沉淀 D、若取d点固体,有反应生成的铜与银,加入稀盐酸则无气泡产生8. 今有一混合物的水溶液,只可能含有以下离子中的若干种:K+、、Cl-、Ba2+、、。现取二份100mL溶液进行如下实验:(1)第一份加足量NaOH溶液加热后,收集到0.68g气体(2)第二份加足量BaCl2溶液后,得到干燥沉淀6.27g,经足量盐酸洗涤、干燥后,沉淀质量为2.33g。根据上述实验,以不推测正确的是( )A、一定不存在Ba2+ , 可能存在 B、、定存在,K+、Cl-可能存在 C、Ba2+可能存在,一定不存在 D、K+、、、一定存在,Cl-可能存在9. 有一包白色粉末,可能含有Na2CO3、Na2SO4、K2SO4、Ba(OH)2中的一种或几种,为了探究其成分,实验过程如图所示:
A、a点溶液中有2种阳离子 B、c点溶液中溶质为Zn(NO3)2 C、若取b~c段溶液,滴加稀盐酸,会产生白色沉淀 D、若取d点固体,有反应生成的铜与银,加入稀盐酸则无气泡产生8. 今有一混合物的水溶液,只可能含有以下离子中的若干种:K+、、Cl-、Ba2+、、。现取二份100mL溶液进行如下实验:(1)第一份加足量NaOH溶液加热后,收集到0.68g气体(2)第二份加足量BaCl2溶液后,得到干燥沉淀6.27g,经足量盐酸洗涤、干燥后,沉淀质量为2.33g。根据上述实验,以不推测正确的是( )A、一定不存在Ba2+ , 可能存在 B、、定存在,K+、Cl-可能存在 C、Ba2+可能存在,一定不存在 D、K+、、、一定存在,Cl-可能存在9. 有一包白色粉末,可能含有Na2CO3、Na2SO4、K2SO4、Ba(OH)2中的一种或几种,为了探究其成分,实验过程如图所示:
关于该实验的说法正确的是( )
A、步骤II中沉淀不溶解,则原白色粉末一定有Na2SO4、Ba(OH)2 , 一定没由Na2CO3 B、步骤II中沉淀部分溶解,则原白色粉末一定有Na2CO3、K2SO4、Ba(OH)2 C、步骤II中沉淀部分溶解,则原白色粉末中有Na2CO3、Na2SO4、K2SO4、Ba(OH)2 D、步骤II中沉淀全部溶解,则原白色粉末一定有Na2CO3、Ba(OH)2 , 一定没有Na2SO4、K2SO410. 某公司生产的融雪剂由NaCl、CaCl2、Na2CO3和CuSO4中的一种或两种物质组成。小桐同学将该融雪剂加水溶解,得到无色溶液,向该溶液中加入K2CO3溶液,有白色沉淀生成。由此可知,该融雪剂的组成可能是( )A、CuSO4 NaCl B、Na2CO3 NaCl C、CaCl2 NaCl D、CuSO4 CaCl2二、填空题
-
11. 有一包白色固体可能含有碳酸钾、硫酸钾、硝酸钡、氢氧化钾、硫酸铜中的一种或几种。小宁同学为探究其成分设计并完成了如图实验:
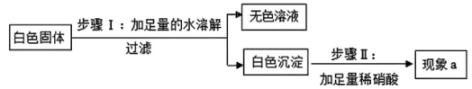 (1)、由步骤Ⅰ的现象,推断白色固体中肯定不含。(2)、小宁根据现象a得出结论:该白色固体中一定含有碳酸钾、硫酸钾和硝酸钡,则现象a为。12. 一包白色粉末,由CuSO4、CaCO3、BaCl2、K2SO4、KOH中的两种或两种以上的物质混合而成。为探究其组成,进行如下实验:
(1)、由步骤Ⅰ的现象,推断白色固体中肯定不含。(2)、小宁根据现象a得出结论:该白色固体中一定含有碳酸钾、硫酸钾和硝酸钡,则现象a为。12. 一包白色粉末,由CuSO4、CaCO3、BaCl2、K2SO4、KOH中的两种或两种以上的物质混合而成。为探究其组成,进行如下实验:
(1)、取少量白色粉末,向其中加入足量的水,充分搅拌后过滤,得到白色沉淀和无色滤液,由此可推断混合物中一定没有;(2)、取实验(1)滤出的白色沉淀,向其中加入足量的盐酸,沉淀全部溶解,并产生无色气体。根据上述实验可推断:原白色粉末中一定有。为进一步探究原白色粉末的组成,取实验(1)得到的滤液,向其中通入二氧化碳,产生白色沉淀,则可推断原白色粉末中一定还含有。13. 有一包白色固体,可能由 BaCl2、NaOH、Na2CO3、Na2SO4 中的一种或几种组成。为确定其成分,实验小组进行实验。实验过程中所加试剂均足量,实验过程及现象如图所示。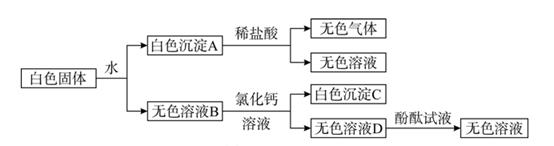 (1)、白色沉淀 A 与稀盐酸反应的化学反应方程式为。(2)、这包白色固体是由(填化学式)组成的。14. 有一包固体粉末,可能含有FeCl3、CaCO3、NaOH、Ba(OH)2、BaCl2、Na2SO4中的几种,为确定其组成,取适量试样进行下列实验。请根据实验现象推断:
(1)、白色沉淀 A 与稀盐酸反应的化学反应方程式为。(2)、这包白色固体是由(填化学式)组成的。14. 有一包固体粉末,可能含有FeCl3、CaCO3、NaOH、Ba(OH)2、BaCl2、Na2SO4中的几种,为确定其组成,取适量试样进行下列实验。请根据实验现象推断:①取试样溶于水,搅拌、过滤,得到无色澄清溶液A和白色沉淀B;
②取上述无色澄清溶液A,通入适量的CO2 , 生成白色沉淀C;
③取上述白色沉淀B,加入过量的稀硝酸,沉淀全部消失。
综合上述实验现象,回答下列问题:
(1)、由步骤①可知:原固体粉末中一定不含(写化学式);(2)、由步骤②③可知:原固体粉末中一定不含(写化学式);(3)、由实验现象综合判断,固体粉末的混合组成中,最多是含有4种物质的混合,最少是含有种物质的混合。15. 固体混合物A是由Mg、CuO、Na2SO4、Na2CO3、BaCl2、BaSO4中的几种混合而成为,为确定其成分,进行如图实验.(假设每步反应均恰好完全反应)试推断: (1)、沉淀C的成分是(2)、固体A的组成有种可能。
(1)、沉淀C的成分是(2)、固体A的组成有种可能。三、实验探究题
-
16. 有一包白色固体样品,可能含有NaOH、Na₂CO₃、K₂SO₄、BaCl₂中的一种或几种,为确定其组成,进行如下实验:
步骤Ⅰ:取少量样品于烧杯中,加足量水,充分搅拌,静置,有固体剩余。
步骤Ⅱ:取步骤Ⅰ所得上层清液于试管中,滴入几滴酚酞溶液,溶液变红色;再滴入过量稀盐酸,无气泡产生,红色逐渐褪去,得到无色溶液。
步骤Ⅲ:取步骤Ⅱ所得溶液于试管中,滴入过量Ba(NO₃)₂溶液,无明显现象。
根据上述实验,回答下列问题:
(1)、步骤Ⅱ中溶液的红色褪去,发生反应的化学方程式。(2)、分析上述实验过程,关于样品的组成,可以得到的结论是。(3)、若要进一步确定样品的组成,还需进行的实验操作是。17. 有一包白色固体样品,可能由硫酸钠、氢氧化钠、碳酸钙、氯化钡、氯化镁中的一种或几种物质组成,为探究该样品的组成,某小组取适量样品按下列流程进行实验。 (1)、过滤操作中用到的玻璃仪器有烧杯、玻璃棒和。(2)、滤渣a的成分是。(填写化学式)(3)、写出反应(1)中生成气体的化学方程式:。(4)、若现象①“滤渣全部溶解”变为“滤渣部分溶解”,现象②不变。则滤渣a的成分一定有。(填写出化学式)18. 某科学探究小组对一包固体粉末中的成分进行鉴别,粉末中可能含有BaCO3、NaCl、Na2CO3、CuSO4、NaOH、CaCl2中的一种或几种,实验操作步骤及现象如图,试回答:
(1)、过滤操作中用到的玻璃仪器有烧杯、玻璃棒和。(2)、滤渣a的成分是。(填写化学式)(3)、写出反应(1)中生成气体的化学方程式:。(4)、若现象①“滤渣全部溶解”变为“滤渣部分溶解”,现象②不变。则滤渣a的成分一定有。(填写出化学式)18. 某科学探究小组对一包固体粉末中的成分进行鉴别,粉末中可能含有BaCO3、NaCl、Na2CO3、CuSO4、NaOH、CaCl2中的一种或几种,实验操作步骤及现象如图,试回答: (1)、仅由步骤Ⅰ可知,固体粉末中不可能含有的物质是(填化学式,下同);(2)、白色沉淀A为;(3)、无色溶液D一定含有的溶质是;(4)、结论:固体粉末中一定含有____。A、Na2CO3 B、NaOH C、NaCl
(1)、仅由步骤Ⅰ可知,固体粉末中不可能含有的物质是(填化学式,下同);(2)、白色沉淀A为;(3)、无色溶液D一定含有的溶质是;(4)、结论:固体粉末中一定含有____。A、Na2CO3 B、NaOH C、NaCl