湖南省长沙市长郡教育集团联考2023-2024学年九年级上学期期末化学试题
试卷更新日期:2024-03-25 类型:期末考试
一、单项选择题(本大题共12小题,每小题3分,共36分。每小题只有一个选项符合题意)
-
1. 化学改变世界的途径是使物质发生化学变化。以下过程一定涉及到化学变化的是( )A、金刚石裁玻璃 B、杂交水稻谷子碾成大米 C、辞旧迎新时燃放爆竹 D、实验人员佩戴防护眼镜2. 具备基本的实验技能是进行科学探究的保证,下列实验操作正确的是( )A、闻气体气味
 B、倾倒液体
B、倾倒液体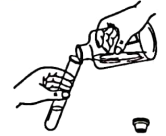 C、添加锌粒
C、添加锌粒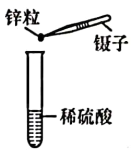 D、溶解氢氧化钠
D、溶解氢氧化钠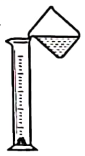 3. 空气是人类赖以生存的物质基础。下列有关说法正确的是( )A、空气中的氧气是一种常见的燃料 B、空气中的二氧化碳属于稀有气体 C、空气中氮气的质量分数约为78% D、植树造林有利于保护空气4. 液氢是航天工业的一种火箭燃料,将氢气加压液化的过程中发生改变的是( )A、分子种类 B、原子种类 C、分子体积 D、分子间隔5. 水是生命之源。下列有关水的说法正确的是( )A、地球上的水含量丰富,无需节约用水 B、电解水可以说明水是由氢气和氧气组成 C、在生活中用煮沸的方法可将硬水软化 D、经过沉淀、过滤、吸附后的湘江水属于纯净物6. 在汽油中加入适量乙醇作为汽车燃料,可节省石油资源。乙醇充分燃烧的化学方程式为C2H5OH+3O22CO2+3X,试推测X的化学式是( )A、H2 B、H2O C、CO D、C2H6O37. 下列有关金刚石、石墨和C60的说法错误的是( )A、石墨导电性良好可用作电极 B、每个C60分子由60个碳原子构成 C、金刚石、石墨和C60都是碳的单质 D、金刚石、石墨和C60的物理性质相同8. 长沙市正在创建国家卫生城市,为力争在2024年创建成功,下列做法不正确的是( )A、减少橘子洲头的烟花燃放活动 B、将城市生活垃圾集中露天焚烧 C、加强对化工园区废气、废水排放的监测 D、减少使用一次性筷子,积极推广公筷制9. 下列有关金属的叙述正确的是( )A、铁和铜都是银白色金属 B、真金不怕火炼说明金是熔点最高的金属 C、生铁和钢都属于铁合金 D、铝制品耐腐蚀是因为铝化学性质不活泼10. 化学需要借助化学专用语言描述。下列化学用语使用正确的是( )A、镁离子:Mg2+ B、2个氧原子:O2 C、过氧化氢中氧元素的化合价: D、2个氮分子:2N11. “证据推理与模型认知”是化学学科核心素养的重要组成部分。下列推理与归纳正确的是( )A、活泼金属与稀盐酸反应产生气泡,则与稀盐酸反应产生气泡的物质一定是活泼金属 B、燃烧需要同时满足三个条件,所以灭火也要同时破坏这三个条件 C、三种常见的具有还原性的物质:C、CO和H2 D、目前,人类大量开采使用的化石燃料:煤、石油和可燃冰12. 为除去下列物质中的杂质,除杂试剂及方法正确的是( )
3. 空气是人类赖以生存的物质基础。下列有关说法正确的是( )A、空气中的氧气是一种常见的燃料 B、空气中的二氧化碳属于稀有气体 C、空气中氮气的质量分数约为78% D、植树造林有利于保护空气4. 液氢是航天工业的一种火箭燃料,将氢气加压液化的过程中发生改变的是( )A、分子种类 B、原子种类 C、分子体积 D、分子间隔5. 水是生命之源。下列有关水的说法正确的是( )A、地球上的水含量丰富,无需节约用水 B、电解水可以说明水是由氢气和氧气组成 C、在生活中用煮沸的方法可将硬水软化 D、经过沉淀、过滤、吸附后的湘江水属于纯净物6. 在汽油中加入适量乙醇作为汽车燃料,可节省石油资源。乙醇充分燃烧的化学方程式为C2H5OH+3O22CO2+3X,试推测X的化学式是( )A、H2 B、H2O C、CO D、C2H6O37. 下列有关金刚石、石墨和C60的说法错误的是( )A、石墨导电性良好可用作电极 B、每个C60分子由60个碳原子构成 C、金刚石、石墨和C60都是碳的单质 D、金刚石、石墨和C60的物理性质相同8. 长沙市正在创建国家卫生城市,为力争在2024年创建成功,下列做法不正确的是( )A、减少橘子洲头的烟花燃放活动 B、将城市生活垃圾集中露天焚烧 C、加强对化工园区废气、废水排放的监测 D、减少使用一次性筷子,积极推广公筷制9. 下列有关金属的叙述正确的是( )A、铁和铜都是银白色金属 B、真金不怕火炼说明金是熔点最高的金属 C、生铁和钢都属于铁合金 D、铝制品耐腐蚀是因为铝化学性质不活泼10. 化学需要借助化学专用语言描述。下列化学用语使用正确的是( )A、镁离子:Mg2+ B、2个氧原子:O2 C、过氧化氢中氧元素的化合价: D、2个氮分子:2N11. “证据推理与模型认知”是化学学科核心素养的重要组成部分。下列推理与归纳正确的是( )A、活泼金属与稀盐酸反应产生气泡,则与稀盐酸反应产生气泡的物质一定是活泼金属 B、燃烧需要同时满足三个条件,所以灭火也要同时破坏这三个条件 C、三种常见的具有还原性的物质:C、CO和H2 D、目前,人类大量开采使用的化石燃料:煤、石油和可燃冰12. 为除去下列物质中的杂质,除杂试剂及方法正确的是( )选项
物质(括号内为杂质)
除杂试剂及方法
A
锰酸钾(高锰酸钾)
充分加热
B
氧气(水蒸气)
将混合气体通过装有氧化钙的玻璃管
C
硫酸铜溶液(硫酸锌)
加入过量的铜粉,过滤
D
木炭粉(氧化铜)
在空气中充分灼烧
A、A B、B C、C D、D二、不定项选择题(本大题共3小题,每小题3分,共9分。在每小题给出的四个选项中,有一个或两个选项符合题意。全部选对的得3分,选对但不全对的得2分,有选错的得0分。)
-
13. 将下列四种家庭常用的调味品分别放入水中,能形成溶液的是( )A、食盐 B、植物油 C、辣椒粉 D、白砂糖14. 基于“宏观一微观一符号”建立联系是化学学科重要的思维方法,结合图示分析正确的是( )
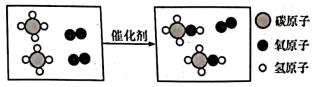 A、从物质类别上看:图示物质中有1种氧化物 B、从微观构成上看:图示物质均由分子构成 C、从元素价态上看:反应前后元素化合价都没有改变 D、从表示方法上看:化学方程式为2CH4+2O22CH3OH+O215. 下列各组物质的鉴别方法与结论均正确的是( )
A、从物质类别上看:图示物质中有1种氧化物 B、从微观构成上看:图示物质均由分子构成 C、从元素价态上看:反应前后元素化合价都没有改变 D、从表示方法上看:化学方程式为2CH4+2O22CH3OH+O215. 下列各组物质的鉴别方法与结论均正确的是( )选项
物质
方法与结论
A
硬水与软水
取样,加入肥皂水振荡,产生大量泡沫的是软水
B
黄铜片与铜片
相互刻画,面上被刻出痕迹的是黄铜
C
一氧化碳与二氧化碳
分别通入澄清石灰水中,能使澄清石灰水变浑浊的是一氧化碳
D
固态的氯化钠与氢氧化钠
取样,加水溶解,溶液温度升高的是氢氧化钠
A、A B、B C、C D、D三、填空题(本大题共5小题,化学方程式每个3分,其余每空2分,共30分)
-
16. 据《诗经》中的“窈窕淑女,钟鼓乐之”可知,钟是古代常见的乐器,位居金属乐器之首。铸钟的材料铜为上等,铁为下等。(1)、古代炼铜的方法之一是用铁与硫酸铜溶液反应,该反应的化学方程式为。(2)、现存世最早的铜钟保存于陕西延安市富县文物局,距今将近1400年。该铜钟的材质为铜合金,这是因为铜合金的抗腐蚀性比纯铜更。17. 2023年12月18日23时59分,甘肃省积石山县发生6.2级地震,众多救援队赶赴灾区抗震救灾。(1)、救援队借助搜救犬寻找被埋在废墟下的幸存者,这是利用了分子的性质。(2)、此次救援最大的困难是零下十几度的低温天气。为防冻伤,积石中学的老师组织学生点燃废旧书纸和树枝烤火。“书纸和树枝”为燃烧提供的条件是。(3)、震前的地壳活动,使得水中的硫磺微粒增加而显现淡蓝色的光,这是地震的前兆之一。我们知道硫在空气中燃烧也会发出淡蓝色火焰,请写出硫在空气中燃烧的化学方程式:。18. 下面是NH4Cl、KNO3在不同温度时的溶解度表以及它们的溶解度曲线。
温度/℃
10
20
30
40
60
80
溶解度/g
NH4Cl
33.3
37.2
41.4
45.8
55.2
65.6
KNO3
20.9
31.6
45.8
63.9
110
169
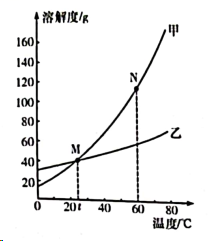
请回答:
(1)、20℃时,NH4Cl的溶解度(填“>”“<”或“=”)KNO3的溶解度。(2)、60℃时,图中N点对应甲的溶解度为g。(3)、将一定质量60℃的饱和NH4Cl溶液和饱和KNO3溶液同时降温到t℃,所得溶液的溶质质量分数:NH4Cl溶液(填“>”“<”“=”或“不能确定”)KNO3溶液。19. 认真阅读下列材料,回答有关问题。铝在高温的条件下能将某些金属氧化物置换为金属单质,这样的反应又称为铝热反应。铝热反应的特点是释放大量的热,能将生成的金属单质熔化。因而广泛应用于轨道焊接、冶金工业、耐火陶瓷和复合材料的合成等领域。
能够发生铝热反应的含能材料被称作铝热剂。如图,滤纸中装有由铝和氧化铁等物质组成的铝热剂。反应过程为:点燃镁条,燃烧产生的热量能使氯酸钾快速产生氧气,进而支持镁条更剧烈的燃烧。产生的高温,引发铝和氧化铁的铝热反应。
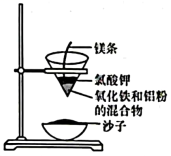 (1)、氧化铝是铝和氧化铁发生铝热反应的生成物之一,请写出氧化铝的化学式。(2)、请结合铁丝在氧气中燃烧的实验,推测蒸发皿中盛放的沙子的作用。(3)、短文中画横线的文字部分,涉及的基本反应类型包括。20. 金属资源不可再生,为节约金属资源,从某种固体废弃物(成分为Cu、CuO、Mg、Zn)中回收金属铜和锌,并得到硫酸镁溶液的回收流程如图:
(1)、氧化铝是铝和氧化铁发生铝热反应的生成物之一,请写出氧化铝的化学式。(2)、请结合铁丝在氧气中燃烧的实验,推测蒸发皿中盛放的沙子的作用。(3)、短文中画横线的文字部分,涉及的基本反应类型包括。20. 金属资源不可再生,为节约金属资源,从某种固体废弃物(成分为Cu、CuO、Mg、Zn)中回收金属铜和锌,并得到硫酸镁溶液的回收流程如图: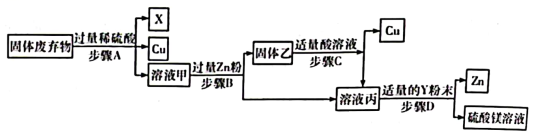
资料:CuO+H2SO4=CuSO4+H2O
(1)、上图中步骤A~D均进行了操作(填操作名称)。(2)、步骤B加入过量的Zn粉,对应的实验现象为。(3)、结合上图回收流程,下列说法正确的有____(填标号)。A、步骤A产生的物质X为H2 B、若溶液甲的颜色为蓝色,可得出活动性:Cu>H C、步骤C加入的酸溶液可以是稀盐酸 D、步骤D加入的Y粉末为Mg四、实验与探究题(本大题共2小题,每空2分,共20分)
-
21. 化学实验是科学探究的重要手段,如图是实验室常用的装置。
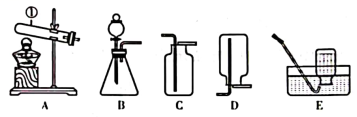
请回答下列问题:
(1)、写出标号①的仪器名称。(2)、收集二氧化碳气体时,将燃着的木条放在集气瓶口,发现木条 , 说明二氧化碳已收集满。(3)、若实验室选用AE装置制取氧气,当导管口时,再把导管口伸入盛满水的集气瓶。(4)、硫化氢(H2S)是一种密度比空气大、能溶于水的气体,实验室用硫化亚铁(FeS)固体和稀盐酸溶液反应可制取H2S气体。该过程应选择的发生装置和收集装置为(填装置字母)。22. 某研究性学习小组利用如图装置探究温度对CO还原Fe2O3的影响(固定装置已省略)。查阅资料:①CO2+ZnCO+ZnO;
②FeO+8HCl=2FeCl3+FeCl2+4H2O;
③FeCl3的溶液为黄色,遇KSCN溶液变红。
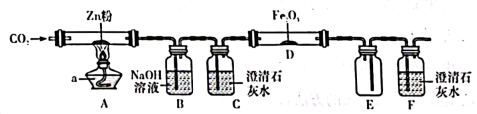
请回答下列问题:
(1)、回顾CO2的性质可知,CO2(填“有”或“没有”)还原性。(2)、装置B中发生的反应为:CO2+2NaOH=Na2CO3+H2O,推测装置C的作用是。(3)、将研究小组分为两组,按如图装置进行对比实验,甲组在D处用酒精灯进行加热,乙组在D处用酒精喷灯进行加热,其产物均为黑色粉末(纯净物)。两组分别对产物进行以下实验:实验
操作
甲组现象
乙组现象
1
取黑色粉末加入盐酸,充分反应
溶解,无气泡,溶液呈浅黄绿色(含两种金属离子)
溶解,有气泡,溶液呈浅绿色
2
取实验1所得溶液,滴加KSCN溶液
溶液变红
无明显现象
根据表中的实验现象,推测乙组得到的黑色粉末是。
(4)、实验反思与评价①从安全角度考虑,在装置之间应添加一个E装置(填字母编号)。
②从环保角度考虑,本实验还存在的缺陷是。
(5)、该对比实验的结果表明CO的还原能力随温度的升高而(填“增强”或“减弱”)。五、计算题(本大题共1小题,共5分)
-
23. 如表是某品牌钙片标签的部分信息。初三化学社团为测定该药片中碳酸钙的量是否与标签相符,开展了以下实验:取8片药片,研碎后逐渐加入质量分数为7.3%的稀盐酸,充分反应。实验相关数据如图所示(假设其他成分不参加反应)。
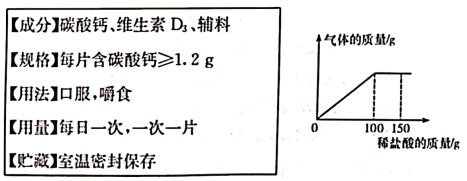 (1)、恰好完全反应时消耗稀盐酸的质量为g。(2)、计算每片药片中碳酸钙的质量。(写出计算过程)
(1)、恰好完全反应时消耗稀盐酸的质量为g。(2)、计算每片药片中碳酸钙的质量。(写出计算过程)