天津市河北区2023-2024学年高三上学期期末质量检测化学试题
试卷更新日期:2024-03-21 类型:期末考试
一、单选题
-
1. 从深邃的海底到浩瀚的太空,中国科学家探索的脚步从未停止。下列成果所涉及的材料为金属材料的是( )A、“神舟十五号”飞船使用的耐辐照光学窗材料——石英玻璃 B、“长征五号”运载火箭使用的燃料——液氢 C、“福建号”航母使用的高强度甲板材料——合金钢 D、“C919”大飞机使用的机身复合材料——碳纤维和环氧树脂2. 化学创造美好生活,下列生产活动与对应化学原理没有关联或关联性不正确的是( )
选项
生产活动
化学原理
A
社区服务:用84消毒液清洗公共桌椅
84消毒液中的有强氧化性
B
实践活动:点燃天然气做饭
天然气的燃烧为放热反应
C
自主探究:将铁丝分别放在有水和无水环境中观察较长时间
钢铁在有水存在的条件下更容易生锈
D
家务劳动:白醋除去水壶中的水垢
白醋可以溶解碳酸钙等难溶物
A、A B、B C、C D、D3. 下列化学用语表示不正确的是( )A、烧碱的化学式: B、中Fe元素的化合价:+6 C、的结构示意图: D、氯化钾的电离方程式:
4. 根据元素周期表和元素周期律,判断下列叙述正确的是( )A、氢卤酸的酸性由强到弱的顺序: B、同周期第ⅡA族和第ⅢA族元素原子序数可能相差1、11、25 C、铁元素位于元素周期表中第四周期第ⅧA族 D、主族元素都有最高正价,且都等于该元素原子的最外层电子数5. 下列有关有机物的说法中不正确的是( )A、属于取代反应 B、分子式为的有机物属于卤代烃 C、苯的二氯取代物有三种结构 D、分子组成上相差一个或若干个原子团的有机物之间一定互为同系物6. 下列反应的离子方程式正确的是( )A、向氢氧化亚铁中加入足量的稀硝酸: B、泡沫灭火器原理: C、浓氨水中滴加少量硫酸铜溶液: D、澄清石灰水与过量反应:7. 用如图所示装置进行下列实验(尾气处理装置已省略),装置正确并能达到实验目的的是( )
D、氯化钾的电离方程式:
4. 根据元素周期表和元素周期律,判断下列叙述正确的是( )A、氢卤酸的酸性由强到弱的顺序: B、同周期第ⅡA族和第ⅢA族元素原子序数可能相差1、11、25 C、铁元素位于元素周期表中第四周期第ⅧA族 D、主族元素都有最高正价,且都等于该元素原子的最外层电子数5. 下列有关有机物的说法中不正确的是( )A、属于取代反应 B、分子式为的有机物属于卤代烃 C、苯的二氯取代物有三种结构 D、分子组成上相差一个或若干个原子团的有机物之间一定互为同系物6. 下列反应的离子方程式正确的是( )A、向氢氧化亚铁中加入足量的稀硝酸: B、泡沫灭火器原理: C、浓氨水中滴加少量硫酸铜溶液: D、澄清石灰水与过量反应:7. 用如图所示装置进行下列实验(尾气处理装置已省略),装置正确并能达到实验目的的是( )
选项
①中试剂
②中溶液
实验目的
A
浓硫酸、无水乙醇(沸石)
酸性高锰酸钾溶液
检验有乙烯气体生成
B
乙醇、乙酸、浓硫酸
氢氧化钠溶液
制取乙酸乙酯
C
Cu、浓硫酸
溴水
验证的还原性
D
澄清石灰水
验证的热稳定性
A、A B、B C、C D、D8. 下列说法正确的是( )A、石墨中的碳原子呈杂化,是混合型晶体 B、4.6 g乙醇分子中含有共价键数为(为阿伏加德罗常数) C、和结构相似,但硫化氢晶体中,一个周围有12个紧邻的分子,而冰中一个周围只有4个紧邻的分子 D、臭氧分子是非极性分子9. 室温下,下列各组离子在指定溶液中一定不能大量共存的是( )A、与铝粉反应放出的透明溶液:、 , 、 B、常温下,由水电离的的溶液:、、 , C、使石蕊试液显红色的溶液:、、、 D、含有大量的溶液: , 、、、10. 自然界中时刻存在着氮的转化,下图为分子在催化剂作用下发生一系列转化示意图。
下列叙述正确的是( )
A、 , 均属于氮的固定 B、使用催化剂a、b均可以提高单位时间内生成物的产量 C、催化剂a、b表面均发生了极性共价键的断裂 D、在催化剂a作用下,氮原子发生了氧化反应11. 0.1 mol/L 溶液的pH随温度的变化如图所示,下列说法正确的是( ) A、温度高于60℃时,pH变化主要受水的电离平衡移动的影响 B、常温下: C、常温下: D、升高温度,平衡逆向移动12. 负载有Pt和Ag的活性炭,可选择性去除实现废酸的纯化,其工作原理如图。下列说法正确的是( )
A、温度高于60℃时,pH变化主要受水的电离平衡移动的影响 B、常温下: C、常温下: D、升高温度,平衡逆向移动12. 负载有Pt和Ag的活性炭,可选择性去除实现废酸的纯化,其工作原理如图。下列说法正确的是( ) A、Ag作原电池正极 B、电子由Ag经活性炭流向Pt C、Pt表面发生的电极反应: D、每消耗标准状况下11.2 L的 , 最多去除1 mol Cl-
A、Ag作原电池正极 B、电子由Ag经活性炭流向Pt C、Pt表面发生的电极反应: D、每消耗标准状况下11.2 L的 , 最多去除1 mol Cl-二、填空题
-
13. 太阳能电池的发展已经进入了第三代,即铜钢镓硒CIGs(CIS中掺入Ga)等化合物薄膜太阳能电池以及薄膜Si系太阳能电池。(1)、Si的原子结构示意图为 , 基态Cu原子的价电子排布式为。(2)、硒(Se)为第四周期元素,相邻的元素有砷(As)和溴(Br),则3种元素的第一电离能从大到小顺序为(用元素符号表示)。(3)、硫和碲与硒位于同主族,其简单氢化物和中,分解温度较高的是;键角较大的是 , 其原因是。(4)、β-MnSc的晶胞结构如图所示:

①β-MnSe中Mn的配位数为。
②若该晶体的晶胞参数为apm,阿伏加德罗常数的值为 , β-MnSe的密度g·cm(列出表达式即可)。
14. 酮基布洛芬片是用于治疗各种关节肿痛以及牙痛、术后痛等的非处方药。其合成路线如图所示: (1)、A的化学名称为。(2)、B的分子式为。(3)、酮基布洛芬中官能团的名称为。(4)、写出C的结构简式:。(5)、写出D生成E的化学方程式:。(6)、H为酮基布洛芬的同分异构体,其分子结构中含有
(1)、A的化学名称为。(2)、B的分子式为。(3)、酮基布洛芬中官能团的名称为。(4)、写出C的结构简式:。(5)、写出D生成E的化学方程式:。(6)、H为酮基布洛芬的同分异构体,其分子结构中含有 的酯类化合物,写出任意一种H的结构简式。 (7)、参照上述合成路线,以
的酯类化合物,写出任意一种H的结构简式。 (7)、参照上述合成路线,以 和苯为原料(试剂任选),设计制备
和苯为原料(试剂任选),设计制备 的一种合成路线。 15. 氨基甲酸铵()是一种白色固体,易溶于水和乙醇,难溶于。易分解、极易水解,可用作肥料、灭火剂、洗涤剂等。实验室用下图所
的一种合成路线。 15. 氨基甲酸铵()是一种白色固体,易溶于水和乙醇,难溶于。易分解、极易水解,可用作肥料、灭火剂、洗涤剂等。实验室用下图所示装置制备氨基甲酸铵,已知有关反应原理:
 (1)、仪器E的名称为。(2)、装置F用于制备合成所需的原料气,写出实验室利用F制取该气体的化学反应方程式:。(3)、装置C、E中所盛的药品分别是、。(4)、装置D采用的是冰水浴,其原因是。(5)、如果将D中连接气球的导管改连装置G,则G装置能控制原料气按化学计量数充分反应。若反应初期观察到G装置内浓硫酸中产生气泡,应该(填“加快”、“减慢”或“不改变”)产生氨气的流速;此外,装置G还能(用字母选项填空)。
(1)、仪器E的名称为。(2)、装置F用于制备合成所需的原料气,写出实验室利用F制取该气体的化学反应方程式:。(3)、装置C、E中所盛的药品分别是、。(4)、装置D采用的是冰水浴,其原因是。(5)、如果将D中连接气球的导管改连装置G,则G装置能控制原料气按化学计量数充分反应。若反应初期观察到G装置内浓硫酸中产生气泡,应该(填“加快”、“减慢”或“不改变”)产生氨气的流速;此外,装置G还能(用字母选项填空)。A.吸收尾气中的氨气,防止污染
B.防倒吸
C.防止空气中的水蒸气进入反应器
(6)、已知氨基甲酸铵遇水可完全水解为碳酸氢铵,现取长期存放的样品4.69 g(内含杂质),用足量石灰水处理后,使样品中碳元素完全转化为碳酸钙,过滤、洗涤、干燥测得质量为6 g。求样品中氨基甲酸铵的质量分数为(计算结果保留2位有效数字)。
16. 氮及其化合物在工农业生产中有着重要应用,减少氮的氧化物在大气中的排放是环境保护的重要内容之一。(1)、Ⅰ.和完全反应,每生成0.1 mol NO时,吸收8.9 kJ的热量,写出该反应的热化学方程式。又知,一定条件下,用催化还原可消除NO污染。
kJ⋅mol
kJ⋅mol
则 kJ⋅mol。
(2)、一定温度下,向一体积不变的密闭容器中加入适量的和NO,发生上述反应,下列条件能判断该反应到达平衡状态的有____(填序号)。A、混合气体的平均相对分子质量不变 B、 C、单位时间里有4n mol断开同时有4n mol 断开 D、混合气体的压强不变 E、混合气体的密度不变(3)、80℃时,将0.40 mol ;气体充入2 L已经抽空的固定容积的密闭容器中发生反应 , 隔一段时间对该容器内的物质进行分析,得到如下数据:时间
0
20
40
60
80
100
/mol
0.40
a
0.20
c
d
e
/mol
0.00
0.24
b
0.52
0.60
0.60
①计算:mol。
②平衡后,向该容器中再充入0.2 mol 气体,平衡向移动。(填“正反应方向”或“逆反应方向”)。
(4)、Ⅱ.利用如图所示原理去除NO。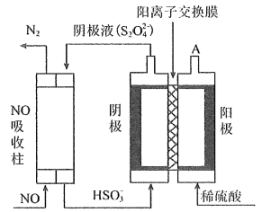
基态N原子中,电子占据的最高能级为能级,该能级轨道的形状为。电解池中阴极反应式为。