贵州省黔东南州从江县停洞中学2023-2024学年九年级下学期学期2月质量监测九年级化学试卷
试卷更新日期:2024-03-13 类型:月考试卷
一、选择题(本题共7小题,每小题2分,共14分,每小题只有一个选项符合题意)
-
1. 生活中的下列常见物质不属于溶液的是( )A、牛奶 B、生理盐水 C、苏打水 D、碘酒2. 从植物“地不容”中提取千金藤素,需用到5%的Na2CO3溶液。若配制100 g该溶液,需要称取Na2CO3的质量为( )A、95 g B、90 g C、20 g D、5 g3. 下列属于乳化现象的是( )A、碘溶于酒精中 B、用汽油洗去机器上的油污 C、用洗洁精洗去碗上的油污 D、用水洗去衣服上的污渍4. 下列有关水与溶液的说法错误的是( )A、电解水时,负极产生的气体是氢气 B、饱和溶液就是不能再溶解任何物质的溶液 C、溶液是均一、稳定的混合物 D、天然淡水生产自来水需要经过沉淀、过滤、杀菌消毒等净化过程5. 不同温度下KNO3的溶解度如下表所示。下列说法正确的是( )
温度/℃
20
30
40
溶解度/g
31.6
45.8
63.9
A、20 ℃时,100 g KNO3饱和溶液中溶质质量为31.6 g B、30 ℃时,100 g KNO3饱和溶液的溶质质量分数为45.8% C、30 ℃时,将50 g KNO3放入100 g水中得到150 g溶液 D、40 ℃时,100 g水中最多溶解63.9 g KNO36. 氯化铵、硫酸钠两种物质的溶解度曲线如图所示,下列有关说法正确的是( )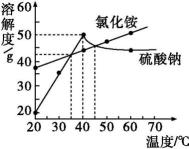 A、40 ℃时,100 g 硫酸钠饱和溶液中含硫酸钠50 g B、两种物质的溶解度都随温度的升高不断增大 C、60 ℃时,两种物质的饱和溶液中,硫酸钠溶液的溶质质量分数低 D、将60 ℃时硫酸钠的不饱和溶液变成饱和溶液,最好采用冷却热饱和溶液的方法7. 依据下列20 ℃时的实验和数据回答。已知20 ℃时,NaCl和NaNO3的溶解度分别为36 g 和88 g 。
A、40 ℃时,100 g 硫酸钠饱和溶液中含硫酸钠50 g B、两种物质的溶解度都随温度的升高不断增大 C、60 ℃时,两种物质的饱和溶液中,硫酸钠溶液的溶质质量分数低 D、将60 ℃时硫酸钠的不饱和溶液变成饱和溶液,最好采用冷却热饱和溶液的方法7. 依据下列20 ℃时的实验和数据回答。已知20 ℃时,NaCl和NaNO3的溶解度分别为36 g 和88 g 。
序号
①
②
③
④
⑤
固体种类
NaCl
NaCl
NaNO3
NaNO3
NaNO3
固体的质量/g
30
60
30
60
90
水的质量/g
100
100
100
100
100
下列关于①~⑤所得溶液的说法不正确的是( )
A、溶质质量:①<② B、溶液质量:②<④ C、溶质质量分数:①=③ D、⑤中溶质与溶剂的质量比为9∶10二、非选择题(本题共7小题,共46分)
-
8. 用化学式填写下列表格。
溶液
碳酸钠溶液
高锰酸钾溶液
碘酒
食盐水
溶质
KMnO4
溶剂
H2O
9. 如图是a、b、c三种固体物质的溶解度曲线。请结合图示回答下列问题: (1)、P点的含义是。(2)、t1℃时,a、b、c三种物质的溶解度由大到小的关系是(用“>”“<”或“=”表示)。(3)、t2℃时,把50 g a放入50 g水中,充分溶解后,得到的a的溶液的质量为g。(4)、t1 ℃时,a的饱和溶液的溶质质量分数为(保留小数点后一位),将该饱和溶液变为不饱和溶液,可采取的措施有(写一种)。(5)、a的固体中混有了少量的c物质,分离提纯a的操作:配成高温下的a的饱和溶液、、过滤、洗涤、干燥。10. 水和溶液在生产、生活中起着重要的作用。请回答下列问题。(1)、下列各种“水”中,属于纯净物的是____(填字母)。A、矿泉水 B、自来水 C、蒸馏水 D、冰水共存物(2)、保持水的化学性质的最小粒子是(填名称,下同),在通电分解水的过程中保持不变的粒子是。(3)、某同学做了在常温下将碘分别在水和汽油中分散的实验:在两支试管中各加入1~2小粒碘,然后分别加入5 mL水、5 mL无色溶剂汽油,振荡,静置。观察到的现象如下表。
(1)、P点的含义是。(2)、t1℃时,a、b、c三种物质的溶解度由大到小的关系是(用“>”“<”或“=”表示)。(3)、t2℃时,把50 g a放入50 g水中,充分溶解后,得到的a的溶液的质量为g。(4)、t1 ℃时,a的饱和溶液的溶质质量分数为(保留小数点后一位),将该饱和溶液变为不饱和溶液,可采取的措施有(写一种)。(5)、a的固体中混有了少量的c物质,分离提纯a的操作:配成高温下的a的饱和溶液、、过滤、洗涤、干燥。10. 水和溶液在生产、生活中起着重要的作用。请回答下列问题。(1)、下列各种“水”中,属于纯净物的是____(填字母)。A、矿泉水 B、自来水 C、蒸馏水 D、冰水共存物(2)、保持水的化学性质的最小粒子是(填名称,下同),在通电分解水的过程中保持不变的粒子是。(3)、某同学做了在常温下将碘分别在水和汽油中分散的实验:在两支试管中各加入1~2小粒碘,然后分别加入5 mL水、5 mL无色溶剂汽油,振荡,静置。观察到的现象如下表。编号
溶剂
溶质
现象
A
水
碘
试管底部有固体,液体呈淡黄色
B
汽油
碘
试管底部无固体,液体呈紫红色
①实验目的是。
②将试管B中的液体密封放置一段时间后,不会出现浑浊现象,为什么?。
(4)、如图是几种固体物质的溶解度曲线。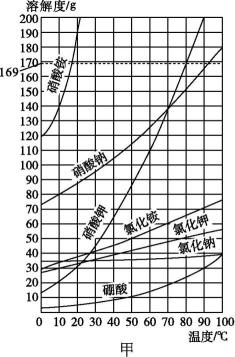
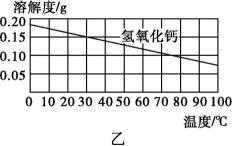
①根据图甲、图乙分析,固体物质的溶解度随温度的变化有什么规律,完成填空:少数固体物质的 , 如氯化钠;极少数固体物质的 , 如氢氧化钙。
②80 ℃时,将200 g KNO3固体放入100 g水中,充分溶解后,所得溶液的质量为g。
③KNO3中混有少量的NaCl,可用的方法提纯KNO3。
11. 结合下表中氯化钠的溶解度回答下列问题。温度/ ℃
0
10
20
30
40
50
溶解度/g
35.7
35.8
36.0
36.3
36.6
37.0
(1)、氯化钠属于(填“易溶”“可溶”“微溶”或“难溶”)物质。(2)、30 ℃时,氯化钠的溶解度为g。(3)、从表中数据发现氯化钠溶解度的主要特点是。(4)、从食盐水中得到食盐固体,一般采用的方法是结晶法。(5)、如果有358 g氯化钠,10 ℃时最少需用g水才能完全溶解。(6)、20 ℃时,将20 g食盐放入50 g水中,搅拌溶解,所得溶液中溶质的质量分数为(结果精确至0.1%)。12. 下表是氯化钠和硝酸钾在不同温度下的溶解度(假设硝酸钾与氯化钠同时溶解在水中时各自的溶解度不变,实验过程中水分损失忽略不计)。温度/ ℃
0
20
40
60
80
100
溶解
度/g
KNO3
13.3
31.6
63.9
110.0
169.0
246.0
NaCl
35.7
36.0
36.6
37.3
38.4
39.8
(1)、硝酸钾和氯化钠的溶解度相等时的温度范围是____(填字母)。A、0~20 ℃ B、20~40 ℃ C、40~60 ℃ D、60~80 ℃(2)、20 ℃时,将20 g KNO3放入50 g 水中,充分搅拌,所得溶液的质量是g。(3)、在80 ℃的100 g 水中溶解NaCl和KNO3 , 进行如图实验,已知溶液a中的硝酸钾恰好饱和。
①操作1的名称是。x=g,固体c的成分是。
②对整个实验过程分析正确的是(填字母)。
A.40~60 ℃开始析出晶体
B.氯化钠在整个过程中一直保持不饱和状态
C.上述方法不能将氯化钠和硝酸钾完全分离
D.原溶液直接冷却热饱和溶液,析出硝酸钾的质量不变
13. 某化学兴趣小组的同学对溶解过程中的能量变化和溶液配制进行探究。探究一:溶解过程中的能量变化
如图所示,同学们设计了不同的实验方案进行探究:
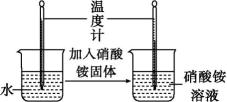
实验一 硝酸铵的溶解

实验二 氢氧化钠的溶解
(1)、实验一中的硝酸铵溶解后,溶液温度(填“升高”“降低”或“不变”)。(2)、实验二所加试剂及用量如图,将分液漏斗中的水全部加入试管后,立即关闭分液漏斗的活塞,此时观察到U形管的液面左低右高,由此小明得出“氢氧化钠溶于水时放出热量”的结论,你是否同意小明的结论?(填“同意”或“不同意”),写出你的理由:。(3)、探究二:溶液的配制如图是配制50 g溶质质量分数为10%的氯化钠溶液的有关操作示
意图:
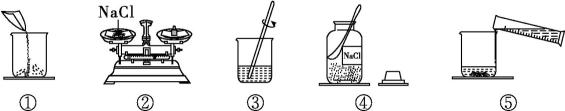
需要称取氯化钠的质量是g,称量时出现了指针偏向右盘的现象,接下来的操作是。
(4)、量取所需的水时,应该选择(填“10 mL”“50 mL”或“100 mL”)的量筒,读数时视线应该与保持水平。
(5)、配制氯化钠溶液的正确顺序是(填序号),步骤③中玻璃棒的作用是。(6)、在配制氯化钠溶液时,会使氯化钠的溶质质量分数偏大的是____(填字母)。A、图④中的氯化钠含有杂质 B、图②中的天平砝码生锈 C、图①中的食盐撒落在烧杯外 D、图⑤中量筒内的水洒落在烧杯外14. 某实验探究小组为了测定实验室一瓶稀硫酸中溶质的质量分数,他们用铜锌合金和稀硫酸完成了如图所示的实验。 (1)、反应生成氢气的质量为g。(2)、该瓶稀硫酸中溶质的质量分数是多少?
(1)、反应生成氢气的质量为g。(2)、该瓶稀硫酸中溶质的质量分数是多少?