辽宁省阜新市太平区2023-2024学年九年级上学期期末化学试题
试卷更新日期:2024-03-12 类型:期末考试
一、选择题(共10分
-
1. 学校开设的劳动课安排的下列活动中,主要发生化学变化的是( )A、修剪盆栽 B、制作木雕 C、烧制瓷器 D、整理桌椅2. 下列化学用语表示两个分子的是( )A、O2- B、2O3 C、SO2 D、2O3. 下列有关硬水性质实验的操作,正确的是( )A、
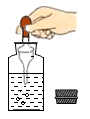 取样品
B、
取样品
B、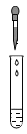 滴加肥皂水
C、
滴加肥皂水
C、 振荡
D、
振荡
D、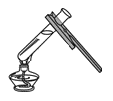 加热水样
4. 下列有关空气的说法错误的是( )A、空气是一种宝贵的资源 B、空气中含有稀有气体 C、空气中的氧气极易溶于水 D、空气中氮气的体积分数最大5. 科学家对人类文明和社会可持续发展作出了重要贡献。下列选项正确的是( )A、拉瓦锡编制了元素周期表 B、门捷列夫提出了近代原子学说 C、道尔顿确定了空气的组成 D、屠呦呦因研究青蒿素获诺贝尔奖6. 在一次家庭小实验中,当点燃装有半杯水的纸杯时,发现水面以下部分没有燃烧,其主要原因是( )
加热水样
4. 下列有关空气的说法错误的是( )A、空气是一种宝贵的资源 B、空气中含有稀有气体 C、空气中的氧气极易溶于水 D、空气中氮气的体积分数最大5. 科学家对人类文明和社会可持续发展作出了重要贡献。下列选项正确的是( )A、拉瓦锡编制了元素周期表 B、门捷列夫提出了近代原子学说 C、道尔顿确定了空气的组成 D、屠呦呦因研究青蒿素获诺贝尔奖6. 在一次家庭小实验中,当点燃装有半杯水的纸杯时,发现水面以下部分没有燃烧,其主要原因是( ) A、纸杯着火点变低 B、温度低于着火点 C、与氧气接触面太小 D、纸杯不是可燃物7. 研究发现千金藤素(C37H38N2O6)可抑制某些冠状病毒在细胞中的复制。下列关于千金藤素的说法正确的是( )A、属于混合物 B、含有氮分子 C、由四种元素组成 D、氢元素的质量分数最小8. 化学让生活更美好。下列说法正确的是( )A、制糖工业中用活性炭脱色,利用的是其吸附性 B、氦气通电发出粉红色的光,发生的是化学变化 C、用干冰营造舞台意境时,看到的白雾是二氧化碳气体 D、硬水软化后口感更好,因煮沸时除去了硬水中的所有杂质9. 阜新被称为“玛瑙之都”,玛瑙的主要成分是二氧化硅,部分玛瑙还可能包含金属元素如钴等。如图是钻元素在元素周期表中的相关信息,下列说法正确的是( )
A、纸杯着火点变低 B、温度低于着火点 C、与氧气接触面太小 D、纸杯不是可燃物7. 研究发现千金藤素(C37H38N2O6)可抑制某些冠状病毒在细胞中的复制。下列关于千金藤素的说法正确的是( )A、属于混合物 B、含有氮分子 C、由四种元素组成 D、氢元素的质量分数最小8. 化学让生活更美好。下列说法正确的是( )A、制糖工业中用活性炭脱色,利用的是其吸附性 B、氦气通电发出粉红色的光,发生的是化学变化 C、用干冰营造舞台意境时,看到的白雾是二氧化碳气体 D、硬水软化后口感更好,因煮沸时除去了硬水中的所有杂质9. 阜新被称为“玛瑙之都”,玛瑙的主要成分是二氧化硅,部分玛瑙还可能包含金属元素如钴等。如图是钻元素在元素周期表中的相关信息,下列说法正确的是( ) A、钴的元素符号为CO B、钴原子中的质子数为27 C、钴的原子序数为58 D、钴的相对原子质量是3210. 从不同角度认识如图中的反应,其中错误的是( )
A、钴的元素符号为CO B、钴原子中的质子数为27 C、钴的原子序数为58 D、钴的相对原子质量是3210. 从不同角度认识如图中的反应,其中错误的是( ) A、宏观描述:氢气在氯气中燃烧生成氯化氢 B、微观解析:反应前后原子种类不变 C、符号描述:H2+Cl2=2HCl D、反应类型:化合反应
A、宏观描述:氢气在氯气中燃烧生成氯化氢 B、微观解析:反应前后原子种类不变 C、符号描述:H2+Cl2=2HCl D、反应类型:化合反应二、非选择题(共40分
-
11. 阅读下列短文并回答问题。
氢在太阳中的核聚变放出大量光和热,是太阳能的来源,掌握可控核聚变技术对人类未来文明发展至关重要。2021年5月,中科院“人造太阳”EAST实验装置创造了氘、氚核聚变在1.2亿摄氏度下运行101秒的新纪录,为世界核聚变研究的发展做出巨大贡献。
氢气是高热值清洁燃料,目前主要通过电解水和天然气重整的方法获取氢气,其中天然气重整制氢的一种原理为:CH4+H2OCO+3H2 , CO+H2OCO2+H2 , 氢氧燃料电池已被用作汽车驱动电源,H2和O2在电池内部(含有H2SO4或KOH等物质的溶液)发生反应产生电能。另外,CH4、C2H5OH等也可用作燃料电池的燃料,它们在燃料电池中的反应本质上与它们在O2中的燃烧相同,
原子名称
质子数
中子数
核外电子数
氘(dao)
1
1
1
氚(chuan)
1
2
X
(1)、表中x数值应为 , 氘、氚原子都属于氢元素的原因是相同。(2)、上述短文出现的物质中,属于氧化物的是(填化学式,至少写两种)。(3)、电解18gH2O理论上能获得gH2。氢气属于清洁燃料的原因是。(4)、上述天然气重整制氢原理的两个反应中,化合价保持不变的元素是。(5)、燃料电池工作时H2SO4溶液中起导电作用之一的是硫酸根离子,其符号表示为。(6)、CH4在O2中充分燃烧的化学方程式是。12. 航天员王亚平在“天宫课堂”中介绍了空间站中的生活,在轨演示了水球变气球等炫酷的实验。(1)、I.“天宫”中水和氧气的最大化利用是生活保障的重要措施。如图是空间站资源再利用模拟图。
在“水净化系统"中,利用活性炭的吸附性可以除去水中的;高分子膜可以除去水中大分子杂质,与实验室常用的操作原理相同。(2)、“水电解系统”中产生氧气的电极应接在电源的(选填“正"或“负”)极。(3)、“萨巳蒂尔反应器”中,在一定条件下可以除去CO2 , 该反应的化学方程式是。(4)、II.在“天宫课堂"中王亚平将少量蓝色颜料注入水球,很快整个水球变成蓝色。然后将泡腾片放入水球中,产生了大量气泡向四周扩散,气泡充满整个水球。
蓝色颜料能让整个水球全部变蓝,是因为颜料分子具有的特征。(5)、气泡是泡腾片中含有的柠檬酸(具有酸性)和碳酸氢钠溶于水后发生反应生成的二氧化碳形成的。在实验室中制取该气体一般用的药品是 , 发生反应的化学方程式为。(6)、如果在空间站失重状态下收集制得的O2可选用下列装置中的(填序号),如果在我们学校实验室中收集制得的O2 , 通常选用下列装置中的(填序号)。 13. 碳元素是人类接触和利用最早的元素之一。由碳元素组成的单质可分为无定形碳、过渡态碳和晶形碳三大类,如图1。
13. 碳元素是人类接触和利用最早的元素之一。由碳元素组成的单质可分为无定形碳、过渡态碳和晶形碳三大类,如图1。
石墨是制铅笔芯的原料之一,在16世纪被发现后,曾被误认为是含铅的物质。直到18世纪,化学家将石量与KNO3共熔后产生CO2 , 才确定了它是含碳的物质。
碳纤维既有碳材料的固有本质特性,又有纺织纤维的柔软可加工性,综合性能优异。目前,我国已形成碳纤维生产、碳纤维复合材料成型、应用等产业链,碳纤维复合材料应用领域分布如图2。

科学界不断研发出新型碳材料,碳气凝胶就是其中一种。碳气凝胶具有优良的吸附性能,在环境净化中发挥重要作用。我国科研人员在不同温度下制备了三种碳气凝胶样品,比较其对CO2的选择性吸附性能。他们在不同压强下测定了上述样晶对混合气体中CO2吸附的选择性值,实验结果如图3。

图中选择性值越高,表明碳气凝胶对CO2的选择性吸附性能越好。
随着科学技术的发展,碳材料的潜能不断被激发,应用领域越来越广泛。依据所学知识并参考文章内容,回答下列问题。
(1)、①碳元素能组成多种单质,下列关于碳单质的说法中,正确的是。A.硬度都很大 B.C60是原子构成的
C.都是黑色固体 D.常温下化学性质都不活泼
②金刚石属于(填字母序号)。石墨在一定条件下转化为金刚石是改变了其。
A.无定形碳 B.过渡态碳 C.晶形碳
(2)、①石量与KNO3共熔,能发生如下反应,配平该反应的化学方程式,内需填的数值分别为。5C+4KNO3K2O+CO2↑+N2↑
②从元素守恒角度说明石量是一种含碳物质的理由。
(3)、由图2可知,我国碳纤维复合材料应用占比最高的领域是。(4)、判断下列说法是否正确(填“对”或“错”)。①石墨是一种含铅的物质。
②碳材料具有广阔的应用和发展前景。
(5)、对比图3中三条曲线,得到的实验结论是。14. 某校化学兴趣小组同学在学习完“碳和碳的氧化物”后,在实验室中做了如图实验,请你一起参与完成。I.通过实验研究一氧化碳和氧化铜的反应,其操作步骤及观察到的现象如图:

步骤1:连接装置并____。
步骤2:按图甲所示向双具支试管内加入木炭粉和氧化铜,用向上排空气法使双具支试管内集满二氧化碳后塞上带有导管和瘪气球的橡皮塞。
步骤3:按图乙所示将双具支试管固定在铁架台上,井使木炭粉平铺于试管底部;酒精喷灯加热氧化铜一段时间,未观察到明显现象。
步骤4:将酒精喷灯移至木炭粉处,加热一段时间,观察到气球明显胀大:再次将酒精喷灯移至氧化铜处,加热一段时间,观察到鼎色粉末变为紫红色固体。
(1)、将步骤1补充完整。步骤2中,可用燃著的木条检验二氧化碳是否集满,燃着的木条应(填“放置在双具支试管口”或“伸入到双具支试管内”)。(2)、该小组设计步骤3的目的是。(3)、实验中能表明一氧化碳具有还原性的实验现象是。反应的化学方程式为;本实验中(填物质名称)也具有还原性。(4)、图乙装置中气球的作用是。(5)、如图是实验室中常用的仪器:
①仪器A的名称是。
②从图中选择合适的仪器组装一套CO2发生装置,要求添加盐酸无需拆开装置,需要用到的仪器有哪些?(填字母)。
(6)、该小组的实验设计和数据记录如表。每个实验均在反应开始后,就立即用持水法连续收集多瓶CO2表中“—”表示气泡太少,不再收集。序号
反应物
收集每瓶气体所用时间(单位:秒)
盐酸浓度
盐酸体积
大理石形状
第1瓶
第2瓶
第3瓶
第4瓶
第5瓶
第6瓶
实验1
10%
70mL
小颗粒
8
9
10
12
14
19
实验2
块状
11
12
15
17
21
23
实验3
15%
70mL
小颗粒
10
12
13
15
17
26
实验4
块状
t
14
16
19
22
24
实验5
5%
70mL
小颗粒
14
18
19
32
63
实验6
块状
20
31
59
①该小组研究了哪些因素对反应快慢的影响?。
②为了分析浓度对反应快慢的影响,可对比表中实验。
A.2和3 B.2和4 C.4和5 D.1和6
③根据实验数据反映出的规律,表中数值(的合理范围是<t<。
(7)、该小组在反应开始后立即收集第1瓶气体,你认为该做法合理吗?说出你的观点并阐述理由。