北京市房山区2023-2024学年高二上学期期末考试化学试卷
试卷更新日期:2024-03-12 类型:期末考试
一、部分共14小题,每小题3分,共42分。在每小题列出的四个选项中,选出最符合题目要求的一项。
-
1. 关于下列现象的分析不合理的是( )

醋酸溶液能导电

氧炔焰切割金属

五彩缤纷的烟花

铸钢模具须提前干燥
A.与盐类水解有关
B.与乙炔和氧气反应放热有关
C.与核外电子的跃迁有关
D.与铁与水能发生反应有关
A、A B、B C、C D、D2. 下列化学用语书写不正确的是( )A、F的原子结构示意图: B、NaCl的电子式:
B、NaCl的电子式: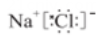 C、基态铬原子(24Cr)的价层电子排布式:3d44s2
D、基态氧原子的轨道表示式:
C、基态铬原子(24Cr)的价层电子排布式:3d44s2
D、基态氧原子的轨道表示式: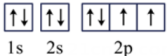 3. 下列措施是为了增大化学反应速率的是( )A、用锌粒代替镁粉制备氢气 B、将食物放进冰箱避免变质 C、自行车车架镀漆避免生锈 D、工业合成氨时加入催化剂4. 融雪剂可以降低冰雪融化的温度,利于道路通畅,通常分为氯盐类的无机融雪剂和非氯盐类的有机融雪剂两类。氯化钠、醋酸钾两种融雪剂相同条件下融冰量和对碳钢(铁碳合金)腐蚀速率图像如下所示。回答问题。
3. 下列措施是为了增大化学反应速率的是( )A、用锌粒代替镁粉制备氢气 B、将食物放进冰箱避免变质 C、自行车车架镀漆避免生锈 D、工业合成氨时加入催化剂4. 融雪剂可以降低冰雪融化的温度,利于道路通畅,通常分为氯盐类的无机融雪剂和非氯盐类的有机融雪剂两类。氯化钠、醋酸钾两种融雪剂相同条件下融冰量和对碳钢(铁碳合金)腐蚀速率图像如下所示。回答问题。图1 不同融雪剂融冰量比较
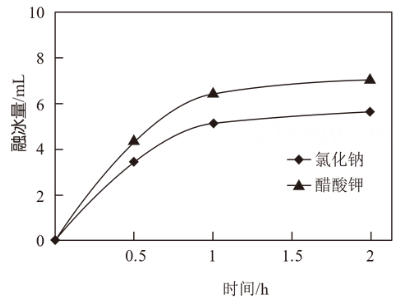 图2 不同盐溶液对碳钢腐蚀比较
图2 不同盐溶液对碳钢腐蚀比较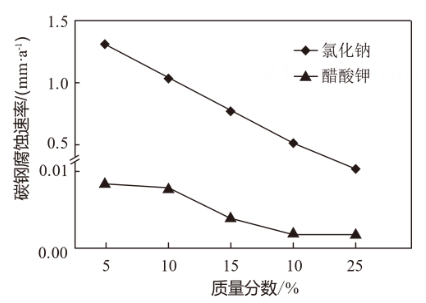 (1)、下列关于醋酸钾(CH3COOK)的说法中,不正确的是( )A、是强电解质 B、电离方程式为CH3COOK=CH3COO-+K+ C、使用CH3COOK融雪后,附近水土酸碱性不受影响 D、由图1可知,与氯化钠相比醋酸钾融冰量高,是更加高效的融雪剂(2)、结合图2分析下列关于碳钢(铁碳合金)腐蚀的说法中,不正确的是( )A、盐类融雪剂能够造成碳钢的腐蚀 B、碳钢腐蚀的负极反应为Fe-2e-=Fe2+ C、融雪剂浓度越大,碳钢腐蚀速率越快 D、寻找环保、高效的融雪剂是新型融雪剂的研究方向5. 下列离子方程式与所给事实不相符的是( )A、Cl2制备84消毒液(主要成分是NaClO):Cl2 + 2OH- = Cl- + ClO- + H2O B、食醋去除水垢中的CaCO3:CaCO3 + 2H+ = Ca2+ + H2O + CO2↑ C、利用覆铜板制作印刷电路板:2Fe3+ + Cu = 2Fe2+ + Cu2+ D、Na2S去除废水中的Hg2+:Hg2+ += HgS↓6. 下图表示的是元素的某种性质(X)随原子序数的变化关系,则X可能是( )
(1)、下列关于醋酸钾(CH3COOK)的说法中,不正确的是( )A、是强电解质 B、电离方程式为CH3COOK=CH3COO-+K+ C、使用CH3COOK融雪后,附近水土酸碱性不受影响 D、由图1可知,与氯化钠相比醋酸钾融冰量高,是更加高效的融雪剂(2)、结合图2分析下列关于碳钢(铁碳合金)腐蚀的说法中,不正确的是( )A、盐类融雪剂能够造成碳钢的腐蚀 B、碳钢腐蚀的负极反应为Fe-2e-=Fe2+ C、融雪剂浓度越大,碳钢腐蚀速率越快 D、寻找环保、高效的融雪剂是新型融雪剂的研究方向5. 下列离子方程式与所给事实不相符的是( )A、Cl2制备84消毒液(主要成分是NaClO):Cl2 + 2OH- = Cl- + ClO- + H2O B、食醋去除水垢中的CaCO3:CaCO3 + 2H+ = Ca2+ + H2O + CO2↑ C、利用覆铜板制作印刷电路板:2Fe3+ + Cu = 2Fe2+ + Cu2+ D、Na2S去除废水中的Hg2+:Hg2+ += HgS↓6. 下图表示的是元素的某种性质(X)随原子序数的变化关系,则X可能是( ) A、元素原子的价电子数 B、元素的原子半径 C、元素的电负性 D、元素的第一电离能7. 一定条件下的密闭容器中发生反应:C2H6(g) C2H4 (g) +H2(g) ΔH > 0。达到平衡后升高反应温度,下列叙述不正确的是( )A、正、逆反应速率都增大 B、平衡向逆反应方向移动 C、C2H6的转化率增大 D、化学平衡常数增大8. 下列事实能用平衡移动原理解释的是( )A、溶液中加入少量固体,促进分解 B、密闭烧瓶内的和的混合气体,受热后颜色加深 C、铁钉放入浓中,待不再变化后,加热能产生大量红棕色气体 D、锌片与稀反应过程中,加入少量固体,促进的产生9. 用0.100 0 mol·L−1 HCl溶液滴定未知浓度的NaOH溶液。下列说法不正确的是( )A、锥形瓶盛装未知浓度的NaOH溶液前必须保持干燥 B、使用滴定管前,要先检查活塞是否漏水,在确保不漏水后方可使用 C、酸式滴定管在盛装0.100 0 mol·L−1 HCl溶液前要用该溶液润洗2~3次 D、用酚酞作指示剂,溶液颜色从粉红色刚好变为无色,且半分钟内不褪色,即达到滴定终点10. 相同温度下,在三个密闭容器中分别进行反应:H2(g) + I2(g) 2HI(g)。达到化学平衡状态时,相关数据如下表。下列说法不正确的是( )
A、元素原子的价电子数 B、元素的原子半径 C、元素的电负性 D、元素的第一电离能7. 一定条件下的密闭容器中发生反应:C2H6(g) C2H4 (g) +H2(g) ΔH > 0。达到平衡后升高反应温度,下列叙述不正确的是( )A、正、逆反应速率都增大 B、平衡向逆反应方向移动 C、C2H6的转化率增大 D、化学平衡常数增大8. 下列事实能用平衡移动原理解释的是( )A、溶液中加入少量固体,促进分解 B、密闭烧瓶内的和的混合气体,受热后颜色加深 C、铁钉放入浓中,待不再变化后,加热能产生大量红棕色气体 D、锌片与稀反应过程中,加入少量固体,促进的产生9. 用0.100 0 mol·L−1 HCl溶液滴定未知浓度的NaOH溶液。下列说法不正确的是( )A、锥形瓶盛装未知浓度的NaOH溶液前必须保持干燥 B、使用滴定管前,要先检查活塞是否漏水,在确保不漏水后方可使用 C、酸式滴定管在盛装0.100 0 mol·L−1 HCl溶液前要用该溶液润洗2~3次 D、用酚酞作指示剂,溶液颜色从粉红色刚好变为无色,且半分钟内不褪色,即达到滴定终点10. 相同温度下,在三个密闭容器中分别进行反应:H2(g) + I2(g) 2HI(g)。达到化学平衡状态时,相关数据如下表。下列说法不正确的是( )实验
起始时各物质的浓度/(mol·L-1 )
平衡时物质的浓度/(mol·L-1 )
c(H2)
c(I2)
c(HI)
c(H2)
Ⅰ
0.01
0.01
0
0.008
Ⅱ
0.02
0.02
0
a
Ⅲ
0.02
0.02
0.04
A、该温度下,反应的平衡常数为0.25 B、实验Ⅱ达平衡时,a=0.016 C、实验Ⅲ开始时,反应向消耗H2的方向移动 D、达到化学平衡后,压缩三个容器的体积,平衡均不发生移动11. 回收利用工业废气中的CO2和SO2 , 实验原理示意图如下。
下列说法不正确的是( )
A、废气中SO2排放到大气中会形成酸雨 B、装置a中溶液的作用是吸收废气中的CO2和SO2 C、装置a中溶液显碱性的原因是HCO3-的水解程度大于HCO3-的电离程度 D、装置b中的总反应为12. “中国芯”的主要原料是单晶硅,“精炼硅”反应历程中的能量变化如下图所示。下列有关描述正确的是( )
 A、历程Ⅰ是吸热反应 B、历程Ⅱ发生了化学变化 C、历程Ⅲ的热化学方程式是:SiHCl3(l) + H2(g) = Si(s)+3HCl(g) ΔH=+238 kJ/mol D、实际工业生产中,粗硅变为精硅的过程无需外界能量供给13. 某实验小组研究经打磨的镁条与1 mol·L−1 NaHCO3溶液(pH≈8.4)的反应。室温时,用CO2传感器检测生成的气体,并测定反应后溶液的pH。实验如下表:
A、历程Ⅰ是吸热反应 B、历程Ⅱ发生了化学变化 C、历程Ⅲ的热化学方程式是:SiHCl3(l) + H2(g) = Si(s)+3HCl(g) ΔH=+238 kJ/mol D、实际工业生产中,粗硅变为精硅的过程无需外界能量供给13. 某实验小组研究经打磨的镁条与1 mol·L−1 NaHCO3溶液(pH≈8.4)的反应。室温时,用CO2传感器检测生成的气体,并测定反应后溶液的pH。实验如下表:实验装置
编号
锥形瓶中的
试剂
实验现象
锥形瓶内CO2的浓度变化
①
6.0 g 1 mol·L−1 NaHCO3溶液
有极微量气泡生成,15 min后测得溶液的pH无明显变化

②
6.0 g 1 mol·L−1 NaHCO3溶液和0.1g镁条
持续产生大量气泡(净化后可点燃),溶液中有白色浑浊生成。15 min后测得溶液的pH上升至9.0
③
6.0 g H2O(滴有酚酞溶液)和0.1 g镁条
镁条表面有微量气泡,一段时间后,镁条表面微红
下列说法不正确的是( )
A、由①可知,NaHCO3在溶液中可发生分解反应 B、由②可知,镁与NaHCO3溶液反应,生成的气体中有H2 C、对比②③可知,室温下,NaHCO3溶液中c(H+)大于水中c(H+) D、由②③推测,HCO3-可能对镁与H2O反应生成的Mg(OH)2覆膜有破坏作用二、本部分共6小题,共58分。
-
14. 锂(Li)元素在新能源领域应用广泛。(1)、基态Li原子的电子排布式是 。(2)、Li元素在周期表中的位置是(填写周期、族、区)。(3)、比较第一电离能的大到小:I1(Li) I1(Na)(填“>”、“=”或“<”),从原子结构的角度解释原因。(4)、碳酸锂(Li2CO3)是一种电池原料,其中所含元素的电负性从大到小的顺序是>>。15. 研究电解质在水溶液中的离子反应与平衡有重要的意义。(1)、常温下,用0.100 mol/L NaOH溶液滴定10 mL 0.100 mol/L CH3COOH溶液的滴定曲线如右图所示。a、b、c三点中:

①c(Na+) =c(CH3COO−)的点是.(填“a”、“b”或“c”,下同)。
②水的电离程度最大的点是 。
(2)、已知:25 ℃时CH3COOH、H2CO3和HClO的电离平衡常数:化学式
CH3COOH
H2CO3
HClO
电离平衡常数
(Ka)
1.75×10–5
Ka1=4.5×10–7
Ka2=4.7×10–11
4.0×10–8
①CH3COOH的电离平衡常数表达式Ka=。
②比较等物质的量浓度溶液的pH:pH(NaClO) pH(CH3COONa) (填“>”、“<”或“=”)。
③预测下列化学反应能够发生的是。
A.HClO + CH3COONa = CH3COOH + NaClO
B.CO2 + H2O + NaClO = NaHCO3 + HClO
C.2CH3COOH + Na2CO3 = 2CH3COONa + H2O+CO2
16. 镁基储氢材料MgH2具有储氢量高、成本低廉等优点,发展前景广阔。Ⅰ.MgH2热分解放出H2 , 反应的能量变化如图所示。
 (1)、写出MgH2热分解的热化学方程式。(2)、提高H2平衡产率的措施有(答1条即可)。(3)、Ⅱ.MgH2水解制备H2
(1)、写出MgH2热分解的热化学方程式。(2)、提高H2平衡产率的措施有(答1条即可)。(3)、Ⅱ.MgH2水解制备H2MgH2与H2O反应制备H2的化学方程式是。
(4)、资料:25℃时,有关物质的溶度积常数如下物质
Mg(OH)2
Ni(OH)2
Cu(OH)2
Ksp
5.6×10−12
5.5×10−16
2.2×10−20
①MgH2与H2O反应时,最初生成H2的速率很快,但随后变得缓慢,原因是。
②在水中加入优先与OH-结合的离子,能够避免①中现象发生,提升H2的制备效率。下列物质中,能达到此目的的是。
a.NaNO3 b.NiCl2 c.CuCl2
17. 改进工艺,降低能耗是氯碱工业发展的重要方向。(1)、写出氯碱工业原理的方程式。(2)、将氢燃料电站应用于氯碱工业,其示意图如下:
① a极为(填“正”或“负”)极。
② 甲装置中,Na+向极移动(填“a”或“b”)
③下列关于乙装置说法中,正确的是。
A.在c极区获得氯气
B.在d极区获得的产物,可供甲装置使用
C.当NaCl溶液浓度较低时,及时更换为精制饱和NaCl溶液,以保证生产效率
(3)、向乙装置中的阴极区通入O2 , 能够替代水中的H+获得电子,降低电解电压,减少电耗。写出O2在阴极区发生反应的电极反应式。(4)、杂质离子可造成交换膜损伤,导致OH−迁移至阳极区,对产品质量造成不良影响。请结合化学用语说明原因。18. 我国科学家用粗氢氧化高钴[主要含Co(OH)3]制备硫酸钴晶体(CoSO4•7H2O),其工艺流程如下。
已知:i.还原浸出液中的阳离子有:Co2+、H+、Fe2+和Ca2+等
ii.部分物质的溶度积常数如下(25℃)
物质
Ksp
CaF2
4.0×10−11
Fe(OH)3
2.8×10−39
iii.CoSO4•7H2O溶解度随温度升高而明显增大
(1)、氢氧化高钴溶于硫酸的化学方程式是。(2)、还原浸出Co2+时,理论上氧化性离子和还原性离子物质的量之比为。(3)、氧化沉铁后,浊液中铁离子浓度为 mol/L(此时25℃,溶液pH为4)。(4)、结合平衡移动原理解释“氟化沉钙”步骤加入过量NaF的原因。(5)、萃取后,经反萃取得到硫酸钴溶液。将硫酸钴溶液经操作,分离后得到硫酸钴晶体。(6)、用滴定法测定硫酸钴晶体中钴的含量,其原理和操作如下。在溶液中,用铁氰化钾将Co(Ⅱ)氧化为Co(Ⅲ),过量的铁氰化钾以Co(Ⅱ)标准液返滴定。反应的方程式为:Co2+ + [Fe(CN)6]3− = Co3+ + [Fe(CN)6]4−。
已知:铁氰化钾标准液浓度为c mol/L,Co(Ⅱ)标准液质量浓度为ρg/L。
取m g硫酸钴晶体,加水配成200 mL溶液,取20 mL待测液进行滴定,消耗V1 mL铁氰化钾标准液、V2 mL Co(Ⅱ)标准液。(Co的相对原子质量为59)
计算样品中钴含量ω=(以钴的质量分数ω计)。
19. 某实验小组探究Cu与Fe(NO3)3溶液的反应。取3 g 铜粉加入到100 mL 0.6 mol/L Fe(NO3)3溶液(用HNO3调pH=1)中,振荡、静置30分钟,铜粉减少,溶液呈棕绿色,未见有气泡产生。(1)、预测NO3-和Fe3+分别与Cu发生了反应,补充反应Ⅱ的离子方程式。反应 Ⅰ 3Cu + 2NO + 8H+ = 3Cu2+ + 2NO↑ + 4H2O
反应 Ⅱ 。
(2)、探究反应Ⅰ是否发生①设计实验:取3 g 铜粉加入到100 mL 溶液中,振荡、静置30分钟。
②若反应 Ⅰ能够发生,预计观察到的现象有。
实际现象不明显,借助传感器证明反应Ⅰ能够发生。
(3)、探究反应Ⅱ是否发生步骤1:取3 g 铜粉加入到100 mL 0.3 mol/L Fe2(SO4)3溶液(用H2SO4调pH=1)中,溶液迅速变为蓝绿色。
步骤2:取步骤1中上层清液,滴加少量KSCN溶液,出现白色浑浊,溶液变红,振荡后红色褪去。
①KSCN溶液的作用是 。
②已知,CuSCN是难溶于水的白色固体。结合平衡移动原理,解释步骤2中“溶液变红,振荡后红色褪去”的原因。
(4)、查阅资料可知,反应 Ⅰ和反应Ⅱ 的平衡常数分别为KⅠ=6.3×1062 和KⅡ=5×1014。请从化学反应速率和限度的角度简述对Cu与Fe(NO3)3溶液反应的认识。