黑龙江省哈尔滨市六校联考2023-2024学年高二上学期1月期末联考试题化学
试卷更新日期:2024-03-12 类型:期末考试
一、选择题(本大题共15小题,每小题3分,共计45分。在每小题列出的四个选项中,只有一项是符合题目要求的)
-
1. 下列表示氮原子的符号和图示中能反映能级差别和电子自旋状态的是( )A、
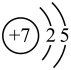 B、
C、
D、
B、
C、
D、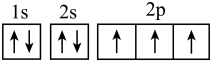 2. 下列溶液一定呈酸性的是( )A、含有的溶液 B、的溶液 C、的某电解质溶液 D、的溶液3. 图1和图2分别是1s电子的概率密度分布图和电子云轮廓图。下列有关说法正确的是( )
2. 下列溶液一定呈酸性的是( )A、含有的溶液 B、的溶液 C、的某电解质溶液 D、的溶液3. 图1和图2分别是1s电子的概率密度分布图和电子云轮廓图。下列有关说法正确的是( ) A、图1中的每个小黑点都表示1个电子 B、图1中的小黑点表示电子在核外所处的位置 C、图2表明1s轨道呈球形,有无数对称轴 D、图2表示1s电子只能在球体内出现4. 化学与生产、生活密切相关。下列说法错误的是( )A、氯化铵溶液可以除铁锈 B、刷牙用含氟牙膏可使牙齿更坚固 C、氯碱工业电解槽采用阴离子交换膜 D、铝盐与小苏打可以作泡沫灭火器药品5. 在一刚性密闭容器内发生反应 , 若内B减少了 , 则下列说法正确的是( )A、反应达到平衡时 B、容器内气体总密度不再改变是该反应达到平衡的标志 C、末时用B表示反应速率为 D、升高温度能加快反应速率主要是其使活化分子的能量明显增加6. 下列说法错误的是( )A、原子核外电子填充能级的顺序为 B、基态铁原子的价层电子排布式为 C、少数基态原子的核外电子排布不遵循构造原理 D、构造原理中的电子排布能级顺序,实质是各能级能量由低到高的顺序7. 下列实验设计或装置能达到实验目的的是( )
A、图1中的每个小黑点都表示1个电子 B、图1中的小黑点表示电子在核外所处的位置 C、图2表明1s轨道呈球形,有无数对称轴 D、图2表示1s电子只能在球体内出现4. 化学与生产、生活密切相关。下列说法错误的是( )A、氯化铵溶液可以除铁锈 B、刷牙用含氟牙膏可使牙齿更坚固 C、氯碱工业电解槽采用阴离子交换膜 D、铝盐与小苏打可以作泡沫灭火器药品5. 在一刚性密闭容器内发生反应 , 若内B减少了 , 则下列说法正确的是( )A、反应达到平衡时 B、容器内气体总密度不再改变是该反应达到平衡的标志 C、末时用B表示反应速率为 D、升高温度能加快反应速率主要是其使活化分子的能量明显增加6. 下列说法错误的是( )A、原子核外电子填充能级的顺序为 B、基态铁原子的价层电子排布式为 C、少数基态原子的核外电子排布不遵循构造原理 D、构造原理中的电子排布能级顺序,实质是各能级能量由低到高的顺序7. 下列实验设计或装置能达到实验目的的是( ) A、按甲的电路连接对反应塔进行防腐保护 B、用乙测定中和反应的反应热 C、用丙探究硫酸浓度对化学反应速率的影响 D、按丁设计锌铜“双液原电池”实现化学能持续转化为电能8. 锅炉水垢是一种安全隐患,为除去水垢中的 , 可先用溶液处理,很容易使之转化为 , 再用酸除去 , 下列说法错误的是( )A、 B、沉淀转化的难易与溶解度大小有关 C、转化反应的平衡常数 D、沉淀转化的实质是沉淀溶解平衡的移动9. 下表列出了某短周期元素的各级电离能数据(用、表示,单位为)。
A、按甲的电路连接对反应塔进行防腐保护 B、用乙测定中和反应的反应热 C、用丙探究硫酸浓度对化学反应速率的影响 D、按丁设计锌铜“双液原电池”实现化学能持续转化为电能8. 锅炉水垢是一种安全隐患,为除去水垢中的 , 可先用溶液处理,很容易使之转化为 , 再用酸除去 , 下列说法错误的是( )A、 B、沉淀转化的难易与溶解度大小有关 C、转化反应的平衡常数 D、沉淀转化的实质是沉淀溶解平衡的移动9. 下表列出了某短周期元素的各级电离能数据(用、表示,单位为)。……
R
740
1500
7700
10500
……
下列关于元素的判断中一定正确的是( )
A、R的最高正价为+3 B、R元素位于元素周期表中第IIA族 C、R元素的原子最外层共有4个电子 D、R元素基态原子的电子排布式为10. 银锌电池广泛用作各种电子仪器的电源,它的充电和放电过程可以表示为:。下列说法不正确的是( )A、该电池属于二次电池和碱性电池 B、电极是电池的负极,发生氧化反应 C、电池工作过程中,电解质溶液的浓度保持不变 D、充电时,电池的正极应与电源的正极相连11. 具有下列电子层结构的原子或离子,其对应元素一定属于同一周期的是( )A、两原子核外全部都是s电子 B、最外层电子排布式为的原子和最外层电子排布式为的离子 C、能级上只有一个空轨道的原子和能级上只有一个未成对电子的原子 D、原子核外M层上的s、p能级都充满电子,而能级上没有电子的原子和离子12. 如图为水的电离平衡曲线,下列说法正确的是( )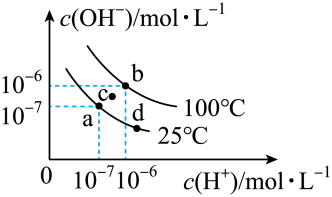 A、图中四点所对应的的大小关系: B、时,的溶液中, C、若d点为盐酸溶液,稀释该溶液可由d点变化到a点 D、时,向溶液中逐滴加入溶液,溶液中的值会逐渐增大13. 如图为阳离子交换膜法以石墨为电极电解饱和溶液的原理示意图。已知溶液从A口进料,含少量的水从B口进料,下列说法错误的是( )
A、图中四点所对应的的大小关系: B、时,的溶液中, C、若d点为盐酸溶液,稀释该溶液可由d点变化到a点 D、时,向溶液中逐滴加入溶液,溶液中的值会逐渐增大13. 如图为阳离子交换膜法以石墨为电极电解饱和溶液的原理示意图。已知溶液从A口进料,含少量的水从B口进料,下列说法错误的是( ) A、阳极发生氧化反应,有氧气生成 B、从E出口逸出的气体是 C、从D出口流出的是较浓的溶液 D、电路中转移电子时,阳极区有生成14. 在恒温、恒容,体积为的容器中发生下列反应: , T温度下的部分实验数据为:
A、阳极发生氧化反应,有氧气生成 B、从E出口逸出的气体是 C、从D出口流出的是较浓的溶液 D、电路中转移电子时,阳极区有生成14. 在恒温、恒容,体积为的容器中发生下列反应: , T温度下的部分实验数据为:0
50
100
150
4.00
2.50
2.00
2.00
下列说法错误的是:( )
A、时的转化率为50% B、内分解速率为 C、温度下的平衡常数为温度下的平衡常数为 , 若 , 则 D、T温度下的平衡常数为15. 科学家近年发明了一种新型Zn-CO2水介质电池。电池示意图如下,电极为金属锌和选择性催化材料,放电时,温室气体CO2被转化为储氢物质甲酸等,为解决环境和能源问题提供了一种新途径。下列说法不正确的是( )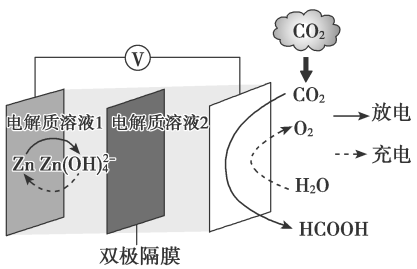 A、充电时,电池总反应为2=2Zn+O2↑+4OH-+2H2O B、充电时,正极溶液中OH-浓度升高 C、放电时,1molCO2转化为HCOOH,转移的电子数为2mol D、放电时,负极反应为Zn-2e-+4OH-=
A、充电时,电池总反应为2=2Zn+O2↑+4OH-+2H2O B、充电时,正极溶液中OH-浓度升高 C、放电时,1molCO2转化为HCOOH,转移的电子数为2mol D、放电时,负极反应为Zn-2e-+4OH-=二、非选择题(本题共4小题,共55分)
-
16. 电化学知识与我们的生产、生活密切相关。回答下列问题:(1)、某兴趣小组同学利用氧化还原反应 , 设计了如图所示原电池,其中甲、乙两烧杯中各物质的量浓度均为 , 盐桥中装有饱和溶液。

①发生还原反应的烧杯是(填“甲”或“乙”)。
②外电路的电流方向:(填“”或“”)。
③电池工作时,盐桥中的移向(填“甲”或“乙”)烧杯。
④甲烧杯中发生的电极反应式为。
(2)、利用反应(未配平)消除的简易装置如图所示,电极b的反应式为 , 消耗标准状况下时,被消除的的物质的量为。 17. 短周期主族元素的原子序数依次增大,原子序数是6,Q元素基态原子核外有三个未成对电子,与同主族,的原子序数是的2倍,元素在同周期中原子半径最大。回答下列问题:(1)、可以正确描述W原子结构的是____(填字母)。A、原子结构示意图:
17. 短周期主族元素的原子序数依次增大,原子序数是6,Q元素基态原子核外有三个未成对电子,与同主族,的原子序数是的2倍,元素在同周期中原子半径最大。回答下列问题:(1)、可以正确描述W原子结构的是____(填字母)。A、原子结构示意图: B、原子核外能量最高的电子云图像:
B、原子核外能量最高的电子云图像: C、碳原子:
D、原子的轨道表示式:
C、碳原子:
D、原子的轨道表示式: (2)、Z元素基态原子
(2)、Z元素基态原子 电子排布式为 , 基态Z原子的价电子中,两种自旋状态的电子数之比为。 (3)、基态X原子的未成对电子数为 , 其价电子轨道表示式为。(4)、图a、b、c分别表示W、Q,X和F的逐级电离能(Ⅰ)变化趋势(纵坐标的标度不同)。第一电离能的变化图是(填标号)。
电子排布式为 , 基态Z原子的价电子中,两种自旋状态的电子数之比为。 (3)、基态X原子的未成对电子数为 , 其价电子轨道表示式为。(4)、图a、b、c分别表示W、Q,X和F的逐级电离能(Ⅰ)变化趋势(纵坐标的标度不同)。第一电离能的变化图是(填标号)。 (5)、W、Q、X、Y四种元素的电负性由大到小的顺序为(用元素符号表示);最高价氧化物对应水化物的酸性:W(填“>”或“<”)Q。18. 盐的水解及沉淀的溶解平衡是中学化学研究的重点之一、回答下列问题:(1)、已知常温下甲酸()的电离常数。
(5)、W、Q、X、Y四种元素的电负性由大到小的顺序为(用元素符号表示);最高价氧化物对应水化物的酸性:W(填“>”或“<”)Q。18. 盐的水解及沉淀的溶解平衡是中学化学研究的重点之一、回答下列问题:(1)、已知常温下甲酸()的电离常数。①写出水解反应的离子方程式: , 往其溶液中加入下列物质,能促进水解的是 (填字母)。
A. B. C. D.
②常温下,向溶液中滴入的溶液,溶液的变化曲线如图所示,d点溶液中(保留两位有效数字);b点溶液中:(填“>”“<”或“=”)。
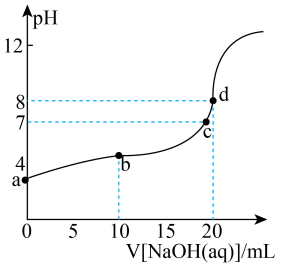 (2)、某酸性工业废水中含有一定量的硫酸铜,其物质的量的浓度为 , 向该溶液中加入氢氧化钠稀溶液除去(、、)
(2)、某酸性工业废水中含有一定量的硫酸铜,其物质的量的浓度为 , 向该溶液中加入氢氧化钠稀溶液除去(、、)①常温下要使降低为 , 溶液的应调至。
②向硫酸铜溶液中通入气体,该反应的离子方程式为 , 当溶液中的时,。
(3)、时,向溶液中滴加溶液(一种酸,酸性强弱未知)时,溶液中由水电离的浓度随加入的体积的变化如图所示:
①若稀释a点溶液,则与稀释前相比,稀释后的溶液中水的电离程度会(填“增大”“不变”或“减小”)。
②若c点溶液中溶质的总物质的量为 , 向c点溶液中加入的 , 此时溶液满足的元素质量守恒式为。
19. 是存在于燃气中的一种有害气体,脱除的方法有多种。回答下列问题:(1)、氧化回收硫的反应原理为:i: ;
ii:
iii:
①根据盖斯定律,反应iii中的。
②化学反应的焓变与反应物和生成物的键能(气态分子中化学键解离成气态原子所吸收的能量)有关。已知某些化学键的键能如下表所示:
共价键
键能
339
246
a
120
结合(1)中反应原理a=。
(2)、电解法治理是先用溶液吸收含的工业废气,所得溶液用惰性电极电解,阳极区所得溶液循环利用。
①进入电解池的溶液中,溶质是(填化学式)。
②阳极的电极反应式为。
(3)、天然气中含有杂质,某科研小组用氨水吸收得到溶液,已知时, , , , 溶液中所含粒子浓度大小关系正确的是____(填字母)。A、 B、 C、 D、(4)、工业上采用高温热分解的方法制取 , 在膜反应器中分离出。下,分解:。保持压强不变,反应达到平衡时,气体的体积分数随温度的变化曲线如图:
①在密闭容器中,关于上述反应的说法正确的是(填字母)。
A.随温度的升高而增大
B.低压有利于提高的平衡分解率
C.维持温度、气体总压强不变时,向平衡体系中通入氩气,则
D.在恒容密闭容器中进行反应,当气体密度不再变化时,反应达到平衡状态
②图中Q点:的平衡转化率为;时,反应的(为以分压表示的平衡常数,分压=总压×物质的量分数)。