安徽省合肥市六校联盟2023-2024学年高二上学期期末联考化学试卷
试卷更新日期:2024-03-12 类型:期末考试
一、选择题(本大题共16小题,每题3分,共48分。每小题只有一个正确答案,请把答案涂在答题卡上)
-
1. 创造美好幸福生活离不开化学。下列有关叙述正确的是( )A、硅光电池工作时能量转化:光能→化学能→电能。 B、杭州第19届亚运会主火炬首次采用“零碳甲醇”为燃料,“零碳甲醇”燃烧不产生CO2。 C、成都大运会上璀璨的焰火与电子的跃迁有关 D、我国西周时期发明的“酒曲”酿酒工艺,是利用了催化剂使平衡正向移动的原理2. 三氯蔗糖(结构如图所示),又名蔗糖素,其甜度约为蔗糖的600倍,具有热量低、安全性高等优点,可供糖尿病患者食用,被认为是几乎完美的甜味剂。下列说法正确的是( )
 A、氯元素的和轨道形状均为球形 B、氧元素的能级的轨道数相同 C、基态碳原子的L层没有成对电子 D、基态氯原子的价电子排布式为3s23p63. NF3是微电子工业中一种优良的等离子蚀刻气体,在空气中性质稳定。其中N—F键能为283 kJ·mol , 测得断裂氮气、氟气中的化学键所需的能量如图:
A、氯元素的和轨道形状均为球形 B、氧元素的能级的轨道数相同 C、基态碳原子的L层没有成对电子 D、基态氯原子的价电子排布式为3s23p63. NF3是微电子工业中一种优良的等离子蚀刻气体,在空气中性质稳定。其中N—F键能为283 kJ·mol , 测得断裂氮气、氟气中的化学键所需的能量如图:
下列说法错误的是( )
A、相同条件下,N2化学性质比F2更稳定 B、氮气和氟气的能量总和比NF3低 C、N2(g)+3F2(g)⇌2NF3(g) ∆H=-287.6kJ·mol-1 D、NF3在大气中性质比较稳定,不易发生化学反应4. 根据下列图示所得出的结论正确的是( )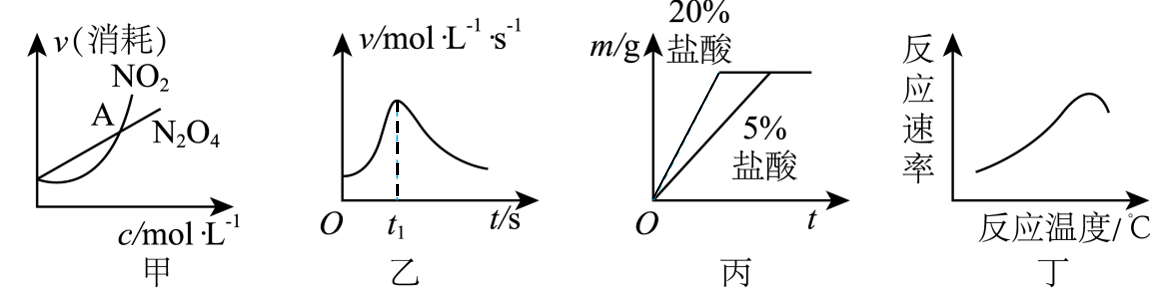 A、图甲表示恒温恒容条件下,2NO2(g)⇌N2O4(g)中各物质的浓度与其消耗速率之间的关系,其中交点A对应的状态为化学平衡状态 B、图乙是镁条与盐酸反应的化学反应速率随反应时间变化的曲线,说明t1时刻溶液的温度最高 C、图丙表示取规格相同的铝片,分别放入等质量20%、5%的稀盐酸中,生成氢气的质量与反应时间的关系曲线 D、图丁可以表示酶催化反应的反应速率随反应温度的变化5. MnO2-CeO2催化剂能催化NH3脱除烟气中的NO,反应方程为:4NH3(g)+4NO(g)+O2(g)=4N2(g)+6H2O(g),其机理如图所示。下列说法正确的是( )
A、图甲表示恒温恒容条件下,2NO2(g)⇌N2O4(g)中各物质的浓度与其消耗速率之间的关系,其中交点A对应的状态为化学平衡状态 B、图乙是镁条与盐酸反应的化学反应速率随反应时间变化的曲线,说明t1时刻溶液的温度最高 C、图丙表示取规格相同的铝片,分别放入等质量20%、5%的稀盐酸中,生成氢气的质量与反应时间的关系曲线 D、图丁可以表示酶催化反应的反应速率随反应温度的变化5. MnO2-CeO2催化剂能催化NH3脱除烟气中的NO,反应方程为:4NH3(g)+4NO(g)+O2(g)=4N2(g)+6H2O(g),其机理如图所示。下列说法正确的是( )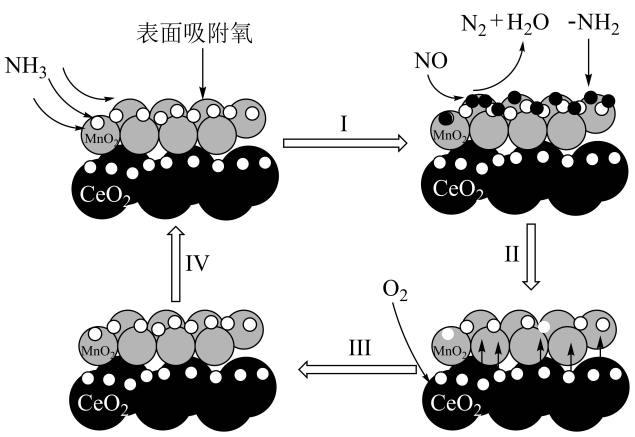 A、该反应∆S<0 B、该反应的平衡常数 C、步骤Ⅰ可描述为NH3吸附到MnO2表面与表面吸附氧反应生成—NH2和H2O,同时MnO2被还原为Mn2O3;烟气中的NO和—NH2反应生成N2和H2O D、该反应中每消耗1mol O2 , 转移电子的数目约为4×6.02×10236. 某兴趣小组进行了如下实验:向酸化的H2O2溶液中同时加入KI溶液、维生素C和淀粉溶液,发现一段时间后溶液变蓝。查阅资料可知体系中存在两个主要反应:
A、该反应∆S<0 B、该反应的平衡常数 C、步骤Ⅰ可描述为NH3吸附到MnO2表面与表面吸附氧反应生成—NH2和H2O,同时MnO2被还原为Mn2O3;烟气中的NO和—NH2反应生成N2和H2O D、该反应中每消耗1mol O2 , 转移电子的数目约为4×6.02×10236. 某兴趣小组进行了如下实验:向酸化的H2O2溶液中同时加入KI溶液、维生素C和淀粉溶液,发现一段时间后溶液变蓝。查阅资料可知体系中存在两个主要反应:反应ⅰ:H2O2+2I-+2H+=I2+2H2O
反应ⅱ:C6H8O6(维生素C)+I2=C6H6O6+2I-+2H+
下列说法不正确的是( )
A、反应速率:反应ⅰ<反应ⅱ B、可得氧化性强弱:H2O2>I2>C6H6O6 C、溶液的pH始终保持不变 D、溶液最终变蓝,说明所加n(H2O2)>n(C6H6O6)7. 已知制备光气COCl2的反应为CO(g)+Cl2(g)⇌COCl2(g) ∆H<0,将等物质的量的CO(g)和Cl2(g)充入密闭容器中,平衡体系中,平衡混合物的平均摩尔质量M()在不同温度下随压强的变化曲线如图所示。下列说法正确的是( ) A、温度:T1<T2 B、平衡常数:Ka=Kb<Kc C、Cl2的平衡转化率:c>b>a D、b点时,若M=66g·mol-1 , 则CO的平衡转化率为50%8. 氨是一种重要的化工原料,主要用于化肥工业,也广泛用于硝酸、纯碱、制药等工业;合成氨反应为:N2(g)+3H2(g)⇌2NH3(g) ∆H,工业上可利用氨气等制取硝酸。有关工业合成氨的反应下列有关说法正确的是( )A、其它条件不变,升高温度,可提高活化分子百分数,加快反应速率 B、反应的∆H=3E(N-N)+3E(H-H)-6E(N-H) (E表示键能) C、2mol N—H断裂同时有1mol H-H形成,说明达该条件下的平衡状态 D、将氨气液化并移走,可提高原料的平衡转化率及平衡时的反应速率9. A、B、C、D、E 五种元素在周期表中的相对位置如图所示,下列说法正确的是( )
A、温度:T1<T2 B、平衡常数:Ka=Kb<Kc C、Cl2的平衡转化率:c>b>a D、b点时,若M=66g·mol-1 , 则CO的平衡转化率为50%8. 氨是一种重要的化工原料,主要用于化肥工业,也广泛用于硝酸、纯碱、制药等工业;合成氨反应为:N2(g)+3H2(g)⇌2NH3(g) ∆H,工业上可利用氨气等制取硝酸。有关工业合成氨的反应下列有关说法正确的是( )A、其它条件不变,升高温度,可提高活化分子百分数,加快反应速率 B、反应的∆H=3E(N-N)+3E(H-H)-6E(N-H) (E表示键能) C、2mol N—H断裂同时有1mol H-H形成,说明达该条件下的平衡状态 D、将氨气液化并移走,可提高原料的平衡转化率及平衡时的反应速率9. A、B、C、D、E 五种元素在周期表中的相对位置如图所示,下列说法正确的是( )A
B
C
D
E
A、C的简单离子是它所在周期元素中离子半径最小的离子 B、D和E两元素的氧化物对应水化物的酸性E>D C、B是周期表中电负性最强的元素 D、该五种元素中第一电离能由大到小进行排序为:B>A>E>D>C10. 我国科学家在一颗距离地球100光年的行星上发现了不可思议的“水世界”,引起了全球科学界的轰动。下列有关说法错误的是( )A、温度升高,水的电离平衡正向移动,c(H+)增大,但溶液仍然保持中性 B、室温下,pH=4的盐酸溶液中,c水(H+)=5×10-9mol·L-1 C、由水电离出的c水(H+)=c水(OH-)时,溶液不一定呈中性 D、向水中加入固体后(溶液温度不变),水的电离程度减小11. 下图是利用滴定管进行实验,对于滴定实验过程,下列说法错误的是( ) A、滴定管润洗后,润洗液应从滴定管下口流出 B、用0.1000mol·L-1NaOH溶液滴定20.00mLHA溶液过程中,若使用酚酞作指示剂,会产生系统误差,测得HA溶液浓度会偏大 C、除去碱式滴定管胶管内气泡时,将尖嘴垂直向下,挤压胶管内玻璃球 D、该滴定管可以盛装酸性高锰酸钾溶液12. 下列有关实验的操作、现象和结论都正确的是( )
A、滴定管润洗后,润洗液应从滴定管下口流出 B、用0.1000mol·L-1NaOH溶液滴定20.00mLHA溶液过程中,若使用酚酞作指示剂,会产生系统误差,测得HA溶液浓度会偏大 C、除去碱式滴定管胶管内气泡时,将尖嘴垂直向下,挤压胶管内玻璃球 D、该滴定管可以盛装酸性高锰酸钾溶液12. 下列有关实验的操作、现象和结论都正确的是( )选项
实验操作
现象
结论
A
测定等物质的量浓度的Na2CO3和NaClO的pH
Na2CO3>NaClO
酸性:H2CO3<HClO
B
向浓度均为0.10mol/L的KCl和KI混合溶液中滴加少量AgNO3溶液
先出现黄色沉淀
Ksp(AgCl)>Ksp(AgI)
C
向FeCl3+3KSCN⇌Fe(SCN)3+3KCl的溶液平衡体系中加入少量KCl固体
溶液血红色变浅
增大生成物浓度,平衡逆向移动
D
用pH试纸测量同浓度的CH3COOH、HClO的pH,比较溶液pH大小
HClO的pH比CH3COOH大
说明CH3COOH酸性比HClO强
A、A B、B C、C D、D13. 下列有关平衡移动的说法错误的是( )A、将2mL0.5mol·L-1 CuCl2溶液加热,溶液由蓝绿色变黄绿色,说明CuCl2溶液中[Cu(H2O)4]2+(蓝色)+4Cl- ⇌[CuCl4]2-(黄色)+4H2O是吸热过程 B、向2 mL0.1mol·L-1K2Cr2O7溶液加几滴6 mol/L硫酸,溶液橙色加深,说明增大c(H+)使平衡Cr2O72-+H2O⇌2CrO42-+2H+逆向移动 C、恒温恒容密闭容器,通入2mol SO2和1mol O2 , 反应达到平衡后,再向其中通入1mol氦气,平衡不移动。 D、加水稀释0.1mol·L-1的醋酸溶液,CH3COOH电离程度变大,从c(H+)变大14. 我国某大学科研团队提出用多孔泡沫铁、高度膨化的纳米泡沫碳(CFs)和添加了NH4Cl的FeSO4溶液构建独特的“摇椅式”全铁离子电池,电池结构如图(阴离子未标出)。下列说法错误的是( ) A、NH4Cl可增加电解质溶液的导电性 B、充电时,阳极的电极反应式为 C、放电时,电极N为负极 D、放电时,每转移 , 参与反应的铁元素的总质量为112g15. 某水样中含一定浓度的CO32-、HCO3-和其他不与酸碱反应的离子。取10.00mL水样,用0.01000mol•L-1的HCl溶液进行滴定,溶液pH随滴加HCl溶液体积V(HCl)的变化关系如图(混合后溶液体积变化忽略不计)。
A、NH4Cl可增加电解质溶液的导电性 B、充电时,阳极的电极反应式为 C、放电时,电极N为负极 D、放电时,每转移 , 参与反应的铁元素的总质量为112g15. 某水样中含一定浓度的CO32-、HCO3-和其他不与酸碱反应的离子。取10.00mL水样,用0.01000mol•L-1的HCl溶液进行滴定,溶液pH随滴加HCl溶液体积V(HCl)的变化关系如图(混合后溶液体积变化忽略不计)。下列说法正确的是( )
 A、该水样中c(CO32-)=0.01mol•L-1 B、a点处c(H2CO3)+c(H+)=c(OH-) C、曲线上任意一点存在c(CO32-)+c(HCO3-)+c(H2CO3)=0.03mol•L-1 D、当V(HCl)≤20.00mL时,溶液中c(HCO3-)基本保持不变16. 常温下,将0.025molBaSO4粉末置于盛有蒸馏水的烧杯中形成1L悬浊液,然后向烧杯中加入Na2CO3固体(忽略溶液体积的变化)并充分搅拌,加入Na2CO3固体的过程中,溶液中几种离子的浓度变化曲线如图所示,下列说法中不正确的是( )
A、该水样中c(CO32-)=0.01mol•L-1 B、a点处c(H2CO3)+c(H+)=c(OH-) C、曲线上任意一点存在c(CO32-)+c(HCO3-)+c(H2CO3)=0.03mol•L-1 D、当V(HCl)≤20.00mL时,溶液中c(HCO3-)基本保持不变16. 常温下,将0.025molBaSO4粉末置于盛有蒸馏水的烧杯中形成1L悬浊液,然后向烧杯中加入Na2CO3固体(忽略溶液体积的变化)并充分搅拌,加入Na2CO3固体的过程中,溶液中几种离子的浓度变化曲线如图所示,下列说法中不正确的是( )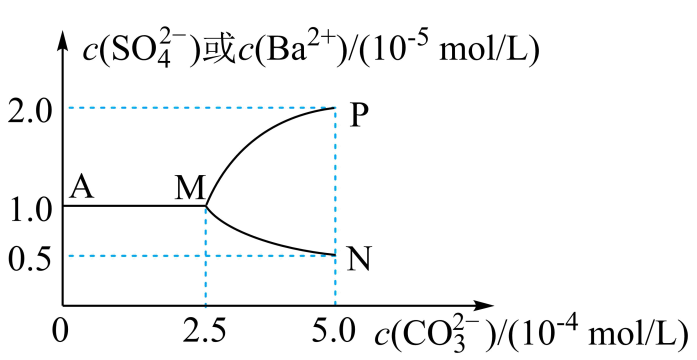 A、曲线MP表示c(SO42-)的变化 B、BaSO4固体恰好完全溶解时,溶液中离子浓度关系为c(CO32-)>c(SO42-)>c(Ba2+)>c(OH-) C、BaSO4的Ksp为1×10-10 D、若要使反应BaSO4+CO32- ⇌BaCO3+SO42-正向进行,需满足
A、曲线MP表示c(SO42-)的变化 B、BaSO4固体恰好完全溶解时,溶液中离子浓度关系为c(CO32-)>c(SO42-)>c(Ba2+)>c(OH-) C、BaSO4的Ksp为1×10-10 D、若要使反应BaSO4+CO32- ⇌BaCO3+SO42-正向进行,需满足二、非选择题(本大题共4大题,共52分。)
-
17. 化学反应中常伴随着能量的变化。回答下列问题:(1)、S8分子可形成单斜硫和斜方硫,转化过程为:S(s,单斜)S(s,斜方)∆H= -0.398kJ·mol-1 , 则S(单斜)与S(斜方)相比,较稳定的是 , 基态S原子的原子核外电子有种空间运动状态,其能量最高的电子电子云轮廓图为形。(2)、Cu的价层电子排布式为 , 位于在周期表区(填s、p、d或ds)。(3)、下列属于氧原子激发态的轨道表示式的有(填字母)。
a.
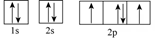 b.
b.
c.
 d.
d.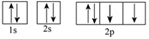 (4)、已知稀溶液中:H+(aq)+OH-(aq)=H2O(l) ∆H= -57.3 kJ·mol-1 , 则浓硫酸与稀氢氧化钠溶液反应生成1mol水,放出的热量(填“>”“<”或“=”)57.3kJ。(5)、1molNO2(g)和1molCO(g)反应生成CO2(g)和NO(g)过程中的能量变化如图所示:
(4)、已知稀溶液中:H+(aq)+OH-(aq)=H2O(l) ∆H= -57.3 kJ·mol-1 , 则浓硫酸与稀氢氧化钠溶液反应生成1mol水,放出的热量(填“>”“<”或“=”)57.3kJ。(5)、1molNO2(g)和1molCO(g)反应生成CO2(g)和NO(g)过程中的能量变化如图所示: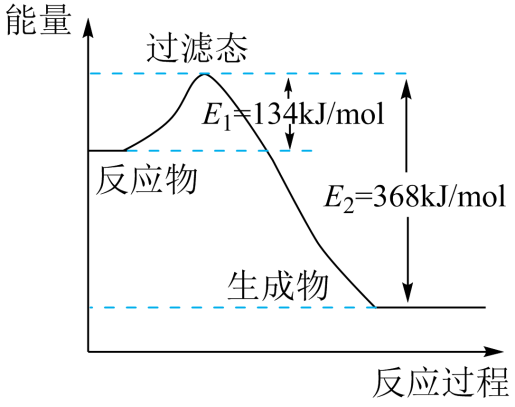
①若在反应体系中加入催化剂,反应速率增大,E1(填“增大”“减小”或“不变”)。
②写出NO2和CO反应的热化学方程式。
(6)、标准摩尔生成焓是指在25℃和101kPa时,最稳定的单质生成1mol化合物的焓变。已知25℃和101kPa时下列反应:①
②
③
写出乙烷(C2H6)标准摩尔生成焓的焓变∆H=(用含∆H1、∆H2、∆H3的式子表示)。
18. 二氧化碳的捕集、利用与封存是我国能源领域的一个重要战略方向,发展成一项重要的新兴产业。(1)、一种脱除和利用水煤气中CO2方法的示意图如下: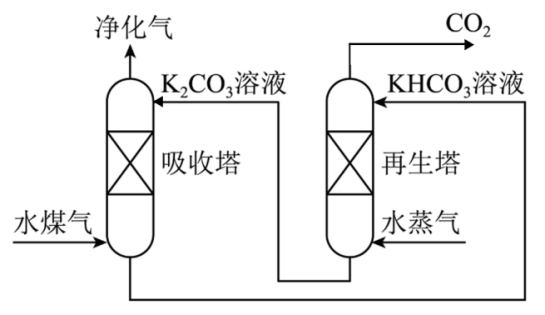
①在某温度下,吸收塔中的K2CO3溶液吸收一定量的CO2后,溶液的pH等于10,则此时溶液中c(CO32-):c(HCO3-)=(该温度下H2CO3的Ka1=4.6×10-7 , Ka2=5.0×10-11)。②再生塔中产生CO2的化学方程式为
(2)、科学家提出由CO2制取C的太阳能工艺如图所示。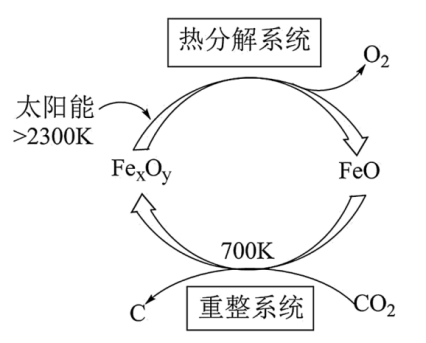
已知“重整系统”发生的反应中 , 则“重整系统”发生反应的化学方程式为。
(3)、用二氧化碳催化加氢来合成低碳烯烃,起始时以0.1MPa,n(H2):n(CO2)=3:1的投料比充入反应器中,发生反应:2CO2(g)+6H2(g)⇌C2H4(g)+4H2O(g),不同温度下平衡时的四种气态物质的物质的量如图所示: ①该反应在自发进行(填“低温”或“高温”)。
①该反应在自发进行(填“低温”或“高温”)。②b代表的物质是。
③为提高CO2的平衡转化率,除改变温度外,还可采取的措施是(列举2项)。
④温度下CO2的平衡转化率为。
19. 氯化亚铜(CuCl)是一种重要化工原料,难溶于水,在潮湿空气中易水解氧化。回答下列问题:(1)、向CuSO4与NaCl的混合溶液中通入SO2即可制得CuCl,制备过程中主要发生了以下三步反应,请写出第三步的化学反应方程式:CuSO4+4NaCl(过量)=Na2[CuCl4]+Na2SO4
2Na2[CuCl4]+SO2+2H2O=2NaH[CuCl3]+H2SO4+2NaCl
。(2)、CuCl在含一定浓度Cl-溶液中会部分溶解,存在如下平衡:2CuCl(s)⇌Cu++CuCl2- ∆H<0,溶液中c(Cu+)和c(CuCl2-)的关系如图所示: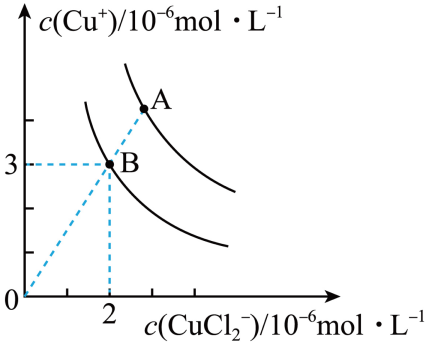
①上述反应在B点的平衡常数K=。
②使图中的A点变为B点的措施可以是。
(3)、利用CuCl难溶于水的性质,可以除去水溶液中的Cl-。①除Cl-的方法是向含Cl-的溶液同时加入Cu和CuSO4 , 该反应的离子方程式为。
②若用Zn替换Cu可加快除Cl-速率,但需控制溶液的pH。若pH过低,除Cl-效果下降的原因是。
(4)、产品纯度的测定:准确称取氯化亚铜产品2.3900g,溶于过量的FeCl3溶液中得250mL待测液,从中量取25.00mL于锥形瓶中,加入2滴邻菲罗啉指示剂,立即用0.1000mol·L-1硫酸铈Ce(SO4)2标准溶液滴定至终点,共完成三次滴定,每次消耗Ce(SO4)2溶液体积见下表。产品中CuCl的质量分数为%。(已知:CuCl+Fe3+=Cu2++Fe2++Cl- , Fe2++Ce4+=Fe3++Ce3+)1
2
3
消耗硫酸铈标准溶液的体积(mL)
23.85
24.35
23.95
若未用标准溶液润洗滴定管,则会使测定结果(填“偏大”、“偏小”或“不变”)。
20. 氮的相关化合物在化工生产中占有重要地位。(1)、N2O4与NO2之间存在反应N2O4(g)⇌2NO2(g)。将一定量的N2O4放入恒容密闭容器中,测得其平衡转化率[α(N2O4)]随温度的变化如图所示。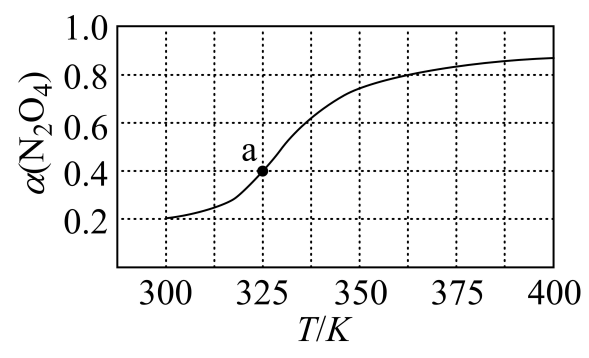 ①由图推测该反应的∆H0(填“>”或“<”),理由为。
①由图推测该反应的∆H0(填“>”或“<”),理由为。②a点对应的温度下,已知N2O4的起始压强为90kPa,平衡后总压强为kPa,该温度下反应的平衡常数Kp=kPa(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(2)、化工废水中常常含有以二甲胺((CH3)2NH)为代表的含氮有机物,可以通过电解法将二甲胺转化为无毒无害的气体排放,装置如图所示。反应原理是:①Cl-在阳极转化为Cl2;②Cl2在碱性溶液中歧化为ClO-;③ClO-将二甲胺氧化为N2 , CO32-和H2O。
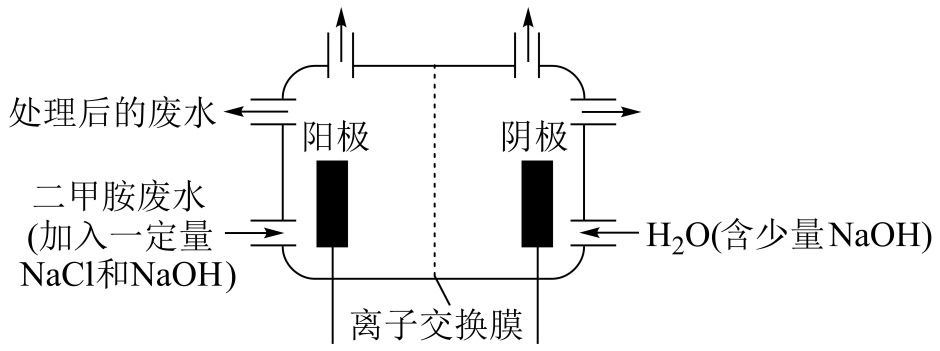
①写出电解池中阴极发生反应的方程式。
②电解池中选择阴离子交换膜而不选择阳离子交换膜的原因是。
③当阴极区收集到6.72L (标况下)H2时,阳极区收集到N2的体积(标况下)是L。