安徽省蚌埠市2023-2024学年高二上学期化学期末考试
试卷更新日期:2024-03-12 类型:期末考试
一、单选题(本题包括14小题,每小题只有一个选项符合题意。每小题3分,共42分)
-
1. 我国古代就掌握了青铜(铜-锡合金)的冶炼、加工技术,制造出许多精美的青铜器;Pb、是铅蓄电池的电极材料,不同铅化合物一般具有不同颜色,历史上曾广泛用作颜料,下列物质性质与用途具有对应关系的是( )A、石墨能导电,可用作润滑剂 B、单晶硅熔点高,可用作半导体材料 C、青铜比纯铜熔点低、硬度大,古代用青铜铸剑 D、含铅化合物颜色丰富,可用作电极材料2. 酸式盐是盐的一种,可看作多元酸中的氢离子未被完全中和所得到的盐,常见的有NaHCO3、NaHSO4、KH2PO4、K2HPO4等。已知H3PO2(次磷酸)与足量的NaOH反应只生成一种盐NaH2PO2 , 则下列说法不正确的是( )A、H3PO2属于三元酸 B、NaH2PO2属于正盐 C、H3PO2与NaOH反应中的反应物与生成物都是电解质 D、溶液中NaH2PO2的电离方程式:3. 某反应的反应过程中能量变化如图所示(图中E1表示正反应的活化能,E2表示逆反应的活化能)。下列有关叙述正确的是
 A、该反应为放热反应 B、催化剂能改变该反应的焓变 C、催化剂能降低该反应的活化能 D、逆反应的活化能大于正反应的活化能4. 常温下,下列各组离子在指定溶液中能大量共存的是( )A、无色透明的溶液中:Fe3+、Mg2+、SCN-、Cl- B、pH=12的溶液中:K+、Na+、、 C、c(Fe2+)=1mol/L的溶液中:K+、、、 D、能使甲基橙变红的溶液中:Na+、、、5. 铜板上铁铆钉处的吸氧腐蚀原理如图所示,下列有关说法正确的是( )
A、该反应为放热反应 B、催化剂能改变该反应的焓变 C、催化剂能降低该反应的活化能 D、逆反应的活化能大于正反应的活化能4. 常温下,下列各组离子在指定溶液中能大量共存的是( )A、无色透明的溶液中:Fe3+、Mg2+、SCN-、Cl- B、pH=12的溶液中:K+、Na+、、 C、c(Fe2+)=1mol/L的溶液中:K+、、、 D、能使甲基橙变红的溶液中:Na+、、、5. 铜板上铁铆钉处的吸氧腐蚀原理如图所示,下列有关说法正确的是( ) A、阳极电极反应式为:2H++2e→H2↑ B、此过程中电子从 Fe 移向 Cu,铁铆钉发生还原反应 C、此过程中铜会被腐蚀,发生氧化反应 D、此过程中铁做负极,被氧化6. 下列事实中,不能用勒夏特列原理解释的是( )A、向稀盐酸中加入少量蒸馏水,盐酸中氯离子浓度降低 B、常温时,AgCl在饱和氯化钠溶液中的溶解度小于在水中的溶解度 C、热的纯碱溶液去油污效果更好 D、开启啤酒瓶后,瓶中马上泛起大量泡沫7. 阿伏加德罗常数符号为NA。关于100mL1mol/L的Fe2(SO4)3溶液,下列说法正确的是( )A、加NaOH溶液可制得Fe(OH)3胶粒数目为0.2NA B、溶液中阳离子数目为0.2NA C、加Na2CO3溶液发生的反应为3+2Fe3+=Fe2(CO3)3↓ D、Fe2(SO4)3溶液可用于止血8. Na2Cr2O7的酸性水溶液随着H+浓度的增大会转化为CrO3。电解法制备CrO3的原理如图所示。下列说法错误的是( )
A、阳极电极反应式为:2H++2e→H2↑ B、此过程中电子从 Fe 移向 Cu,铁铆钉发生还原反应 C、此过程中铜会被腐蚀,发生氧化反应 D、此过程中铁做负极,被氧化6. 下列事实中,不能用勒夏特列原理解释的是( )A、向稀盐酸中加入少量蒸馏水,盐酸中氯离子浓度降低 B、常温时,AgCl在饱和氯化钠溶液中的溶解度小于在水中的溶解度 C、热的纯碱溶液去油污效果更好 D、开启啤酒瓶后,瓶中马上泛起大量泡沫7. 阿伏加德罗常数符号为NA。关于100mL1mol/L的Fe2(SO4)3溶液,下列说法正确的是( )A、加NaOH溶液可制得Fe(OH)3胶粒数目为0.2NA B、溶液中阳离子数目为0.2NA C、加Na2CO3溶液发生的反应为3+2Fe3+=Fe2(CO3)3↓ D、Fe2(SO4)3溶液可用于止血8. Na2Cr2O7的酸性水溶液随着H+浓度的增大会转化为CrO3。电解法制备CrO3的原理如图所示。下列说法错误的是( )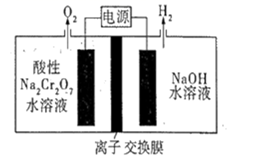 A、电解时只允许H+通过离子交换膜 B、生成O2和H2的质量比为8∶1 C、电解一段时间后阴极区溶液OH-的浓度增大 D、CrO3的生成反应为:Cr2O +2H+=2CrO3+H2O9. 下列反应的离子方程式正确的是( )A、向AlCl3溶液中加入过量氨水:Al3++3OH-=Al(OH)3↓ B、用FeCl3溶液腐蚀印刷电路板:Fe3++Cu=Fe2++Cu2+ C、硫酸氢钠溶液中加入氢氧化钡溶液至中性:2H+++Ba2++2OH-=BaSO4↓+2H2O D、过量铁粉与稀硝酸:Fe+4H++=Fe3++NO↑+2H2O10. 下列实验中,不能达到实验目的的是( )
A、电解时只允许H+通过离子交换膜 B、生成O2和H2的质量比为8∶1 C、电解一段时间后阴极区溶液OH-的浓度增大 D、CrO3的生成反应为:Cr2O +2H+=2CrO3+H2O9. 下列反应的离子方程式正确的是( )A、向AlCl3溶液中加入过量氨水:Al3++3OH-=Al(OH)3↓ B、用FeCl3溶液腐蚀印刷电路板:Fe3++Cu=Fe2++Cu2+ C、硫酸氢钠溶液中加入氢氧化钡溶液至中性:2H+++Ba2++2OH-=BaSO4↓+2H2O D、过量铁粉与稀硝酸:Fe+4H++=Fe3++NO↑+2H2O10. 下列实验中,不能达到实验目的的是( )由海水制取蒸馏水
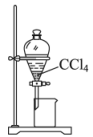
萃取碘水中的碘
分离粗盐中的不溶物
由制取无水固体



A
B
C
D
A、A B、B C、C D、D11. Al-Ag2O电池用作水下动力电源,其原理如图所示。电池工作时,下列说法错误的是( ) A、电子由Al电极通过外电路流向Ag2O/Ag电极 B、电池负极附近溶液pH下降 C、溶液中OH-向Al电极移动 D、Al极反应式为:Al-3e-+3OH-=Al(OH)312. 下列研究目的和示意图相符的是( )
A、电子由Al电极通过外电路流向Ag2O/Ag电极 B、电池负极附近溶液pH下降 C、溶液中OH-向Al电极移动 D、Al极反应式为:Al-3e-+3OH-=Al(OH)312. 下列研究目的和示意图相符的是( )选项
A
B
C
D
研究目的
密闭容器中,压强对反应:2SO2(g)+O2(g)2SO3(g)的影响
固定容积的密闭容器中,温度对反应:N2(g)+3H2(g)2NH3(g) ΔH<0的影响
等质量Na、K分别与足量水反应
固定容积的密闭容器中,增大CO2浓度,对已达平衡的反应:CO(g)+H2O(g)CO2(g)+H2(g)的影响
示意图



 A、A B、B C、C D、D13. 俄罗斯用“质子—M”号运载火箭成功将“光线”号卫星送入预定轨道,发射用的运载火箭使用的是以液氢为燃烧剂,液氧为氧化剂的高能低温推进剂,反应过程如下图:
A、A B、B C、C D、D13. 俄罗斯用“质子—M”号运载火箭成功将“光线”号卫星送入预定轨道,发射用的运载火箭使用的是以液氢为燃烧剂,液氧为氧化剂的高能低温推进剂,反应过程如下图:
下列说法正确的是( )
A、2molH2(g)与1molO2(g)所具有的总能量比2molH2O(g)所具有的总能量低 B、一定条件下,反应2H2(g)+O2(g)=2H2O(g)能自发进行 C、火箭中液氢燃烧的热化学方程式为:2H2(l)+O2(l)=2H2O(g)△H=-483.6kJ/mol D、H2O(g)变成H2O(l)的过程中,断键吸收的能量小于成键放出的能量14. 25℃下,向20 mL 0.1 mol·L-1H2A溶液中滴加0.1 mol·L-1NaOH溶液,有关粒子物质的量的变化如图所示。下列有关说法正确的是( ) A、H2A属于强酸 B、c(HA-)/c(H2A)随着V[NaOH(aq)]的增大而减小 C、V[NaOH(aq)]=20mL时,溶液中存在关系:c(HA-)+c(A2-)+c(H2A)=0.1mol/L D、V[NaOH(aq)]=20mL时,溶液中存在关系:c(Na+)>c(HA-)>c(H+)>c(A2-)>c(OH-)
A、H2A属于强酸 B、c(HA-)/c(H2A)随着V[NaOH(aq)]的增大而减小 C、V[NaOH(aq)]=20mL时,溶液中存在关系:c(HA-)+c(A2-)+c(H2A)=0.1mol/L D、V[NaOH(aq)]=20mL时,溶液中存在关系:c(Na+)>c(HA-)>c(H+)>c(A2-)>c(OH-)二、实验探究题(本大题共1小题,共12分)
-
15. 铁是人体必需的微量元素之一。黑木耳中的含铁量较高,为检验和测定干黑木耳样品中的铁元素,设计实验如下。回答下列问题:
Ⅰ.铁元素的检验
 (1)、Ⅰ.铁元素的检验
(1)、Ⅰ.铁元素的检验
“操作”是指。上述流程中需要用到的仪器有托盘天平、烧杯、玻璃棒、酒精灯、漏斗,还有下图中的(填写仪器名称)。
 (2)、取待测液少许,滴加K3[Fe(CN)6]溶液,观察到有蓝色沉淀生成;另取待测液少许,滴加(填化学式)溶液,观察到溶液变为红色,由此可得出结论(填字母序号)。
(2)、取待测液少许,滴加K3[Fe(CN)6]溶液,观察到有蓝色沉淀生成;另取待测液少许,滴加(填化学式)溶液,观察到溶液变为红色,由此可得出结论(填字母序号)。a.黑木耳中一定含Fe2+和Fe3+
b.待测液中一定含Fe2+和Fe3+
(3)、Ⅱ.铁元素含量的测定利用KMnO4标准溶液测定干黑木耳样品中铁元素的含量
步骤Ⅰ:取10.00mL待测液,加入过量铜粉至反应完全后,过滤、洗涤,将滤液及洗涤液全部收集到锥形瓶中。
步骤Ⅱ:向步骤Ⅰ所得的溶液中加入适量稀H2SO4溶液,用0.0020mol/L的KMnO4标准溶液滴定至终点,消耗KMnO4溶液2.20mL。
①用KMnO4标准溶液滴定至终点的标志是。
②黑木耳中铁的含量为mg/100g(即每100g黑木耳中含铁元素的质量)。
三、简答题(本大题共3小题,共34分)
-
16. CoC2O4是制备氧化钴和金属钴的原料。一种利用含钴废料(主要成分为Co2O3 , 含少量Fe2O3、Al2O3、MnO、CaO、MgO碳及有机物等)制取CoC2O4的工艺流程如下:
 (1)、为了加快“碱浸”速率,可采用的方法有(写一种即可)。“浸出液”的主要成分是(填化学式)。(2)、“钴浸出”过程中Co3+转化为Co2+ , 反应的离子方程式为。(3)、“除杂1”过程中,在40~50℃加入H2O2 , 写出加入H2O2反应的主要离子方程式为。(4)、“除杂2”可将钙、镁离子转化为沉淀过滤除去,若所得滤液中c(Ca2+)=1.0×10-5mol/L,则滤液中c(Mg2+)为[已知Ksp(MgF2)=7.35×10-11、Ksp(CaF2) =1.05×10-10]。(5)、萃取剂对金属离子的萃取率与pH的关系如图所示,经过萃取可除去Mn2+ , 需控制溶液的pH范围是____(填字母)。
(1)、为了加快“碱浸”速率,可采用的方法有(写一种即可)。“浸出液”的主要成分是(填化学式)。(2)、“钴浸出”过程中Co3+转化为Co2+ , 反应的离子方程式为。(3)、“除杂1”过程中,在40~50℃加入H2O2 , 写出加入H2O2反应的主要离子方程式为。(4)、“除杂2”可将钙、镁离子转化为沉淀过滤除去,若所得滤液中c(Ca2+)=1.0×10-5mol/L,则滤液中c(Mg2+)为[已知Ksp(MgF2)=7.35×10-11、Ksp(CaF2) =1.05×10-10]。(5)、萃取剂对金属离子的萃取率与pH的关系如图所示,经过萃取可除去Mn2+ , 需控制溶液的pH范围是____(填字母)。 A、1.0~2.0 B、2.0~3.0 C、3.0~3.517. 电解质水溶液中存在电离平衡、水解平衡、溶解平衡,请回答下列问题。(1)、已知部分弱酸的电离常数如下表:
A、1.0~2.0 B、2.0~3.0 C、3.0~3.517. 电解质水溶液中存在电离平衡、水解平衡、溶解平衡,请回答下列问题。(1)、已知部分弱酸的电离常数如下表:弱酸
CH3COOH
HCN
H2CO3
电离常数(25℃)
Ka = 1.8×10-5
Ka=4.3×10-10
Ka1=5.0×10-7 Ka2=5.6×10-11
①常温下,pH相同的三种溶液:A.CH3COONa B.NaCN C.Na2CO3 , 其物质的量浓度由大到小的顺序是(填编号)。
②将少量CO2通入NaCN溶液,反应的离子方程式是。
③室温下,-定浓度的CH3COONa溶液pH=9,用离子方程式表示溶液呈碱性的原因是 , 溶液中c(CH3COO-)/c(CH3COOH) =
(2)、室温下,用0.100 mol/L盐酸溶液滴定20.00mL0.100mol/L 的某氨水溶液,滴定曲线如图所示(横坐标为盐酸的体积)。
① d点所示的溶液中离子浓度由大到小的顺序依次为。
② b点所示的溶液中c(NH3·H2O)-c(NH4+)=(用溶液中的其它离子浓度表示)。
18. 二氧化碳、甲烷是地球大气中的主要温室气体,它们能吸收地面反射的太阳辐射,使地球表面变暖,因此,对二氧化碳、甲烷的高效利用有着举足轻重的作用。回答下列问题:(1)、已知下列反应①CH4(g)+H2O(g)CO(g)+3H2(g) △H1
②CO(g)+H2O(g)CO2(g)+H2(g) △H2
则二氧化碳重整甲烷反应:CH4(g)+CO2(g)2CO(g)+2H2(g)△H3=。
(2)、恒温恒容密闭容器中,反应CH4(g)+CO2(g)2CO(g)+2H2(g)达到平衡状态的标志是____。A、容器内的压强保持不变 B、c(CH4):c(CO2):c(CO):c(H2)=1:1:2:2 C、混合气体的平均分子量保持不变 D、混合气体的颜色保持不变 E、单位时间内断裂C-H键和形成H-H键的数目之比为2:1(3)、反应CH4(g)+CO2(g)2CO(g)+2H2(g)的平衡常数的表达式为。(4)、T℃时,向恒容密闭容器中投入CH4和CO2各1mol,发生反应CH4(g)+CO2(g) 2CO(g)+2H2(g),测得容器内的气体压强随时间的变化如下表所示(气态物质分压=总压×气态物质的物质的量分数,不考虑其他副反应):时间/min
0
10
20
30
50
60
总压/kPa
100
118
132
141
148
148
①在0~20min内,平均反应速率v(CO)=kPa/min。
②若在恒温恒压密闭容器中进行上述反应,CH4的转化率将(填增大、减小、不变)。
四、计算题(共12分)
-
19. 已知H2S与CO2在高温下发生反应:H2S(g)+CO2(g)COS(g)+H2O(g),在610K时,将0.10molCO2与0.40molH2S充入1L的空钢瓶中,反应平衡后水的物质的量分数为0.02。(1)、计算H2S的平衡转化率a= (写出计算过程)。(2)、计算浓度平衡常数K=。(写出计算过程)。
-