河北省唐山市路南区2023-2024学年九年级上学期化学期末复习试题
试卷更新日期:2024-03-11 类型:期末考试
一、选择题(本题共20个小题,每小题2分,共 40分。下列各题,每小题只有一个选项符合题意。)
-
1. 东京奥运会、残奥会主火炬第一次采用了氢气作为燃料。采用这种零排放燃料是对氢气的致敬,氢气是日本未来脱碳的核心之一、氢气的下列性质属于化学性质的是( )A、无色、无气味 B、密度比空气小 C、难溶于水 D、可以燃烧2. 9月29日,宁波一家日用品加工企业的香水灌装车间起火,车间员工的一系列错误行为让原本很容易扑灭的小火扩散,酿成19人死亡、3人受伤的悲剧,如果掌握一些灭火措施和安全知识,可以减少悲剧的发生。下列说法你认为错误的是( )A、酒精灯不慎打翻起火,立即用湿抹布扑灭 B、香水、酒精、油等燃料着火时最好用水扑灭 C、炒菜时油锅中的油不慎着火,可用锅盖盖灭 D、发现厨房内天然气管道漏气,应立即关闭气阀并轻轻开窗通风3. 化学实验技能是学习化学和实验探究的基础和保证。下列实验操作正确的是( )A、
 点燃酒精灯
B、
点燃酒精灯
B、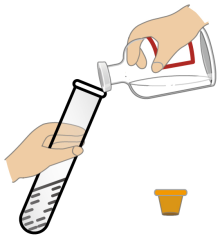 倾倒液体
C、
倾倒液体
C、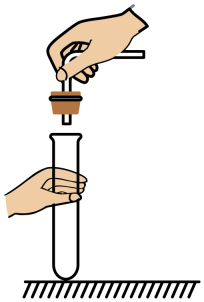 连接仪器
D、
连接仪器
D、 熄灭酒精灯
4. 元宵佳节,很多地方有放孔明灯(如图)祈福许愿的习俗,但孔明灯属于明火,极易引发火灾!孔明灯的灯芯燃烧时,火焰温度可达到300℃,但纸质灯罩却没被点燃,其原因是( )
熄灭酒精灯
4. 元宵佳节,很多地方有放孔明灯(如图)祈福许愿的习俗,但孔明灯属于明火,极易引发火灾!孔明灯的灯芯燃烧时,火焰温度可达到300℃,但纸质灯罩却没被点燃,其原因是( ) A、纸张不是可燃物不能燃烧 B、灯芯燃烧时灯罩不接触空气 C、风吹灯罩降低了灯罩的着火点 D、热量散失温度低于纸的着火点5. 物质是由微观粒子构成的。下列物质由分子构成的是( )A、金刚石 B、液氧 C、氯化钠 D、铜6. 下列实验方案不能达到实验目的的是( )
A、纸张不是可燃物不能燃烧 B、灯芯燃烧时灯罩不接触空气 C、风吹灯罩降低了灯罩的着火点 D、热量散失温度低于纸的着火点5. 物质是由微观粒子构成的。下列物质由分子构成的是( )A、金刚石 B、液氧 C、氯化钠 D、铜6. 下列实验方案不能达到实验目的的是( )选项
实验目的
实验方案
A
检验CH4中是否会有H2
点燃,在火焰上方罩一个干冷烧杯
B
鉴别二氧化碳、氧气和空气
将燃着的木条分别伸入瓶中,观察现象
C
分离KCl和MnO2的混合物
取样,加水溶解、过滤、洗涤、蒸发
D
除去CO2中的少量CO
将混合气体通过足量灼热的氧化铜
A、A B、B C、C D、D7. 建立模型是学习化学的重要方法,下列有关模型错误的是( )A、原子结构模型 B、二氧化碳分子模型
B、二氧化碳分子模型  C、燃烧条件模型
C、燃烧条件模型  D、空气组成模型
D、空气组成模型  8. 连花清瘟胶囊源自传统中医名方,可用于治疗流感,现代仪器测得其成分之一是没食子酸(化学式为C7H6O5)。下列有关没食子酸的说法正确的是( )A、属于氧化物 B、碳、氢、氧元素的质量比为12:1:16 C、含有18个原子 D、完全燃烧生成CO2和H2O9. 下表是同学们做溶液形成的实验记录。以下说法不正确的是( )
8. 连花清瘟胶囊源自传统中医名方,可用于治疗流感,现代仪器测得其成分之一是没食子酸(化学式为C7H6O5)。下列有关没食子酸的说法正确的是( )A、属于氧化物 B、碳、氢、氧元素的质量比为12:1:16 C、含有18个原子 D、完全燃烧生成CO2和H2O9. 下表是同学们做溶液形成的实验记录。以下说法不正确的是( )溶质
碘
高锰酸钾
溶剂
水
汽油
酒精
水
汽油
溶解性
微溶
易溶
可溶
易溶
不溶
A、衣服上不慎沾上碘酒,可用汽油擦洗 B、同一物质在不同溶剂中的溶解性不同 C、溶液都是均一、稳定、无色的混合物 D、水、汽油、酒精都可以作溶剂10. 如图所示:能够使气球先膨胀,过一段时间又恢复到原状的一组固体和液体是(该装置气密性良好)( ) A、硝酸铵、水 B、氢氧化钠、水 C、锌、稀硫酸 D、氯化钠、水11. 有机玻璃是由甲基丙烯酸甲酯聚合而成的,结合如图甲基丙烯酸甲酯分子结构模型分析下列的说法不正确的是( )
A、硝酸铵、水 B、氢氧化钠、水 C、锌、稀硫酸 D、氯化钠、水11. 有机玻璃是由甲基丙烯酸甲酯聚合而成的,结合如图甲基丙烯酸甲酯分子结构模型分析下列的说法不正确的是( ) A、甲基丙烯酸甲酯是由碳、氢、氧三种元素组成的 B、甲基丙烯酸甲酯分子中碳、氧原子个数3:2 C、甲基丙烯酸甲酯是氧化物 D、甲基丙烯酸甲酯中氢元素的质量分数最小12. 如图所示装置可用于实验室测定空气中氧气的含量,实验前在集气瓶内加入少量水,并将水面上方空间分为5等份,用弹簧夹加紧胶皮管,下列说法中不正确的是( )
A、甲基丙烯酸甲酯是由碳、氢、氧三种元素组成的 B、甲基丙烯酸甲酯分子中碳、氧原子个数3:2 C、甲基丙烯酸甲酯是氧化物 D、甲基丙烯酸甲酯中氢元素的质量分数最小12. 如图所示装置可用于实验室测定空气中氧气的含量,实验前在集气瓶内加入少量水,并将水面上方空间分为5等份,用弹簧夹加紧胶皮管,下列说法中不正确的是( ) A、实验时,点燃的红磷要立即伸入集气瓶中,并塞紧橡皮塞 B、集气瓶内加入少量水可防止瓶底炸裂 C、该实验所用红磷的量不足可能造成气体减少的体积小于五分之一 D、可用木炭代替红磷13. 下列化学方程式中,书写正确的是( )A、 B、 C、 D、14. 下列实验设计中不能达到目的的是( )A、探究同种物质在不同溶剂中的溶解性
A、实验时,点燃的红磷要立即伸入集气瓶中,并塞紧橡皮塞 B、集气瓶内加入少量水可防止瓶底炸裂 C、该实验所用红磷的量不足可能造成气体减少的体积小于五分之一 D、可用木炭代替红磷13. 下列化学方程式中,书写正确的是( )A、 B、 C、 D、14. 下列实验设计中不能达到目的的是( )A、探究同种物质在不同溶剂中的溶解性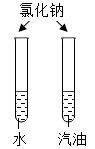 B、探究可燃物燃烧的条件
B、探究可燃物燃烧的条件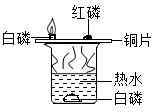 C、探究铁生锈的条件
C、探究铁生锈的条件 D、探究二氧化碳和水的反应
D、探究二氧化碳和水的反应 15. 用下图装置进行实验。升温至60℃的过程中,仅①燃烧;继续升温至260℃的过程中,仅③燃烧。下列分析不正确的是( )
15. 用下图装置进行实验。升温至60℃的过程中,仅①燃烧;继续升温至260℃的过程中,仅③燃烧。下列分析不正确的是( ) A、①燃烧,说明白磷是可燃物 B、对比①③,可说明红磷的着火点比白磷的高 C、对比②③,可验证燃烧需可燃物与氧气接触 D、④未燃烧,说明无烟煤不
A、①燃烧,说明白磷是可燃物 B、对比①③,可说明红磷的着火点比白磷的高 C、对比②③,可验证燃烧需可燃物与氧气接触 D、④未燃烧,说明无烟煤不 可燃物
16. 物质的性质决定物质的用途。下列物质的性质与其用途相匹配的是( )A、氧气具有助燃性,用作火箭发射的燃料 B、焊锡熔点低,用于焊接金属 C、石墨是黑色质软的固体,用于制作电池电极 D、二氧化碳能与水反应,用于灭火17. 将燃着的蜡烛放在图1所示的密闭容器中,同时用氧气传感器测出密闭容器中氧气含量的变化如图2所示。下列说法不正确的是( )
可燃物
16. 物质的性质决定物质的用途。下列物质的性质与其用途相匹配的是( )A、氧气具有助燃性,用作火箭发射的燃料 B、焊锡熔点低,用于焊接金属 C、石墨是黑色质软的固体,用于制作电池电极 D、二氧化碳能与水反应,用于灭火17. 将燃着的蜡烛放在图1所示的密闭容器中,同时用氧气传感器测出密闭容器中氧气含量的变化如图2所示。下列说法不正确的是( ) A、蜡烛燃烧前,密闭容器中氧气的体积分数为21% B、蜡烛燃烧需要氧气 C、蜡烛熄灭后,密闭容器中还有氧气 D、蜡烛熄灭后,密闭容器中二氧化碳的体积分数为84%18. 用分子、原子的观点解释下列现象,其中不合理的是( )A、水结成冰——0℃分子停止运动 B、电解水生成氢气和氧气——分子发生了变化 C、气体可以压缩——分子间有间隔 D、1g水约有3.01×1023个分子——分子质量很小19. 如图是a、b. c三种固体物质(不含结晶水)的溶解度曲线,下列说法正确的是( )
A、蜡烛燃烧前,密闭容器中氧气的体积分数为21% B、蜡烛燃烧需要氧气 C、蜡烛熄灭后,密闭容器中还有氧气 D、蜡烛熄灭后,密闭容器中二氧化碳的体积分数为84%18. 用分子、原子的观点解释下列现象,其中不合理的是( )A、水结成冰——0℃分子停止运动 B、电解水生成氢气和氧气——分子发生了变化 C、气体可以压缩——分子间有间隔 D、1g水约有3.01×1023个分子——分子质量很小19. 如图是a、b. c三种固体物质(不含结晶水)的溶解度曲线,下列说法正确的是( ) A、a的溶解度大于b的溶解度 B、P点表示t1℃时a、c两物质溶解度相等 C、将t1℃饱和的c溶液升温到t2℃,得到的是不饱和溶液 D、将t2℃,等质量a、b、c三种物质的饱和溶液降温到t1℃时,所得溶液中溶质质量分数由大到小的顺序为: b>a=c20. 取镁、铝两种金属的混合物12.6g,加入到一定量的稀硫酸中恰好完全反应,反应后溶液质量增加了11.4g。将反应后的溶液蒸发结晶、干燥,所得固体质量为( )A、24.0g B、36.6g C、70.2g D、82.4g
A、a的溶解度大于b的溶解度 B、P点表示t1℃时a、c两物质溶解度相等 C、将t1℃饱和的c溶液升温到t2℃,得到的是不饱和溶液 D、将t2℃,等质量a、b、c三种物质的饱和溶液降温到t1℃时,所得溶液中溶质质量分数由大到小的顺序为: b>a=c20. 取镁、铝两种金属的混合物12.6g,加入到一定量的稀硫酸中恰好完全反应,反应后溶液质量增加了11.4g。将反应后的溶液蒸发结晶、干燥,所得固体质量为( )A、24.0g B、36.6g C、70.2g D、82.4g二、填空题(共6题,总计 35分)
-
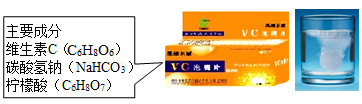
21. 用化学用语填空:(1)、可以用于人工降雨的气体是。(2)、2个氮原子(3)、5个硫酸根离子。22. 年初,我国科学家利用显微镜针头手工“敲打”原子,成功合成三角烯(化学式为C22H14),它将在量子计算、量子信息处理和自旋电子学等领域展现巨大应用潜力。则三角烯中两种元素的质量比为;一个三角烯分子由个原子构成的。23. 铝、铁、铜是人类广泛使用的三种金属,与我们生活息息相关。(1)、在空气中铝制品更耐腐蚀,原因是。(写出化学方程式)(2)、人们大量使用的是合金而不是纯金属,这是因为合金具有更多优良性能,例如钢比纯铁硬度(填“大”或“小”)。(3)、用下列试剂验证这三种金属的活动性顺序,每种实验方案所需试剂如下,其中能达到实验目的的是____。A、Al、Fe、CuSO4溶液 B、Al(NO)3溶液、FeCl2溶液、Cu C、Al、FeSO4溶液、Cu24. 将乙醇和汽油按一定比例混合可制成乙醇汽油,乙醇完全燃烧的化学方程式为 , 将4.8g的甲烷和16.0g氧气充分反应后(反应物无剩余),生成4.4gCO2、xgM和10.8gH2O,则x的值为;M中碳元素的质量为。25. Vc泡腾片,可增强机体抵抗力,某品牌维C泡腾片主要成分如图所示。将其溶于水,有许多气泡产生。实验产生的气泡中不可能含有N2 , 是因为;把纯净的维生素C(C6H8O6)在一定质量的氧气中充分燃烧,生成了CO、CO2和H2O,测得生成物的总质量为30.4g,其中水的质量为7.2g,则参加反应的氧气质量为g。
 26. 金属活动性顺序中,不能与盐酸发生置换反应,且元素符号小写字母为g的金属有(填元素符号)。含有铝粉2.7g、锌粉6.5g、铁粉5.6g、铜粉6.4g与一定质量的稀硫酸充分反应后有9.2g金属剩余,则生成氢气的质量为g。
26. 金属活动性顺序中,不能与盐酸发生置换反应,且元素符号小写字母为g的金属有(填元素符号)。含有铝粉2.7g、锌粉6.5g、铁粉5.6g、铜粉6.4g与一定质量的稀硫酸充分反应后有9.2g金属剩余,则生成氢气的质量为g。三、实验探究题(共3题,总计20分)
-
27. 通过一年的化学学习,你已经掌握了实验室制取气体的有关知识,请结合下图回答相关问题。
 (1)、写出图中标有序号①的仪器名称。(2)、实验室欲使用高锰酸钾制取氧气,应选择的发生装置和收集装置是;若选择F装置收集氧气,气体应从(填端口字母)端进入。(3)、实验室欲制取二氧化碳,反应原理用化学方程式表示为。用D装置收集二氧化碳,验满的方法是。28. 甲同学设计了如下实验装置验证一氧化碳的部分性质并验证产物。实验时在点燃B处酒精灯之前先通入一氧化碳排出装置中的空气,然后继续实验。
(1)、写出图中标有序号①的仪器名称。(2)、实验室欲使用高锰酸钾制取氧气,应选择的发生装置和收集装置是;若选择F装置收集氧气,气体应从(填端口字母)端进入。(3)、实验室欲制取二氧化碳,反应原理用化学方程式表示为。用D装置收集二氧化碳,验满的方法是。28. 甲同学设计了如下实验装置验证一氧化碳的部分性质并验证产物。实验时在点燃B处酒精灯之前先通入一氧化碳排出装置中的空气,然后继续实验。 (1)、B中反应的化学方程式是;此处出现的现象是。(2)、实验过程中,D处点燃的目的是。(3)、对该实验的分析正确的是(选填编号)。
(1)、B中反应的化学方程式是;此处出现的现象是。(2)、实验过程中,D处点燃的目的是。(3)、对该实验的分析正确的是(选填编号)。a.实验结束时应先熄灭B处酒精灯
b.C中增加的质量与B中固体减少的质量相等
c.反应结束后继续通入一氧化碳的目的是防止铜被氧化
(4)、甲同学认为A装置用于证明一氧化碳不能和石灰水反应,乙同学认为省略A可达到同样的目的,因为。29. 常温下没有氧气存在时,铁与水几乎不反应,但高温下,铁与水蒸气能反应生成一种常见铁的氧化物和一种气体。小明很好奇,设计如下实验探究铁粉与水蒸气反应后的产物。 (1)、 试管尾部放一团湿棉花的目的是。(2)、探究生成的气体是什么?
(1)、 试管尾部放一团湿棉花的目的是。(2)、探究生成的气体是什么?用燃着的木条靠近肥皂泡,有爆鸣声,稍后有肥皂泡飘到空中。说明生成的气体是。
(3)、探究试管中剩余固体成分是什么?【查阅资料】
①
常见铁的氧化物
FeO
Fe2O3
Fe3O4
颜色、状态
黑色粉末
红棕色粉末
黑色晶体
能否被磁铁吸引
否
否
能
②四氧化三铁能与稀酸反应,但不产生气体。
【初步验证】试管中剩余固体为黑色,能全部被磁铁吸引。
【猜想与假设】猜想一:剩余固体是Fe与Fe3O4:猜想二:剩余固体是。
【实验探究】
实验操作
实验现象及结论
【实验结论】铁和水蒸气反应的化学方程式为。
【反思与交流】该黑色固体不可能是Fe2O3 , 理由是。
四、计算题(共5分)
-
30. 为测定某含杂质的镁带中镁的质量分数,某同学取3g该镁带样品于烧杯中,逐滴加入稀硫酸,当加入50g稀硫酸时,恰好完全反应,反应后得到的混合物总质量是52.8g(杂质不与稀硫酸反应)。求:(1)、生成氢气的质量是g。(2)、该镁带中镁的质量分数。