广东省深圳市2023-2024学年九年级下学期开学质量检测化学题
试卷更新日期:2024-03-07 类型:开学考试
一、选择题I (每小题只有一个选项符合题意,每小题1.5分,共计12分)
-
1. 中国诗词中蕴藏着丰富的化学知识,下列描述不正确的是 ( )A、“蜡烛有心还惜别,替人垂泪到天明”中只涉及化学变化 B、“酒香不怕巷子深”说明分子是在不断地运动 C、“真金不怕火炼”中的金在加热条件下也不能与O2发生反应, D、“两编千片白雪茧,六百二斗青铜钱”中的“青铜”属于金属材料,2. 小圳同学在寒假看到如下标志并判断,则他的错误之处是( )A、毒性物质
 B、禁止烟火
B、禁止烟火 C、可以燃烧
C、可以燃烧 D、当心爆炸物
D、当心爆炸物 3. 化学与人类的生活、安全、生产以及科技等密切相关。下列描述不正确的是( )A、生活中常食用的“高钙奶”、“加碘盐”中的钙、碘指的是元素 B、发现液化气泄漏,应立即打开排风扇开关 C、使用乙醇汽油可减少对空气的污染,也可缓解化石燃料紧缺 D、钛合金广泛应用于火箭和航天飞机等4. 下列化学用语与其对应的描述都正确的是( )A、2N——两个氮气分子 B、CO32−——碳酸根离子 C、Co——氧化碳的化学式 D、——氯化铁中铁的化合价为+25. 学习氧气相关知识后,小深和同学组队开启了“过氧化氢溶液制取氧气”的项目式学习,
3. 化学与人类的生活、安全、生产以及科技等密切相关。下列描述不正确的是( )A、生活中常食用的“高钙奶”、“加碘盐”中的钙、碘指的是元素 B、发现液化气泄漏,应立即打开排风扇开关 C、使用乙醇汽油可减少对空气的污染,也可缓解化石燃料紧缺 D、钛合金广泛应用于火箭和航天飞机等4. 下列化学用语与其对应的描述都正确的是( )A、2N——两个氮气分子 B、CO32−——碳酸根离子 C、Co——氧化碳的化学式 D、——氯化铁中铁的化合价为+25. 学习氧气相关知识后,小深和同学组队开启了“过氧化氢溶液制取氧气”的项目式学习,下图实验操作中正确的是( )
A、取少量MnO2 B、倾倒H2O2溶液
B、倾倒H2O2溶液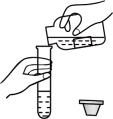 C、回收MnO2
C、回收MnO2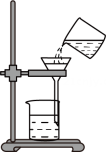 D、称回收的MnO2质量
D、称回收的MnO2质量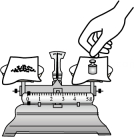 6. 科学家通过在DNA或RNA的核苷酸分子中化学修饰的发现,能快速研发出新疫苗。核苷酸的化学式为C10H14N5O6P (其相对分子质量是331),下列有关说法正确的是( )A、核苷酸属于氧化物 B、一个核苷酸分子中共有35个原子 C、核苷酸中碳与氢元素质量比为5:7 D、核苷酸中碳元素的质量分数最大7. 2023年诺贝尔化学奖授予发现和合成量子点的三位科学家。量子点组成中常含镉等元素。下图是镉的结构示意图及其在元素周期表中的信息,则有关镉的说法不正确的是( )
6. 科学家通过在DNA或RNA的核苷酸分子中化学修饰的发现,能快速研发出新疫苗。核苷酸的化学式为C10H14N5O6P (其相对分子质量是331),下列有关说法正确的是( )A、核苷酸属于氧化物 B、一个核苷酸分子中共有35个原子 C、核苷酸中碳与氢元素质量比为5:7 D、核苷酸中碳元素的质量分数最大7. 2023年诺贝尔化学奖授予发现和合成量子点的三位科学家。量子点组成中常含镉等元素。下图是镉的结构示意图及其在元素周期表中的信息,则有关镉的说法不正确的是( ) A、镉属于金属元素 B、镉的质子数为48 C、镉的相对原子质量是112.4 D、镉原子在反应中易得到电子8. 近几年,深圳实行“一芯两核多支点”发展战略,通过科技创新打造“湾东智芯”。三氟化氮(NF3) 是一种优良的等离子蚀刻气体,用NF3蚀刻硅芯片时的产物均为气体,在芯片表面没有任何残留物。该反应的微观示意图如下,下列有关说法正确的是( )
A、镉属于金属元素 B、镉的质子数为48 C、镉的相对原子质量是112.4 D、镉原子在反应中易得到电子8. 近几年,深圳实行“一芯两核多支点”发展战略,通过科技创新打造“湾东智芯”。三氟化氮(NF3) 是一种优良的等离子蚀刻气体,用NF3蚀刻硅芯片时的产物均为气体,在芯片表面没有任何残留物。该反应的微观示意图如下,下列有关说法正确的是( )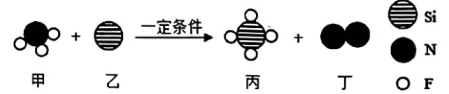 A、该反应四种物质中只有一种单质 B、该反应前后原子数目发生了改变 C、反应物甲与乙粒子个数比为4:3 D、物质丙与丁质量比为26:7
A、该反应四种物质中只有一种单质 B、该反应前后原子数目发生了改变 C、反应物甲与乙粒子个数比为4:3 D、物质丙与丁质量比为26:7二、选择题Ⅱ(每小题只有一个选项符合题意,每小题2分,共计8分)
-
9. 下列实验设计能达到实验目的的是( )
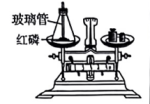
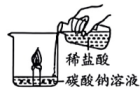
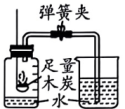
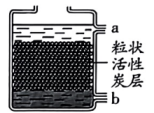
A.验证质量守恒定律
B.探究灭火的原理之一
C.用于测定空气中O2的含量
D.海水从b口进入净化后可得纯净水
A、A B、B C、C D、D10. 物质之间关系图如下(“一”表示两端物质能发生反应,“→” 表示物质之间的转化关系),反应条件和部分反应物已经省略。下列有关说法正确的是( )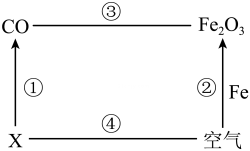 A、若X为碳,则反应①只能是碳燃烧不充分 B、反应②的发生有利于金属资源的保护 C、反应③的现象中固体由黑色逐渐变成红色 D、若X为煤,反应④一些产物溶于雨水会形成酸雨11. 下列实验方案不能达到实验目的是( )
A、若X为碳,则反应①只能是碳燃烧不充分 B、反应②的发生有利于金属资源的保护 C、反应③的现象中固体由黑色逐渐变成红色 D、若X为煤,反应④一些产物溶于雨水会形成酸雨11. 下列实验方案不能达到实验目的是( )选项
实验目的
实验方案
A
除去CO中的CO2
将气体通过灼热的CuO
B
鉴别水与酒精
闻气味
C
比较呼出气体与空气中O2的含量
燃着的小木条
D
验证Cu与Ag的金属活动性
将Cu丝浸入AgNO3溶液中
A、A B、B C、C D、D12. 小圳同学在探究金属与酸的反应时做了如下图1实验,分别将形状、质量相同的Mg、Al、Zn、Fe和Cu打磨后放入烧瓶中,再注入足量体积和浓度均相同的稀硫酸,利用压强传感器采集数据,得到下图2所示的气压变化情况。下列有关说法错误的是( )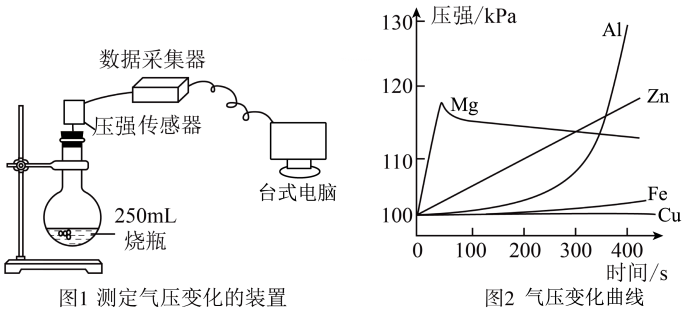 A、五种金属中Mg的金属活动性最强 B、Zn与稀硫酸反应产生H2速率比Fe快 C、反应结束后消耗稀硫酸最少的金属是Al D、由图2可知金属Cu不能与稀硫酸反应
A、五种金属中Mg的金属活动性最强 B、Zn与稀硫酸反应产生H2速率比Fe快 C、反应结束后消耗稀硫酸最少的金属是Al D、由图2可知金属Cu不能与稀硫酸反应三、非选择题(每空1分,化学方程式1.5分,16题根据本题标准给分,共计30分)
-
13. 实验室现有药品:高锰酸钾、氯酸钾、过氧化氢溶液、二氧化锰粉末、块状石灰石、稀盐酸、稀硫酸。使用装置C反应物须块状固体和液体,反应条件是常温,优点是可控制反应的发生和停止。请根据实验室现有药品和下列装置回答问题。
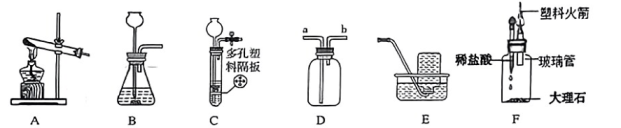 (1)、反应原理:实验室加热混合物制取O2的化学方程式为 。(2)、仪器选用:用过氧化氢溶液制取较纯净的O2时,则发生装置和收集装置选用(填写字母)。(3)、药品选用:用C装置来制取某气体,选用的药品为 (填写药品名称)。(4)、收集气体:收集CO2用装置D,则气体应从 口进 (填“a”或“b”)。(5)、趣味实验:小圳同学在社团活动中利用F装置“发射火箭”,先挤压胶头滴管,套在玻璃管上的塑料火箭向上冲出,完成发射:则F装置中发生反应的化学方程式为 。14. H2、CO和CH4都具有可燃性,CO和H2还具有还原性,但CH4有没有还原性呢?于是化学社团的同学在老师的指导下进行如下实验(装置气密性良好,控制一定的温度)。
(1)、反应原理:实验室加热混合物制取O2的化学方程式为 。(2)、仪器选用:用过氧化氢溶液制取较纯净的O2时,则发生装置和收集装置选用(填写字母)。(3)、药品选用:用C装置来制取某气体,选用的药品为 (填写药品名称)。(4)、收集气体:收集CO2用装置D,则气体应从 口进 (填“a”或“b”)。(5)、趣味实验:小圳同学在社团活动中利用F装置“发射火箭”,先挤压胶头滴管,套在玻璃管上的塑料火箭向上冲出,完成发射:则F装置中发生反应的化学方程式为 。14. H2、CO和CH4都具有可燃性,CO和H2还具有还原性,但CH4有没有还原性呢?于是化学社团的同学在老师的指导下进行如下实验(装置气密性良好,控制一定的温度)。[查阅资料]①白色的无水硫酸铜遇水变成蓝色; CH4、CO2、 CO均不能与无水硫酸铜反应。
②CO能与银氨溶液反应产生银白色沉淀。
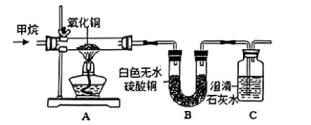 (1)、点燃酒精灯前先通一会儿CH4 , 其目的是。(2)、①实验中装置A中的现象是固体粉末由黑色逐渐变成红色,实验结束后,取少量红色粉末于试管中并加入稀硫酸,则无明显现象。
(1)、点燃酒精灯前先通一会儿CH4 , 其目的是。(2)、①实验中装置A中的现象是固体粉末由黑色逐渐变成红色,实验结束后,取少量红色粉末于试管中并加入稀硫酸,则无明显现象。②装置B的实验现象是。
③装置C中澄清石灰水变浑浊,该反应的化学方程式为。
(3)、该实验装置的缺陷是没有尾气处理,为确认尾气是否对空气造成污染,可进行如下检测。④将尾气通入盛有溶液的试管中, 根据是否产生银白色沉淀确定对空气有无污染。
⑤由上述实验记录了如下数据,可得出尾气对空气 (填 “有”或“无”)污染。
装置A中玻璃管(含药品)的质量
装置B的质量
装置C的质量
反应前
150g
152.6g
254.8g
反应后
143.6g
156.2g
259.2g
综上述,CH4具有还原性。CH4与氧化铜反应的化学方程式为。
15. 明矾矿加工排出大量的矾浆(其中氧化铝Al2O3 可达50%等),会造成大量有用成分流失和污染环境。以矾浆为原料生产Al(OH)3是矾浆综合利用的有效途径。AI(OH)3性质较稳定,无味无毒,可作阻燃剂,广泛应用于造纸、医药、化工等方面。下图是用矾浆制取Al(OH)3的工艺流程。请回答下列问题。已知:①滤液1中硫酸铝[Al2(SO4)3]和部分水是矾浆中 的Al2O3与硫酸[H2SO4]反应生成的;滤液2中主要成分是Al2(SO4)3和水等。
②Al2(SO4)3和NaOH反应的产物与NaOH的量有关,当NaOH少量或恰好时生成Al(OH)3沉淀;当NaOH过量时生成可溶性的偏铝酸钠[NaAlO2].
③Al(OH)3温度在200-300℃时就生成Al2O3和H2O。
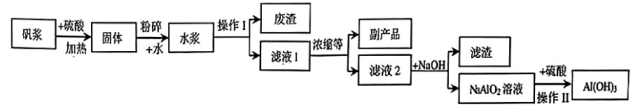 (1)、粉碎的目的是 。(2)、操作Ⅰ和操作Ⅱ都是与初中化学操作 ( 填写实验操作名称)的原理相同。(3)、写出Al2O3 与H2SO4反应的化学方程式为。(4)、在滤液2中加入NaOH的量应该为 (填 “少量"、“恰好” 或“过量”)。(5)、操作Ⅱ所得的Al(OH)3沉淀需经过水洗、干燥才能获得较纯净的Al(OH)3;但在干燥过程中温度需控制在200℃以下,其原因是(用化学方程式表示) , 此化学反应属于反应. (填写化学反应基本类型)。(6)、利用矾浆制取Al(OH)3的优点是 (写一条即可) 。16. 我国2023年制氢产量约计4000万吨,位列世界第一。但我国制氢技术主要是以化石燃料制H2和工业副产品制H2为主,只有5%的比例是通过电解水制取H2的方式。P2G技术(工作原理如下图Ⅰ所示)实现综合能源系统中电(尤其是将廉价盈余的电)到气的能量的转换,反应生成CH4最后通入天然气管网中。但电解水制取的H2转化为CH4会造成额外的能量损失;随着氢燃料电池(如下图Ⅱ所示) 和氢气天然气混合输送技术的相关研究进展,实现了氢能的高效利用。
(1)、粉碎的目的是 。(2)、操作Ⅰ和操作Ⅱ都是与初中化学操作 ( 填写实验操作名称)的原理相同。(3)、写出Al2O3 与H2SO4反应的化学方程式为。(4)、在滤液2中加入NaOH的量应该为 (填 “少量"、“恰好” 或“过量”)。(5)、操作Ⅱ所得的Al(OH)3沉淀需经过水洗、干燥才能获得较纯净的Al(OH)3;但在干燥过程中温度需控制在200℃以下,其原因是(用化学方程式表示) , 此化学反应属于反应. (填写化学反应基本类型)。(6)、利用矾浆制取Al(OH)3的优点是 (写一条即可) 。16. 我国2023年制氢产量约计4000万吨,位列世界第一。但我国制氢技术主要是以化石燃料制H2和工业副产品制H2为主,只有5%的比例是通过电解水制取H2的方式。P2G技术(工作原理如下图Ⅰ所示)实现综合能源系统中电(尤其是将廉价盈余的电)到气的能量的转换,反应生成CH4最后通入天然气管网中。但电解水制取的H2转化为CH4会造成额外的能量损失;随着氢燃料电池(如下图Ⅱ所示) 和氢气天然气混合输送技术的相关研究进展,实现了氢能的高效利用。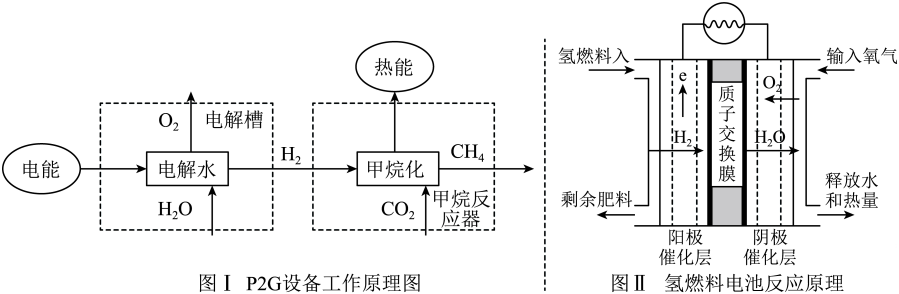 (1)、图Ⅰ中电解水说明水是由组成;电解槽中正极与负极产生气体的体积之比为 。(2)、图Ⅱ中氢燃料发生反应的化学方程式为。(3)、氢能源是 (填写 “可再生”或“不可再生”)能源。(4)、将2023年我国电解H2O制取氢气的40%用P2G设备生成CH4 , 其发生反应的化学方程式为: 4H2+CO2 CH4+2H2O,则理论上约能生成CH4的质量是多少?(写出规范的计算步骤)
(1)、图Ⅰ中电解水说明水是由组成;电解槽中正极与负极产生气体的体积之比为 。(2)、图Ⅱ中氢燃料发生反应的化学方程式为。(3)、氢能源是 (填写 “可再生”或“不可再生”)能源。(4)、将2023年我国电解H2O制取氢气的40%用P2G设备生成CH4 , 其发生反应的化学方程式为: 4H2+CO2 CH4+2H2O,则理论上约能生成CH4的质量是多少?(写出规范的计算步骤)