第2章 粒子的模型与符号(B卷)--2023-2024学年浙教版科学八年级下册
试卷更新日期:2024-03-06 类型:单元试卷
一、选择题
-
1. 下列表达方式中属于符号的是( )A、水分子
 B、电压表
B、电压表  C、漏斗
C、漏斗  D、电路
D、电路 2. 如图是教材中用来表示电解水过程的示意图(其中“O”“●”分别表示氢原子和氧原子)分析示意图,可作出的正确判断是( )
2. 如图是教材中用来表示电解水过程的示意图(其中“O”“●”分别表示氢原子和氧原子)分析示意图,可作出的正确判断是( ) A、常温常压下水可以分解 B、氢原子在该变化过程中不可再分 C、1个水分子中含有1个氢分子和1个氧原子 D、电解水的最终产物是氢、氧原子3. 有关Mg和Mg2+两种粒子的比较,下列说法正确的是( )
A、常温常压下水可以分解 B、氢原子在该变化过程中不可再分 C、1个水分子中含有1个氢分子和1个氧原子 D、电解水的最终产物是氢、氧原子3. 有关Mg和Mg2+两种粒子的比较,下列说法正确的是( )①具有相同的质子数 ②化学性质相同 ③核外电子总数相同
④属于同种元素 ⑤相对原子质量相同
A、①②④ B、②③④ C、①④⑤ D、③④⑤4. 下列关于原子核的叙述:①通常是由分子和电子构成;②通常是由质子和中子构成;③带正电荷;④不显电性;⑤不能再分;⑥跟原子比较体积较小,但却集中了原子的主要质量。其中正确的是( )A、②④⑥ B、②③⑥ C、①③⑤ D、①④⑤5. 据报道,一种新型铝离子电池,比现今普遍使用的锂离子电池具有更加优良的性能。未来该铝离子电池或将成为下一代高性价比电池的理想选择。如图是元素周期表中锂、铝两种元素的有关信息,下列说法不正确的是( ) A、锂、铝元素在周期表中分别位于第二、三周期 B、锂、铝元素都属于金属元素 C、锂、铝属于不同元素是因为中子数不同 D、核外电子数Al3+比Li+多8个6. 如图所示,1911年卢瑟福用带正电的α粒子轰击金属箔,实验发现:
A、锂、铝元素在周期表中分别位于第二、三周期 B、锂、铝元素都属于金属元素 C、锂、铝属于不同元素是因为中子数不同 D、核外电子数Al3+比Li+多8个6. 如图所示,1911年卢瑟福用带正电的α粒子轰击金属箔,实验发现:
①大多数α粒子能穿透金属箔而不改变原来的运动方向;②一小部分α粒子改变了原来的运动方向;
③有极少数α粒子被弹了回来。根据以上实验现象, 可以得到( )
A、原子核带正电荷 B、原子是一个实心球体 C、电子只能在原子内的一些特定的稳定轨道上运动 D、原子核体积很大,但是质量比α粒子小得多7. 如图是地壳中各元素的含量 (质量分数)分布图,下列说法正确的是 ( )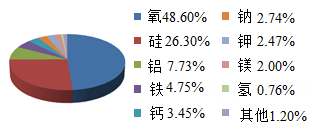 A、地壳中含量最多的元素是金属元素 B、由图可知,各元素在地壳中的含量相差不大 C、地壳中最多的金属元素是铝,也就是金属铝 D、地壳中非金属元素的总含量大于金属元素,种类少于金属元素8. 对于下列几种化学符号,有关说法正确的是( )
A、地壳中含量最多的元素是金属元素 B、由图可知,各元素在地壳中的含量相差不大 C、地壳中最多的金属元素是铝,也就是金属铝 D、地壳中非金属元素的总含量大于金属元素,种类少于金属元素8. 对于下列几种化学符号,有关说法正确的是( )①H ②Fe2+ ③He ④P2O5 ⑤Fe3+ ⑥NaCl
A、能表示一个分子的是①④⑥ B、表示物质组成的化学式是③④⑥ C、②⑤的质子数相同,化学性质也相同 D、④中的数字“5”表示五氧化二磷中有 5 个氧原子9. 溴元素的原子结构示意图及其在周期表中的信息如图所示,下列说法正确的是( )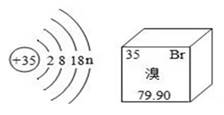 A、n=7 B、该元素为金属元素 C、相对原子质量和中子数均为35g D、原子序数、核电荷数、质子数均为79.9010. 如图氢氧化钠溶液与稀盐酸恰好完全反应的微观示意图,由此得出的结论不正确的是( )
A、n=7 B、该元素为金属元素 C、相对原子质量和中子数均为35g D、原子序数、核电荷数、质子数均为79.9010. 如图氢氧化钠溶液与稀盐酸恰好完全反应的微观示意图,由此得出的结论不正确的是( )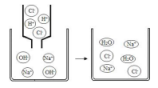 A、反应结束时溶液的pH=7 B、反应前后元素的种类没有变化 C、反应后溶液中存在的粒子只有Na+和Cl- D、该反应的实质是H+和OH-结合生成H2O分子11. 现在有些年轻人喜欢染发,染发时一般要用到一种着色剂--对苯二胺,它是一种有毒的化学药品,有致癌性,会对染发者的身体带来伤害,其分子结构如图,下列有关对苯二胺的说法不正确的是( )
A、反应结束时溶液的pH=7 B、反应前后元素的种类没有变化 C、反应后溶液中存在的粒子只有Na+和Cl- D、该反应的实质是H+和OH-结合生成H2O分子11. 现在有些年轻人喜欢染发,染发时一般要用到一种着色剂--对苯二胺,它是一种有毒的化学药品,有致癌性,会对染发者的身体带来伤害,其分子结构如图,下列有关对苯二胺的说法不正确的是( ) A、对苯二胺的化学式为C6H8N2 B、对苯二胺的相对分子质量为108g C、对苯二胺中碳、氢、氮元素的质量比为18:2:7 D、对苯二胺能被皮肤少量吸收12. X元素1个原子的质量是m克,Y元素的相对原子质量为A;化合物XY2的相对分子质量是M,则W克XY2中含有Y的原子数是( )A、 B、 C、 D、
A、对苯二胺的化学式为C6H8N2 B、对苯二胺的相对分子质量为108g C、对苯二胺中碳、氢、氮元素的质量比为18:2:7 D、对苯二胺能被皮肤少量吸收12. X元素1个原子的质量是m克,Y元素的相对原子质量为A;化合物XY2的相对分子质量是M,则W克XY2中含有Y的原子数是( )A、 B、 C、 D、二、填空题
-
13. 2019年诺贝尔化学奖颁发给了在锂电池领域作出重大贡献的吉野彰等三位科学家,分析回答下列问题:
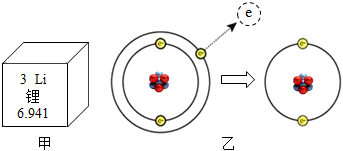 (1)、图甲是元素周期表中锂元素的相关信息,可知锂元素的原子核电荷数是。(2)、图乙表示锂原子转变为锂离子的过程,锂离子符号可表示为。14. 如图表示的是地壳里所含各种元素的质量分数。请根据下图回答下列问题:
(1)、图甲是元素周期表中锂元素的相关信息,可知锂元素的原子核电荷数是。(2)、图乙表示锂原子转变为锂离子的过程,锂离子符号可表示为。14. 如图表示的是地壳里所含各种元素的质量分数。请根据下图回答下列问题: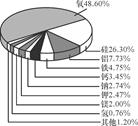 (1)、地壳中含量最多的非金属元素是;(2)、图中表示出的金属元素共有种;(3)、地壳中含量最多的金属元素是;(4)、这幅图属于符号还是模型?。15. 2018 年 1 月 31 日,与地球分别 150 年的“超级蓝色血月全食”,终于又来了。此次月食让全世界的目光再次聚焦月球,其实月球并没有我们想象的那么贫瘠,它的矿产资源极为丰富,地球上最常见的 17种元素,在月球上比比皆是。以铁为例,仅月面表层 5 厘米厚的沙土就含有上亿吨铁,这里的“铁”指的是(填“元素”、“分子”或“原子”),已知铁原子的核电荷数为 26,相对原子质量为 56,则铁原子的核外电子数是 , 核内中子数是。假如某一天地球铁矿产资源耗尽,我们可以用“磁选”的方式对月球沙子进行处理,从而获得一部分铁(填“单质”、“化合物”)。
(1)、地壳中含量最多的非金属元素是;(2)、图中表示出的金属元素共有种;(3)、地壳中含量最多的金属元素是;(4)、这幅图属于符号还是模型?。15. 2018 年 1 月 31 日,与地球分别 150 年的“超级蓝色血月全食”,终于又来了。此次月食让全世界的目光再次聚焦月球,其实月球并没有我们想象的那么贫瘠,它的矿产资源极为丰富,地球上最常见的 17种元素,在月球上比比皆是。以铁为例,仅月面表层 5 厘米厚的沙土就含有上亿吨铁,这里的“铁”指的是(填“元素”、“分子”或“原子”),已知铁原子的核电荷数为 26,相对原子质量为 56,则铁原子的核外电子数是 , 核内中子数是。假如某一天地球铁矿产资源耗尽,我们可以用“磁选”的方式对月球沙子进行处理,从而获得一部分铁(填“单质”、“化合物”)。 16.(1)、用化学符号填空。
16.(1)、用化学符号填空。①地壳中含量最高的金属元素:;②5个碳酸根离子:;③氦气。
④过氧化氢:;⑤硝酸亚铁:;⑥碳酸氢铵:;⑦氯化银:。
⑧3O2中数字“2”的意义; ⑨中数字“2”的意义 。
(2)、有下列物质:①氧气;②液氮;③洁净的空气:④冰水混合物;⑤二氧化碳;⑥食盐水;⑦氖气;⑧铜丝,请用这些物质的数字代号填空。a.属于金属单质的是;b.属于非金属单质的是;c.属于稀有气体的是;d.属于混合物的;e.属于化合物的是。
17. 元素周期表将已知元素科学有序地排列起来,便于我们研究它们的性质和用途.下表表示元素周期表的一部分,请回答下列问题。H
He
①
N
②
Ne
③
Ar
(1)、元素在周期表中的分布是有规律的,其中①②③所代表的元素中是非金属元素。(填写元素符号)(2)、表中氮元素的化合价有多种,请写出化合价为+1价的氮的氧化物。(用化学式表示)。(3)、最近,科学家用大量高速钙原子轰击锫原子,形成了117号元素的原子,该元素原子核中一定含有117个。18. 如图所示是1-18号元素中某些元素的部分化合价,回答下列问题。1 H
2He
3Li
4Be
5B
6C
7N
8O
9F
10Ne
11Na
+1
12Mg
+2
13Al
+3
14 Si
+4 -4
15P
16S
+6 -2
17Cl
18Ar
(1)、9号元素属于(选填“金属元素”或非金属元素)。(2)、11号元素与16号元素组成的化合物为(填化学式)。(3)、12号元素形成的离子符号为。(4)、2H216O的相对分子质量约为 。三、实验探究题
-
19. 卢瑟福用α粒子(α粒子是带两个单位正电荷的氦原子核)轰击金箔的实验,推翻了汤姆生在1903年提出的原子结构模型,为建立现代原子理论打下了基础(如图)。
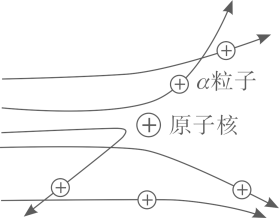
现象1:大多数α粒子能穿透金箔而不改变原来的运动方向。
现象2:一小部分α粒子改变原来的运动方向。
现象3:极少数α粒子被弹了回来。
(1)、请你根据原子结构知识分析现象1产生的原因:。(2)、通过该实验的上述三种现象 (选填“能”或“不能”)获得核外电子带有负电荷的结论。(3)、1919年,卢瑟福用加速了的高能a粒子轰击氮原子,结果有种微粒从氮原子中被打出,而α粒子留在了氮原子中,使氮原子变成了氧原子,从现代观点看,被打出的微粒一定是 。20. 了解物质的组成和结构,有助于认识物质的性质.(1)、如图表示核电荷数为11~17的元素最高和最低化合价.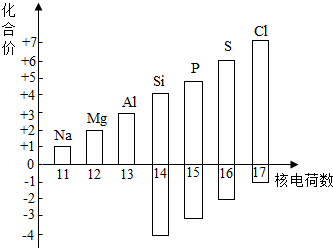
①从图中可以看出,氯元素的最高正价是 .
②若某元素既可显正价,又可显负价,则最高正价与最低负价绝对值的代数和为 .
③写出图中元素的化合价随着核电荷数递增的一条变化规律 .
四、解答题
-
21. “青团”是宁波的一种传统食物。在“青团”制作过程中,需要往糯米粉中添加艾草(或艾草汁)。艾草含有侧柏莲酮芳香油(C10H10O),侧柏莲酮芳香油是一种淡黄色液体,具有香脂香气,所以“青团”具有独特风味。(1)、侧柏莲酮芳香油由种元素组成。(2)、侧柏莲酮芳香油的相对分子质量是。(3)、7.3g侧柏莲桐芳香油中碳元素的质量为g。22. 每年11月是橘子丰收的时节,橘子中含有丰富的核黄素即维生素B2(分子式:C17H20N4O6)
相对分子质量:376,黄至橙黄色结晶性粉末,微臭,味微苦。核黄素具有热稳定性,不受空气中氧的影响,在酸性溶液中稳定,但在碱性溶液中不稳定,光照射容易分解。
(1)、核黄素在物质分类上属于。(选填“氧化物”“酸”“碱”“盐”“有机物”)(2)、写出一条核黄素的化学性质。(3)、一个核黄素分子中共有个原子。(4)、计算94克核黄素中含有多少克氢元素?