第2章 粒子的模型与符号(A卷)--2023-2024学年浙教版科学八年级下册
试卷更新日期:2024-03-06 类型:单元试卷
一、选择题
-
1. 原子结构模型是经过一代代科学家不断地发现和提出新的原子结构模型的过程。下列有关图①②③④所示的四种原子结构模型的叙述错误的是( )
 A、汤姆生认为图①模型中正电荷均匀分布在整个面包内,电子像葡萄干镶嵌其中 B、如图②模型波尔认为电子只能在原子内的一些特定的稳定轨道上绕核运动 C、卢瑟福在实验基础上提出带负电的电子绕带正电且体积很小的原子核运动的图④模型 D、依据提出时间先后顺序,正确的排列是①②④③2. 元素“Al”的名称是( )A、氦 B、氯 C、硅 D、铝3. 2022年3月16日,日本福岛县附近海域发生强烈地震,福岛核电站中上百万吨核污水险些排入大海。核污水中含有氚(氢的一种同位素),右图为氚原子结构示意图,由图可知氚原子( )
A、汤姆生认为图①模型中正电荷均匀分布在整个面包内,电子像葡萄干镶嵌其中 B、如图②模型波尔认为电子只能在原子内的一些特定的稳定轨道上绕核运动 C、卢瑟福在实验基础上提出带负电的电子绕带正电且体积很小的原子核运动的图④模型 D、依据提出时间先后顺序,正确的排列是①②④③2. 元素“Al”的名称是( )A、氦 B、氯 C、硅 D、铝3. 2022年3月16日,日本福岛县附近海域发生强烈地震,福岛核电站中上百万吨核污水险些排入大海。核污水中含有氚(氢的一种同位素),右图为氚原子结构示意图,由图可知氚原子( )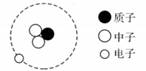 A、含有2个质子 B、核电荷数为1 C、相对原子质量为4 D、质子数和中子数相等4. 近日,某省发现部分大米镉超标,镉超标易引起镉中毒。镉元素核电荷数为48,原子核内质子数与中子数和为 112,则镉原子的核外电子数是( )A、48 B、64 C、112 D、1605. 元素符号能表示一定的意义,不同的元素符号表示的意义不同。下列对元素符号表示的意义解释正确的是( )
A、含有2个质子 B、核电荷数为1 C、相对原子质量为4 D、质子数和中子数相等4. 近日,某省发现部分大米镉超标,镉超标易引起镉中毒。镉元素核电荷数为48,原子核内质子数与中子数和为 112,则镉原子的核外电子数是( )A、48 B、64 C、112 D、1605. 元素符号能表示一定的意义,不同的元素符号表示的意义不同。下列对元素符号表示的意义解释正确的是( )选项
元素符号
元素符号所表示的意义
A
H
只表示氢元素
B
Fe
表示铁元素,表示一个铁原子,表示铁这种物质
C
N
只表示一个氮原子
D
O
表示氧元素,表示一个氧原子,表示氧气这种物质
A、A B、B C、C D、D6. 下列物质的化学式书写正确的是( )A、硫酸钠Na2SO4 B、氯化钙CaCl C、氦气He2 D、氧化铁FeO7. 知识梳理有助于我们对已学知识的巩固,小科同学学习物质结构知识后,以二氧化碳为 例进行了梳理,如图所示,下列选项中与 a 、b 、c 相对应的是 ( ) A、原子、原子核、核外电子 B、原子核、核外电子、原子 C、原子、核外电子、原子核 D、原子核、原子、核外电子8. 2019年7月6日,中国良渚古城遗址获准列入世界遗产名录。考古学家对有关遗址出土文物的碳-14含量进行测定,推测其年代距今约4700-5300年。碳-14原子与碳-12原子互为同位素的原因是( )A、质子数相同 B、电子数相同 C、质子数相同,中子数不同 D、核电荷数和电子数均相同9. 根据如图有关信息判断,下列说法错误的是( )
A、原子、原子核、核外电子 B、原子核、核外电子、原子 C、原子、核外电子、原子核 D、原子核、原子、核外电子8. 2019年7月6日,中国良渚古城遗址获准列入世界遗产名录。考古学家对有关遗址出土文物的碳-14含量进行测定,推测其年代距今约4700-5300年。碳-14原子与碳-12原子互为同位素的原因是( )A、质子数相同 B、电子数相同 C、质子数相同,中子数不同 D、核电荷数和电子数均相同9. 根据如图有关信息判断,下列说法错误的是( )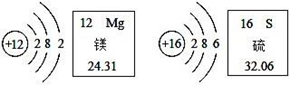 A、镁的相对原子质量为 24.31 B、一个镁离子(Mg2+)核内有 12 个质子 C、在化学反应中,硫原子容易失去 2 个电子 D、镁离子 Mg2+与硫离子S2-的最外层电子数相等10. 下图是表示气体分子的示意图,图中“●”和“○”分别表示两种不同质子数的原子,其中表示化合物的是( )A、
A、镁的相对原子质量为 24.31 B、一个镁离子(Mg2+)核内有 12 个质子 C、在化学反应中,硫原子容易失去 2 个电子 D、镁离子 Mg2+与硫离子S2-的最外层电子数相等10. 下图是表示气体分子的示意图,图中“●”和“○”分别表示两种不同质子数的原子,其中表示化合物的是( )A、 B、
B、 C、
C、 D、
D、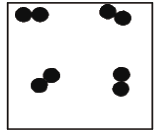 11. 2015年2月17日,《大河报》道了发红的甘蔗中吉有剧毒物质的事实。报道中指出.因为发霉而变红的甘蔗中会产生一种名叫3--硝基丙酸(化学式为(C3H5NO4)的剧毒物质,误食后会出现呕吐瑚搐等症状。下列有关3一硝基丙酸的描述正确的是 ( )
11. 2015年2月17日,《大河报》道了发红的甘蔗中吉有剧毒物质的事实。报道中指出.因为发霉而变红的甘蔗中会产生一种名叫3--硝基丙酸(化学式为(C3H5NO4)的剧毒物质,误食后会出现呕吐瑚搐等症状。下列有关3一硝基丙酸的描述正确的是 ( )
A、3一硝基丙酸是一种氧化物 B、3一硝基丙酸的相对分子质量为119 C、3一硝基丙酸由3个C原子、5个H原子、1个N原子和4个O原子构成 D、3一硝基丙酸中,碳元素与氧元素的质量比为3:412.“三效催化转换器”可将汽车尾气中的有害气体转化为无毒气体,其中某个反应的微观示意图如图.从图示获得的下列信息错误的是( )
 A、该图示能反映质量守恒定律 B、反应前后共有四种分子 C、甲和丁中同种元素的化合价不同 D、乙和丙中所含原子种类相同
A、该图示能反映质量守恒定律 B、反应前后共有四种分子 C、甲和丁中同种元素的化合价不同 D、乙和丙中所含原子种类相同二、填空题
-
13. 用化学符号或符号的意义填空。(1)、铁粉在氧气中燃烧形成的黑色物质是;(2)、SO42﹣:2表示;(3)、保持碘单质化学性质的最小微粒是。14. 已知原子中:质子数(Z)+中子数(N)=质量数(A),表示 X 元素原子的质子数和质量数可用符号表示。据报道钬元素的原子 可有效治疗肝癌,该原子的中子数是 , 核电荷数是。现有和两种原子,则 X 和 Y 是否是同种元素?15. 我们已经学习以下几种微粒;①分子,②原子,③电子,④原子核,⑤质子,⑥中子,⑦阳离子,⑧阴离子。请用序号填空。(1)、带正电的是,(2)、带负电的是,(3)、不带电的是,(4)、能直接构成物的是,(5)、化学变化中最小的微粒,(6)、决定原子质量大小的是数和数.16. 人类对原子结构的认识永无止境。请根据所学知识回答:
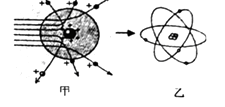 (1)、道尔顿最早提出原子的概念并认为原子是“不可再分的实心球体”,汤姆生认为原子是“嵌着葡萄干的面包”,如今这些观点均 (填“正确”或“错误”)(2)、卢瑟福进行α粒子散射实验后,认为原子是“行星模型”,即原子是由原子核和核外电子构成。如图甲是卢瑟福用α粒子轰击原子而产生散射的实验,在分析实验结果的基础上,他提出了图乙所示的原子核式结构,卢瑟福的这一研究过程是一个 。A、建立模型的过程 B、得出结论的过程 C、提出问题的过程 D、验证证据的过程(3)、卢瑟福在α散射实验中(α粒子带正电荷),断定原子中的绝大部分空间是空的,他的依据是:。
(1)、道尔顿最早提出原子的概念并认为原子是“不可再分的实心球体”,汤姆生认为原子是“嵌着葡萄干的面包”,如今这些观点均 (填“正确”或“错误”)(2)、卢瑟福进行α粒子散射实验后,认为原子是“行星模型”,即原子是由原子核和核外电子构成。如图甲是卢瑟福用α粒子轰击原子而产生散射的实验,在分析实验结果的基础上,他提出了图乙所示的原子核式结构,卢瑟福的这一研究过程是一个 。A、建立模型的过程 B、得出结论的过程 C、提出问题的过程 D、验证证据的过程(3)、卢瑟福在α散射实验中(α粒子带正电荷),断定原子中的绝大部分空间是空的,他的依据是:。
17.从分子、原子的角度认识化学反应是化学研究的基本方法.如图是某密闭容器中物质变化过程的微观示意图.(“
 ”表示氧原子,“
”表示氧原子,“ 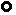 ”表示氢原子)
”表示氢原子)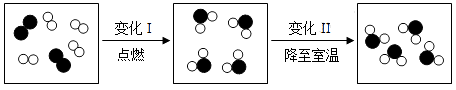
请回答:
(1)、下列关于变化Ⅱ的说法中,正确的是_____(填写序号).A、分子的数目增多了 B、分子变小了 C、分子间的距离变小了 D、分子的种类发生了改变(2)、从变化I的微观过程可分析出,该变化的实质是 .三、实验探究题
-
18. 碘是一种由碘分子构成的非金属单质,某同学利用碘进行了如下的实验:
①把少量的固体碘放在湿润的馒头上,发现馒头会变蓝色(提示:碘分子能使馒头中的淀粉变蓝色);
②再取少量的碘溶解在水中,用馒头去蘸取碘液,发现馒头也会变蓝色。则:
(1)、取少量的碘放入烧杯中,用酒精灯加热,碘升华变成碘蒸气,把湿润的馒头放在碘蒸气中,馒头 (填会或不会)变蓝色。(2)、由上述三个实验可知,分子是。(3)、现在市场上买来的食盐都是加碘盐(含有KIO3 , ),用馒头沾取少量的食盐水(填会或不会)变蓝色。19. 卢瑟福用α粒子(α粒子是带两个单位正电荷的氦原子核)轰击金箔的实验,推翻了汤姆生在1903年提出的原子结构模型,为建立现代原子理论打下了基础(如图)。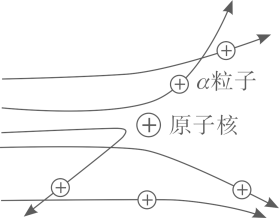
现象1:大多数α粒子能穿透金箔而不改变原来的运动方向。
现象2:一小部分α粒子改变原来的运动方向。
现象3:极少数α粒子被弹了回来。
(1)、请你根据原子结构知识分析现象1产生的原因:。(2)、通过该实验的上述三种现象 (选填“能”或“不能”)获得核外电子带有负电荷的结论。(3)、1919年,卢瑟福用加速了的高能a粒子轰击氮原子,结果有种微粒从氮原子中被打出,而α粒子留在了氮原子中,使氮原子变成了氧原子,从现代观点看,被打出的微粒一定是 。20. 了解物质的组成和结构,有助于认识物质的性质.(1)、如图表示核电荷数为11~17的元素最高和最低化合价.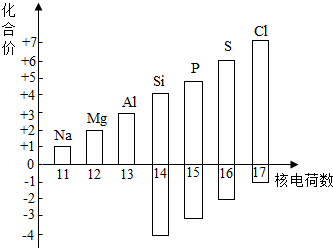
①从图中可以看出,氯元素的最高正价是 .
②若某元素既可显正价,又可显负价,则最高正价与最低负价绝对值的代数和为 .
③写出图中元素的化合价随着核电荷数递增的一条变化规律 .
21. 元素周期表将已知元素科学有序地排列起来,便于我们研究它们的性质和用途。下表表示元素周期表的一部分,请回答下列问题。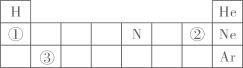 (1)、元素在周期表中的分布是有规律的,表中①②③所代表的三种元素中,属于非金属的是。(2)、表中氮元素的化合价有多种,请写出化合价为+1价的氮的氧化物(用化学式表示)。(3)、氦气的化学式为。(4)、随着新元素的不断发现,元素周期表还将逐渐完善。最近,科学家用大量高速钙原子轰击锫原子,形成了117号元素的原子,该元素原子核中一定含有117个。
(1)、元素在周期表中的分布是有规律的,表中①②③所代表的三种元素中,属于非金属的是。(2)、表中氮元素的化合价有多种,请写出化合价为+1价的氮的氧化物(用化学式表示)。(3)、氦气的化学式为。(4)、随着新元素的不断发现,元素周期表还将逐渐完善。最近,科学家用大量高速钙原子轰击锫原子,形成了117号元素的原子,该元素原子核中一定含有117个。四、解答题
-
22. 在现代生活中,人们越来越注重微量元素的摄取。碘元素对人体有着至关重要的作用,如图是某地市场销售的一种“加碘食盐”包装袋上的部分说明,根据图回答下列问题。
 (1)、“食用碘盐”属于(填“纯净物”或“混合物”)。(2)、碘酸钾(KIO3)中碘元素的化合价为。(3)、碘酸钾(KIO3)分子中钾原子、碘原子、氧原子的个数比是.(4)、碘酸钾(KIO3)的相对分子质量是?23. 如图为某牙膏的部分标签,活性成分单氟磷酸钠的化学式为Na2PO3F,请计算下列问题:
(1)、“食用碘盐”属于(填“纯净物”或“混合物”)。(2)、碘酸钾(KIO3)中碘元素的化合价为。(3)、碘酸钾(KIO3)分子中钾原子、碘原子、氧原子的个数比是.(4)、碘酸钾(KIO3)的相对分子质量是?23. 如图为某牙膏的部分标签,活性成分单氟磷酸钠的化学式为Na2PO3F,请计算下列问题: (1)、单氟磷酸钠中氟元素的质量分数(结果精确到0.1%)。(2)、若牙膏中其它成分不含氟,则每支这种牙膏中,含Na2PO3F的质量为多少克?(结果保留小数点后一位)
(1)、单氟磷酸钠中氟元素的质量分数(结果精确到0.1%)。(2)、若牙膏中其它成分不含氟,则每支这种牙膏中,含Na2PO3F的质量为多少克?(结果保留小数点后一位)