吉林省长春市2023-2024学年九年级下学期开学考化学试卷
试卷更新日期:2024-03-05 类型:开学考试
一、选择题:本大题共10小题,共10分。
-
1. 养成洗手是良好习惯,下图属“用后必须洗手”标志贴在微毒或有毒的试剂瓶上的是( )A、
 B、
B、 C、
C、 D、
D、 2. 为了防治大气污染,打赢蓝天保卫战,下列做法不提倡的是( )A、积极植树造林 B、使用清洁能源 C、直接排放废气 D、公共交通出行3. 下列过程中,只涉及物理变化的是( )A、葡萄糖在酶的作用下转变成二氧化碳和水 B、用燃烧实验鉴别天然纤维和合成纤维 C、净化水时的吸附、沉淀、过滤和蒸馏 D、维生素将食品中的三价铁还原4. 如图是木炭、铁丝、红磷、硫粉四种单质在氧气中燃烧实验操作图示,以下判断错误的是( )
2. 为了防治大气污染,打赢蓝天保卫战,下列做法不提倡的是( )A、积极植树造林 B、使用清洁能源 C、直接排放废气 D、公共交通出行3. 下列过程中,只涉及物理变化的是( )A、葡萄糖在酶的作用下转变成二氧化碳和水 B、用燃烧实验鉴别天然纤维和合成纤维 C、净化水时的吸附、沉淀、过滤和蒸馏 D、维生素将食品中的三价铁还原4. 如图是木炭、铁丝、红磷、硫粉四种单质在氧气中燃烧实验操作图示,以下判断错误的是( )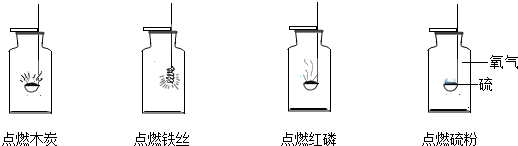 A、都有气体生成 B、都能发光放热 C、都是化合反应 D、反应条件都是点燃5. 逻辑推理是一种重要的化学思维方法。以下推理合理的是( )A、因为氧化物中含有氧元素,所以含有氧元素的化合物一定是氧化物 B、因为蜡烛燃烧生成和 , 所以蜡烛组成里一定含有碳、氢元素 C、因为单质中含有一种元素,所以含一种元素的物质一定是单质 D、因为质子数决定了元素的种类,所以质子数相同的粒子一定是同种元素6. 下列图示的实验操作中,不正确的是( )A、
A、都有气体生成 B、都能发光放热 C、都是化合反应 D、反应条件都是点燃5. 逻辑推理是一种重要的化学思维方法。以下推理合理的是( )A、因为氧化物中含有氧元素,所以含有氧元素的化合物一定是氧化物 B、因为蜡烛燃烧生成和 , 所以蜡烛组成里一定含有碳、氢元素 C、因为单质中含有一种元素,所以含一种元素的物质一定是单质 D、因为质子数决定了元素的种类,所以质子数相同的粒子一定是同种元素6. 下列图示的实验操作中,不正确的是( )A、 熄灭酒精灯
B、
熄灭酒精灯
B、 检查装置气密性
C、
检查装置气密性
C、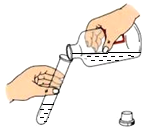 倾倒液体
D、
倾倒液体
D、 加热液体
7. 下列加点元素的化合价为价的是( )A、 B、 C、 D、8. 年中国科学家发现的新冠治疗新药千金藤素获得国家发明专利授权。以下关于千金藤素的说法正确的是( )A、千金藤素分子由碳、氢、氮、氧四种元素组成 B、千金藤素中碳、氢、氮、氧四种元素的质量比是::: C、千金藤素是由碳原子、氢原子、氮原子和氧原子构成 D、千金藤素属于有机物9. 工业生产硫酸中的某一步反应用微观模型图表示如图,下列说法正确的是 ( )
加热液体
7. 下列加点元素的化合价为价的是( )A、 B、 C、 D、8. 年中国科学家发现的新冠治疗新药千金藤素获得国家发明专利授权。以下关于千金藤素的说法正确的是( )A、千金藤素分子由碳、氢、氮、氧四种元素组成 B、千金藤素中碳、氢、氮、氧四种元素的质量比是::: C、千金藤素是由碳原子、氢原子、氮原子和氧原子构成 D、千金藤素属于有机物9. 工业生产硫酸中的某一步反应用微观模型图表示如图,下列说法正确的是 ( ) A、该反应属于化合反应 B、反应前后分子数目不变 C、参加反应的反应物间分子个数比是: D、反应前后硫元素的化合价从价变成价10. 为判断某化合物是否含碳、氢、氧三种元素,取一定质量该化合物在氧气中充分燃烧,接下来还需进行的实验有下列试验中的 ( )个.
A、该反应属于化合反应 B、反应前后分子数目不变 C、参加反应的反应物间分子个数比是: D、反应前后硫元素的化合价从价变成价10. 为判断某化合物是否含碳、氢、氧三种元素,取一定质量该化合物在氧气中充分燃烧,接下来还需进行的实验有下列试验中的 ( )个.用无水硫酸铜检验是否有水生成;
用澄清石灰水检验是否有二氧化碳生成;
用带火星的木条检验氧气;
测定生成的水的质量
测定生成的二氧化碳的质量.
A、 B、 C、 D、二、填空题:本大题共6小题,共24分。
-
11. 化学用语是学习化学的重要工具。请用化学符号填写:(1)、镁元素:;(2)、保持水化学性质的最小的微粒是:;(3)、三个氧原子:;(4)、两个钠离子:;(5)、地壳中含量最高的金属元素。12. 生活中处处有化学。请根据自己所学的化学知识完成下列空白。(1)、“”消毒液的消毒原理是 , 生成的具有杀菌作用。化学方程式中的化学式为 , 依据是。(2)、如图是某品牌矿物质水的标签,则:
饮用矿物质水
净含量:
配料表:纯净水、硫酸镁、氯化钾
保质期:个月
主要成分:
钾离子:
镁离子:
氯离子:
硫酸根离子:
写出镁离子符号。
写出由钾离子和硫酸根离子构成的物质化学式为。
矿物质水的主要成分是 , 请说出其中“”的含义。
(3)、选择下列物质对应的化学式填空:冰、干冰、可燃冰、氮气、金刚石用作燃料的是;
可用于人工降雨的物质是;
可充入食品包装袋防腐的气态物质是。
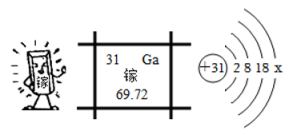
13. 化学源于生活,生活中处处存在着化学知识,请回答下列问题。(1)、中国馆屋顶采用了暴露在阳光下便会产生电的光伏板,产生的电能可以供给馆内运营使用,光伏板将能转化为电能。生产光伏板需用高纯硅,构成硅的粒子是填粒子名称。屋顶还设置了雨水收集系统,请你从爱护水资源方面说说这样做的目的是。(2)、市场上常用的净水器中一般含有活性炭,其作用是。(3)、下列生活现象中属于缓慢氧化的是____填字母序号A、动植物呼吸 B、点燃鞭炮 C、木材燃烧 D、大白菜腐烂14. 镓是一种奇妙的金属,放在手心马上熔化,犹如荷叶上的水珠流来流去。请阅读信息后回答:镓原子结构示意图中的数值为。该元素的原子在化学反应中容易填“得到”或“失去”电子,它的离子属于填“阴离子”或“阳离子” , 符号表示为。
 15. 空气是宝贵的自然资源,如图是以空气等为原料合成尿素的流程。请按要求回答相关问题:
15. 空气是宝贵的自然资源,如图是以空气等为原料合成尿素的流程。请按要求回答相关问题: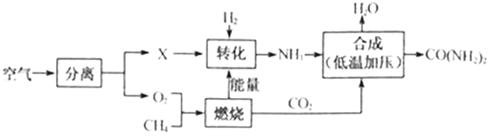 (1)、空气属于填“纯净物”或“混合物” , 是空气中含量最多的气体,其分子式为。(2)、图中分离空气的过程属于变化填“物理”或“化学”。(3)、空气中含有的少量稀有气体的化学性质填“活泼”或“稳定”。(4)、天然气的主要成分是 , 天然气属于再生资源填“可”或“不可” , 天然气等料燃烧的使用会导致大气中含量的增加,以下建议可行的是填序号
(1)、空气属于填“纯净物”或“混合物” , 是空气中含量最多的气体,其分子式为。(2)、图中分离空气的过程属于变化填“物理”或“化学”。(3)、空气中含有的少量稀有气体的化学性质填“活泼”或“稳定”。(4)、天然气的主要成分是 , 天然气属于再生资源填“可”或“不可” , 天然气等料燃烧的使用会导致大气中含量的增加,以下建议可行的是填序号A.开发太阳能、水能、风能、地热能等新能源
B.禁止使用内、石油、天然气等矿物质燃料
C.大量植树造林,禁止乱砍乱伐
(5)、尿素是目前含氮量最高的氮肥,在低温低压条件下,和能反应生成尿素和 , 写出该反应的方程式。16. 根据如图所示的溶解度曲线,回答下列问题.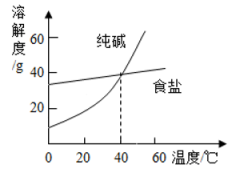 (1)、写出两种物质的化学式:纯碱 , 食盐 , 这两种物质均属于填物质类别 .(2)、我国某些盐湖里出产天然碱主要成分为纯碱晶体,并含有少量食盐杂质 , 实验室里从天然碱中分离出较纯的纯碱晶体应采用的方法.(3)、具体的实验操作步骤为加热溶解;;;洗涤晾于.(4)、完成中操作的必备的实验仪器有、、、和 .
(1)、写出两种物质的化学式:纯碱 , 食盐 , 这两种物质均属于填物质类别 .(2)、我国某些盐湖里出产天然碱主要成分为纯碱晶体,并含有少量食盐杂质 , 实验室里从天然碱中分离出较纯的纯碱晶体应采用的方法.(3)、具体的实验操作步骤为加热溶解;;;洗涤晾于.(4)、完成中操作的必备的实验仪器有、、、和 .三、实验题:本大题共2小题,共7分。
-
17. 实验是实现科学探究的重要途径。请结合下列实验装置,回答有关问题:
 (1)、A实验为利用型管探究燃烧条件的改进实验,能验证可燃物燃烧需要氧气的现象是。(2)、B实验为探究水的组成所做的电解水实验,发生反应的化学方程式为 , 负极与正极气体的体积比为 , 该实验结论是。(3)、C实验中当观察到 , 说明二者发生了中和反应,该反应的微观实质是 , 请举出一例中和反应在生产生活中的应用:。(4)、D实验中燃烧产生火焰的颜色是 , 实验中水的作用是。(5)、E实验中发生反应的化学方程式为 , 请根据该实验结论,为施用铵态氮肥提出一条合理化建议。18. 实验室制取某些气体的装置如下:
(1)、A实验为利用型管探究燃烧条件的改进实验,能验证可燃物燃烧需要氧气的现象是。(2)、B实验为探究水的组成所做的电解水实验,发生反应的化学方程式为 , 负极与正极气体的体积比为 , 该实验结论是。(3)、C实验中当观察到 , 说明二者发生了中和反应,该反应的微观实质是 , 请举出一例中和反应在生产生活中的应用:。(4)、D实验中燃烧产生火焰的颜色是 , 实验中水的作用是。(5)、E实验中发生反应的化学方程式为 , 请根据该实验结论,为施用铵态氮肥提出一条合理化建议。18. 实验室制取某些气体的装置如下: (1)、仪器的名称为。(2)、写出实验室用装置制氧气的化学方程式: , 该反应属于基本反应类型中的。(3)、若收集的氧气用来做铁丝燃烧的实验,最好选择装置收集。(4)、实验室用稀盐酸和石灰石制取二氧化碳,应选择发生装置填字母序号。(5)、用装置收集氧气时,证明是否集满的方法是。
(1)、仪器的名称为。(2)、写出实验室用装置制氧气的化学方程式: , 该反应属于基本反应类型中的。(3)、若收集的氧气用来做铁丝燃烧的实验,最好选择装置收集。(4)、实验室用稀盐酸和石灰石制取二氧化碳,应选择发生装置填字母序号。(5)、用装置收集氧气时,证明是否集满的方法是。四、探究题:本大题共1小题,共5分。
-
19. 九年级二班的同学们在学校开展的综合实践活动课上,探究碱的性质实验时,发现两个异常现象:
金属铝放入新制的氢氧化钠溶液中,铝表面有气泡产生。
将氢氧化钠溶液与稀盐酸混合有气泡产生。对以上两个实验,同学们展开了下列探究活动。
【探究主题】铝能与溶液反应吗?生成了什么物质呢?
【查阅资料】铝能与溶液发生化学反应,并生成一种气体。
【假设与猜想】
猜想:该气体为
猜想:该气体为
【设计实验】同学们利用如图装置对该气体进行验证。
 (1)、将带火星的木条放在口处,观察到 , 证明猜想错误。(2)、将装置、、组合,干燥并点燃生成的气体,则装置内盛放的液体是浓硫酸装置内出现的现象是 , 则证明猜想正确。(3)、【探究主题】氢氧化钠溶液与稀盐酸混合产生气泡的原因。
(1)、将带火星的木条放在口处,观察到 , 证明猜想错误。(2)、将装置、、组合,干燥并点燃生成的气体,则装置内盛放的液体是浓硫酸装置内出现的现象是 , 则证明猜想正确。(3)、【探究主题】氢氧化钠溶液与稀盐酸混合产生气泡的原因。【解释分析】可能是氢氧化钠溶液发生了变质。用化学方程式解释变质的原因:。
(4)、【设计实验】对该氢氧化钠溶液的变质程度进行以下探究。实验操作与步骤
实验现象
实验结论
Ⅰ:取适量实验所用溶液,先向其中滴加无色酚试液,溶液变为红色,再向其中滴入过量的
氢氧化钠完全变质
Ⅱ:取适量实验所用溶液,先滴加过量的氢氯化钙溶液,静置后,再向上层清液中滴加硫酸铜溶液
先有白色沉生成,后有蓝色沉淀生成
氢氧化钠部分变质
(5)、【反思与交流】某同学认为上述实验Ⅱ不能证明氢氧化钠部分变质,原因是。
碱类溶液因保存不当会发生变质,这是出现某些异常的原因,因此碱类溶液要密封保存。
五、计算题:本大题共1小题,共4分。
-
20. 向盛有稀硫酸的烧杯中加入一定量的镁粉,固体完全溶解后,再向所得溶液中加入溶液,所得沉淀质量与加入溶液的质量关系如图所示。
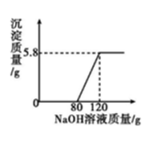 (1)、是由种元素组成。(2)、中、、的质量比为。(3)、的相对分子质量为。(4)、所用氢氧化钠溶液的溶质质量分数为。(5)、求恰好完全反应时所得溶液的溶质质量分数。要求写出计算过程,精确到
(1)、是由种元素组成。(2)、中、、的质量比为。(3)、的相对分子质量为。(4)、所用氢氧化钠溶液的溶质质量分数为。(5)、求恰好完全反应时所得溶液的溶质质量分数。要求写出计算过程,精确到
-