广东省珠海市香洲区2023-2024学年九年级上学期期末考试化学试题
试卷更新日期:2024-03-05 类型:期末考试
一、选择题:本大题包括15小题,每小题3分,共45分。在每小题给出的四个选项中,只有一项是符合题目要求的。
-
1. 2023年,珠海市水质监测中心检测发现8家重点自来水厂出厂水合格率达100%。水是生命之源,我们要爱水护水。根据对水的认识,回答下面小题。(1)、下图属于我国“国家节水标志”的是( )A、
 B、
B、 C、
C、 D、
D、 (2)、以下是珠海市化学实验操作考试“加热2mL水至沸腾”的部分操作,其中正确的是( )A、倾倒水
(2)、以下是珠海市化学实验操作考试“加热2mL水至沸腾”的部分操作,其中正确的是( )A、倾倒水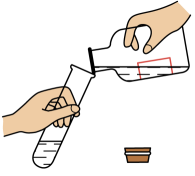 B、点燃酒精灯
B、点燃酒精灯 C、夹持试管
C、夹持试管 D、加热水
D、加热水 (3)、下列生活用水的四个情景中,描述错误的是( )A、将自来水煮沸可降低其硬度 B、茶香四溢是因为分子在不停地运动 C、水中生物靠易溶于水的氧气呼吸 D、用水灭火可降低温度至可燃物的着火点以下2. “生命吸管”是一种户外净水装置,能对天然水进行处理。下列说法错误的是( )
(3)、下列生活用水的四个情景中,描述错误的是( )A、将自来水煮沸可降低其硬度 B、茶香四溢是因为分子在不停地运动 C、水中生物靠易溶于水的氧气呼吸 D、用水灭火可降低温度至可燃物的着火点以下2. “生命吸管”是一种户外净水装置,能对天然水进行处理。下列说法错误的是( ) A、超滤膜可以除去难溶性杂质 B、利用椰壳活性炭的吸附性可以消除异味 C、抗菌颗粒可以消灭细菌 D、通过“生命吸管”得到的水是纯净物3. 下列化学用语正确的是( )A、保持氧气化学性质的最小粒子:O B、氧化铁:FeO C、2个镁离子:2Mg2+ D、60个碳原子:C604. “珠海蓝”是一道靓丽的城市风景,图为香洲区某日空气质量日报。下列说法错误的是( )
A、超滤膜可以除去难溶性杂质 B、利用椰壳活性炭的吸附性可以消除异味 C、抗菌颗粒可以消灭细菌 D、通过“生命吸管”得到的水是纯净物3. 下列化学用语正确的是( )A、保持氧气化学性质的最小粒子:O B、氧化铁:FeO C、2个镁离子:2Mg2+ D、60个碳原子:C604. “珠海蓝”是一道靓丽的城市风景,图为香洲区某日空气质量日报。下列说法错误的是( ) A、空气质量指数越大,空气质量越好 B、B.日报中的NO2、SO2会导致酸雨的形成 C、当日CO未对香洲区空气造成污染 D、D.当日的首要污染物为O35. “天宫”建造全面展开,我国载人航天进入“空间站时代”。化学为航空、航天领域的发展提供了强有力的支撑。结合所学知识,回答下面小题。(1)、中国航天科技的发展令世界瞩目,下列涉及化学变化的是( )A、舱外太空行走 B、宇航员的呼吸作用 C、接收图像信号 D、抓取月球土壤样品(2)、生产航天服的原料之一是二苯甲烷二异氰酸酯(Cl5H10N2O2),关于二苯甲烷二异氰酸酯的说法正确的是( )A、是一种氧化物 B、含有1个氮分子和1个氧分子 C、由碳元素、氢元素、氮元素和氧元素组成 D、由15个碳原子、10个氢原子、2个氮原子、2个氧原子构成(3)、制造载人飞船时使用大量钛合金。根据图所示,下列关于钛元素的说法正确的是( )
A、空气质量指数越大,空气质量越好 B、B.日报中的NO2、SO2会导致酸雨的形成 C、当日CO未对香洲区空气造成污染 D、D.当日的首要污染物为O35. “天宫”建造全面展开,我国载人航天进入“空间站时代”。化学为航空、航天领域的发展提供了强有力的支撑。结合所学知识,回答下面小题。(1)、中国航天科技的发展令世界瞩目,下列涉及化学变化的是( )A、舱外太空行走 B、宇航员的呼吸作用 C、接收图像信号 D、抓取月球土壤样品(2)、生产航天服的原料之一是二苯甲烷二异氰酸酯(Cl5H10N2O2),关于二苯甲烷二异氰酸酯的说法正确的是( )A、是一种氧化物 B、含有1个氮分子和1个氧分子 C、由碳元素、氢元素、氮元素和氧元素组成 D、由15个碳原子、10个氢原子、2个氮原子、2个氧原子构成(3)、制造载人飞船时使用大量钛合金。根据图所示,下列关于钛元素的说法正确的是( ) A、位于元素周期表第二周期 B、核电荷数为22 C、化学性质与氦元素相似 D、相对原子质量为47.87g6. 化学学科核心素养展现了化学课程对学生发展的重要价值。下列说法正确的是( )A、化学观念:单质由同种元素组成,所以由同种元素组成的物质一定是单质 B、科学思维:催化剂能改变化学反应速率,所以要改变化学反应速率必须添加催化剂 C、科学探究与实践:用隔绝空气加强热的方法除去氧化铜中的炭粉 D、科学态度与责任:实验后的废液集中回收处理,避免污染环境7. 火灾给人们敲响了警钟,下列做法正确的是( )A、发现天然气泄漏,点火检查泄漏处 B、室内起火时要赶紧打开门窗通风 C、逃离火灾现场时,可用湿毛巾捂住口鼻,尽量贴近地面逃离 D、把电动车推进室内长时间充电8. 控制变量法是实验探究的重要方法。下列实验不能达到目的的是( )
A、位于元素周期表第二周期 B、核电荷数为22 C、化学性质与氦元素相似 D、相对原子质量为47.87g6. 化学学科核心素养展现了化学课程对学生发展的重要价值。下列说法正确的是( )A、化学观念:单质由同种元素组成,所以由同种元素组成的物质一定是单质 B、科学思维:催化剂能改变化学反应速率,所以要改变化学反应速率必须添加催化剂 C、科学探究与实践:用隔绝空气加强热的方法除去氧化铜中的炭粉 D、科学态度与责任:实验后的废液集中回收处理,避免污染环境7. 火灾给人们敲响了警钟,下列做法正确的是( )A、发现天然气泄漏,点火检查泄漏处 B、室内起火时要赶紧打开门窗通风 C、逃离火灾现场时,可用湿毛巾捂住口鼻,尽量贴近地面逃离 D、把电动车推进室内长时间充电8. 控制变量法是实验探究的重要方法。下列实验不能达到目的的是( )
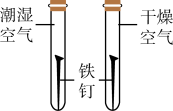
A.验证二氧化碳的温室效应
B.探究铁的锈蚀是否需要水蒸气
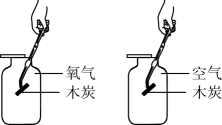
C.探究氧气含量对燃烧剧烈程度的影响
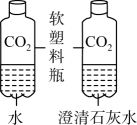
D.比较水和澄清石灰水吸收CO2的效果
A、A B、B C、C D、D9. 以下知识归纳完全正确的一组是( )A.化学变化与守恒
B.化学发展与科学家
①碳酸分解前后各元素种类及质量都不变
②10g水结成10g冰符合质量守恒定律
①定量研究空气的成分——拉瓦锡
②测定某些原子的相对原子质量——张青莲
C.化学物质与构成
D.化学性质与用途
①汞——由汞原子构成
②氯化钠——由氯化钠分子构成
①氧气支持燃烧可用作燃料
②氮气化学性质不活泼可用作保护气
A、A B、B C、C D、D10. 杭州亚运会开幕式主火炬采用甲醇作为燃料。如图是甲醇燃烧的微观示意图,下列说法正确的是( )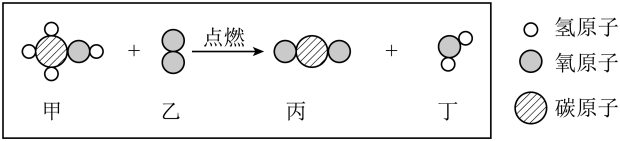 A、甲醇的化学式为CH3O B、生成物丙、丁的质量比为11:9 C、反应前后元素的化合价都不变 D、反应前后分子的种类和总数都不变11. 以化合价为纵坐标,物质类别为横坐标所绘制的图像叫价类图,如图为碳元素的价类图,下列说法正确的是( )
A、甲醇的化学式为CH3O B、生成物丙、丁的质量比为11:9 C、反应前后元素的化合价都不变 D、反应前后分子的种类和总数都不变11. 以化合价为纵坐标,物质类别为横坐标所绘制的图像叫价类图,如图为碳元素的价类图,下列说法正确的是( )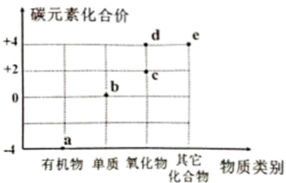 A、已知a点对应的物质是天然气的主要成分,a物质作为燃料大量使用有利于减少碳排放 B、b点物质只能通过化合反应转化为d点物质 C、c、d两点物质组成元素相同,化学性质相似 D、已知d点物质可转化为e点物质,e点物质不止一种可能
A、已知a点对应的物质是天然气的主要成分,a物质作为燃料大量使用有利于减少碳排放 B、b点物质只能通过化合反应转化为d点物质 C、c、d两点物质组成元素相同,化学性质相似 D、已知d点物质可转化为e点物质,e点物质不止一种可能二、非选择题:本大题共6小题,第16小题8分,第17小题7分,18-21小题各10分,共55分。
-
12. 《天工开物》中记载了采矿和冶炼金属锡的场景。
 (1)、采矿如图:“水锡……其质黑色……愈经淘取”是指水中淘取锡砂(锡矿石)。锡砂主要成分为SnO2 , (填“易”或“难”)溶于水,图中用筛子淘取锡砂的过程与化学上的操作原理相似,SnO2中锡元素的化合价为。(2)、冶炼如图:“凡煎炼亦用洪炉,入砂数百斤,丛架木炭亦数百斤,鼓鞴(鼓入空气)熔化。”
(1)、采矿如图:“水锡……其质黑色……愈经淘取”是指水中淘取锡砂(锡矿石)。锡砂主要成分为SnO2 , (填“易”或“难”)溶于水,图中用筛子淘取锡砂的过程与化学上的操作原理相似,SnO2中锡元素的化合价为。(2)、冶炼如图:“凡煎炼亦用洪炉,入砂数百斤,丛架木炭亦数百斤,鼓鞴(鼓入空气)熔化。”①高温条件下,木炭能把锡从锡砂中还原出来,反应的化学方程式为 , 属于反应(填基本反应类型)。
②炼锡时,有关键的一步“点铅勾锡”,即加铅能使锡更易熔化,其原因是加铅后形成的锡铅合金。
(3)、使用:古代锡器很少装酸性物质,原因是。13. 【科普阅读】最近的刷屏榜,非“酱香拿铁”莫属了。这款新型饮品,将中国传统白酒与现代咖啡巧妙地融合在一起,既具有独特的风味和口感,也承载着传播中国酒文化的使命。
白酒的主要成分是酒精(乙醇),由高粱、小麦等谷物为原料发酵而成。白酒的“度数”是指室温下白酒中酒精的体积分数。“53度”表示100mL的酒中有53mL酒精。白酒讲究的“口感醇厚”,可以用“粘度”来衡量,粘度越大口感越醇厚。酒精度数与粘度的关系如图所示。

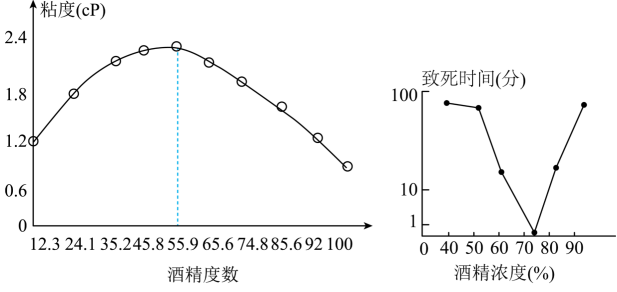
医用酒精的主要成分也是乙醇,还含有醚、醛等成分,不能饮用,但可杀菌消毒。如图为不同浓度酒精杀灭病菌所需时间。
依据上文,回答下列问题:
(1)、用粮食发酵酿酒属于氧化(填“剧烈”或“缓慢”)。(2)、乙醇的化学式为 , 酒精度数为度时,白酒口感最醇厚。(3)、下列说法正确的是____(多选,填字母)。A、乙醇汽化时分子的间隔变大 B、白酒的度数越大,粘度越大 C、48度的白酒中乙醇的质量分数为48% D、青少年饮酒有害健康(4)、生活中一般选75%的酒精进行消毒。依据图,解释原因:。(5)、除杀菌消毒外,酒精在实验室中还可用作。14. 【基础实验与跨学科实践】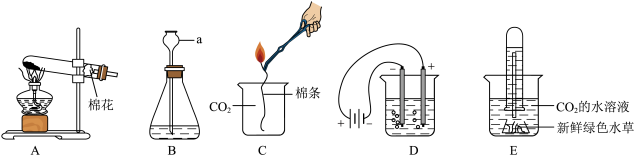 (1)、实验室制氧气
(1)、实验室制氧气①写出仪器a的名称:。
②用高锰酸钾制取O2 , 应选择的发生装置为(填字母),该反应的化学方程式为。
③如装置C所示,点燃沾有酒精的棉条,将其缓慢放入集满CO2的烧杯中,看到棉条上的火焰熄灭,再将其提起,棉条由上到下复燃。根据实验现象,说明燃烧的条件之一是。
(2)、电解水制氧气设计并制作电解水简易装置,如装置D所示,将铅笔芯作为电极是利用铅笔芯中石墨的性,接通电源后水中的两支铅笔芯电极附近的现象是。
(3)、光合作用制氧气向装置E的水中通入适量CO2 , 放在阳光下一段时间后,观察到水草表面有气泡产生,利用法收集到少量氧气(如装置E图所示),此时试管内的气体压强比外界大气压(填“大”“小”或“相等”)。
15. 【科学探究】铁制品容易生锈,但将铁加热熔入金属铬,可制成不锈钢。化学兴趣小组进行以下实验,比较铬、铁、铜的金属活动性强弱。
【查阅资料】铬是一种抗腐蚀性强的银白色金属。硫酸亚铬(CrSO4)溶液呈亮蓝色,在空气中能迅速被氧化成碱性硫酸铬[Cr(OH)SO4],其溶液呈绿色。
【提出猜想】
(1)、三种金属的活动性强弱为:猜想一:Cr>Fe>Cu
猜想二:Fe>Cr>Cu
猜想三:。
(2)、【实验探究】步骤1:取大小相同的三种金属片,用砂纸打磨光亮。
步骤2:将三种金属片分别放入三支装有等量、等浓度稀硫酸的试管中。
实验序号
实验操作
实验现象
实验结论
①
将铁片放入稀硫酸
铁片表面产生气泡较慢,溶液逐渐变为色
猜想成立
②
将铬片放入稀硫酸
铬片表面产生气泡较快,溶液逐渐变为色
③
将铜片放入稀硫酸
无明显现象
(3)、【分析解释】请写出铬与稀硫酸反应生成CrSO4的化学方程式:。反应后的溶液一段时间后变成绿色,其原因是: , 反应的化学方程式为:4CrSO4+O2+2X=4Cr(OH)SO4 , 其中X的化学式为。
(4)、【反思评价】实验结束后有同学提出质疑:金属和酸反应放出的热量会对反应速率造成影响,因此上述实验结论不够科学。建议用铬片、铜片和溶液进一步验证铬、铁、铜三种金属的活动性强弱。
16. 2023年5月30日神舟十六号载人飞船升空,三位宇航员在空间站生活,氧气和水基本由循环系统提供,如图所示,请分析过程,回答下列问题。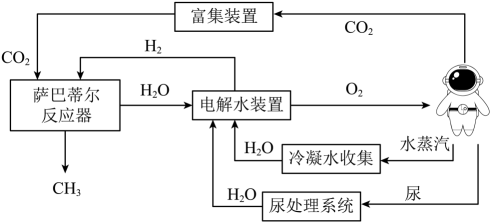 (1)、尿处理系统:利用尿中的水和其它物质的不同,将预处理后的尿液进行旋转蒸馏,再将收集到的水蒸气冷凝,实现了从尿中取水。(2)、富集装置中的分子筛与活性炭类似,都有的结构。(3)、萨巴蒂尔反应器内,在400℃和镍(Ni)作为催化剂的条件下,反应的化学方程式为。(4)、在空间站失重状态下收集O2 , 最好选用下列装置中的____(填字母)。A、
(1)、尿处理系统:利用尿中的水和其它物质的不同,将预处理后的尿液进行旋转蒸馏,再将收集到的水蒸气冷凝,实现了从尿中取水。(2)、富集装置中的分子筛与活性炭类似,都有的结构。(3)、萨巴蒂尔反应器内,在400℃和镍(Ni)作为催化剂的条件下,反应的化学方程式为。(4)、在空间站失重状态下收集O2 , 最好选用下列装置中的____(填字母)。A、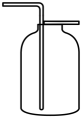 B、
B、 C、
C、 D、
D、 (5)、如图是同学们利用学过的6种常见物质Fe、H2、H2O、CO2、CO、Ca(OH)2搭建的火箭模型。已知C、E、F均能在氧气中燃烧,且E为金属单质,F为化合物,D可作为气体肥料。(“”表示C与E之间能相互转化,“B→A”表示B能转化成A)
(5)、如图是同学们利用学过的6种常见物质Fe、H2、H2O、CO2、CO、Ca(OH)2搭建的火箭模型。已知C、E、F均能在氧气中燃烧,且E为金属单质,F为化合物,D可作为气体肥料。(“”表示C与E之间能相互转化,“B→A”表示B能转化成A)
①E、F的化学式分别是、。
②B→A的化学方程式为。
③D—F的反应属于(填“吸热”或“放热”)反应。
17. 木糖醇(C5H12O5)的甜度和风味与白砂糖相当,热量却更低,市场需求量越来越大。目前制备木糖醇的主要方法如图所示。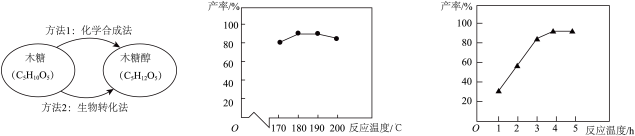 (1)、C5H10O5中碳、氢、氧原子的个数比为。(2)、方法1中反应的化学方程式为:C5H10O5+H2C5H12O5 , 用20t原料(含木糖75%)合成木糖醇,理论上可制得木糖醇的质量为多少?(写出计算过程)。(3)、30g木糖和g木糖醇中碳元素的质量相等。(4)、在制备物质时,除了考虑产率外,还要考虑成本等因素。如图表示不同反应温度和时间下的木糖醇产率,你认为最适宜的反应温度和反应时间分别为℃和h。(5)、如图是某专利公开的通过方法2制备木糖醇的过程,但该方法目前无法用于实现木糖醇的规模化生产,你认为可能的原因是(写一条)。
(1)、C5H10O5中碳、氢、氧原子的个数比为。(2)、方法1中反应的化学方程式为:C5H10O5+H2C5H12O5 , 用20t原料(含木糖75%)合成木糖醇,理论上可制得木糖醇的质量为多少?(写出计算过程)。(3)、30g木糖和g木糖醇中碳元素的质量相等。(4)、在制备物质时,除了考虑产率外,还要考虑成本等因素。如图表示不同反应温度和时间下的木糖醇产率,你认为最适宜的反应温度和反应时间分别为℃和h。(5)、如图是某专利公开的通过方法2制备木糖醇的过程,但该方法目前无法用于实现木糖醇的规模化生产,你认为可能的原因是(写一条)。