广东省佛山市顺德区2023-2024学年九年级上学期12月月考化学试题
试卷更新日期:2024-03-05 类型:月考试卷
一、选择题(45分,每题3分)
-
1. 在面粉厂内应张贴的标志是A、
 B、
B、 C、
C、 D、
D、 2. 下列物质中属于金属材料的是A、赤铁矿 B、武德合金 C、木材 D、矿泉水瓶3. 发现元素周期律并编制元素周期表的科学家是( )A、道尔顿 B、张青莲 C、拉瓦锡 D、门捷列夫4. 下列化学用语正确的是A、汞元素:2Hg B、镁离子: C、两个钾原子:2K D、氧化铁:Fe3O45. 下列是我们自常生活中接触到的物质,属于纯净物的是A、18K金 B、洁净的空气 C、生石灰 D、石灰石6. 某消毒液标签的部分内容如图所示,下列说法正确的是
2. 下列物质中属于金属材料的是A、赤铁矿 B、武德合金 C、木材 D、矿泉水瓶3. 发现元素周期律并编制元素周期表的科学家是( )A、道尔顿 B、张青莲 C、拉瓦锡 D、门捷列夫4. 下列化学用语正确的是A、汞元素:2Hg B、镁离子: C、两个钾原子:2K D、氧化铁:Fe3O45. 下列是我们自常生活中接触到的物质,属于纯净物的是A、18K金 B、洁净的空气 C、生石灰 D、石灰石6. 某消毒液标签的部分内容如图所示,下列说法正确的是XX牌84消毒液
主要有效成分为次氯酸钠(NaClO)。
有效氯含量8000~10500mg/L
主要用途:消毒杀菌,可杀灭肠道致病菌和化脓性球菌。
注意事项:避光、避热,置阴凉处保存。
A、消毒属于物理变化 B、次氯酸钠是钠、氯、氧三种原子构成 C、有效氯含量是指氯分子含量 D、次氯酸钠受热易分解7. 元素Eu是一种稀土元素,在激光材料及原子能工业中有重要的应用。下列说法中正确的是 A、铕原子的中子数为63 B、铕的质子数为152 C、铕原子核外电子数是63 D、稀土元素铕属于非金属元素8. 下列有关金属材料的说法错误的是A、铝有很好的抗腐蚀性,是因为铝化学性质不活泼 B、金属的回收利用是保护金属资源的有效途径之一 C、在潮湿的空气中铁易生锈 D、高炉炼铁的原理是在高温条件下,用一氧化碳把铁从铁矿石里还原出来9. 下列说法正确的是A、发现煤气泄漏时应打开换气扇通风 B、用干冰升华吸热可做食品制冷剂 C、煤炉上放一壶水可预防一氧化碳中毒 D、开发利用太阳能、风能、氢能等新能源,有利于保护环境10. 考古人员使用碳14(质子数为6,14为质子数和中子数之和)年代检测法,测出三星堆出土的“鸟形金饰片”(如图)距金约3200年至3000年。下列模型能表示碳14原子结构的是( )
A、铕原子的中子数为63 B、铕的质子数为152 C、铕原子核外电子数是63 D、稀土元素铕属于非金属元素8. 下列有关金属材料的说法错误的是A、铝有很好的抗腐蚀性,是因为铝化学性质不活泼 B、金属的回收利用是保护金属资源的有效途径之一 C、在潮湿的空气中铁易生锈 D、高炉炼铁的原理是在高温条件下,用一氧化碳把铁从铁矿石里还原出来9. 下列说法正确的是A、发现煤气泄漏时应打开换气扇通风 B、用干冰升华吸热可做食品制冷剂 C、煤炉上放一壶水可预防一氧化碳中毒 D、开发利用太阳能、风能、氢能等新能源,有利于保护环境10. 考古人员使用碳14(质子数为6,14为质子数和中子数之和)年代检测法,测出三星堆出土的“鸟形金饰片”(如图)距金约3200年至3000年。下列模型能表示碳14原子结构的是( )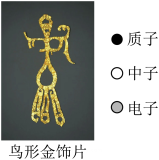 A、
A、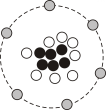 B、
B、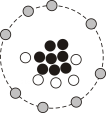 C、
C、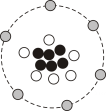 D、
D、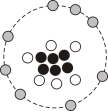 11. 阅读以下材料,回答下列题
11. 阅读以下材料,回答下列题碳在日常生活、工业生产等领域具有重要的作用。
(1)、下列含碳物质的性质与用途对应关系错误的是A、石墨能导电,可用作电池电极 B、金刚石坚硬,可制作首饰钻戒 C、木炭有可燃性,可做燃料 D、活性炭具有吸附性,可做除味剂(2)、工业上采用碳单质高温炼镍的原理是: , 说法错误的是A、反应中X的化学式为CO2 B、NiO是一种氧化物 C、碳过量时,气体产物中可能有CO D、此反应说明碳具有氧化性12. 现有等质量甲、乙、丙三种金属,分别放入三份浓度相同的足量稀硫酸中,产生氢气的质量与反应时间的关系如图所示(已知甲、乙、丙在生成物中化合价均为+2价),则下列说法中不正确的是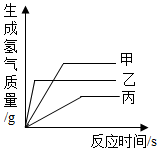 A、生成氢气
A、生成氢气 质量:甲>乙>丙
B、金属活动性:乙>甲>丙
C、相对原子质量:乙>丙>甲
D、消耗硫酸的质量:甲>乙>丙
13. 化学是一门以实验为基础的学科,下列实验能达到实验目的的是
质量:甲>乙>丙
B、金属活动性:乙>甲>丙
C、相对原子质量:乙>丙>甲
D、消耗硫酸的质量:甲>乙>丙
13. 化学是一门以实验为基础的学科,下列实验能达到实验目的的是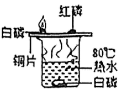
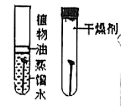

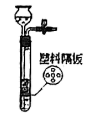
A.探究燃烧的条件
B.探究铁生锈的条件
C.除去水中钙、镁化合物
D.用过氧化氢溶液和二氧化锰制氧气,实现随关随停
A、A B、B C、C D、D14. 暖宝宝(主要成分为铁粉)通过生锈发热,利用图1装置探究生锈过程中压强、氧气浓度、温度的变化过程,一段时间后变化图像如图2所示,说法不正确的是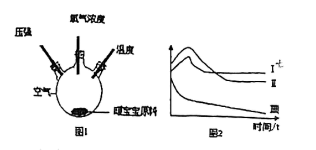 A、I为温度变化曲线 B、Ⅲ为氧气浓度变化曲线 C、I和Ⅱ开始增大是因为铁发生氧化反应放热 D、暖宝宝原料足量时,瓶内压强可降至0
A、I为温度变化曲线 B、Ⅲ为氧气浓度变化曲线 C、I和Ⅱ开始增大是因为铁发生氧化反应放热 D、暖宝宝原料足量时,瓶内压强可降至0二、填空题(15分,每空1分,方程式2分)
-
15. 2023年9月23日,第19届亚运会在杭州正式拉开帷幕。(1)、杭州亚运会火炬金属部分采用铝合金工艺,该合金密度小,有独特的金属光泽,耐腐蚀,属于该合金的物理性质的是。(2)、在火炬上涂了具有显色功能的钠的化合物能使火焰变得更鲜艳,其中钠离子符号是。(3)、火炬燃料采用由工业废气中CO2合成甲醇CH3OH,甲醇由构成;其中氢元素与氧元素的质量比为。(4)、杭州亚运会践行低碳理念,场馆大多采用绿色能源供电,“低碳”指的是减少气体的排放;说出生活中践行“低碳”理念的具体措施。16. 科普阅读:
如图是2023年某城市空气污染物的主要来源分布图,治理汽车尾气成为城市改善空气质量重要工作。汽车尾气治理可以在汽车的排气管上装一个催化转换器。在催化转换器催化下使一氧化碳与一氧化氮转化为无害气体,还有改进发动机的燃烧方式,使汽油充分燃烧!有些城市的部分汽车改用压缩天然气,以减少对空气的污染。
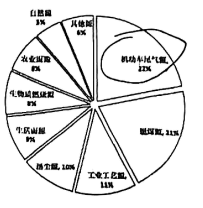 (1)、由图可知城市空气的主要污染源是。(2)、由材料分析汽车尾气中污染物有(填一种),该污染物在可以转化为的无害气体是。(填化学式)(3)、材料中介绍种治理汽车尾气方法;天然气燃烧化学方程式为。(4)、洁净的空气对人类非常重要。下列有利于保护大气的做法有。
(1)、由图可知城市空气的主要污染源是。(2)、由材料分析汽车尾气中污染物有(填一种),该污染物在可以转化为的无害气体是。(填化学式)(3)、材料中介绍种治理汽车尾气方法;天然气燃烧化学方程式为。(4)、洁净的空气对人类非常重要。下列有利于保护大气的做法有。a.使用新能源共享汽车 b.将工厂烟囱造高减少大气污染
c.植树造林,防止扬尘污染 d.加强大气监测,改善环境状况
三、实验题(20分,每空1分,方程式2分)
-
17.(1)、I.气体制取实验:
写出①中两种玻璃仪器名称:。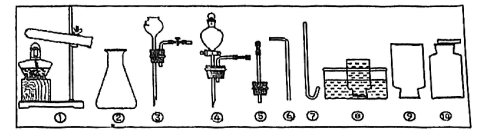 (2)、若在实验室制取并收集CO2气体并能得到平稳的气流,应选用仪器(填序号),该化学方程式为。(3)、Ⅱ.某款家用制氧机利用过碳酸钠(2Na2CO3.3H2O2)二氧化锰同时加入水中制取氧气;制氧机制氧说明(部分)见下表,其中A、B剂的成分是过碳酸钠或二氧化锰。
(2)、若在实验室制取并收集CO2气体并能得到平稳的气流,应选用仪器(填序号),该化学方程式为。(3)、Ⅱ.某款家用制氧机利用过碳酸钠(2Na2CO3.3H2O2)二氧化锰同时加入水中制取氧气;制氧机制氧说明(部分)见下表,其中A、B剂的成分是过碳酸钠或二氧化锰。查阅资料:①过碳酸的易溶于水,遇水分解为Na2CO3和H2O2;②H2O2可以将KI转化为I2 , 淀粉遇I2变蓝色。
A剂
B剂
平均供氧量(毫升分钟)
供氧时间(分钟)
配方一
1袋
1袋
≥320
≥15
配方二
2袋
1袋
≥500
≥25
配方三
3袋
2袋
≥1000
≥15
A剂的成分是(填名称),若突发缺氧性疾病,在呼叫救护的同时进行吸氧,应选择配方进行紧急制氧。
(4)、写出制氧机产生氧气的化学方程式为和 , 取配方一反应后的溶液,滴加KI溶液,再加入淀粉,溶液变为 , 证明溶液中仍含有H2O2。18. 甜叶菊苷具有高甜度低热能的特点,是一种新型甜味剂,实验小组欲探究甜叶菊苷的元素组成,进行如下实验:【提出猜想】甜叶菊苷可能含有碳、氢、氧三种元素
(1)、【进行实验】实验操作
实验现象
实验结论
取适量的甜叶菊苷按图甲进行操作分别将干冷的烧杯和蘸有澄清石灰水的烧杯倒置与火焰上方。
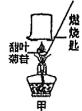
。
甜叶菊苷含有氢元素
石灰水变浑浊
甜叶菊苷含有碳元素
(2)、【交流讨论】澄清石灰水变浑浊化学反应方程式为:。(3)、有同学认为实验操作与结论不严谨,原因是。(4)、【继续探究】为了进步确定氧元素存在。利用如图乙进行实验,(氢氧化钠固体可吸收水蒸气和二氧化碳、浓硫酸可以吸收水蒸气)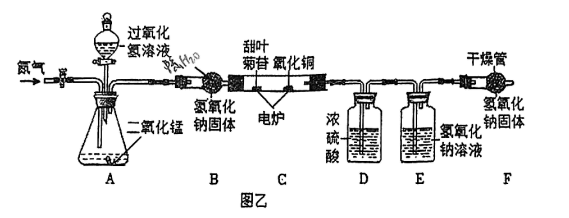
先通一段时间N2 , 打开分液漏斗活塞,加热电炉;C装置中氧化铜处理甜叶菊苷燃烧不充分产生的CO,化学方程为: , 体现CO具有性。
(5)、反应后需要再通入一段时间的氮气,原因是。(6)、根据实验结果4.02g甜叶菊苷充分燃烧后,D增重2.7g,E装置增重8.8g(假设产物被完全吸收),由此可以确定甜叶菊苷(填“含有”或“没有”)氧元素。(7)、F装置为了防止空气中的进入装置影响结果判断。四、综合能力题(10分,每空1分,方程式2分)
-
19. 钼(Mo)是一种稀有金属,是国民经济中重要的原料和不可替代的战略物资。下图是利用辉钼矿(主要成分MoS2)冶炼金属钼的工艺流程:
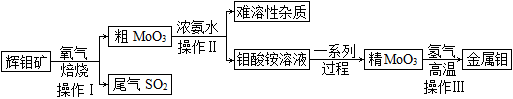
请回答下列问题:
(1)、操作Ⅰ焙烧前需将辉钼矿粉碎,目的是;焙烧反应的化学方程式为。(2)、操作Ⅱ的名称是 , 目的是为了除去。(3)、尾气SO2任意排放会形成 , 污染环境,工业上常用NaOH溶液进行尾气处理,反应的化学方程式为SO2+2NaOH=Na2SO3+。(4)、MoO3中钼元素的化合价为 , 操作Ⅲ反应的化学方程式为。五、计算题(10分)
-
20. Mg2Ni合金被被认为是最具应用前景的储氢合金。一种Mg2Ni储氢材料的制备与应用的过程如图1所示。
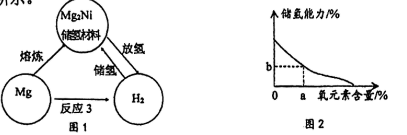 (1)、Mg2Ni合金熔炼过程属于变化(填“物理”或“化学”)(2)、氢气的储存过程发生的主要反应为。该反应中,若有107gMg2Ni可以储存H2的质量是多少?(写出计算过程)(3)、 Mg2Ni储氢材料在使用过程中Mg表面容易被氧化形成氧化层(MgO)。由图2分析,Mg氧化程度越高,储氢能力(填“越高”或“越低”)。当储氢材料中氧元素的含量为a%时,MgO的质量分数为。(用a的代数式表示)
(1)、Mg2Ni合金熔炼过程属于变化(填“物理”或“化学”)(2)、氢气的储存过程发生的主要反应为。该反应中,若有107gMg2Ni可以储存H2的质量是多少?(写出计算过程)(3)、 Mg2Ni储氢材料在使用过程中Mg表面容易被氧化形成氧化层(MgO)。由图2分析,Mg氧化程度越高,储氢能力(填“越高”或“越低”)。当储氢材料中氧元素的含量为a%时,MgO的质量分数为。(用a的代数式表示)
-