广东省河源市紫金县2023-2024学年九年级上学期第三次月考化学试题
试卷更新日期:2024-03-05 类型:月考试卷
一、单项选择题(每小题3分,共45分)
-
1. 2020年习近平主席在联合国大会上指出:中国力争到2060年针对人为排放的二氧化碳,采取各种方式实现全部吸收,实现“碳中和”。下列做法有利于“碳中和”的是( )A、大力发展火力发电 B、就地焚烧农作物秸秆 C、积极开展植树造林 D、尽量选择私家车出行2. 下列有关X、Y表示的概念之间存在如下图所示的“包含”关系的是
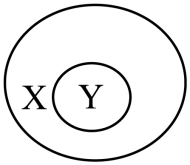
选项
X
Y
A
化学反应
分解反应
B
混合物
纯净物
C
物理变化
化学变化
D
氧化反应
化合反应
A、A B、B C、C D、D3. 吸烟有害健康,烟气中含有一种能与血液中血红蛋白结合的有毒气体,它是()A、氢气 B、一氧化碳 C、二氧化碳 D、氧气4. 生活、工作场所常见到一些警示图标。下列图标放置地点错误的是( )A、 运输浓硫酸的槽罐车
B、
运输浓硫酸的槽罐车
B、 存放酒精的试剂柜
C、
存放酒精的试剂柜
C、 面粉加工厂
D、
面粉加工厂
D、 城市居民住宅区
5. 下列对实验现象的描述正确的是A、高温条件下木炭还原氧化铜:黑色固体逐渐变成光亮的铜 B、铁丝在氧气中燃烧:银白色固体剧烈燃烧,火星四射,放出大量的热,生成黑色固体 C、电解水实验:两个电极附近产生气泡,一段时间后,正、负极产生的气体体积比约为2∶1 D、甲烷在空气中燃烧产生蓝色火焰,生成水和二氧化碳6. 水是生命之源。城市生活用水经自来水厂净化处理的过程如下图。下列说法错误的是( )
城市居民住宅区
5. 下列对实验现象的描述正确的是A、高温条件下木炭还原氧化铜:黑色固体逐渐变成光亮的铜 B、铁丝在氧气中燃烧:银白色固体剧烈燃烧,火星四射,放出大量的热,生成黑色固体 C、电解水实验:两个电极附近产生气泡,一段时间后,正、负极产生的气体体积比约为2∶1 D、甲烷在空气中燃烧产生蓝色火焰,生成水和二氧化碳6. 水是生命之源。城市生活用水经自来水厂净化处理的过程如下图。下列说法错误的是( )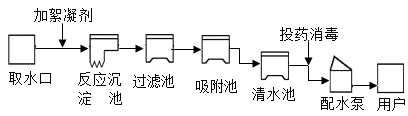 A、通过反应沉淀池、过滤池除去水中不溶性杂质 B、吸附池内常用活性炭吸附色素和异味 C、自来水厂投入明矾进行消毒 D、硬度较高的自来水,用户可用煮沸的方法来降低其硬度7. 葡萄糖的化学式为C6H12O6 , 下列有关葡萄糖的说法正确的是A、葡萄糖是由 24个原子构成的 B、葡萄糖是由碳、氢气和氧气组成的 C、葡萄糖分子是由碳原子和水分子构成的 D、葡萄糖是由碳、氢、氧三种元素组成的8. 下图分别是某元素的原子结构示意图及该元素在元素周期表中的相关信息,下列说法正确的是( )
A、通过反应沉淀池、过滤池除去水中不溶性杂质 B、吸附池内常用活性炭吸附色素和异味 C、自来水厂投入明矾进行消毒 D、硬度较高的自来水,用户可用煮沸的方法来降低其硬度7. 葡萄糖的化学式为C6H12O6 , 下列有关葡萄糖的说法正确的是A、葡萄糖是由 24个原子构成的 B、葡萄糖是由碳、氢气和氧气组成的 C、葡萄糖分子是由碳原子和水分子构成的 D、葡萄糖是由碳、氢、氧三种元素组成的8. 下图分别是某元素的原子结构示意图及该元素在元素周期表中的相关信息,下列说法正确的是( )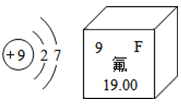 A、该元素原子的最外层电子数为7 B、该元素的原子序数为19 C、该元素是金属元素 D、在化学反应过程中该元素原子容易失去电子形成阳离子9. 下图是甲转化为丙的微观过程。下列说法不正确的是
A、该元素原子的最外层电子数为7 B、该元素的原子序数为19 C、该元素是金属元素 D、在化学反应过程中该元素原子容易失去电子形成阳离子9. 下图是甲转化为丙的微观过程。下列说法不正确的是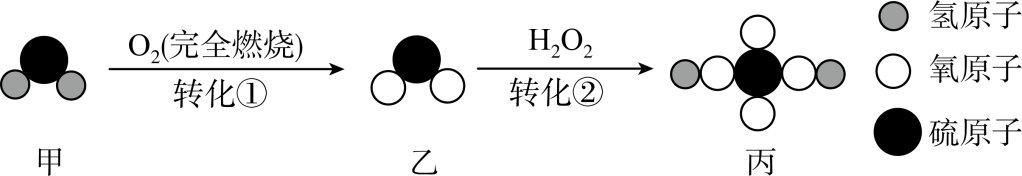 A、甲、乙均为氧化物 B、反应前后原子种类和个数不变 C、转化①中有元素的化合价发生改变 D、丙的化学式为H2SO410. 密闭容器内有a、b、c、d四种物质,在一定条件下充分反应,测得反应前后各物质的质量如下:
A、甲、乙均为氧化物 B、反应前后原子种类和个数不变 C、转化①中有元素的化合价发生改变 D、丙的化学式为H2SO410. 密闭容器内有a、b、c、d四种物质,在一定条件下充分反应,测得反应前后各物质的质量如下:物质
a
b
c
d
反应前质量/g
17
10
25
48
反应后质量/g
19
10
41
x
下列说法不正确的是
A、d一定是化合物,c可能是单质 B、b在反应中是催化剂 C、参与该反应的a与c的质量比为1:8 D、x为3011. 下列对现象或事实的解释错误的是A、液氧和氧气都能使带火星的木条复燃—同种分子的化学性质相同 B、金刚石很坚硬,而石墨却很软—碳原子的排列方式不同 C、酒精作温度计的指示液—酒精分子的体积受热变大,遇冷变小 D、食物变质—分子本身发生了变化12. 小华在做加热氯酸钾与二氧化锰的混合物制取氧气的实验时,错把高锰酸钾当作了二氧化锰,其结果与只加氯酸钾相比,以下推论中错误的是A、反应速率加快,生成氧气的质量增加 B、高锰酸钾的产物二氧化锰可作氯酸钾制氧气反应的催化剂 C、反应速率加快,生成氧气的质量不变 D、完全反应后试管内的固体物质有三种13. 证据推理是化学学科的核心素养,下列基于事实的推理正确的是( )A、元素周期表每一个横行叫一个周期,因此现行周期表有七个横行即有七个周期 B、燃烧必须温度达到可燃物的着火点,因此只有温度低于着火点才能灭火 C、自来水厂净水时需要杀菌消毒,因此净水时加入活性炭的目的就是杀菌消毒 D、硫在空气中燃烧产生淡蓝色火焰,因此在空气中燃烧产生淡蓝色火焰的一定是硫14. 森林灭火的有效方法之一,是在大火蔓延路线的前方开辟一条“隔离带”,大火会逐渐熄灭。该灭火方法的原理是A、隔离空气 B、隔离可燃物 C、降低温度到可燃物的着火点以下 D、以上方法全部正确15. 下列4个图像,能正确反映对应关系的是A、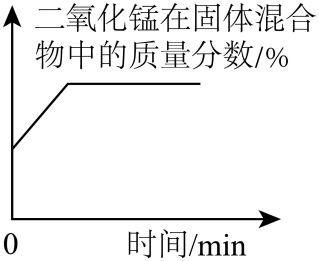 酒精灯加热一定量的高锰酸钾固体
B、
酒精灯加热一定量的高锰酸钾固体
B、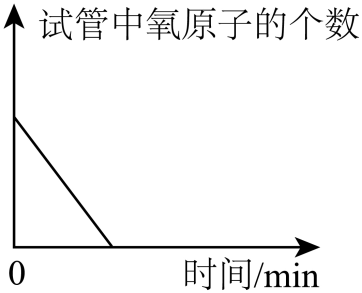 过氧化氢制取氧气
C、
过氧化氢制取氧气
C、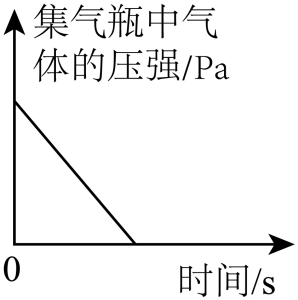 利用红磷燃烧测定空气中氧气的含量
D、
利用红磷燃烧测定空气中氧气的含量
D、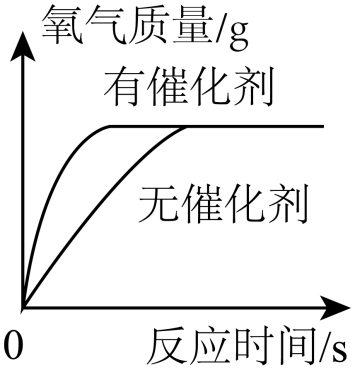 过氧化氢溶液在有无催化剂条件下制氧气
过氧化氢溶液在有无催化剂条件下制氧气
二、非选择题:本题共6个小题,共55分。
-
16. 水与人类的生活和生产密切相关。(1)、节约用水,防止水污染应成为我们的自觉行为。下列叙述正确的是 ____(填字母)。A、为了节约用水,用工业废水直接浇灌农田 B、水的天然循环能实现水的重新分配,不需兴建水利工程 C、将生活用水、地表雨水分类处理,可减少污染,保护水资源(2)、生活中硬水和软水常用的方法来区分,日常生活中常用的方法除去硬水中过多的(填离子符号)和Ca2+来得到软水。如需制备更纯净的水,可用方法(实验室净水操作)。(3)、图甲是水电解实验示意图。

①实验中,试管a中产生的气体为(填名称)。
②写出该反应的化学方程式。
(4)、有的同学利用所学的知识将浑浊的水用简易净水器(如图乙所示)进行净化,其中小卵石、石英砂的作用是。(填操作名称)17. 请回答下列问题。(1)、能源、环境和安全已成为人类日益关注的问题。①目前世界上多数国家利用的能量主要来自煤、石油和等化石燃料的燃烧。在工业上,利用石油中各成分的不同将它们分离,得到汽油、柴油等产品。
②为了节省石油资源,在一定程度上减少汽车尾气的污染,推广使用乙醇汽油,乙醇属于(填“可再生”或“不可再生”)能源。
(2)、如图为探究燃烧条件的实验装置,已知:白磷有毒,且燃烧时产生的P2O5对环境有污染。
①对比图1中铜片上的白磷和红磷的现象,说明燃烧的条件之一是;对比图1中铜片上的白磷和图3白磷的现象,说明燃烧的条件之一是;
②图2和图1相比,图2的优点是(NaOH溶液可吸收燃烧生成物)。
(3)、乙醇(C2H5OH)是常用的燃料,现有4.6g乙醇与一定量氧气混合于密闭容器内,一定条件下反应物全部转化为二氧化碳和水。恢复至室温,则反应过程中生成水的质量为g。18. 根据如图所示的实验装置,回答有关问题。 (1)、仪器a的名称是;图中可用于加热KClO3制备O2的发生装置为(填字母),化学反应方程式为。(2)、若用锌片与稀硫酸在A装置中制备H2 , 锌片应放在;用F收集H2时导入气体的导管端为(填“b”或“c”)。(3)、图中可用于固液反应制备气体的装置中,不能使反应随时发生或停止的装置是(填字母),原因是反应过程中若用止水夹夹紧橡胶管后,。(4)、把F装满水,用排水法收集O2并测定气体体积,应在端(填“b”或“c” )连接上一个量筒。19. 兴趣小组同学用下图装置进行氧化铜与炭粉的反应实验,并对生成气体的成分进行探究。
(1)、仪器a的名称是;图中可用于加热KClO3制备O2的发生装置为(填字母),化学反应方程式为。(2)、若用锌片与稀硫酸在A装置中制备H2 , 锌片应放在;用F收集H2时导入气体的导管端为(填“b”或“c”)。(3)、图中可用于固液反应制备气体的装置中,不能使反应随时发生或停止的装置是(填字母),原因是反应过程中若用止水夹夹紧橡胶管后,。(4)、把F装满水,用排水法收集O2并测定气体体积,应在端(填“b”或“c” )连接上一个量筒。19. 兴趣小组同学用下图装置进行氧化铜与炭粉的反应实验,并对生成气体的成分进行探究。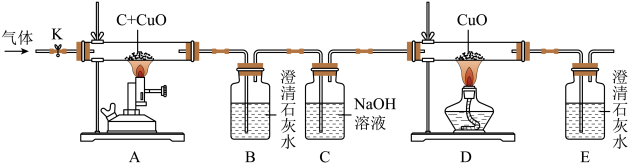
【查阅资料】a.NaOH溶液能吸收CO2; b.
(1)、根据质量守恒定律,对生成气体的成分作如下猜想:①只有二氧化碳; ②。 ③只有一氧化碳。
写出猜想①所发生反应的化学方程式。
(2)、装置A中可观察到的实验现象是 , 装置B中可观察到的实验现象是 , 装置C的作用是。(3)、如果观察到装置B、D、E中都有明显的变化发生,说明猜想成立。(4)、小组分析讨论后认为:CO可能是反应生成的CO2和过量木炭在高温下反应生成的,写出该反应的化学方程式。(5)、当装置B中不再有气泡冒出时,反应停止,待A装置中玻璃管冷却后倒出固体残留物,其中一定含有铜,可能含有。20. 科学家提出工业生产回收利用空气中CO2的构想:把空气吹入装有碳酸钠(Na2CO3)和水的混合物的吸收池中,通过吸收CO2生成碳酸氢钠(NaHCO3);把碳酸氢钠固体放入分解池进行加热,又放出CO2 , 同时生成碳酸钠和水;在合成塔内高温条件下CO2与氢气反应生成甲醇(CH3OH)和水。简要的生产流程如图所示: (1)、回收利用空气中的CO2 , 可降低大气中CO2浓度。CO2(填“是”或“不是”)空气污染物。(2)、“其它气体”中的主要成分是 , 其化学性质(填“活泼”或“稳定”)。(3)、吸收池中发生了化合反应,化学方程式为。(4)、在合成塔装置内要避免空气进入其中,其目的是。(5)、该流程中,能被循环利用的物质有。21. 某实验小组称量了12.5g大理石样品,将其加入足量稀盐酸中,完全反应(样品中杂质不溶于水且不与稀盐酸反应)后,称得剩余固体的质量为2.5g。请计算:(1)、该样品中碳酸钙的质量为g。(2)、12.5g该样品最多可制得二氧化碳的质量。(写出必要的计算过程)
(1)、回收利用空气中的CO2 , 可降低大气中CO2浓度。CO2(填“是”或“不是”)空气污染物。(2)、“其它气体”中的主要成分是 , 其化学性质(填“活泼”或“稳定”)。(3)、吸收池中发生了化合反应,化学方程式为。(4)、在合成塔装置内要避免空气进入其中,其目的是。(5)、该流程中,能被循环利用的物质有。21. 某实验小组称量了12.5g大理石样品,将其加入足量稀盐酸中,完全反应(样品中杂质不溶于水且不与稀盐酸反应)后,称得剩余固体的质量为2.5g。请计算:(1)、该样品中碳酸钙的质量为g。(2)、12.5g该样品最多可制得二氧化碳的质量。(写出必要的计算过程)