广东省广州市教育集团2023-2024学年九年级上学期12月月考化学试题
试卷更新日期:2024-03-05 类型:月考试卷
一、选择题:本题包括14小题,每小题3分,共42分。每小题给出的四个选项中,只有一项最符合题意。错选、不选、多选或涂改不清的,均不给分。
-
1. 化学作为一门科学的神奇之处在于它不仅能改进现有的物质世界,还能创造一个崭新的物质世界。以下变化涉及化学领域的是( )A、抗疫工作者穿戴隔离衣,佩戴防护眼罩 B、高压风机将冰片粉碎、吹出,形成片状雪花 C、给神舟十三号的“再生水”通电,它能分解产生氧气 D、分离空气,制取液态氮和液态氧2. 下列有关化学史的叙述中错误的是( )A、拉瓦锡发现空气是由氧气和氮气组成的 B、张青莲精确测定了铟(In)的相对原子质量 C、门捷列夫制得了第一张元素周期表 D、波义耳在实验中发现质量守恒定律3. 化学教会我们从微观角度去认识宏观现象。下列对生活中现象的解释不合理的是( )A、春天公园里柳絮纷飞,因为分子在不停地运动 B、氮气不如氯气活泼,说明不同分子化学性质不同 C、水烧开后易把壶盖顶起,因为温度升高,分子间间隔增大 D、一滴水大约有1.6×1021个水分子,说明分子的体积很小4. 水是生命之源。下列有关说法正确的是( )A、经自制简易净水器净化后的山泉水是纯净物 B、过滤除去水中含有的少量泥沙,其中玻璃棒的作用是搅拌 C、地球上总水储量很大,淡水却很少 D、电解水实验中水分子的化学性质没有改变5. 中国科学院天津工业生物技术研究所研究成果“无细胞化学酶系统催化合成淀粉”相关论文在国际学术期刊《Nature》上发表,是合成过程中的一种中间产物。下列有关的说法正确的是( )A、该物质由碳原子、氢原子和氧原子构成 B、碳元素的质量分数为×100% C、碳、氢、氧三种元素的质量比为1:2:1 D、该物质有12个原子6. 南京理工大学胡炳成团队用新方法制得了NaN5·3H2O,该化合物中含有等微粒。则下列说法不正确的是( )A、是一种单质 B、1个中含有五个原子核 C、1个中共含有35个质子 D、1个中共含有36个电子7. 模型认知是化学核心素养之一,下列化学模型正确的是( )A、
 物质的性质和用途
B、
物质的性质和用途
B、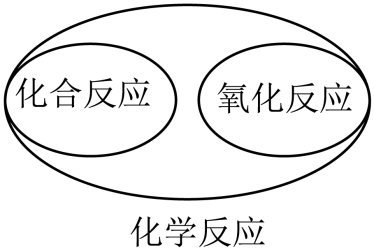 化学变化类型
C、
化学变化类型
C、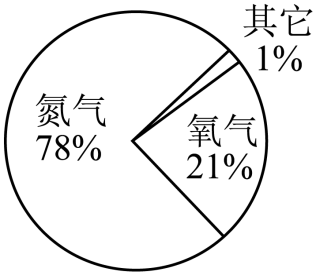 空气成分质量分数
D、
空气成分质量分数
D、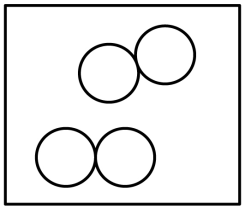 四个氮原子模型
8. 氨气(NH3)是一种无色、密度比空气小、极易溶于水的气体,实验室通常采用加热熟石灰和氯化铵固体混合物制取氨气。实验室制取并收集NH3的实验操作中不正确的是( )A、检查气密性
四个氮原子模型
8. 氨气(NH3)是一种无色、密度比空气小、极易溶于水的气体,实验室通常采用加热熟石灰和氯化铵固体混合物制取氨气。实验室制取并收集NH3的实验操作中不正确的是( )A、检查气密性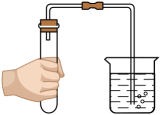 B、装入固体
B、装入固体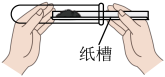 C、加热反应
C、加热反应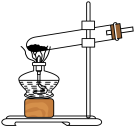 D、收集NH3
D、收集NH3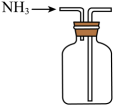 9. 除去下列物质中的少量杂质,所选用的试剂或方法正确的是( )
9. 除去下列物质中的少量杂质,所选用的试剂或方法正确的是( )选项
物质
杂质
所用试剂或方法
A
MnO2
KMnO4
充分加热
B
CaO
CaCO3
高温煅烧
C
N2
O2
放入燃着的蜡烛
D
Cu
C
在空气中充分加热
A、A B、B C、C D、D10. 两位英国科学家因在石墨烯材料方面的开创性研究获得2020年诺贝尔奖。石墨烯是由碳元素组成的单质,下列有关说法正确的是( )A、石墨烯不能与氧气反应 B、金刚石和石墨烯的碳原子排列相同 C、石墨烯有金属光泽,具有优良的导电性能 D、金刚石、石墨和足球烯(C60)都是由碳原子直接构成的单质11. 在一个密闭容器中加入甲、乙、丙、丁四种物质,在一定条件下发生化学反应,测得反应前及反应后各物质的质量如图所示,下列说法不正确的是( )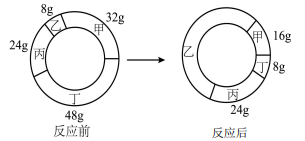 A、该反应是化合反应 B、丙可能是该反应的催化剂 C、反应后乙的质量是64g D、该反应中乙、丁的质量变化之比为7: 212. CO2与H2在一定条件下转化为CH4(反应过程如图所示,虚线处部分中间产物略去),可实现CO2的再利用。下列说法不正确的是( )
A、该反应是化合反应 B、丙可能是该反应的催化剂 C、反应后乙的质量是64g D、该反应中乙、丁的质量变化之比为7: 212. CO2与H2在一定条件下转化为CH4(反应过程如图所示,虚线处部分中间产物略去),可实现CO2的再利用。下列说法不正确的是( )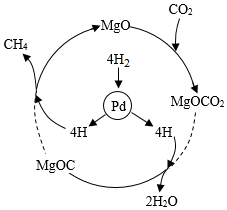 A、该反应中,除CH4外另一种生成物为H2O B、MgO的作用是催化作用 C、CH4在空气中燃烧时放出热量 D、参加反应的CO2与H2质量比是11:113. 证据推理是化学学科核心素养的重要内容,下列合理的是A、化学变化一定伴随着能量的改变,所以有能量改变的变化一定是化学变化 B、阴离子带负电荷,所以带负电荷的粒子一定是阴离子 C、化合反应的生成物只有一种,所以只有一种生成物的反应一定是化合反应 D、含有一种元素的纯净物是单质,所以单质中只含有一种元素14. 下列图像中不能正确反映对应变化关系的是( )A、
A、该反应中,除CH4外另一种生成物为H2O B、MgO的作用是催化作用 C、CH4在空气中燃烧时放出热量 D、参加反应的CO2与H2质量比是11:113. 证据推理是化学学科核心素养的重要内容,下列合理的是A、化学变化一定伴随着能量的改变,所以有能量改变的变化一定是化学变化 B、阴离子带负电荷,所以带负电荷的粒子一定是阴离子 C、化合反应的生成物只有一种,所以只有一种生成物的反应一定是化合反应 D、含有一种元素的纯净物是单质,所以单质中只含有一种元素14. 下列图像中不能正确反映对应变化关系的是( )A、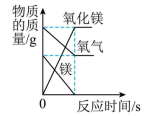 一定量的镁在过量氧气中充分燃烧
B、
一定量的镁在过量氧气中充分燃烧
B、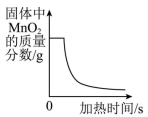 加热一定质量的氯酸钾和二氧化锰固体混合物
C、
加热一定质量的氯酸钾和二氧化锰固体混合物
C、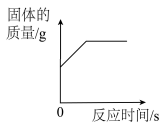 在盛有空气的密闭容器中灼烧一定质量的铜
D、
在盛有空气的密闭容器中灼烧一定质量的铜
D、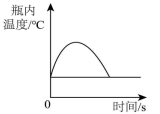 木炭在充满氧气的密闭集气瓶中燃烧
木炭在充满氧气的密闭集气瓶中燃烧
二、非选择题:本题包括 6 小题,共 48 分。
-
15. 稀土元素是指元素周期表中ⅢB 族的钪(Se)、钇(Y)以及铜系元素。这些元素的氧化物都不溶于水,外形像泥土,而且又稀少,因而人们喜欢称它们为“稀土元素”。稀土元素的化学性质较为活泼,若与其他元素结合,便可组成种类繁多、功能多样、用途广泛的新型材料,且性能会有较大提高,被称作当代的“工业味精”稀土元素的镧(La)、铈(Ce)、镨(Pr)、钕(Nd)在元素周期表中的位置如图所示。
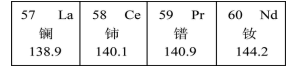
稀土元素的化合物还是生产特种玻璃和陶瓷的重要原料。如将三氧化二铈(Ce2O3)加入玻璃中,可制成低散射、高折射的光学玻璃,用于生产精密的光学器材。在铜铁、铸铁和合盒中加入少量稀土能大大改善性能;用稀土制作的催化剂,具有活性高、选择性好,抗重金属中毒能力强的优点;稀土氧化物是重要的发光材料激光材料;稀土元素可以提高植物的叶绿素含量,增强光合作用,促进根系发育,增加根系对养分吸收;稀土还能促进种子萌发,提高种子发芽率,促进幼苗生长,甚至还具有使某些作物增强抗病、抗寒、抗旱的能力。
根据短文内容,回答下列问题:
(1)、从材料中可得出,稀土元素的化学性质 。(2)、镧元素的质子数是 , 钕的相对原子质量是。(3)、请标出Ce2O3中Ce元素的化合价 。(4)、CeO2是汽车尾气净化器中的关键催化剂,CeO2读作 。(5)、稀土及其化合物具有的用途有____(填字母)A、制成低散射、高折射的光学玻璃 B、制作发光材料、激光材料 C、制作电缆 D、制作高选择性的催化剂16. 在探究分子的特征时设计了以下的实验: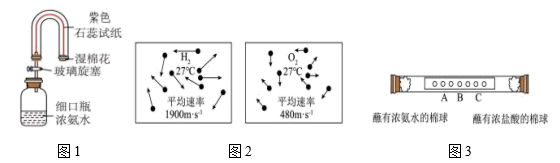 (1)、图1是“探究微粒性质”。打开玻璃旋塞,观察到润湿的紫色石蕊试纸从左到右先后变蓝(浓氨水能使紫色石蕊试纸变蓝),用分子的知识解释出现该现象的原因 , 湿棉花的作用是 。(2)、图2是27℃时氢分子和氧分子运动的微观示意图,说明:温度相同时,气体分子 越大,分子运动越 (填“快”或“慢”)。(3)、图3是“探究分子运动现象”的实验。浓氨水与浓盐酸混合后会产生白烟,图3中A、B、C 三处最先产生白烟的是处(填序号)。理由是。17. 水是生命之源,人类从未停止过对水的探究。
(1)、图1是“探究微粒性质”。打开玻璃旋塞,观察到润湿的紫色石蕊试纸从左到右先后变蓝(浓氨水能使紫色石蕊试纸变蓝),用分子的知识解释出现该现象的原因 , 湿棉花的作用是 。(2)、图2是27℃时氢分子和氧分子运动的微观示意图,说明:温度相同时,气体分子 越大,分子运动越 (填“快”或“慢”)。(3)、图3是“探究分子运动现象”的实验。浓氨水与浓盐酸混合后会产生白烟,图3中A、B、C 三处最先产生白烟的是处(填序号)。理由是。17. 水是生命之源,人类从未停止过对水的探究。【先贤智慧】
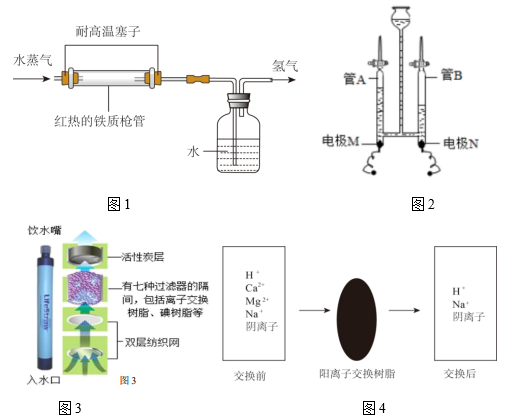 (1)、实验1:1766年英国化学家卡文迪许制得“可燃空气”,在纯氧中燃烧只生成水。他所说的“可燃空气”成分是 (填化学式)。(2)、实验2:1785年拉瓦锡将水蒸气通过红热的铁管(高温条件),生成氢气和四氧化三铁,实验如图1所示。上述反应的化学方程式为 。(3)、实验3:1800年英国化学家尼科尔森利用伏打电池对水进行通电,发现两极上都有气体逸出。实验室常用图2装置进行模拟,则M极与N极管中产生气体质量之比为 。(4)、上述3个实验中,能证明“水由氢元素和氧元素组成”的是____。A、实验1、2 B、实验1、3 C、实验2、3 D、实验1、2、3(5)、【当代成就】
(1)、实验1:1766年英国化学家卡文迪许制得“可燃空气”,在纯氧中燃烧只生成水。他所说的“可燃空气”成分是 (填化学式)。(2)、实验2:1785年拉瓦锡将水蒸气通过红热的铁管(高温条件),生成氢气和四氧化三铁,实验如图1所示。上述反应的化学方程式为 。(3)、实验3:1800年英国化学家尼科尔森利用伏打电池对水进行通电,发现两极上都有气体逸出。实验室常用图2装置进行模拟,则M极与N极管中产生气体质量之比为 。(4)、上述3个实验中,能证明“水由氢元素和氧元素组成”的是____。A、实验1、2 B、实验1、3 C、实验2、3 D、实验1、2、3(5)、【当代成就】“生命吸管”是军事上的重要发明,它可以解决士兵在野外极限环境中饮水问题(如图3)。
“生命吸管”的塑料外壳在空气中完全燃烧后生成水和二氧化碳,则塑料中一定含有的元素为 (填元素名称)。
(6)、纺织网可对污水进行过滤,其目的是拦截 (填“大于”或“小于”)网眼直径的颗粒。(7)、将硬水通过图4所示的阳离子交换柱后,可变成软水,交换后的水仍然呈电中性。①家庭生活中常用的软化硬水的方法是 。
②已知离子在阳离子交换树脂交换后电荷数量不变,因此每1个钙离子可以从阳离子交换树脂中换出 个钠离子。
③阳离子交换柱长时间使用后会失去硬水软化功能。取交换后的溶液少量,滴入 , 振荡,若观察到产生白色浮渣,几乎没有泡沫,则说明阳离子交换柱已失效。
18. 一种“贴身暖宝宝”的使用说明书如下,某化学兴趣小组围绕袋内物质展开探究。品名:XX牌贴身暖宝宝
袋内物质:铁粉、水、活性炭、食盐等
内袋材料:微孔透气无纺布
外袋材料:不透气塑料
用法:临使用前,打开外袋取出内袋,直接贴在衣服上,打开外袋后保持温暖12小时。
【提出问题】铁粉能否在空气中燃烧?
【获取事实】将少许铁粉撒在酒精灯火焰上,铁粉立即剧烈燃烧。
【反思交流】
(1)、铁粉在空气中燃烧的化学方程式。(2)、铁丝在纯氧中燃烧的现象是。(3)、铁丝在纯氧中能燃烧,但在空气中不能燃烧,造成此差异的原因是 。(4)、【拓展探究】用不同可燃物测定空气里氧气的含量:分别在图甲所示装置的燃烧匙内放置铁粉、红磷(均足量)电加热引燃。氧气含量随时间变化情况如图乙、图丙。
实验过程中瓶内温度均 (填“升高”或“降低”);
(5)、待铁粉熄灭并恢复至室温后,打开弹簧夹,进入瓶内的水约占玻璃瓶 。(6)、分析图乙、图丙可知,实验中消耗氧气更彻底的是 (填“铁粉”或“红磷”)。19. 气体的制取是初中化学的重要内容。(1)、实验一:研究氧气的制取
写出有标号的仪器名称:① ,② 。
(2)、实验室用双氧水和二氧化锰制氧气选用的发生装置是 (填序号),反应的化学方程式为 。(3)、实验二:研究二氧化碳的制取选用药品。按下表进行实验,取等质量的同种大理石加入足量酸中(杂质不与酸反应),产生二氧化碳的体积随时间变化曲线如图2所示
实验编号
药品
I
块状大理石、10%稀硫酸
II
块状大理石、7%稀盐酸
Ⅲ
粉状大理石、7%稀盐酸
①制取CO2的反应方程式为 。
②上表中实验Ⅰ对应如图曲线 (选填“甲”、“乙”或“丙”)。小组同学决定用实验Ⅱ的药品制取二氧化碳气体,不用实验Ⅲ药品制备二氧化碳的原因是 。
(4)、选择发生装置。实验小组同学在制取二氧化碳时想要控制反应的发生和停止,应选择图1中的 作发生装置。(5)、选择收集方法。物质种类
水
酒精
饱和NaHCO3溶液
每毫升液体中溶解二氧化碳的体积
1mL
3.6mL
几乎不溶
已知:二氧化碳在不同溶剂中的溶解度如上表。为了收集一瓶纯净的二氧化碳,对集气瓶中的液体(水、酒精、饱和NaHCO3)进行选择。

①选择时首先排除酒精的原因是 。
②最终选择的液体是 。
③用如图装置来收集二氧化碳气体,气体从 (填“a”或“b”)口通入。
(6)、为进一步验证排水实验的可行性,利用下图装置,选择合适的盐酸与块状石灰石反应,利用CO2浓度传感器,测得不同时间排出的CO2浓度如图所示,CO2浓度先逐渐增加后稳定不变。
图中水槽内倒置漏斗的作用是 。
实验结论:选用适当浓度的稀盐酸在适当时机用排水法收集CO2是可行的。
(7)、定量计算。鸡蛋壳的主要成分是碳酸钙。小明同学为了测定鸡蛋壳中碳酸钙的质量分数,分别设计了如下实验并进行计算。将鸡蛋壳洗净、干燥并捣碎后放入锥形瓶里,加入足量的稀盐酸充分反应(假设其他杂质不与盐酸反应)。测得相关数据如图所示:

①生成的二氧化碳质量为 。
②请帮小明计算鸡蛋壳中碳酸钙的质量分数 。
20. 有一个有趣的“黑面包”化学实验是将浓H2SO4与蔗糖在烧杯中混合在一起,用玻璃棒搅拌,发现蔗糖迅速变黑且不断膨胀,同时能闻到刺激性气味,化学兴趣小组的同学们决定对该反应的产物进行探究。【提出问题】浓H2SO4和蔗糖搅拌后的生成物有哪些?
【查阅资料】
①浓H2SO4与蔗糖搅拌后首先使蔗糖脱水变成碳且反应过程中放出大量的热,浓H2SO4再和碳在加热的条件下可以反应生成水和另外两种气态氧化物。
②SO2和CO2都能使澄清石灰水变浑浊,其中,SO2还能与紫红色的酸性KMnO4溶液反应使其褪色。
(1)、【提出猜想】于是他们对除水之外的产物成分进行了如下猜想:猜想一:SO2、CO2;猜想二:SO2、CO;猜想三: 。经过讨论,同学们一致认为猜想三不正确,原因是 。
(2)、【实验探究】实验操作
实验现象
实验结论
(1)将浓硫酸与碳反应产生的气体通入足量
溶液褪色
气体中有
(2)将上述实验后的气体通入澄清石灰水
气体中有CO2
(3)将操作(2)后产生的气体通过盛有灼热的氧化铜的玻璃管
无明显现象
气体中没有CO
(3)、【实验结论】猜想一成立。请写出浓硫酸与碳反应的化学方程式: 。(4)、 【拓展】常温下将浓硫酸与碳混合在一起看不到什么现象,说明浓硫酸与碳反应有关。