安徽省亳州市蒙城县五校2023-2024学年高三上学期11月期中联考化学试题
试卷更新日期:2024-03-01 类型:期中考试
一、选择题:本题共14小题,每小题3分,共42分。每小题只有一个选项符合题目要求。
-
1. 化学与科技、生产、生活密切相关,下列说法错误的是( )A、有机硅橡胶具有弹性大的特点,是一种良好的防振体,有机硅橡胶是纯净物 B、2023年5月成功发射的天舟六号货运飞船的推进剂可用液态肼 C、卡塔尔AI Janoub体育场屋顶采用的聚四氟乙烯板材属于有机高分子材料 D、碳纳米材料是新型无机非金属材料,主要包括富勒烯、碳纳米管、石墨烯等2. 我国古代四大发明之一黑火药的爆炸反应为。设为阿伏加德罗常数的值,下列说法正确的是( )A、含键数目为 B、晶体中含离子数目为 C、每生成转移电子数目为 D、溶液中含数目为3. 某些物质之间可以在一定条件下进行如下转化,下列说法正确的是( )
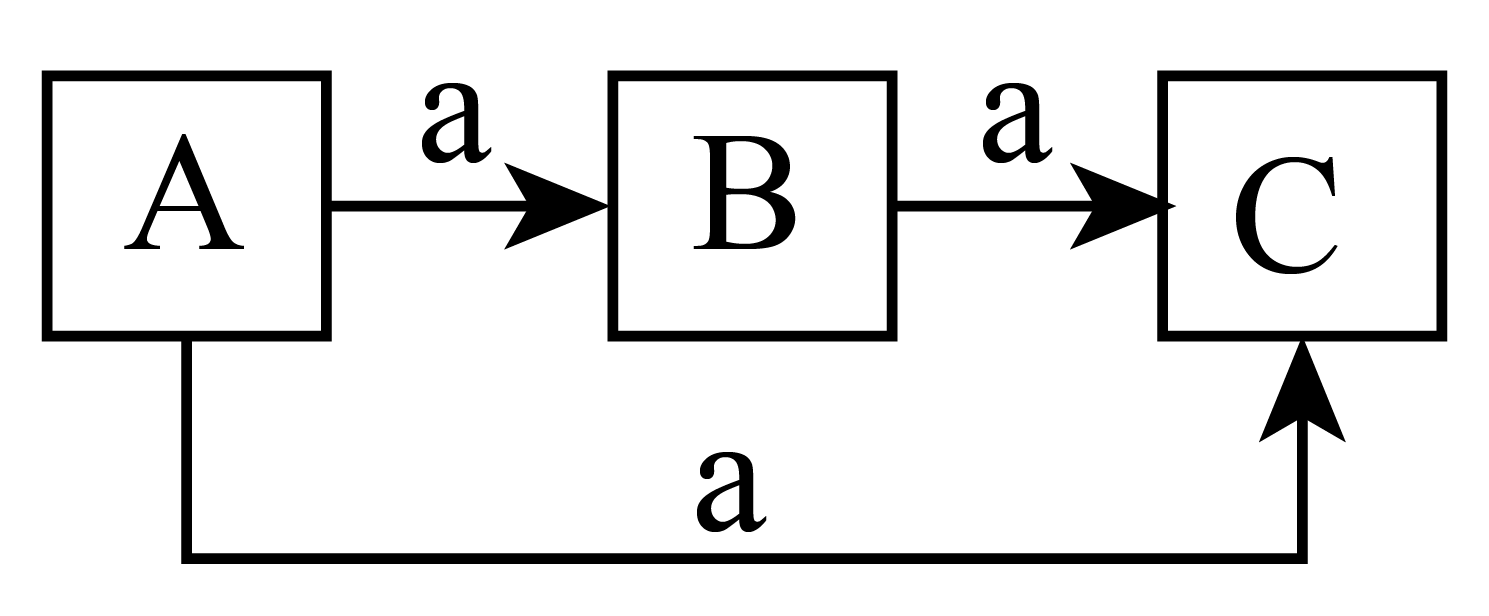 A、若A、B、C含同种金属元素,则a可能是NaOH溶液,也可能是氨水 B、若a为 , 则A可以为NH3 C、若a为 , 则A、B、C可以为NaClO、、 D、若a为 , A为乙醇,B为乙醛,则C一定是乙酸4. 常温下,下列各组离子在给定溶液中可能大量共存的是( )A、麦芽糖溶液中:、、、 B、能使苯酚溶液显紫色的溶液中:、、、 C、水电离出来的的溶液中:、、、 D、滴加甲基橙显红色的水溶液中:、、、5. 在复盐NH4Fe(SO4)2溶液中逐滴加入Ba(OH)2溶液,可能发生的反应的离子方程式是( )A、Fe2+++Ba2++2OH-═BaSO4↓+Fe(OH)2↓ B、+Fe3+++Ba2++4OH-═BaSO4↓+Fe(OH)3↓+NH3•H2O C、2Fe3++3+3Ba2++6OH-═3BaSO4↓+2Fe(OH)3↓ D、3+Fe3++3+3Ba2++6OH-═3BaSO4↓+Fe(OH)3↓+3NH3•H2O6. 向含a mol NaClO的溶液通入b mol SO2充分反应(不考虑二氧化硫与水之间的反应以及次氯酸的分解)。下列说法不正确的是( )A、当0<b< 时:SO2+H2O+3ClO-= +2HClO+Cl- B、当b=a时:SO2+H2O+ClO-=+2H++Cl- C、当 <b<a时;反应后溶液中H+的物质的量:0<n(H+)<2bmol D、当0<b<a时;反应后溶液中Cl-、ClO-和物质的量之比为:(a-b):b:b7. 工业烟气中含有较高浓度的氮氧化物,需进行脱除处理才能排放到大气中。下图是一种利用NH3在催化剂条件下脱除NO的原理示意图:
A、若A、B、C含同种金属元素,则a可能是NaOH溶液,也可能是氨水 B、若a为 , 则A可以为NH3 C、若a为 , 则A、B、C可以为NaClO、、 D、若a为 , A为乙醇,B为乙醛,则C一定是乙酸4. 常温下,下列各组离子在给定溶液中可能大量共存的是( )A、麦芽糖溶液中:、、、 B、能使苯酚溶液显紫色的溶液中:、、、 C、水电离出来的的溶液中:、、、 D、滴加甲基橙显红色的水溶液中:、、、5. 在复盐NH4Fe(SO4)2溶液中逐滴加入Ba(OH)2溶液,可能发生的反应的离子方程式是( )A、Fe2+++Ba2++2OH-═BaSO4↓+Fe(OH)2↓ B、+Fe3+++Ba2++4OH-═BaSO4↓+Fe(OH)3↓+NH3•H2O C、2Fe3++3+3Ba2++6OH-═3BaSO4↓+2Fe(OH)3↓ D、3+Fe3++3+3Ba2++6OH-═3BaSO4↓+Fe(OH)3↓+3NH3•H2O6. 向含a mol NaClO的溶液通入b mol SO2充分反应(不考虑二氧化硫与水之间的反应以及次氯酸的分解)。下列说法不正确的是( )A、当0<b< 时:SO2+H2O+3ClO-= +2HClO+Cl- B、当b=a时:SO2+H2O+ClO-=+2H++Cl- C、当 <b<a时;反应后溶液中H+的物质的量:0<n(H+)<2bmol D、当0<b<a时;反应后溶液中Cl-、ClO-和物质的量之比为:(a-b):b:b7. 工业烟气中含有较高浓度的氮氧化物,需进行脱除处理才能排放到大气中。下图是一种利用NH3在催化剂条件下脱除NO的原理示意图: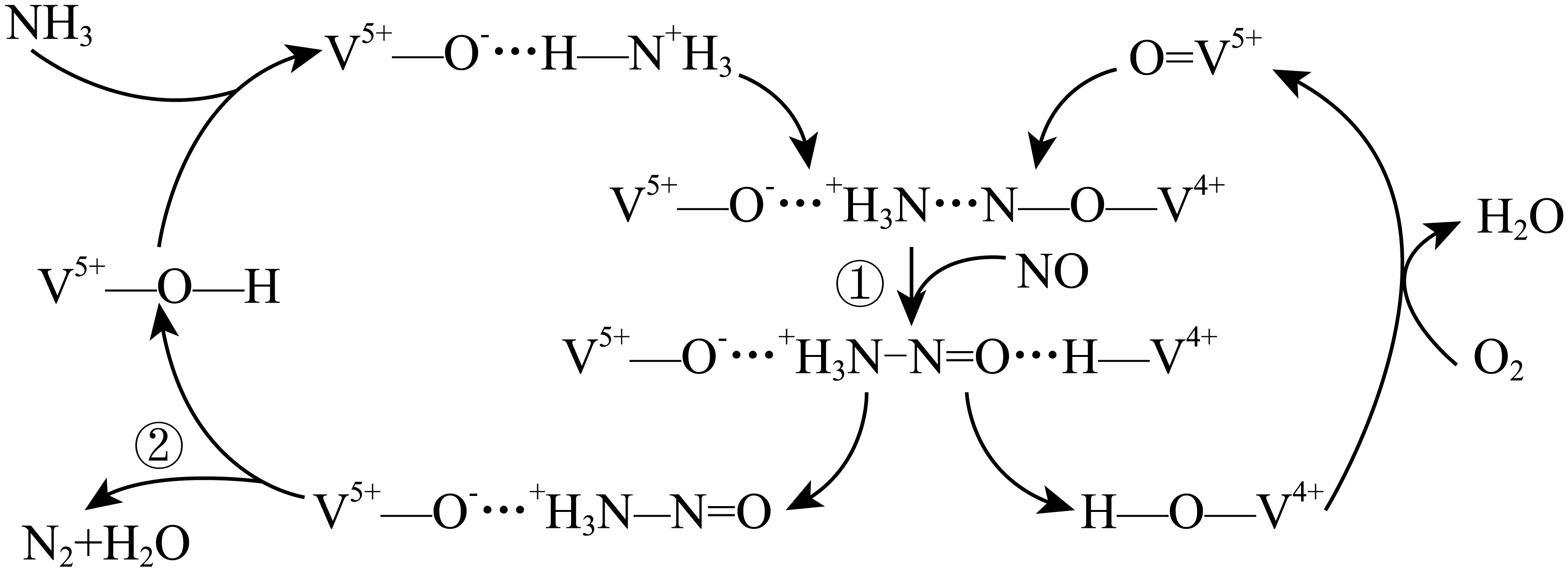
下列说法错误的是( )
A、步骤①中NO发生氧化反应 B、步骤②中包含有σ键和π键的断裂 C、若参与反应的NO和NH3的物质的量相等,则总反应化学方程式为4NH3+4NO+O24N2+6H2O D、当消耗和时,消耗NO的物质的量为8. X、Y、Z、W是原子序数依次增大的位于两个短周期主族元素,Y、W原子核外未成对电子数相同,Z与X的简单化合物很容易液化,X、Z核外最外层电子数之和等于W核外最外层电子数。四种元素能组成一种治疗痛风症的药物M,M的结构简式如图所示。下列说法正确的是( )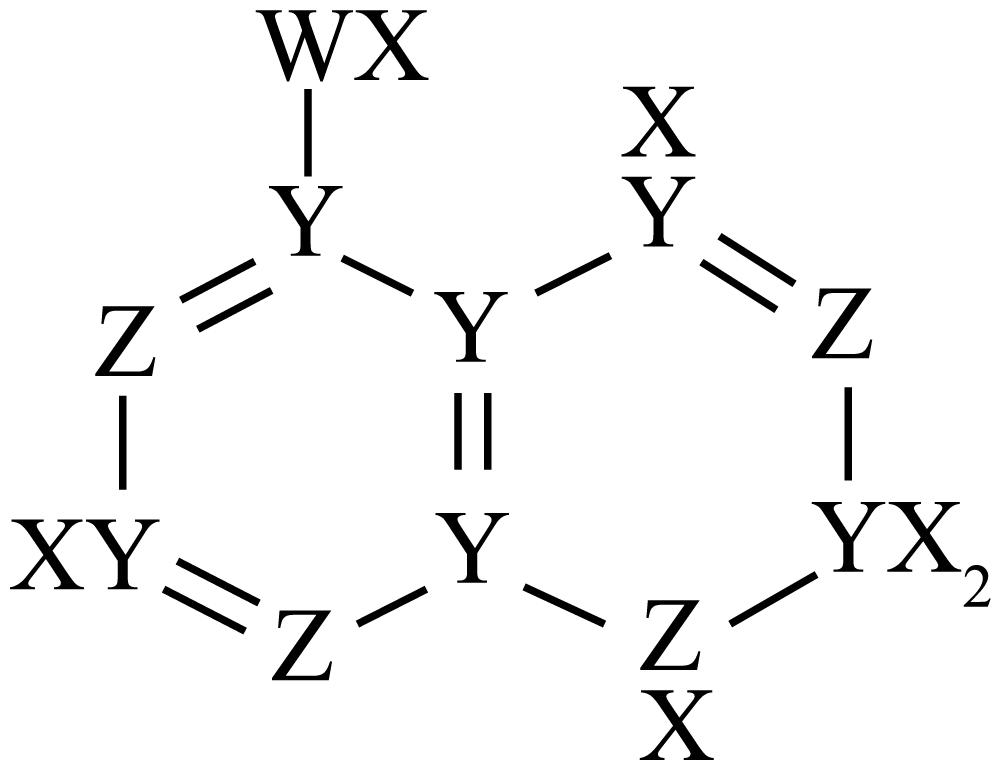 A、元素的第一电离能:W>Z>Y B、X、Z、W三种元素形成的化合物只能是共价化合物 C、M分子中,X、Y、Z、W四种原子均满足8电子稳定结构 D、Y与X,W形成的化合物有可能使酸性高锰酸钾溶液褪色9. 某同学欲验证Fe3+和I-在水溶液中发生可逆反应:2Fe3++2I-=2Fe2 ++I2 , 设计了下列实验操作,并给出了预测现象,其中不必要的实验操作是(不考虑水中溶解的少量氧气的影响)( )
A、元素的第一电离能:W>Z>Y B、X、Z、W三种元素形成的化合物只能是共价化合物 C、M分子中,X、Y、Z、W四种原子均满足8电子稳定结构 D、Y与X,W形成的化合物有可能使酸性高锰酸钾溶液褪色9. 某同学欲验证Fe3+和I-在水溶液中发生可逆反应:2Fe3++2I-=2Fe2 ++I2 , 设计了下列实验操作,并给出了预测现象,其中不必要的实验操作是(不考虑水中溶解的少量氧气的影响)( )实验操作
预测现象
A
在9 mL0.1 mol•L -1 KI溶液中滴加几滴FeCl3溶液,振荡,将溶液分为三等份
溶液颜色发生变化
B
往第一份溶液中滴加淀粉试液,振荡
溶液变蓝色
C
往第二份溶液中滴加几滴AgNO3溶液,振荡
有黄色沉淀产生
D
往第三份溶液中滴加几滴KSCN溶液,振荡
溶液变红色
A、A B、B C、C D、D10. 钒是一种熔点高、硬度大、无磁性的金属,广泛应用于钢铁、航空航天、能源等领域。工业上利用冶炼铝生成的固体废料——赤泥(主要成分为Fe2O3、Al2O3、V2O5及少量稀土金属氧化物)提取金属钒,其工艺流程图如下: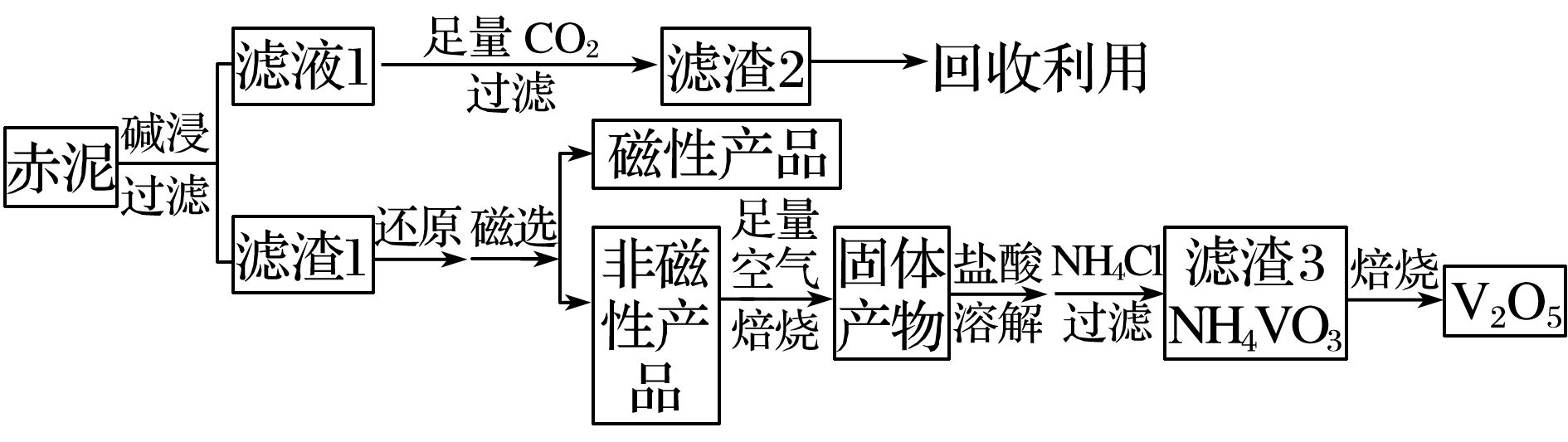
已知:钒有多种价态,其中+5价最稳定。钒在溶液中主要以VO2+和VO3-的形式存在,且存在平衡VO2++H2OVO3-+2H+。下列说法正确的是( )
A、工业生产中,碱浸步骤可选用较为廉价的氨水 B、可以推测VO2Cl溶解度大于NH4VO3 C、焙烧非磁性产品所得的固体产物加酸溶解时,应加入过量盐酸使其溶解完全 D、将磁性产品加入稀硝酸溶解,取上层清液再加入KSCN溶液后未见红色,则磁性产品中一定不含铁元素11. 理论研究表明,在101kPa和298K下, 异构化反应过程的能量变化如图所示。下列说法错误的是( ) A、HCN比HNC稳定 B、该异构化反应的 C、正反应的活化能大于逆反应的活化能 D、使用催化剂,可以改变反应的反应热12. 最近,一家瑞典公司发明了一种新型充电器"Power Trekk'’,仅仅需要一勺水,它便可以产生维持10小时手机使用的电量。其反应原理为:Na4Si+5H2O=2NaOH+Na2SiO3+4H2↑,则下列说法正确的是( )A、该电池可用晶体硅做电极材料 B、Na4Si在电池的负极发生还原反应,生成Na2SiO3 C、电池正极发生的反应为:2H2O+2e-=H2↑+2OH- D、当电池转移0.2 mol电子时,可生成标准状况下1.12 LH213. Cl2O能与水反应生成次氯酸,可杀死新型冠状病毒等多种病毒。一种制备Cl2O的原理为HgO+2Cl2=HgCl2+Cl2O,装置如图所示。
A、HCN比HNC稳定 B、该异构化反应的 C、正反应的活化能大于逆反应的活化能 D、使用催化剂,可以改变反应的反应热12. 最近,一家瑞典公司发明了一种新型充电器"Power Trekk'’,仅仅需要一勺水,它便可以产生维持10小时手机使用的电量。其反应原理为:Na4Si+5H2O=2NaOH+Na2SiO3+4H2↑,则下列说法正确的是( )A、该电池可用晶体硅做电极材料 B、Na4Si在电池的负极发生还原反应,生成Na2SiO3 C、电池正极发生的反应为:2H2O+2e-=H2↑+2OH- D、当电池转移0.2 mol电子时,可生成标准状况下1.12 LH213. Cl2O能与水反应生成次氯酸,可杀死新型冠状病毒等多种病毒。一种制备Cl2O的原理为HgO+2Cl2=HgCl2+Cl2O,装置如图所示。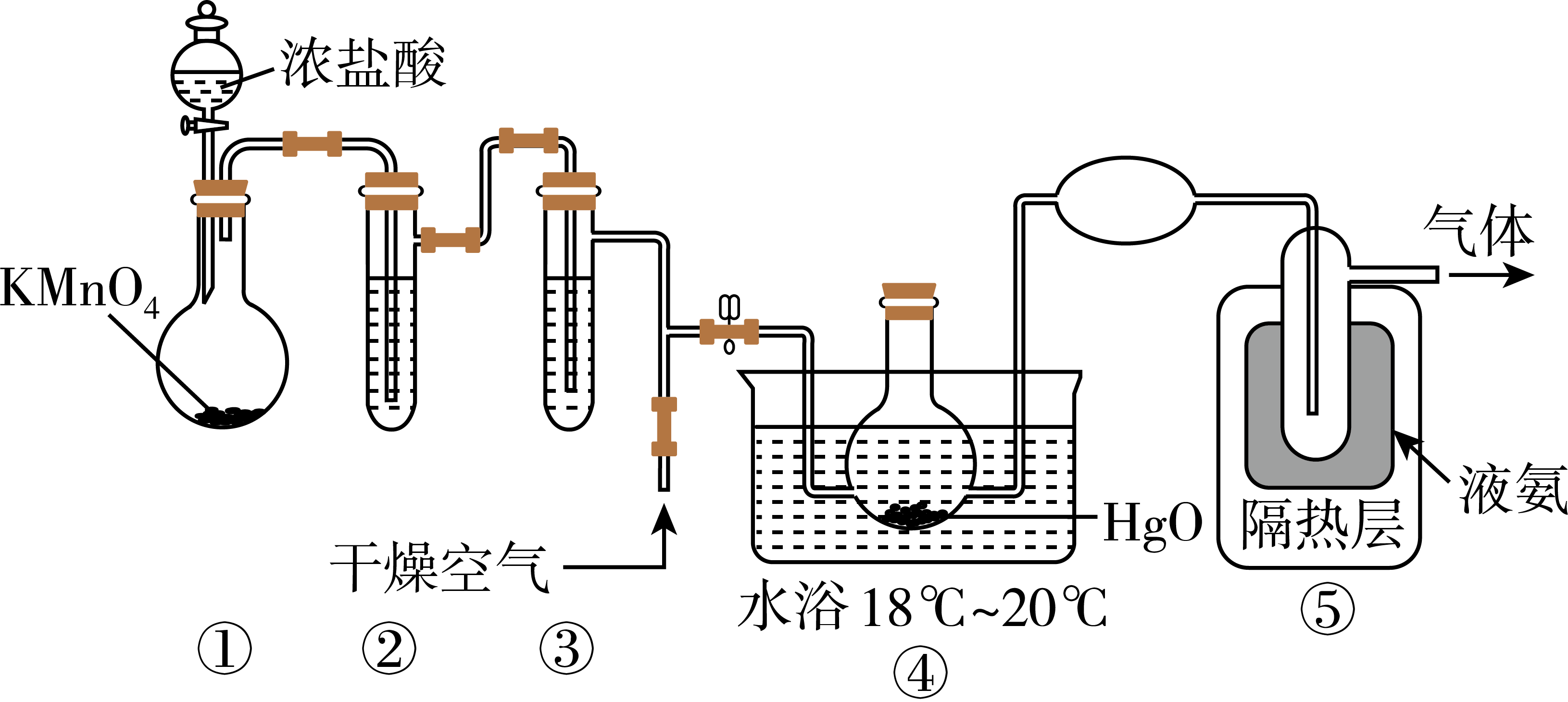
已知:①Cl2O的熔点为-116℃、沸点为3.8℃,具有强烈刺激性气味、易溶于水;
②Cl2O与有机物、还原剂接触或加热时会发生燃烧并爆炸。
下列说法中正确的是( )
A、装置③中盛装的试剂是饱和食盐水 B、装置④与⑤之间可用橡胶管连接 C、从装置⑤中逸出气体的主要成分是Cl2O D、通入干燥空气的目的是将生成的Cl2O稀释,减小爆炸危险14. 过二硫酸是一种疏的含氧酸,化学式。它的结构可以表示成。它的盐称为过二硫酸盐,在工业上用途广泛,用作强氧化剂等。下列反应分别是与过二硫酸盐和高锰酸盐反应的离子方程式(未配平),下列说法中错误的是( )Ⅰ.
Ⅱ.
A、过二硫酸根中显价的氧原子和显价的氧原子的数目比是3∶1 B、反应Ⅰ中氧化剂和还原剂物质的量之比是3∶2 C、反应Ⅱ中每生成 , 转移电子的物质的量为 D、若反应Ⅰ和反应Ⅱ中消耗的的物质的量相同,则Ⅰ和Ⅱ中消耗的氧化剂的物质的量之比为2∶5二、非选择题:本题共4小题,共58分。
-
15. 碘化钠在医药中用作甲状腺肿瘤防治剂、祛痰剂和利尿剂,也用作食品添加剂、感光剂等。工业上用NaOH溶液、水合肼制取碘化钠固体,其制备流程图如下:
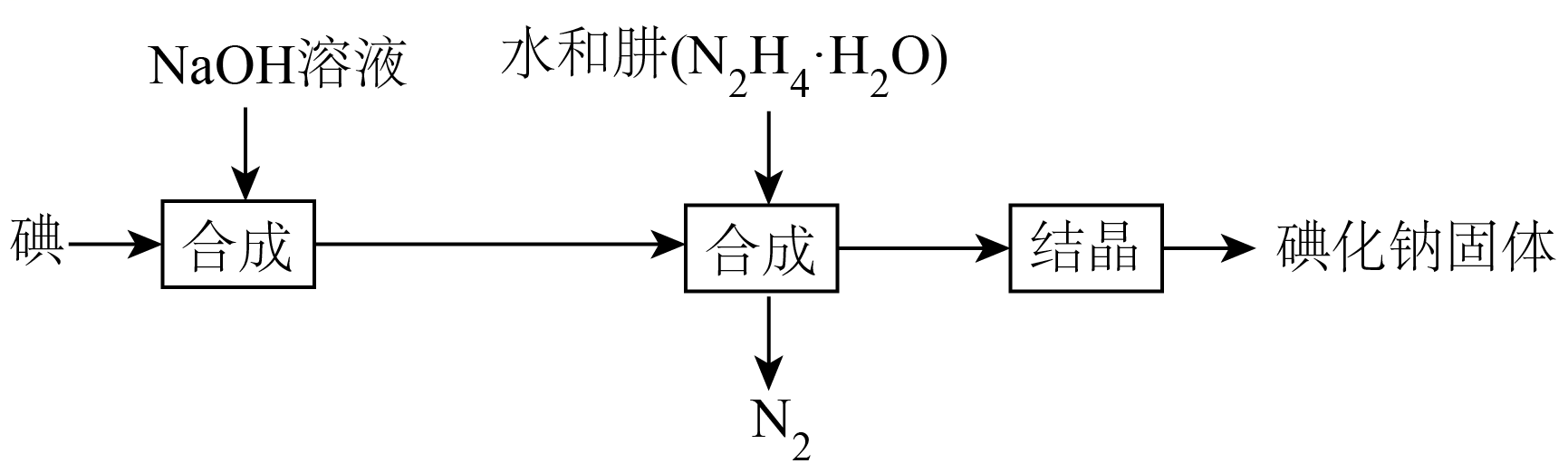
已知:在100℃以上分解。
(1)、已知:在合成过程的反应产物中含有NaIO3 , 则在合成过程中消耗了3molI2 , 所生成NaIO3的物质的量为mol。(2)、写出还原过程中的离子方程式;在还原过程中,为了加快反应,可采取可提高反应温度,但温度不得超过℃;请选择下列试剂检测所得碘化钠固体中是否含有NaIO3杂质(选填字母)。A.FeCl2溶液 B.冰醋酸 C.KI溶液 D.淀粉溶液
(3)、测定产品中NaI含量的实验步骤如下:a.称取4.000g样品、溶解,在250mL容量瓶中定容;
b.量取25.00mL待测液于锥形瓶中,然后加入足量的FeCl3溶液,充分反应后,再加入淀粉溶液作指示剂;
c.用的Na2S2O3溶液进行滴定至终点(发生反应的方程式为:),重复测定2次,所得的相关数据如下表:
测定序号
待测液体积/mL
标准液滴定管起点读数/mL
标准液滴定管终点读数/mL
1
25.00
006
24.04
2
25.00
0.02
24.02
3
25.00
0.12
24.14
①操作b中,加入足量的FeCl3溶液时所发生的离子方程式为。
②滴定终点观察到的现象为。
③计算该样品中NaI的含量为。(只写出有具体数值的表达式即可)
(4)、碘化钠固体的保存方法是。16. 绿色化学在推动社会可持续发展中发挥着重要作用。某科研团队设计了一种熔盐液相氧化法制备高价铬盐的新工艺,该工艺不消耗除铬铁矿、氢氧化钠和空气以外的其他原料,不产生废弃物,实现了Cr-Fe-Al-Mg的深度利用和内循环。工艺流程如下图:
回答下列问题:
(1)、高温连续氧化工序中被氧化的元素是(填元素名称)。(2)、滤渣Ⅰ的主要成分是(填化学式)。(3)、工序③中发生反应的离子方程式为。(4)、物质Ⅴ可代替高温连续氧化工序中的NaOH,此时发生的主要反应的化学方程式为 , 可代替NaOH的化学试剂还有(填化学式)。(5)、热解工序产生的混合气体最适宜返回工序(填①、②、③或④)参与内循环。(6)、工序④溶液中的反应的化学方程式为。17.(1)、Ⅰ.页岩气中含有、、等气体,是可供开采天然气资源。页岩气的有效利用需要处理其中所含的和。
和在Cu/ZnO催化下发生反应可合成清洁能源甲醇: , 该反应实际上分两步进行。断开(或形成)1mol化学键的能量变化数据如下表所示,利用下表中的数据可知,该反应每生成1mol甲醇,需要(填“吸收”或“放出”)kJ的热量。
化学键
H-H
C-O
C=O
O-H
C-H
436
326
803
464
414
(2)、可利用热分解制备 , 已知下列反应的热化学方程式:①
②
③
计算热分解反应④ 。
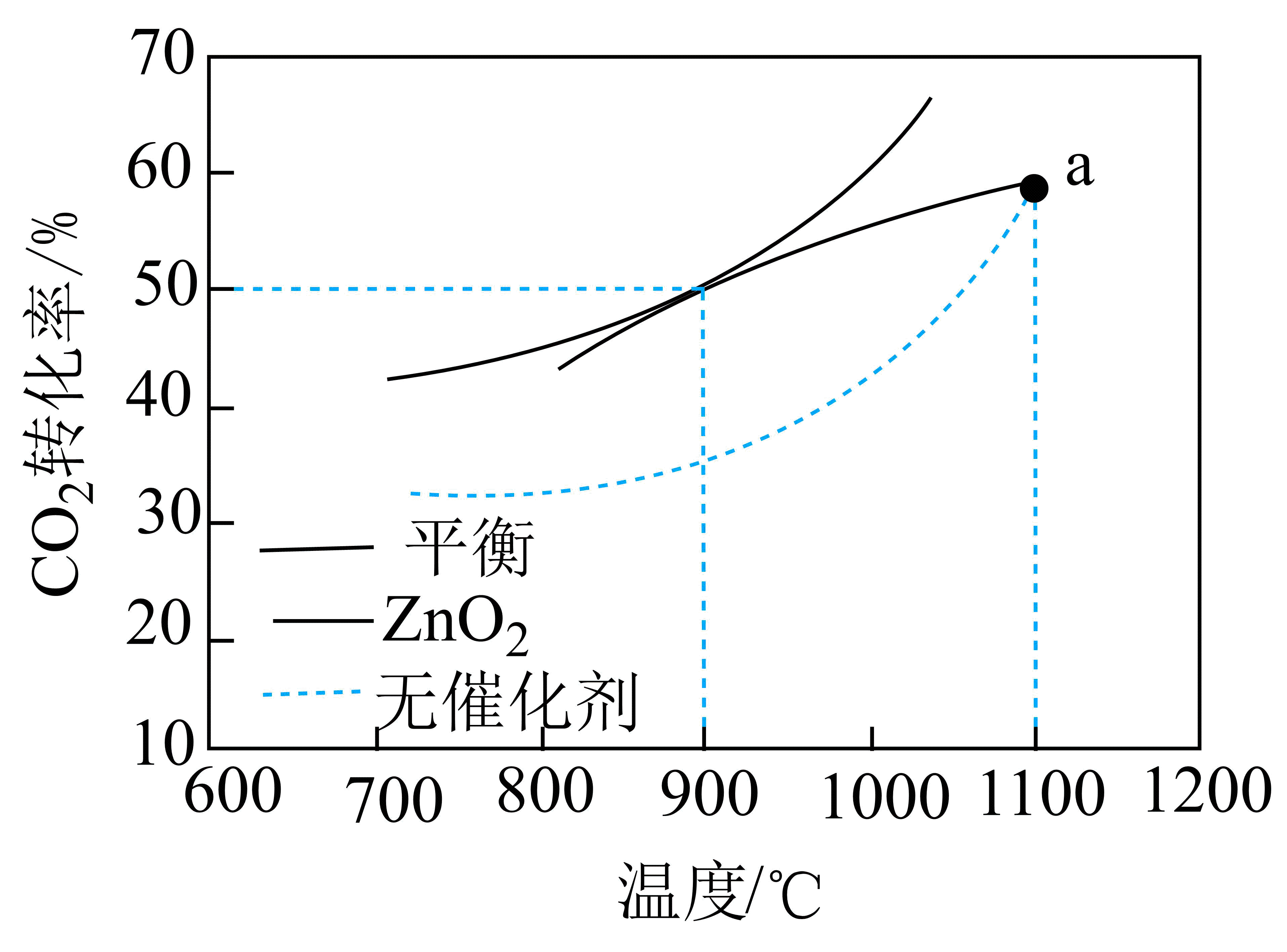
(3)、重整技术是实现“碳中和”的一种理想的利用技术,反应为:。在pMPa时,将和按物质的量之为1:1:充入密闭容器中,分别在无催化剂及催化下反应相同时间,测得的转化率与温度的关系如图所示:在pMPa、900℃、催化条件下,将、、按物质的量之比为充入密闭容器,的平衡转化率为 , 此时平衡常数(以分压表示,分压=总压×物质的量分数;写出含、、的计算表达式)。
 (4)、Ⅱ.回收利用工业废气中的和 , 实验原理示意图如下。
(4)、Ⅱ.回收利用工业废气中的和 , 实验原理示意图如下。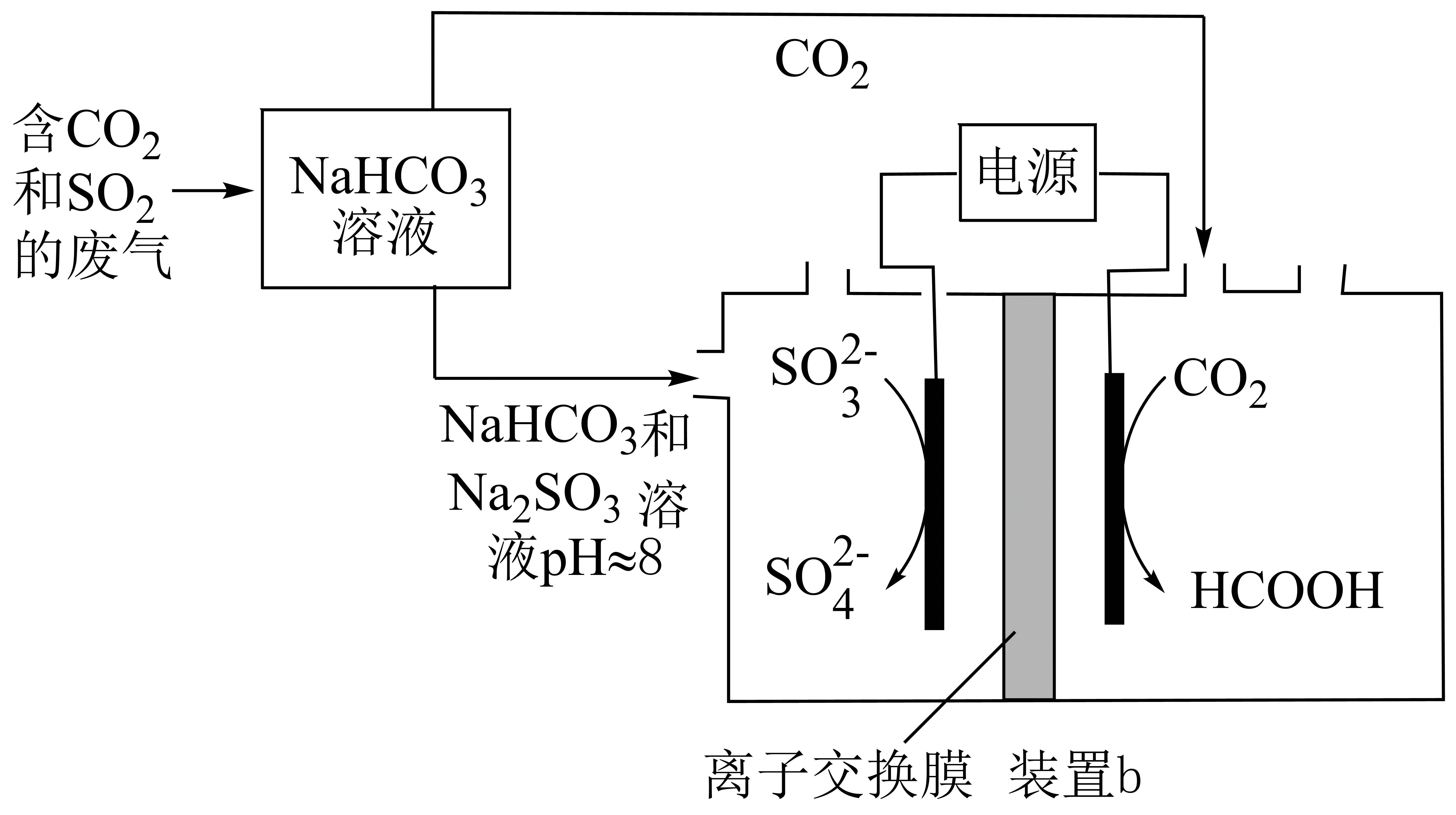
①装置b中参与反应的电极为极(填“正”、“负”、“阴”或“阳”)
②反应后装置b中溶液pH变化(填“增大”、“减小”或“不变”)
③装置b中的总反应的离子方程式为。
18. 1841年美国学者Fremy首次合成了 , 它是一种“环境友好型氧化剂”。某小组拟制备 , 并探究其性质。已知20℃时KCl的溶解度为37.4g,的溶解度为11.1g。(1)、实验(一)制备 , 装置如图所示:
乙装置的作用是。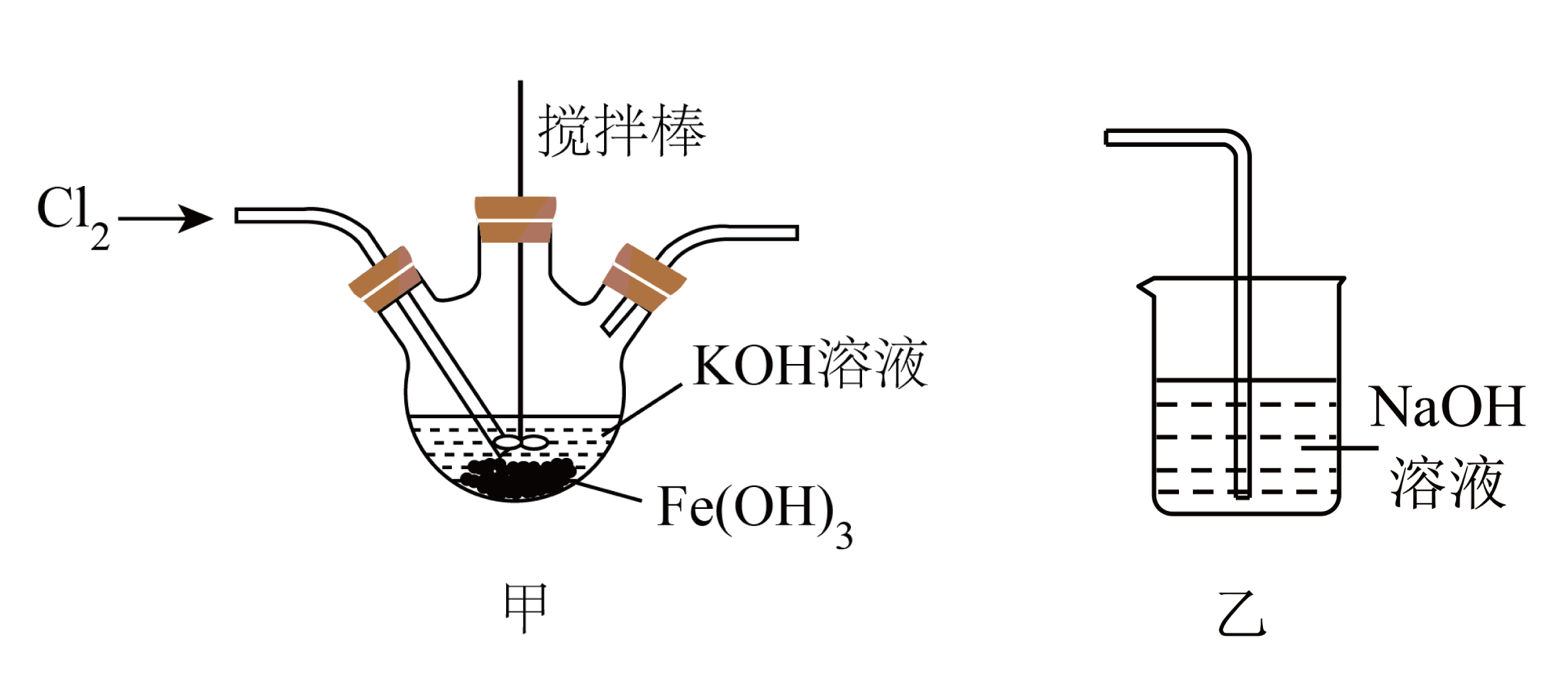 (2)、甲装置中副产物为氯化钾,写出生成的离子方程式: , 实验完毕后,对甲装置中混合液进行过滤、洗涤、低温干燥。(3)、实验(二)探究性质及应用。
(2)、甲装置中副产物为氯化钾,写出生成的离子方程式: , 实验完毕后,对甲装置中混合液进行过滤、洗涤、低温干燥。(3)、实验(二)探究性质及应用。取10g草酸溶于40mL水中,加入粉末,充分混合,观察到有大量气泡产生,并产生黑色固体。将所得气体通入足量澄清石灰水中,溶液变浑浊。根据上述实验现象,可以判断产生的气体中含有 , 经测定所得气体中还含有。
实验完毕后,将混合物经过滤、洗涤、干燥得到黑色固体,利用如图实验装置探究黑色固体的成分,当黑色固体完全反应后,测得浓硫酸质量净增bg,当等于(用最简分数比表示)时,黑色固体为。
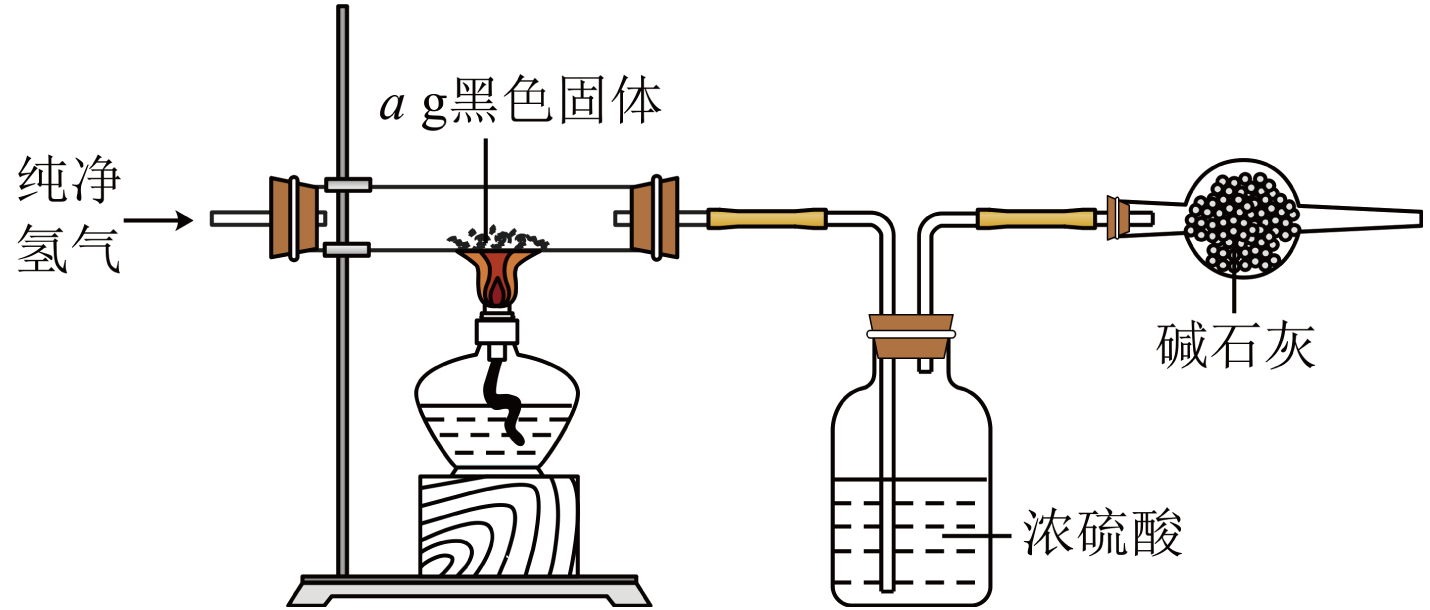 (4)、在其他条件相同时,测得一定浓度的稳定性(用浓度表示)与pH关系如图,其消毒效率与温度关系如图所示:
(4)、在其他条件相同时,测得一定浓度的稳定性(用浓度表示)与pH关系如图,其消毒效率与温度关系如图所示: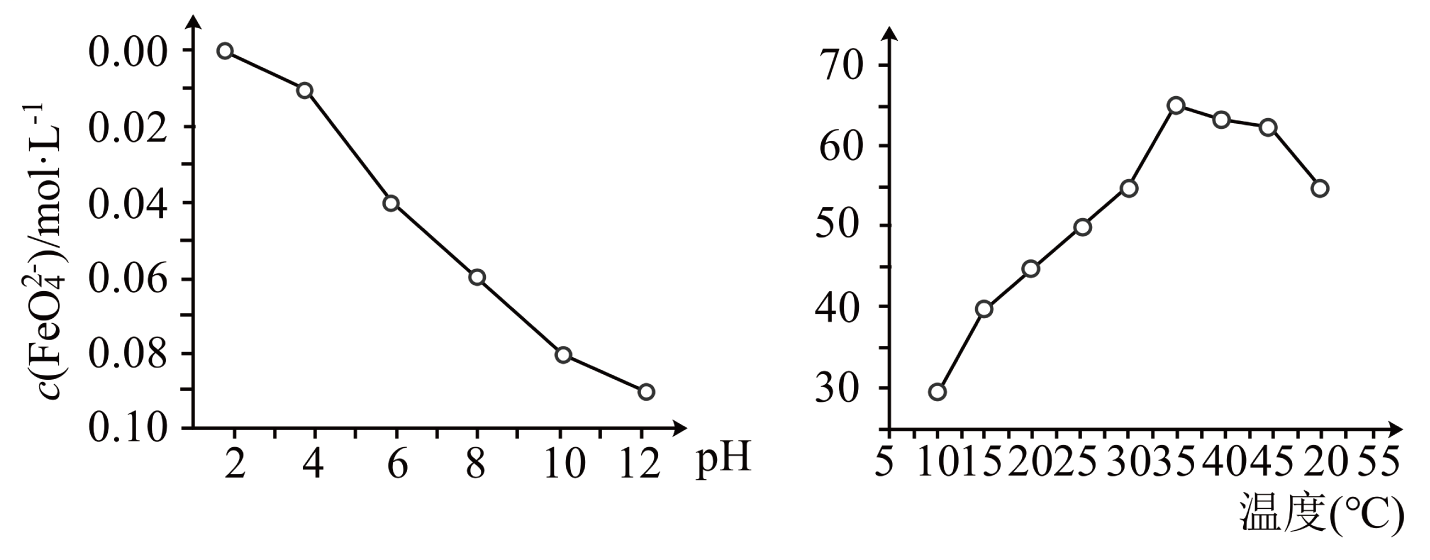
①根据稳定性与pH关系图得出结论是。
②在相同条件下,作消毒剂最佳温度是。
(5)、查阅资料可知,溶液呈紫红色,为探究和的电位相对大小,设计如下方案。(已知:电位一般指“电势”,用“”表示。氧化剂的电位是衡量其氧化性强度主要参数,电位越高,对应2条件下氧化剂的氧化性越强。)方案1:在溶液中加过量的粉末,溶液呈紫红色。
方案2:如图所示,关闭K时,观察到电流计指针偏转,铂极产生红褐色物质,石墨极附近无色溶液变紫红色。
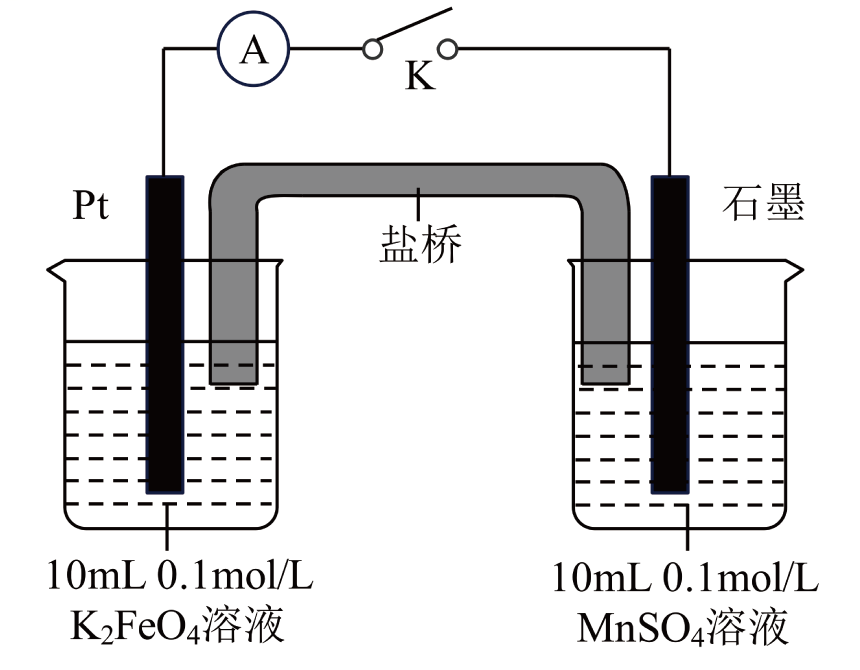
方案(填“1”或“2”)能证明 , 石墨极的电极反应式为。