湖北省黄冈市黄梅县2023-2024学年九年级上学期自主招生化学模拟训练
试卷更新日期:2024-03-01 类型:水平会考
一、单选题(共10小题,20分)
-
1. 2023年5月28日,国产大型客机C919成功完成首次商业飞行。下列C919应用的材料中,不属于金属材料的是( )A、碳纤维复合材料 B、第三代铝锂合金 C、钛合金 D、钢材料2. 《吕氏春秋》中记载“金柔锡柔,合两柔则刚”,说明与纯金属相比,合金的优点是( )A、熔点更低 B、硬度更大 C、密度更小 D、导热更好3. 科技先行,“智”无止境,在杭州亚运会上的“黑科技”体现我国科技的进步与发展。下列相关的说法错误的是( )




A.数形结合的点火方
式:使燃料温度达到
着火点
B.移动摄像机器人锂
电池放电时能量转化:
电能→化学能
C.机器狗:四肢使用
的不锈钢属于金属材料
D.使用“数字烟花”
对环境友好且成本低
A、A B、B C、C D、D4. 走近千年文物,青铜器中含有铜单质,在含有 Cl﹣的环境中易生成 CuCl,随着环境条件的变化而发生锈蚀,锈层物质成分示意图如图所示。下列叙述正确的是( ) A、铜绿和粉状锈中都含有 Cu、O、H、C 四种元素 B、表面发生锈蚀的青铜器中,铜元素的化合价有 3 种 C、CuCl、O2、H2O 三者发生化合反应生成 Cu2(OH)3Cl D、远洋船舶使用的铜制品易生成氯化铜,进而发生锈蚀,需要做好防锈措施5. 已知一包镁粉中含有两种杂质,小明同学取2.4g该粉末,向其中加入足量的稀硫酸,充分反应后得到0.2g氢气,则该样品中的杂质可能是( )A、铁和锌 B、铝和锌 C、锌和铜 D、铁和铜6. 根据金属与酸反应的知识绘制了下列图像,其中正确的是( )A、
A、铜绿和粉状锈中都含有 Cu、O、H、C 四种元素 B、表面发生锈蚀的青铜器中,铜元素的化合价有 3 种 C、CuCl、O2、H2O 三者发生化合反应生成 Cu2(OH)3Cl D、远洋船舶使用的铜制品易生成氯化铜,进而发生锈蚀,需要做好防锈措施5. 已知一包镁粉中含有两种杂质,小明同学取2.4g该粉末,向其中加入足量的稀硫酸,充分反应后得到0.2g氢气,则该样品中的杂质可能是( )A、铁和锌 B、铝和锌 C、锌和铜 D、铁和铜6. 根据金属与酸反应的知识绘制了下列图像,其中正确的是( )A、 向等质量、等质量分数的稀硫酸中分别加入过量的锌粉和铁粉
B、
向等质量、等质量分数的稀硫酸中分别加入过量的锌粉和铁粉
B、 向等质量、等质量分数的稀硫酸中分别加入过量的铝粉和铁粉
C、
向等质量、等质量分数的稀硫酸中分别加入过量的铝粉和铁粉
C、 向等质量的锌粉和铁粉中分别加入溶质质量分数相等的稀硫酸
D、
向等质量的锌粉和铁粉中分别加入溶质质量分数相等的稀硫酸
D、 向等质量的铝粉和铁粉中分别加入溶质质量分数相等的稀硫酸
7. 向质量均为m的锌粉和铁粉中分别滴加100g相同质量分数的稀硫酸,反应过程中产生气体的质量与所加稀硫酸的质量关系如图所示。下列叙述中正确的是( )
向等质量的铝粉和铁粉中分别加入溶质质量分数相等的稀硫酸
7. 向质量均为m的锌粉和铁粉中分别滴加100g相同质量分数的稀硫酸,反应过程中产生气体的质量与所加稀硫酸的质量关系如图所示。下列叙述中正确的是( ) A、反应结束后,两种金属均有剩余 B、反应结束后,消耗硫酸的质量相等 C、b表示的是铁和稀硫酸反应的情况 D、反应结束后,所得溶液的质量相等8. 如图所示探究实验,反应开始杠杆处于平衡状态。下列说法错误的是 ( )
A、反应结束后,两种金属均有剩余 B、反应结束后,消耗硫酸的质量相等 C、b表示的是铁和稀硫酸反应的情况 D、反应结束后,所得溶液的质量相等8. 如图所示探究实验,反应开始杠杆处于平衡状态。下列说法错误的是 ( )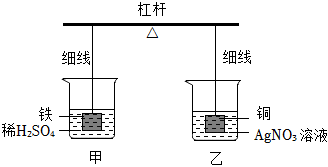 A、铁片逐渐溶解,铁片上有气泡冒出 B、烧杯甲中溶液由无色变浅绿色 C、烧杯乙中溶液由无色变蓝色 D、杠杆失去平衡,左边低右边高9. 将一定量的锌粉加到硫酸亚铁、硫酸铜的混合溶液中,过一段时间后过滤,向滤渣中加入稀盐酸有气泡产生,则下列叙述不正确的是( )A、滤渣中一定含有铜、铁,可能含有锌 B、滤液中溶质一定含有硫酸锌 C、滤液的颜色可能为浅绿色 D、向滤渣中加入稀盐酸,最后溶液一定变成浅绿色10. 向5.6g铁粉中先逐滴加入一定量的Cu(NO3)2溶液,充分反应后再逐滴加入AgNO3溶液,剩余固体质量与所加溶液总质量的关系如图所示,下列说法正确的是( )
A、铁片逐渐溶解,铁片上有气泡冒出 B、烧杯甲中溶液由无色变浅绿色 C、烧杯乙中溶液由无色变蓝色 D、杠杆失去平衡,左边低右边高9. 将一定量的锌粉加到硫酸亚铁、硫酸铜的混合溶液中,过一段时间后过滤,向滤渣中加入稀盐酸有气泡产生,则下列叙述不正确的是( )A、滤渣中一定含有铜、铁,可能含有锌 B、滤液中溶质一定含有硫酸锌 C、滤液的颜色可能为浅绿色 D、向滤渣中加入稀盐酸,最后溶液一定变成浅绿色10. 向5.6g铁粉中先逐滴加入一定量的Cu(NO3)2溶液,充分反应后再逐滴加入AgNO3溶液,剩余固体质量与所加溶液总质量的关系如图所示,下列说法正确的是( ) A、所加溶液质量为M1g时,生成Cu的质量为m1g B、a~b段和b~c段溶液中的溶质均为Fe(NO3)3 C、c点对应的剩余固体中含有Cu、Ag D、e点溶液中只含AgNO3
A、所加溶液质量为M1g时,生成Cu的质量为m1g B、a~b段和b~c段溶液中的溶质均为Fe(NO3)3 C、c点对应的剩余固体中含有Cu、Ag D、e点溶液中只含AgNO3二、填空题(共4小题,共20分)
-
11. 人类文明的发展和社会的进步与材料关系密切。请回答下列问题:(1)、地铁是近年来新兴的城市地下交通工具,动力为电力,开动时电车上裸露的电刷沿架空电线滑动,截止到2022年底南宁市已开通5条地铁线。

请回答下列问题:
①制作电刷的主要材料应选用(填字母)。
A.金刚石 B.石墨 C.铝 D.铜
②地铁的铁轨通常是由铁合金制成的,合金相比于纯铁的优点是(填一点即可)。
③列车表面喷漆除美观外,主要是为了防止外壳生锈,其防锈原理是。
(2)、在空气中铝具有很好的抗腐蚀性,其原因用化学方程式表示:。(3)、向m克Zn和Fe的混合物中加入一定质量的CuCl2溶液,充分反应后过滤:将滤渣洗涤、干燥后称量,质量仍为m克,对所得滤液和滤渣的判断正确的是____。A、滤液可能是无色 B、滤液中一定有ZnCl2和FeCl2 C、滤渣中的物质可能有3种 D、向滤渣中加稀盐酸可能有气泡产生12. 某溶液中含有Cu(NO3)2和AgNO3 , 现向其中逐渐加入一定质量的铁粉进行处理,并绘制出参加反应的铁的质量与溶液中溶质种类的关系图。
请回答:
(1)、a、b两点,溶液的质量ab(填“=”、“<”或“>”)。(2)、请写出c~d段发生反应的化学方程式。(3)、某金属(用R表示)活动性弱于Fe,但能与盐酸发生置换反应,生成RCl2 , 若将一定质量的金属R加入c点对应的溶液中,充分反应后溶液中溶质的成分为一定有 , 可能有。13. 钢件水蒸气发蓝处理在机械制造行业应用广泛。处理方法为将钢件置于水蒸气中,使其表面生成致密的Fe3O4薄膜。资料表明:合格的发蓝钢件在室温下浸泡于3%NaCl溶液中10分钟,取出后暴露在空气中2小时,表面上也不会出现锈蚀斑点。(1)、钢件发蓝处理后,其氧化膜能有效阻止锈蚀的原因是。(2)、研究表明,钢件水蒸气发蓝处理时,温度、时间与氧化膜厚度、色泽的关系如下表。据此可知,钢件水蒸气发蓝处理适宜的温度和时间为。序号
处理湿度/℃
时间/min
氧化膜厚度
氧化膜色泽
1
<500
<30
较薄
颜色浅
2
540~560
60
适中
蓝黑色、均匀美观
3
>600
>90
较厚、容易剥落
颜色深
(3)、不同温度、水蒸气浓度下,水蒸气与铁反应的产物可能是Fe3O4或FeO,具体情况如图所示。
①750℃、水蒸气浓度为50%时,铁与水蒸气发生置换反应的化学方程式为。
②发蓝处理时,为获得蓝黑色且均匀美观的氧化膜,反应体系中水蒸气的浓度应不低于%。
③FeO也能与水蒸气反应生成Fe3O4同时得到一种气体,写出反应方程式。
(4)、为检验某经发蓝处理后的钢件表面是否形成致密的氧化膜,处理后的钢件是否合格,兴趣小组开展如下活动:①检验氧化膜是否致密。将处理后的钢件浸入硫酸铜溶液,—段时间后若未见钢件表面有红色物质析出,则可认为钢件表面形成了致密的氧化膜。原因是。
②检验处理后的钢件是否合格。兴趣小组应开展的活动是。
14. 某校化学实验室废液桶中收集了溶有大量FeSO4、CuSO4的废液,小轩想从中回收金属铜和硫酸亚铁晶体,设计了如下实验方案。结合实验方案回答下列问题: (1)、金属X为。(2)、加入适量溶液Y的目的是 , 溶液Y是 , 有关反应的化学方程式为。
(1)、金属X为。(2)、加入适量溶液Y的目的是 , 溶液Y是 , 有关反应的化学方程式为。三、计算题(4分)
-
15. 现有某铁样品5.6g,含有的杂质为镁、锌、铜中的两种或三种。向其中逐渐加入溶质质量分数为9.8%的稀硫酸,产生氢气质量与加入稀硫酸质量的关系如图所示。
 (1)、则下列结论正确的是(填序号)。
(1)、则下列结论正确的是(填序号)。①恰好完全反应时,一定没有固体剩余
②x的值为0.2
③铁样品中可能含有镁
④M点对应的溶液中含有2种或3种溶质
(2)、用含Fe2O360%的赤铁矿石800t,理论上可炼出含铁98%的生铁吨。(3)、已知某铁的氧化物可表示为FeaOb=xFeO•yFe2O3。经测:15.2克的某铁的氧化物中铁元素的质量为11.2克。则x:y=(填最小整数比)。四、实验题(共1小题,6分)
-
16. 兴趣小组欲探究Fe、Cu、Ag三种金属的活动性顺序,进行了如下实验:
 (1)、进行实验前先将金属打磨干净的目的是。如图所示,将四根金属丝同时插入烧杯中,则甲中发生反应的化学方程式是 , 乙中的现象是 , 由此可以得到三种金属的活动性由弱到强的顺序是。小明认为可以去掉甲也可得出三者活动性强弱,你同意他的观点吗。(2)、若将一定量的铁加入含有硝酸银和硝酸铜的混合溶液中,充分反应后过滤,得到的滤液依旧是蓝色的,则滤液中一定含有的溶质是(填化学式)。
(1)、进行实验前先将金属打磨干净的目的是。如图所示,将四根金属丝同时插入烧杯中,则甲中发生反应的化学方程式是 , 乙中的现象是 , 由此可以得到三种金属的活动性由弱到强的顺序是。小明认为可以去掉甲也可得出三者活动性强弱,你同意他的观点吗。(2)、若将一定量的铁加入含有硝酸银和硝酸铜的混合溶液中,充分反应后过滤,得到的滤液依旧是蓝色的,则滤液中一定含有的溶质是(填化学式)。
-