【备考2024年】高考化学广东卷真题变式分层精准练(第13题)
试卷更新日期:2024-02-26 类型:二轮复习
一、真题重现
-
1. 利用活性石墨电极电解饱和食盐水,进行如图所示实验。闭合 , 一段时间后( )
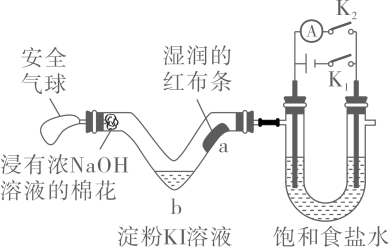 A、U型管两侧均有气泡冒出,分别是和 B、a处布条褪色,说明具有漂白性 C、b处出现蓝色,说明还原性: D、断开 , 立刻闭合 , 电流表发生偏转
A、U型管两侧均有气泡冒出,分别是和 B、a处布条褪色,说明具有漂白性 C、b处出现蓝色,说明还原性: D、断开 , 立刻闭合 , 电流表发生偏转二、基础巩固
-
2. 海洋生物参与氮循环的过程如图所示,下列说法正确的是
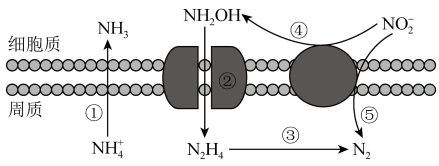 A、图中微粒间的转化均属于氧化还原反应 B、酸性环境有利于反应① C、反应③可能有氧气参与反应 D、反应③、⑤属于氮的固定3. 把锌片和铁片放在盛有稀食盐水和K3[Fe(CN)6]试液混合溶液的培养皿中,经过一段时间后,下列说法中正确的是(提示:Fe2+遇K3[Fe(CN)6]产生蓝色沉淀)( )
A、图中微粒间的转化均属于氧化还原反应 B、酸性环境有利于反应① C、反应③可能有氧气参与反应 D、反应③、⑤属于氮的固定3. 把锌片和铁片放在盛有稀食盐水和K3[Fe(CN)6]试液混合溶液的培养皿中,经过一段时间后,下列说法中正确的是(提示:Fe2+遇K3[Fe(CN)6]产生蓝色沉淀)( ) A、Ⅰ附近产生黄绿色气体 B、Ⅱ附近铁受保护而几乎不被腐蚀 C、Ⅲ附近开始时无明显现象 D、Ⅳ附近很快出现蓝色沉淀4. 用下列实验装置能达到相关实验目的的是( )
A、Ⅰ附近产生黄绿色气体 B、Ⅱ附近铁受保护而几乎不被腐蚀 C、Ⅲ附近开始时无明显现象 D、Ⅳ附近很快出现蓝色沉淀4. 用下列实验装置能达到相关实验目的的是( )A
B
C
D
实验装置
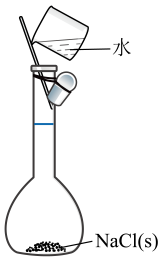
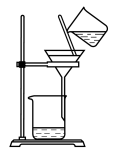
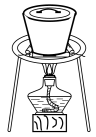
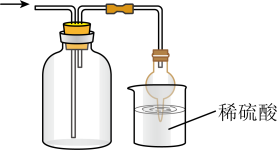
实验目的
配制0.1mol·L-1
NaCl溶液
除去Fe(OH)3胶体中的NaCl溶液
实验室灼烧干海带
收集NH3并吸收尾气
A、A B、B C、C D、D三、能力提升
-
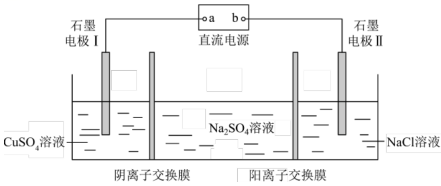
5. 根据下列图示得出的结论正确的是( )
 A、由图1可判断该反应的反应物中化学键的总键能大于生成物中化学键的总键能 B、图2装置能制备并能较长时间观察其颜色 C、图3装置中电流表指针发生明显偏转 D、由图4可证明图示条件下6. 海洋系统中氮循环的主要过程如图,图中虚线为缺氧条件,实线为富氧条件.已知大气中的能与臭氧发生反应,破坏臭氧层.下列叙述错误的是( )
A、由图1可判断该反应的反应物中化学键的总键能大于生成物中化学键的总键能 B、图2装置能制备并能较长时间观察其颜色 C、图3装置中电流表指针发生明显偏转 D、由图4可证明图示条件下6. 海洋系统中氮循环的主要过程如图,图中虚线为缺氧条件,实线为富氧条件.已知大气中的能与臭氧发生反应,破坏臭氧层.下列叙述错误的是( )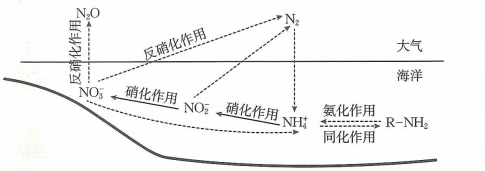 A、属于氮的固定 B、氨化作用中N元素化合价不变,反硝化作用中含氮物质被还原 C、海水富营养化可能促进向大气的释放,引起气候变化 D、在、、和中N原子的杂化方式相同7. 下列叙述正确的是( )。
A、属于氮的固定 B、氨化作用中N元素化合价不变,反硝化作用中含氮物质被还原 C、海水富营养化可能促进向大气的释放,引起气候变化 D、在、、和中N原子的杂化方式相同7. 下列叙述正确的是( )。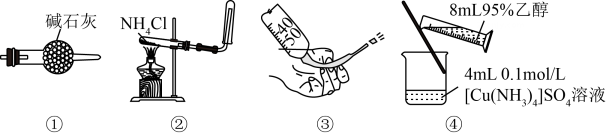 A、图①装置可用于干燥氯气 B、图②装置可用于制取氨气 C、图③操作可排出盛有溶液滴定管尖嘴内的气泡 D、图④装置可用于制备晶体8. 下列实验装置正确且能达到实验目的的是( )
A、图①装置可用于干燥氯气 B、图②装置可用于制取氨气 C、图③操作可排出盛有溶液滴定管尖嘴内的气泡 D、图④装置可用于制备晶体8. 下列实验装置正确且能达到实验目的的是( )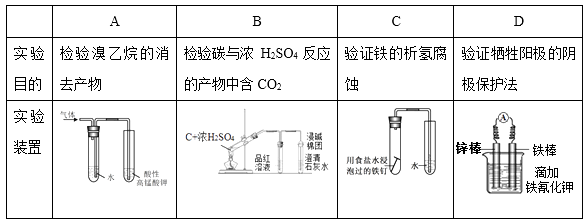 A、A B、B C、C D、D9. 如图所示,利用电化学原理可同时吸收处理和NO,下列说法正确的是( )。
A、A B、B C、C D、D9. 如图所示,利用电化学原理可同时吸收处理和NO,下列说法正确的是( )。
已知是一种弱酸,不考虑与水的反应及能量损耗。
A、b极为直流电源的负极 B、阳极区电极反应为 C、理论上,在相同条件下,该装置吸收的和NO的体积比为 D、电路中若有电子转移,则被吸收的气体体积为10. 下列实验能达到实验目的的是( )A
B
C
D
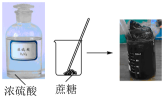

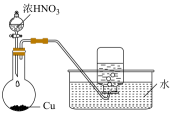
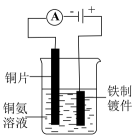
验证浓硫酸具有脱水性
配制100 mL一定物质的量浓度的溶液
制备并收集NO2
铁件镀铜
A、A B、B C、C D、D四、模拟演练
-
11. 下列实验装置及操作完全正确的是( )




A.测定锥形瓶中污水样品中c(OH-)
B.制备O2
C.验证牺牲阳极法保护铁
D.关闭a,打开b,可检查装置的气密性
A、A B、B C、C D、D12. 为探究新制氯水的性质,某学生做了如下实验。由上述实验可得新制氯水的性质与对应的解释或离子方程式不相符的是( )实验 装置 试剂a 现象 ① 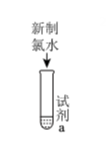
紫色的石蕊试液 溶液先变红后褪色 ② NaHCO3溶液 产生气泡 ③ HNO3酸化的AgNO3溶液 产生白色沉淀 ④ FeCl2溶液、KSCN溶液 溶液变红 A、实验①说明新制氯水中含有H+、HClO B、实验②发生的反应为+HClO=ClO-+CO2↑+H2O C、实验③说明新制氯水中有Cl- , Cl- +Ag+=AgCl↓ D、实验④说明氯气具有强氧化性,Cl2+2Fe2+=2Cl-+ 2Fe3+13. 下列实验装置使用不正确的是( )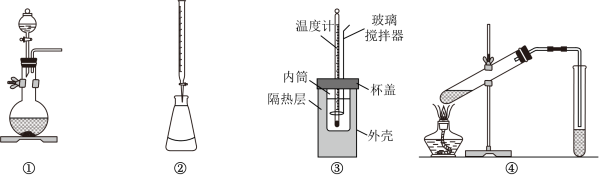 A、图①装置用于二氧化锰和浓盐酸反应制氯气 B、图②装置用于标准酸溶液滴定未知碱溶液 C、图③装置用于测定中和反应的反应热 D、图④装置用于制备乙酸乙酯14. 实验室进行制备和性质探究,下列实验原理和装置不能达到实验目的的是( )
A、图①装置用于二氧化锰和浓盐酸反应制氯气 B、图②装置用于标准酸溶液滴定未知碱溶液 C、图③装置用于测定中和反应的反应热 D、图④装置用于制备乙酸乙酯14. 实验室进行制备和性质探究,下列实验原理和装置不能达到实验目的的是( ) A、制备 B、探究溶解性 C、探究氧化性 D、吸收尾气15. 下列所示装置或操作能达到实验目的的是( )
A、制备 B、探究溶解性 C、探究氧化性 D、吸收尾气15. 下列所示装置或操作能达到实验目的的是( )A
B
C
D
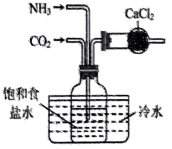
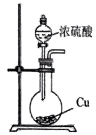
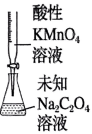
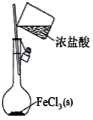
模拟侯氏制碱法获得
制备
测定未知溶液的浓度
配制溶液
A、A B、B C、C D、D
-