【备考2024年】从巩固到提高 高考化学二轮微专题35 氢键
试卷更新日期:2024-02-23 类型:二轮复习
一、选择题
-
1. 下列实验事实中,与氢键无关的是( )A、水结冰体积变大 B、的热稳定性比强 C、乙醇与水互溶 D、邻羟基苯甲醛的沸点低于对羟基苯甲醛2. 氢键对生命活动具有重要意义。DNA中四种碱基间的配对方式如下图(~代表糖苷键)。下列说法错误的是
 A、基态氧原子核外的电子有5种不同的空间运动状态 B、鸟嘌呤分子中2号N原子的杂化类型为sp2 C、所涉及的四种元素电负性大小关系: H<C<O<N D、氢键的强度较小,在DNA解旋和复制时容易断裂和形成3. 下列现象与氢键无关的是( )A、冰的密度小于液态水 B、的沸点高于 C、乙醇可以和水任意比互溶 D、HCl能以1:500的体积比溶于水4. 下列关于氢键的说法正确的是( )A、由于氢键的作用,、、的沸点反常,且沸点高低顺序为 B、氢键只能存在于分子间,不能存在于分子内 C、水在1000℃以上才会部分分解是因为水中含有大量的氢键 D、邻羟基苯甲醛的沸点低于对羟基苯甲醛的原因是前者不存在氢键5. 下列现象不能用氢键解释的是( )A、水分子高温下也很稳定 B、NH3容易液化 C、甲醇极易溶于水 D、液态氟化氢的化学式有时可以写成(HF)n的形式6. 关于氢键,下列说法正确的是( )A、分子中有N、O、F原子,分子间就存在氢键 B、因为氢键的缘故,
A、基态氧原子核外的电子有5种不同的空间运动状态 B、鸟嘌呤分子中2号N原子的杂化类型为sp2 C、所涉及的四种元素电负性大小关系: H<C<O<N D、氢键的强度较小,在DNA解旋和复制时容易断裂和形成3. 下列现象与氢键无关的是( )A、冰的密度小于液态水 B、的沸点高于 C、乙醇可以和水任意比互溶 D、HCl能以1:500的体积比溶于水4. 下列关于氢键的说法正确的是( )A、由于氢键的作用,、、的沸点反常,且沸点高低顺序为 B、氢键只能存在于分子间,不能存在于分子内 C、水在1000℃以上才会部分分解是因为水中含有大量的氢键 D、邻羟基苯甲醛的沸点低于对羟基苯甲醛的原因是前者不存在氢键5. 下列现象不能用氢键解释的是( )A、水分子高温下也很稳定 B、NH3容易液化 C、甲醇极易溶于水 D、液态氟化氢的化学式有时可以写成(HF)n的形式6. 关于氢键,下列说法正确的是( )A、分子中有N、O、F原子,分子间就存在氢键 B、因为氢键的缘故, 比
比 熔沸点低
C、极易溶于水,形成的溶液中存在的氢键类型有4种
D、“可燃冰”——甲烷水合物()中与之间存在氢键
7. 下列现象不能用氢键解释的是( )A、能溶于水 B、氨易液化,用作制冷剂 C、氢键使蛋白质成为具有生物活性的高级结构 D、邻羟基苯甲醛的沸点低于对羟基苯甲醛的沸点8. 氢键的存在对生命的繁衍具有重要意义。下列物质的结构或者性质与氢键无关的是( )A、乙醇可与水以任意比例互溶 B、S单质难溶于水,却易溶于CS2 C、邻羟基苯甲醛(
熔沸点低
C、极易溶于水,形成的溶液中存在的氢键类型有4种
D、“可燃冰”——甲烷水合物()中与之间存在氢键
7. 下列现象不能用氢键解释的是( )A、能溶于水 B、氨易液化,用作制冷剂 C、氢键使蛋白质成为具有生物活性的高级结构 D、邻羟基苯甲醛的沸点低于对羟基苯甲醛的沸点8. 氢键的存在对生命的繁衍具有重要意义。下列物质的结构或者性质与氢键无关的是( )A、乙醇可与水以任意比例互溶 B、S单质难溶于水,却易溶于CS2 C、邻羟基苯甲醛( )的熔点低于对羟基苯甲醛(
)的熔点低于对羟基苯甲醛( )的熔点
D、可燃冰(CH4·8H2O)中水分子笼的形成
9. 下列有关氢键的说法正确的是( )A、H2O比H2S稳定是因为水分子间能形成氢键 B、形成氢键的(X-H···Y)三原子一定在一条直线上 C、氢键能增大很多物质分子之间的作用力,导致沸点升高 D、可燃冰()中甲烷分子和水分子之间形成了氢键10. 下列事实与氢键无关的是( )A、的沸点比的沸点高 B、NaCl的熔点比CsCl的熔点高 C、比更易溶于水 D、邻羟基苯甲醛(
)的熔点
D、可燃冰(CH4·8H2O)中水分子笼的形成
9. 下列有关氢键的说法正确的是( )A、H2O比H2S稳定是因为水分子间能形成氢键 B、形成氢键的(X-H···Y)三原子一定在一条直线上 C、氢键能增大很多物质分子之间的作用力,导致沸点升高 D、可燃冰()中甲烷分子和水分子之间形成了氢键10. 下列事实与氢键无关的是( )A、的沸点比的沸点高 B、NaCl的熔点比CsCl的熔点高 C、比更易溶于水 D、邻羟基苯甲醛(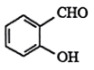 )的沸点比对羟基苯甲醛(
)的沸点比对羟基苯甲醛(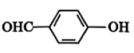 )的低
11. 下列事实与氢键无关的是( )A、水结成冰后能浮在水面上 B、常温下,互为同分异构体的乙醇与甲醚的状态不同 C、CH4、SiH4、GeH4、SnH4的熔点随相对分子质量的增大而升高 D、HF、HCl、HBr、HI各自的水溶液中,只有HF的水溶液为弱酸12. 下列物质的性质或相关数据与氢键无关的是( )A、氨气极易溶于水 B、邻羟基苯甲酸(
)的低
11. 下列事实与氢键无关的是( )A、水结成冰后能浮在水面上 B、常温下,互为同分异构体的乙醇与甲醚的状态不同 C、CH4、SiH4、GeH4、SnH4的熔点随相对分子质量的增大而升高 D、HF、HCl、HBr、HI各自的水溶液中,只有HF的水溶液为弱酸12. 下列物质的性质或相关数据与氢键无关的是( )A、氨气极易溶于水 B、邻羟基苯甲酸( )的熔点为159℃,对羟基苯甲酸(
)的熔点为159℃,对羟基苯甲酸( )的熔点为213℃
C、二甲醚微溶于水,而乙醇可与水以任意比例混溶
D、分解时吸收的热量比分解时吸收的热量多
13. 下列现象与氢键无关的是( )A、的熔、沸点比第VA族其他元素氢化物的高 B、小分子的醇可以和水以任意比互溶 C、冰的密度比液态水的密度小 D、水分子高温下很稳定14. 下列事实与氢键有关的是( )A、水加热到很高的温度都难以分解 B、分子间形成氢键能使物质的熔点和沸点升高 C、CH4、SiH4、 GeH4、 SnH4 的熔点随相对分子质量的增大而升高 D、HCl的稳定性强于HBr15. 下列现象与氢键有关的是( )
)的熔点为213℃
C、二甲醚微溶于水,而乙醇可与水以任意比例混溶
D、分解时吸收的热量比分解时吸收的热量多
13. 下列现象与氢键无关的是( )A、的熔、沸点比第VA族其他元素氢化物的高 B、小分子的醇可以和水以任意比互溶 C、冰的密度比液态水的密度小 D、水分子高温下很稳定14. 下列事实与氢键有关的是( )A、水加热到很高的温度都难以分解 B、分子间形成氢键能使物质的熔点和沸点升高 C、CH4、SiH4、 GeH4、 SnH4 的熔点随相对分子质量的增大而升高 D、HCl的稳定性强于HBr15. 下列现象与氢键有关的是( )①NH3的熔沸点比PH3的高②乙醇可以和水以任意比例互溶③冰的密度比液态水的密度小④水分子在高温下很稳定
A、①②③④ B、①②③ C、①③ D、①②16. 关于氢键,下列说法正确的是( )A、分子中有N、O、F原子,分子间就存在氢键 B、因为氢键的缘故, 熔沸点高
C、NH3的稳定性很强,是因为其分子间能形成氢键
D、“可燃冰” 甲烷水合物(CH4·8H2O)中CH4与H2O之间存在氢键
17. 下列现象与氢键无关的是( )A、的熔沸点比的高 B、水分子高温也很稳定 C、易溶于水 D、乙醇可以和水以任意比互溶18. 下列事实不可以用氢键来解释的是( )A、水是一种非常稳定的化合物 B、在测量氟化氢相对分子质量的实验中,发现实验值总是大于20 C、水结成冰后,体积膨胀,密度变小 D、氨气容易液化19. 关于氢键,下列说法正确的是( )A、分子中有N、O、F原子,分子间就存在氢键 B、因为氢键的缘故,
熔沸点高
C、NH3的稳定性很强,是因为其分子间能形成氢键
D、“可燃冰” 甲烷水合物(CH4·8H2O)中CH4与H2O之间存在氢键
17. 下列现象与氢键无关的是( )A、的熔沸点比的高 B、水分子高温也很稳定 C、易溶于水 D、乙醇可以和水以任意比互溶18. 下列事实不可以用氢键来解释的是( )A、水是一种非常稳定的化合物 B、在测量氟化氢相对分子质量的实验中,发现实验值总是大于20 C、水结成冰后,体积膨胀,密度变小 D、氨气容易液化19. 关于氢键,下列说法正确的是( )A、分子中有N、O、F原子,分子间就存在氢键 B、因为氢键的缘故, 比
比 熔、沸点高
C、由于氢键比范德华力强,所以H2O分子比H2S分子稳定
D、“可燃冰”——烷水合物(例如:8CH4·46H2O)中CH4与H2O之间存在氢键
20. 下列变化或数据与氢键无关的是( )A、甲酸蒸气的密度在373K时为1.335g·L-1 , 在293K时为2.5 g·L-1 B、氨分子与水分子形成一水合氨 C、水结冰体积增大。 D、SbH3的沸点比PH3高21. 下列事实,不能用氢键知识解释的是( )A、水和乙醇可以完全互溶 B、氨容易液化 C、干冰易升华 D、液态氟化氢化学式有时写成(HF)n 的形式
熔、沸点高
C、由于氢键比范德华力强,所以H2O分子比H2S分子稳定
D、“可燃冰”——烷水合物(例如:8CH4·46H2O)中CH4与H2O之间存在氢键
20. 下列变化或数据与氢键无关的是( )A、甲酸蒸气的密度在373K时为1.335g·L-1 , 在293K时为2.5 g·L-1 B、氨分子与水分子形成一水合氨 C、水结冰体积增大。 D、SbH3的沸点比PH3高21. 下列事实,不能用氢键知识解释的是( )A、水和乙醇可以完全互溶 B、氨容易液化 C、干冰易升华 D、液态氟化氢化学式有时写成(HF)n 的形式