【备考2024年】从巩固到提高 高考化学二轮微专题25 中和滴定曲线
试卷更新日期:2024-02-23 类型:二轮复习
一、选择题
-
1. 溶液滴定溶液时,、各含磷元素微粒的和的关系如图。下列说法中正确的是( )
 A、①为的与的关系 B、b点时,溶液中 C、的 D、d点时,溶液中存在着2. 25℃时,向NaHCO3溶液中滴入盐酸,混合溶液的pH与离子浓度变化的关系如图所示。下列叙述正确的是( )
A、①为的与的关系 B、b点时,溶液中 C、的 D、d点时,溶液中存在着2. 25℃时,向NaHCO3溶液中滴入盐酸,混合溶液的pH与离子浓度变化的关系如图所示。下列叙述正确的是( ) A、图中a=2.6 B、25℃时,HCO3-+H2OH2CO3+OH-的Kh=1.0×10-6.4 C、M点溶液中: D、若要表示题目条件下pH与lg的变化关系.则曲线应该在平行于曲线的下方3. 已知草酸()为二元弱酸,在室温下,向一定浓度的草酸溶液中逐滴加入一定浓度的KOH溶液,溶液中、、三种微粒分别在三者中所占的物质的量分数()与溶液pH的关系如图所示。下列说法中正确的是( )
A、图中a=2.6 B、25℃时,HCO3-+H2OH2CO3+OH-的Kh=1.0×10-6.4 C、M点溶液中: D、若要表示题目条件下pH与lg的变化关系.则曲线应该在平行于曲线的下方3. 已知草酸()为二元弱酸,在室温下,向一定浓度的草酸溶液中逐滴加入一定浓度的KOH溶液,溶液中、、三种微粒分别在三者中所占的物质的量分数()与溶液pH的关系如图所示。下列说法中正确的是( ) A、室温时,的水解平衡常数 B、当溶液时, C、当溶液时, D、A点溶液加水稀释,则水的电离程度减小4. 将溶液滴加到己二酸溶液中,混合溶液的与离子浓度变化的关系如图所示。下列叙述错误的是( )
A、室温时,的水解平衡常数 B、当溶液时, C、当溶液时, D、A点溶液加水稀释,则水的电离程度减小4. 将溶液滴加到己二酸溶液中,混合溶液的与离子浓度变化的关系如图所示。下列叙述错误的是( )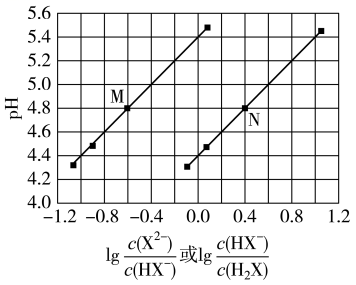 A、当混合溶液呈中性时, B、曲线表示与的变化关系 C、溶液中 D、的数量级为5. 时,用盐酸滴定氨水的图像如图所示,下列说法正确的是( )
A、当混合溶液呈中性时, B、曲线表示与的变化关系 C、溶液中 D、的数量级为5. 时,用盐酸滴定氨水的图像如图所示,下列说法正确的是( ) A、点时: B、水的电离程度: C、滴定过程中,减小 D、、、、均有6. 25℃时,用0.1000mol/L NaOH溶液滴定20.00mL 0.1000mol/L CH3COOH溶液所得滴定曲线如图.下列叙述正确的是( )
A、点时: B、水的电离程度: C、滴定过程中,减小 D、、、、均有6. 25℃时,用0.1000mol/L NaOH溶液滴定20.00mL 0.1000mol/L CH3COOH溶液所得滴定曲线如图.下列叙述正确的是( ) A、点①所示溶液:c(CH3COO﹣)+c(CH3COOH)=c(Na+) B、点②所示溶液:c(Na+)=c(CH3COO﹣)>c(H+)=c(OH﹣) C、点③所示溶液:c(Na+)>c(OH﹣)>c(CH3COO﹣)>c(H+) D、滴定终点时:c(CH3COOH)+c(CH3COO﹣)=c(Na+)7. 常温下,向某浓度的溶液中逐滴加入已知浓度的NaOH溶液,若pC表示溶液中溶质微粒的物质的量浓度的负对数,则所得溶液中、、与溶液pH的变化关系如图所示。已知: ; 。则下列说法正确的是( )
A、点①所示溶液:c(CH3COO﹣)+c(CH3COOH)=c(Na+) B、点②所示溶液:c(Na+)=c(CH3COO﹣)>c(H+)=c(OH﹣) C、点③所示溶液:c(Na+)>c(OH﹣)>c(CH3COO﹣)>c(H+) D、滴定终点时:c(CH3COOH)+c(CH3COO﹣)=c(Na+)7. 常温下,向某浓度的溶液中逐滴加入已知浓度的NaOH溶液,若pC表示溶液中溶质微粒的物质的量浓度的负对数,则所得溶液中、、与溶液pH的变化关系如图所示。已知: ; 。则下列说法正确的是( )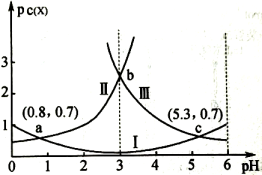 A、当pH=3时,溶液中 B、常温下,的数量级为 C、常温下,NaHA溶液呈碱性 D、常温下随着pH的增大,的值不变8. 常温下,在10mL 0.1 MOH溶液中滴加pH=1的盐酸,溶液AG()与盐酸体积(V)之间的关系如图所示,下列说法不正确的是( )
A、当pH=3时,溶液中 B、常温下,的数量级为 C、常温下,NaHA溶液呈碱性 D、常温下随着pH的增大,的值不变8. 常温下,在10mL 0.1 MOH溶液中滴加pH=1的盐酸,溶液AG()与盐酸体积(V)之间的关系如图所示,下列说法不正确的是( )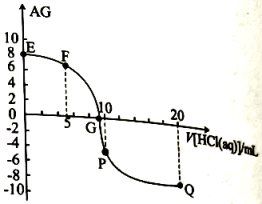 A、常温下,MOH的电离常数约为 B、F点溶液中: C、滴加盐酸过程中,水的电离程度:P点最大 D、Q点溶液中:9. 常温下,将等浓度NaOH溶液分别滴加到pH相同、等体积的HBrO溶液、溶液中,溶液的pH与粒子浓度比值的对数关系如图所示,已知、 , 下列说法正确的是( )
A、常温下,MOH的电离常数约为 B、F点溶液中: C、滴加盐酸过程中,水的电离程度:P点最大 D、Q点溶液中:9. 常温下,将等浓度NaOH溶液分别滴加到pH相同、等体积的HBrO溶液、溶液中,溶液的pH与粒子浓度比值的对数关系如图所示,已知、 , 下列说法正确的是( ) A、a点溶液中 B、向HBrO溶液中滴加NaOH溶液至 , C、N表示溶液的pH与的变化关系 D、b点,溶液中由水电离出的约为mol/L10. 常温下,向0.1mol·L1H3PO4溶液中加入NaOH的过程中各微粒的物质的量分数(δ)随pH的变化关系如图所示(H3PO4的三级电离常数依次为Ka1、Ka2、Ka3)。下列叙述错误的是( )
A、a点溶液中 B、向HBrO溶液中滴加NaOH溶液至 , C、N表示溶液的pH与的变化关系 D、b点,溶液中由水电离出的约为mol/L10. 常温下,向0.1mol·L1H3PO4溶液中加入NaOH的过程中各微粒的物质的量分数(δ)随pH的变化关系如图所示(H3PO4的三级电离常数依次为Ka1、Ka2、Ka3)。下列叙述错误的是( ) A、Ka2=10-7.2 , HPO42-的水解平衡常数为10-6.8 B、为获得尽可能纯的NaH2PO4 , pH应控制在4~5 C、反应H2PO4-+H2O
A、Ka2=10-7.2 , HPO42-的水解平衡常数为10-6.8 B、为获得尽可能纯的NaH2PO4 , pH应控制在4~5 C、反应H2PO4-+H2O H3PO4+OH- 的K=10-11.9
D、Na2HPO4溶液中存在c(OH-)+c(PO43-)=c(H+)+c(H2PO4-)+c(H3PO4)
11. 常温下,以酚酞为指示剂,用的NaOH溶液滴定20.00mL的二元酸溶液.溶液中pH、含A微粒分布系数(物质的量分数)随滴加NaOH溶液体积的变化关系如图所示
H3PO4+OH- 的K=10-11.9
D、Na2HPO4溶液中存在c(OH-)+c(PO43-)=c(H+)+c(H2PO4-)+c(H3PO4)
11. 常温下,以酚酞为指示剂,用的NaOH溶液滴定20.00mL的二元酸溶液.溶液中pH、含A微粒分布系数(物质的量分数)随滴加NaOH溶液体积的变化关系如图所示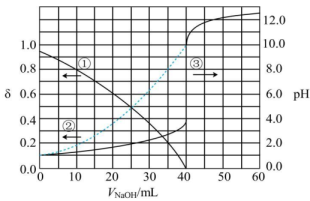
下列说法中正确的是( )
A、在水中电离的方程式为: , B、当溶液时,溶液中离子浓度大小顺序为: C、常温下,的电离平衡常数为 D、当溶液时,12. 常温下,用溶液滴定(二元弱酸)溶液所得滴定曲线如图(混合溶液的体积可看成混合前溶液的体积之和).下列说法正确的是( )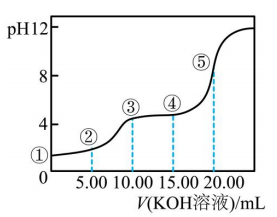 A、点①所示溶液中: B、点②所示溶液中: C、点③所示溶液中: D、点④所示溶液中:13. 常温下,向三元酸溶液中滴加的溶液,溶液中含A微粒的物质的量分数随溶液的变化如图所示,下列说法正确的是( )
A、点①所示溶液中: B、点②所示溶液中: C、点③所示溶液中: D、点④所示溶液中:13. 常温下,向三元酸溶液中滴加的溶液,溶液中含A微粒的物质的量分数随溶液的变化如图所示,下列说法正确的是( )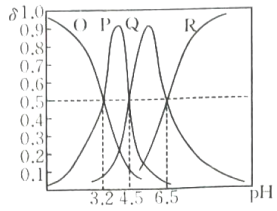 A、P为的物质的量分数与溶液的关系曲线 B、该三元酸的第一步电离是完全的 C、常温下,的水解常数 D、当加入溶液时,溶液显酸性14. 常温下,向一定体积0.2的溶液中逐滴滴入0.2的稀盐酸。溶液中水电离出的氢离子浓度的负对数[用表示,]与加入盐酸体积的关系如图所示。忽略溶液混合时体积变化和温度变化,已知 , 下列叙述错误的是( )
A、P为的物质的量分数与溶液的关系曲线 B、该三元酸的第一步电离是完全的 C、常温下,的水解常数 D、当加入溶液时,溶液显酸性14. 常温下,向一定体积0.2的溶液中逐滴滴入0.2的稀盐酸。溶液中水电离出的氢离子浓度的负对数[用表示,]与加入盐酸体积的关系如图所示。忽略溶液混合时体积变化和温度变化,已知 , 下列叙述错误的是( ) A、的 B、c点溶液中水电离出的 C、b~c点间溶液中: D、d点溶液中:15. 分析化学中“滴定分数”的定义为:所加滴定剂与被滴定组分的物质的量之比。常温下以0.10mol·L-1的HCl溶液滴定同浓度某一元碱MOH溶液并绘制滴定曲线如图所示。下列说法不正确的是( )
A、的 B、c点溶液中水电离出的 C、b~c点间溶液中: D、d点溶液中:15. 分析化学中“滴定分数”的定义为:所加滴定剂与被滴定组分的物质的量之比。常温下以0.10mol·L-1的HCl溶液滴定同浓度某一元碱MOH溶液并绘制滴定曲线如图所示。下列说法不正确的是( ) A、该酸碱中和滴定过程应该选用甲基橙做指示剂 B、从x点到z点的整个过程中,y点的水的电离程度最大 C、x点处的溶液中满足:c(MOH)+c(OH-)<c(M+)+c(H+) D、根据y点坐标可以算得Kb(MOH)=9×10-716. 25℃时,用盐酸滴定氨水的滴定曲线如图所示(已知:滴定剂与被滴定组分的物质的量之比为滴定分数)。下列说法错误的是( )
A、该酸碱中和滴定过程应该选用甲基橙做指示剂 B、从x点到z点的整个过程中,y点的水的电离程度最大 C、x点处的溶液中满足:c(MOH)+c(OH-)<c(M+)+c(H+) D、根据y点坐标可以算得Kb(MOH)=9×10-716. 25℃时,用盐酸滴定氨水的滴定曲线如图所示(已知:滴定剂与被滴定组分的物质的量之比为滴定分数)。下列说法错误的是( ) A、a点溶液中水电离出的小于 B、温度升高,c点溶液的pH减小 C、滴定过程,溶液中不变 D、25℃时,的数量级为17. 四氯金酸()由王水和纯金反应制得,可用于工业元件的镀金。常温时,用0.1mol/L的NaOH溶液滴定20mL0.1mol/L的溶液,滴定过程中测得混合溶液的温度T、NaOH溶液体积V(NaOH)与pH的关系如图所示。下列叙述错误的是( )
A、a点溶液中水电离出的小于 B、温度升高,c点溶液的pH减小 C、滴定过程,溶液中不变 D、25℃时,的数量级为17. 四氯金酸()由王水和纯金反应制得,可用于工业元件的镀金。常温时,用0.1mol/L的NaOH溶液滴定20mL0.1mol/L的溶液,滴定过程中测得混合溶液的温度T、NaOH溶液体积V(NaOH)与pH的关系如图所示。下列叙述错误的是( ) A、常温时,四氯金酸()的电离平衡常数约为 B、n点溶液中, C、p、n、q三点对应的水解平衡常数: D、p点对应的溶液中,18. 乙二酸(用H2A表示)为二元弱酸。25℃时,向0.1mol·L-1NH4HA溶液中滴加适量的0.1mol/L盐酸或0.1mol/LNaOH溶液,溶液中各含氮(或A)微粒的分布分数δ与溶液pH的关系如图所示(不考虑溶液中NH3分子)。例如,溶液中H2A的分布分数。下列说法不正确的是( )
A、常温时,四氯金酸()的电离平衡常数约为 B、n点溶液中, C、p、n、q三点对应的水解平衡常数: D、p点对应的溶液中,18. 乙二酸(用H2A表示)为二元弱酸。25℃时,向0.1mol·L-1NH4HA溶液中滴加适量的0.1mol/L盐酸或0.1mol/LNaOH溶液,溶液中各含氮(或A)微粒的分布分数δ与溶液pH的关系如图所示(不考虑溶液中NH3分子)。例如,溶液中H2A的分布分数。下列说法不正确的是( )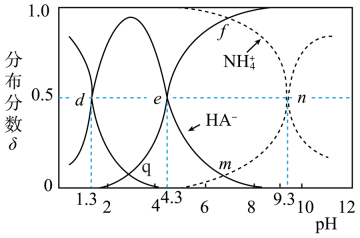 A、溶液pH=8时,存在:c(A2-)>c(NH)>(NH3·H2O)>c(HA-) B、NH4HA溶液中:c(HA-)>c(NH)>c(H+)>c(OH-) C、n点溶液中存在:c(Na+)+c(H2A)+c(HA-)+c(A2-)=0.1mol·L-1 D、2HA-=H2A+A2-的平衡常数K=10-3.019. 常温下,向20 mL 0.2 mol/L H2A溶液中滴加0.2 mol/L NaOH溶液。有关微粒的物质的量变化如下图,根据下图图示判断,下列说法正确的是( )
A、溶液pH=8时,存在:c(A2-)>c(NH)>(NH3·H2O)>c(HA-) B、NH4HA溶液中:c(HA-)>c(NH)>c(H+)>c(OH-) C、n点溶液中存在:c(Na+)+c(H2A)+c(HA-)+c(A2-)=0.1mol·L-1 D、2HA-=H2A+A2-的平衡常数K=10-3.019. 常温下,向20 mL 0.2 mol/L H2A溶液中滴加0.2 mol/L NaOH溶液。有关微粒的物质的量变化如下图,根据下图图示判断,下列说法正确的是( ) A、当V(NaOH溶液)=40 mL时,溶液中离子浓度大小关系:
A、当V(NaOH溶液)=40 mL时,溶液中离子浓度大小关系:c(Na+)>c(A2-)>c(HA-)>c(OH-)>c(H+)
B、NaHA溶液中:c(OH-) + c(A2-) = c(H+) + c(H2A) C、当V((NaOH溶液)=40 mL时,其溶液中水的电离程度比纯水小 D、当V((NaOH溶液)=20 mL时,NaHA水解程度大于电离程度20. 25℃时,等体积两种一元酸HA和HB分别用等浓度的溶液滴定,滴定曲线如图所示。下列说法正确的是( )。 A、酸性:HA<HB B、酸HB的电离度约为0.5% C、起始浓度: , D、用溶液滴定HB可用甲基橙作指示剂21. 已知常温时CH3COOH的电离平衡常数为Ka,该温度下向20mL0.1 mol/L CH3COOH溶液中逐滴加入0.1 mol/L NaOH溶液,其pH变化曲线如图所示(忽略温度变化)。下列说法不正确的是( )
A、酸性:HA<HB B、酸HB的电离度约为0.5% C、起始浓度: , D、用溶液滴定HB可用甲基橙作指示剂21. 已知常温时CH3COOH的电离平衡常数为Ka,该温度下向20mL0.1 mol/L CH3COOH溶液中逐滴加入0.1 mol/L NaOH溶液,其pH变化曲线如图所示(忽略温度变化)。下列说法不正确的是( ) A、d点表示的溶液中c(OH-)>c(H+) B、该滴定实验可以用紫色石蕊试液做指示剂 C、由图可知0.1 mol/L CH3COOH溶液pH=3 D、b、c点表示的溶液中的值相等22. 草酸为二元弱酸,其电离过程为: , 。常温下向溶液中逐滴加入溶液,混合溶液中和的物质的量分数(随变化关系如图所示:
A、d点表示的溶液中c(OH-)>c(H+) B、该滴定实验可以用紫色石蕊试液做指示剂 C、由图可知0.1 mol/L CH3COOH溶液pH=3 D、b、c点表示的溶液中的值相等22. 草酸为二元弱酸,其电离过程为: , 。常温下向溶液中逐滴加入溶液,混合溶液中和的物质的量分数(随变化关系如图所示:
下列说法正确的是( )
A、草酸的一级电离平衡常数的数量级为 B、曲线Ⅰ表示的物质的量分数 C、当加入溶液的体积为时,溶液中存在如下关系: D、时,对应的溶液中存在关系:23. 已知。室温下,向一元弱酸HX溶液中逐滴滴加溶液,溶液的随的变化关系如图所示。下列说法正确的是( ) A、当时,溶液中 B、当时,加入的溶液体积大于 C、当加入溶液时,溶液中 D、a、b、c三点对应溶液中水电离出来的浓度:a点>b点>c点24. 室温下,用0.100mol/L NaOH溶液滴定20.00 mL 溶液。滴定过程中含A微粒的分布分数()和pH随NaOH溶液体积变化如图所示。下列说法正确的是( )
A、当时,溶液中 B、当时,加入的溶液体积大于 C、当加入溶液时,溶液中 D、a、b、c三点对应溶液中水电离出来的浓度:a点>b点>c点24. 室温下,用0.100mol/L NaOH溶液滴定20.00 mL 溶液。滴定过程中含A微粒的分布分数()和pH随NaOH溶液体积变化如图所示。下列说法正确的是( )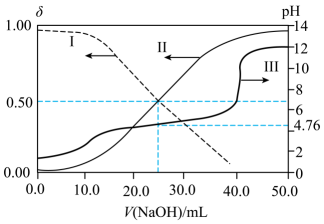 A、原溶液的物质的量浓度为0.125mol/L B、pH=7时, C、加入NaOH溶液越多,越高,水的电离程度越大 D、25. 常温下,用0.1mol·L-1HCl溶液滴定0.1mol·L-1 NH3·H2O溶液,滴定曲线如图a所示,混合溶液的pH与离子浓度变化的关系如图b所示。下列说法不正确的是( )
A、原溶液的物质的量浓度为0.125mol/L B、pH=7时, C、加入NaOH溶液越多,越高,水的电离程度越大 D、25. 常温下,用0.1mol·L-1HCl溶液滴定0.1mol·L-1 NH3·H2O溶液,滴定曲线如图a所示,混合溶液的pH与离子浓度变化的关系如图b所示。下列说法不正确的是( )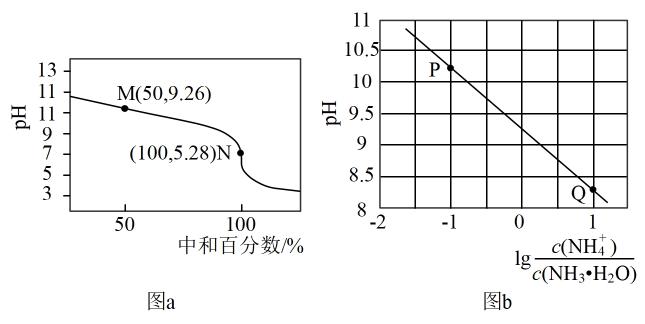 A、Kb(NH3·H2O)的数量级为10-5 B、P到Q过程中,水的电离程度逐渐增大 C、当滴定至溶液呈中性时,c(NH4+)>c(NH3·H2O) D、N点,c(Cl- ) - c(NH4+)=26. 常温时,用溶液滴定二元酸溶液,溶液中含A微粒的分布系数随pH的变化关系如图所示,[如的分布系数:]。下列说法错误的是( )
A、Kb(NH3·H2O)的数量级为10-5 B、P到Q过程中,水的电离程度逐渐增大 C、当滴定至溶液呈中性时,c(NH4+)>c(NH3·H2O) D、N点,c(Cl- ) - c(NH4+)=26. 常温时,用溶液滴定二元酸溶液,溶液中含A微粒的分布系数随pH的变化关系如图所示,[如的分布系数:]。下列说法错误的是( )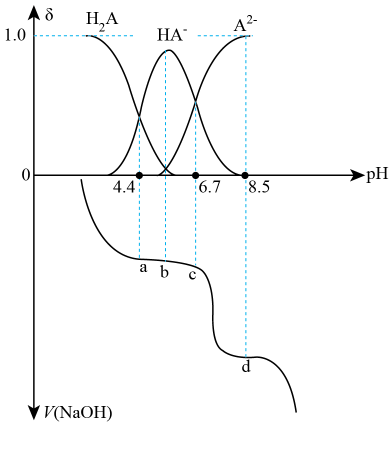 A、第二次突变时,可选用酚酞作指示剂 B、溶液中存在: C、c点存在: D、的平衡常数27. 向某浓度的亚磷酸中滴加NaOH溶液,其pH与溶液中各种含磷微粒的物质的量分数的变化如图所示。下列说法错误的是( )
A、第二次突变时,可选用酚酞作指示剂 B、溶液中存在: C、c点存在: D、的平衡常数27. 向某浓度的亚磷酸中滴加NaOH溶液,其pH与溶液中各种含磷微粒的物质的量分数的变化如图所示。下列说法错误的是( )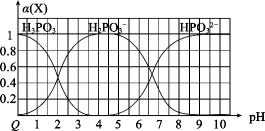 A、H3PO3是二元弱酸 B、该温度下,H3PO3的Ka1=1.0×10-2 C、NaH2PO3溶液显碱性 D、以酚酞为指示剂,当溶液由无色变为浅红色时,发生主要反应的离子方程式为:H2PO+OH-=H2O+HPO28. 常温下,用的盐酸分别滴定20.00mL浓度均为的三种一元弱酸的钠盐(NaX、NaY、NaZ)溶液,滴定曲线如图所示。下列判断错误的是( )
A、H3PO3是二元弱酸 B、该温度下,H3PO3的Ka1=1.0×10-2 C、NaH2PO3溶液显碱性 D、以酚酞为指示剂,当溶液由无色变为浅红色时,发生主要反应的离子方程式为:H2PO+OH-=H2O+HPO28. 常温下,用的盐酸分别滴定20.00mL浓度均为的三种一元弱酸的钠盐(NaX、NaY、NaZ)溶液,滴定曲线如图所示。下列判断错误的是( ) A、的NaX溶液中: B、三种一元弱酸的电离常数: C、当时,三种溶液中: D、分别滴加20.00mL盐酸后,再将三种溶液混合:29. 已知;常温下,用溶液分别滴定浓度均为的溶液和溶液,所得滴定曲线如下图所示,用代表或 , 用代表或 , 下列说法正确的是( )
A、的NaX溶液中: B、三种一元弱酸的电离常数: C、当时,三种溶液中: D、分别滴加20.00mL盐酸后,再将三种溶液混合:29. 已知;常温下,用溶液分别滴定浓度均为的溶液和溶液,所得滴定曲线如下图所示,用代表或 , 用代表或 , 下列说法正确的是( )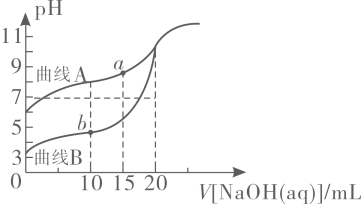 A、曲线表示溶液滴定溶液的滴定曲线 B、点存在 C、点存在 D、若两份溶液滴定都采用甲基橙作为指示剂,则滴定终点消耗氢氧化钠溶液的体积均偏大30. 常温下,用0.10 mol·L-1 NaOH溶液分别滴定20.00 mL浓度均为0.10 mol·L-1 HA溶液和HB溶液,所得滴定曲线如图所示(其中HA的滴定曲线部分未画出)。下列说法错误的是( )
A、曲线表示溶液滴定溶液的滴定曲线 B、点存在 C、点存在 D、若两份溶液滴定都采用甲基橙作为指示剂,则滴定终点消耗氢氧化钠溶液的体积均偏大30. 常温下,用0.10 mol·L-1 NaOH溶液分别滴定20.00 mL浓度均为0.10 mol·L-1 HA溶液和HB溶液,所得滴定曲线如图所示(其中HA的滴定曲线部分未画出)。下列说法错误的是( )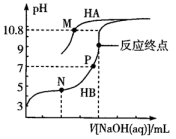
已知:M点溶液中c(A-)=c(HA)
A、=105.8 B、P点溶液中溶质为NaB和HB,由水电离出的c(H+)=1.0×10-7 mol·L-1 C、M点溶液中,2c(Na+)>c(HA)+c(A-) D、等体积等浓度的HB溶液和NaA溶液混合后的溶液中:c(OH-)<c(H+)31. 25℃时,往20.00mL0.1mol/LHA溶液中滴入0.1mol/LNaOH溶液,体系中-lgc(HA)、-lgc(A-)、NaOH溶液的体积与溶液pH的关系如图所示。下列说法不正确的是( ) A、曲线①表示-lgc(HA)与溶液pH的关系 B、a点对应的溶液中:2c(H+)+c(HA)=2c(OH-)+c(A-) C、b点对应的溶液中:c(Na+)>c(A-)>c(OH-)>c(H+) D、25℃时,HA的电离平衡常数的数量级为10-432. 室温下,向20 mL 0.05 mol/L的H2X溶液中逐滴加入0.1 mol/L的NaOH溶液,溶液pH随着NaOH溶液体积变化的关系如图所示。下列叙述错误的是( )
A、曲线①表示-lgc(HA)与溶液pH的关系 B、a点对应的溶液中:2c(H+)+c(HA)=2c(OH-)+c(A-) C、b点对应的溶液中:c(Na+)>c(A-)>c(OH-)>c(H+) D、25℃时,HA的电离平衡常数的数量级为10-432. 室温下,向20 mL 0.05 mol/L的H2X溶液中逐滴加入0.1 mol/L的NaOH溶液,溶液pH随着NaOH溶液体积变化的关系如图所示。下列叙述错误的是( )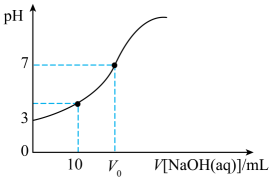 A、 mL时,溶液中 B、随着NaOH溶液的不断加入,水的电离程度先增大后减小 C、室温下,的电离常数 D、时, mL,溶液中
A、 mL时,溶液中 B、随着NaOH溶液的不断加入,水的电离程度先增大后减小 C、室温下,的电离常数 D、时, mL,溶液中