内蒙古巴彦淖尔市杭锦后旗2023-2024学年九年级上学期期末化学试题
试卷更新日期:2024-02-22 类型:期末考试
一、单选题
-
1. 正确的实验操作对人身安全和实验结果都非常重要。下列实验基本操作正确的是( )A、
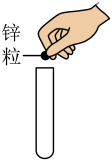 往试管中加入锌粒
B、
往试管中加入锌粒
B、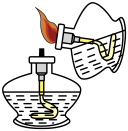 点燃酒精灯
C、
点燃酒精灯
C、 闻气味
D、
闻气味
D、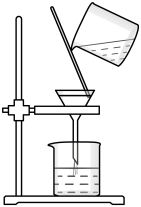 过滤
2. 下列说法正确的是A、海绵能吸水说明分子间有间隔 B、鱼类能在水中生存,是因为水中含有氧原子 C、蜡烛燃烧生成二氧化碳和水说明蜡烛中一定含有碳元素和氧元素 D、金、银等金属化学性质不活泼,在自然界中以单质形式存在3. 规范使用化学用语是学好化学的基础。下列化学用语书写正确的一组是( )
过滤
2. 下列说法正确的是A、海绵能吸水说明分子间有间隔 B、鱼类能在水中生存,是因为水中含有氧原子 C、蜡烛燃烧生成二氧化碳和水说明蜡烛中一定含有碳元素和氧元素 D、金、银等金属化学性质不活泼,在自然界中以单质形式存在3. 规范使用化学用语是学好化学的基础。下列化学用语书写正确的一组是( )①硫酸铁:FeSO4②磷元素:P ③2个氖分子:2Ne2④3个钙离子:3Ca2+
⑤钠原子结构示意图:Na
 ⑥氧化铜中铜元素显+2价:A、①⑤⑥ B、②④⑤ C、①④⑥ D、②③⑤4. 为验证Fe、Cu、Ag三种金属活动性顺序,现提供Fe、Cu、Ag、稀硫酸、FeSO4溶液、CuSO4溶液、AgNO3溶液等七种试剂,相关说法正确的是( )A、AgNO3溶液是不可或缺的试剂 B、据现有试剂最多可以设计两种实验方案 C、为达成实验目的,最少要选择三种试剂 D、只提供Fe、Cu、稀硫酸、FeSO4溶液即可实现实验目的5. 现将20克A和足量B混合加热,A与B发生化学反应,20克A完全反应后生成16克C和8克D,则参加反应的B与生成的C的质量比是A、1∶4 B、5∶4 C、2∶1 D、1:26. 下列劳动实践中涉及化学变化的是A、实践体验:体验葡萄酿酒的操作流程 B、学农活动:用锄头挖农场里的红薯 C、社会实践:和手工艺人学习竹编 D、社区服务:用铲子铲去墙上的污垢7. 甲物质燃烧反应过程的微观示意图如下。下列说法正确的是
⑥氧化铜中铜元素显+2价:A、①⑤⑥ B、②④⑤ C、①④⑥ D、②③⑤4. 为验证Fe、Cu、Ag三种金属活动性顺序,现提供Fe、Cu、Ag、稀硫酸、FeSO4溶液、CuSO4溶液、AgNO3溶液等七种试剂,相关说法正确的是( )A、AgNO3溶液是不可或缺的试剂 B、据现有试剂最多可以设计两种实验方案 C、为达成实验目的,最少要选择三种试剂 D、只提供Fe、Cu、稀硫酸、FeSO4溶液即可实现实验目的5. 现将20克A和足量B混合加热,A与B发生化学反应,20克A完全反应后生成16克C和8克D,则参加反应的B与生成的C的质量比是A、1∶4 B、5∶4 C、2∶1 D、1:26. 下列劳动实践中涉及化学变化的是A、实践体验:体验葡萄酿酒的操作流程 B、学农活动:用锄头挖农场里的红薯 C、社会实践:和手工艺人学习竹编 D、社区服务:用铲子铲去墙上的污垢7. 甲物质燃烧反应过程的微观示意图如下。下列说法正确的是 A、该反应中含两种单质 B、该反应前后原子数目改变 C、该反应前后元素种类改变 D、参加反应的甲和乙分子个数比为1∶58. 有元素化合价均为价的、两种金属。取等质量的、分别与足量盐酸反应时,产生氢气的质量与反应时间的函数关系如图所示。从图示说明的函数关系,可得出的结论是( )
A、该反应中含两种单质 B、该反应前后原子数目改变 C、该反应前后元素种类改变 D、参加反应的甲和乙分子个数比为1∶58. 有元素化合价均为价的、两种金属。取等质量的、分别与足量盐酸反应时,产生氢气的质量与反应时间的函数关系如图所示。从图示说明的函数关系,可得出的结论是( ) A、金属活动性顺序: , 相对原子质量: B、金属活动性顺序: , 相对原子质量: C、金属活动性顺序: , 相对原子质量: D、金属活动性顺序: , 相对原子质量:9. 某同学制作的试剂标签如下,其中化学式书写正确的是A、
A、金属活动性顺序: , 相对原子质量: B、金属活动性顺序: , 相对原子质量: C、金属活动性顺序: , 相对原子质量: D、金属活动性顺序: , 相对原子质量:9. 某同学制作的试剂标签如下,其中化学式书写正确的是A、 B、
B、 C、
C、 D、
D、 10. “84消毒液”可用于环境和物体表面消毒,其主要成分为NaClO,其中氯元素的化合价为( )A、-2 B、-1 C、+1 D、+211. 已知:2H2O2 2H2O + O2↑。如图表示将一定质量的H2O2溶液和MnO2混合后,变量y随时间的变化趋势。变量y是( )
10. “84消毒液”可用于环境和物体表面消毒,其主要成分为NaClO,其中氯元素的化合价为( )A、-2 B、-1 C、+1 D、+211. 已知:2H2O2 2H2O + O2↑。如图表示将一定质量的H2O2溶液和MnO2混合后,变量y随时间的变化趋势。变量y是( ) A、H2O2的质量 B、O2的质量 C、MnO2的质量 D、溶液的总质量12. 鉴别空气、氧气和二氧化碳三瓶气体的方法是( )A、观察气体颜色 B、倒入澄清石灰水 C、闻气体的气味 D、插入燃着的木条13. 氧是地壳中含量最高的元素。一种氧原子的原子核内有8个质子和10个中子,该原子的核外电子数为( )A、8 B、10 C、18 D、214. 建造北京大兴国际机场使用了大量钒钢,下图是钒在元素周期表中的信息及原子结构示意图,由此获得的信息不正确的是
A、H2O2的质量 B、O2的质量 C、MnO2的质量 D、溶液的总质量12. 鉴别空气、氧气和二氧化碳三瓶气体的方法是( )A、观察气体颜色 B、倒入澄清石灰水 C、闻气体的气味 D、插入燃着的木条13. 氧是地壳中含量最高的元素。一种氧原子的原子核内有8个质子和10个中子,该原子的核外电子数为( )A、8 B、10 C、18 D、214. 建造北京大兴国际机场使用了大量钒钢,下图是钒在元素周期表中的信息及原子结构示意图,由此获得的信息不正确的是 A、图中x=23 B、钒属于金属元素 C、钒的中子数为50.94 D、钒原子核外有4个电子层15. 金属钨可用作家用白炽灯泡的灯丝。工业制备高纯钨的主要反应为: ,该反应属于( )A、化合反应 B、分解反应 C、置换反应 D、复分解反应16. 用微观模拟图表示物质的构成是化学学科常用的的表达方法。以下各图能表示纯净物的是(图中不同小球代表不同原子)A、
A、图中x=23 B、钒属于金属元素 C、钒的中子数为50.94 D、钒原子核外有4个电子层15. 金属钨可用作家用白炽灯泡的灯丝。工业制备高纯钨的主要反应为: ,该反应属于( )A、化合反应 B、分解反应 C、置换反应 D、复分解反应16. 用微观模拟图表示物质的构成是化学学科常用的的表达方法。以下各图能表示纯净物的是(图中不同小球代表不同原子)A、 B、
B、 C、
C、 D、
D、 17. 某同学设计化学“消消乐”游戏,点击灰色格,与该格中物质能反应的相邻物质就一起消失(反应条件为常温、加热或点燃),点击下图灰色格,剩余物质最少的是A、
17. 某同学设计化学“消消乐”游戏,点击灰色格,与该格中物质能反应的相邻物质就一起消失(反应条件为常温、加热或点燃),点击下图灰色格,剩余物质最少的是A、 B、
B、 C、
C、 D、
D、 18. 用如图所示4个实验探究二氧化碳能否与水反应(实验中所用的纸花均用石蕊染成紫色并干燥),下列说法正确的是( )
18. 用如图所示4个实验探究二氧化碳能否与水反应(实验中所用的纸花均用石蕊染成紫色并干燥),下列说法正确的是( ) A、最终只有实验④中的紫色石蕊小花会变红 B、实验④就能说明二氧化碳与水发生了反应 C、由实验①④推断,实验④中有酸性物质生成 D、在实验④中,若对比小花放入集气瓶前后的现象,可以不必做实验③19. 粽子的香味源于粽叶的主要成分——对乙烯基苯酚(化学式为C8H8O)。下列有关该物质的说法不正确的是A、属于化合物 B、由3种元素组成 C、碳元素的质量分数最大 D、由8个碳原子、8个氢原子、1个氧原子构成20. 下列物质不属于合金的是( )A、不锈钢 B、硬铝 C、生铁 D、氧化铜21. 下列说法正确的是A、活泼金属能与稀盐酸反应放出气体,则能与稀盐酸反应放出气体的一定是活泼金属 B、“曾青得铁则化为铜”说明铁的金属活动性强于铜 C、在煤炉上放一壶水能防止一氧化碳中毒 D、铁制品表面的铁锈可以保护内层的铁不易锈蚀22. 实验是化学研究的基础。下列对有关实验结果分析正确的是( )A、测定空气中氧气含量,若实验结果偏高,可能是红磷加入过多 B、实验室用高锰酸钾制氧气,集气瓶中收集不到氧气,可能原因是试管口未放棉花 C、将二氧化碳气体倒入有高低蜡烛的烧杯时,蜡烛同时熄灭,可能是气体倾倒太快 D、二氧化碳通入滴加了紫色石蕊试液的蒸馏水后,液体变红,说明二氧化碳有酸性23. 在一密闭容器中加入甲、乙、丙、丁四种物质,在一定条件下发生化学反应,测得反应前及t1、t2时各物质质量如图所示,下列说法中正确的是
A、最终只有实验④中的紫色石蕊小花会变红 B、实验④就能说明二氧化碳与水发生了反应 C、由实验①④推断,实验④中有酸性物质生成 D、在实验④中,若对比小花放入集气瓶前后的现象,可以不必做实验③19. 粽子的香味源于粽叶的主要成分——对乙烯基苯酚(化学式为C8H8O)。下列有关该物质的说法不正确的是A、属于化合物 B、由3种元素组成 C、碳元素的质量分数最大 D、由8个碳原子、8个氢原子、1个氧原子构成20. 下列物质不属于合金的是( )A、不锈钢 B、硬铝 C、生铁 D、氧化铜21. 下列说法正确的是A、活泼金属能与稀盐酸反应放出气体,则能与稀盐酸反应放出气体的一定是活泼金属 B、“曾青得铁则化为铜”说明铁的金属活动性强于铜 C、在煤炉上放一壶水能防止一氧化碳中毒 D、铁制品表面的铁锈可以保护内层的铁不易锈蚀22. 实验是化学研究的基础。下列对有关实验结果分析正确的是( )A、测定空气中氧气含量,若实验结果偏高,可能是红磷加入过多 B、实验室用高锰酸钾制氧气,集气瓶中收集不到氧气,可能原因是试管口未放棉花 C、将二氧化碳气体倒入有高低蜡烛的烧杯时,蜡烛同时熄灭,可能是气体倾倒太快 D、二氧化碳通入滴加了紫色石蕊试液的蒸馏水后,液体变红,说明二氧化碳有酸性23. 在一密闭容器中加入甲、乙、丙、丁四种物质,在一定条件下发生化学反应,测得反应前及t1、t2时各物质质量如图所示,下列说法中正确的是 A、该反应中,乙、丁的质量变化之比为5∶7 B、该反应中,甲和乙是反应物 C、丙为该反应的催化剂 D、该反应为化合反应
A、该反应中,乙、丁的质量变化之比为5∶7 B、该反应中,甲和乙是反应物 C、丙为该反应的催化剂 D、该反应为化合反应二、填空题
-
24. 以化合价为纵坐标,物质类别为横坐标,绘制的图像叫“价类二维图”。如图是碳元素的“价类二维图”,图中A、B、D、E分别表示不同的物质。

回答下列问题:
(1)、A的单质有多种,写出其中一种的名称。(2)、B、D可相互转化,B和(填化学式)在一定条件下发生化合反应能生成D。(3)、科学家将D进行转化实现资源化利用,其中一种方法是:D+4H2CH4+2X,X的化学式为。(4)、D、E可相互转化,若E是由三种元素组成,写出D→E的一个化学方程式。25. H2O2在医疗、军事、工业中应用广泛。科学家发现,在光照及Pt-TiO2做催化剂的条件下,能分解H2O制H2O2。(1)、TiO2中含有种元素。(2)、补全分解H2O制H2O2反应的化学方程式:2H2O H2O2 +。26. 自来水厂净水过程的主要操作流程如下图:
回答下列问题:
(1)、操作X的名称是 , 实验室通常用此操作将和分离开来;试剂A的名称是。(2)、絮凝剂明矾的作用是;(3)、高铁酸钾(K2FeO4)能作消毒剂与絮凝剂。高铁酸钾中铁元素的化合价是。(4)、可用来检验自来水是不是硬水,生活中将硬水软化的方法是。27. 下列是初中化学常见的实验装置,按要求回答问题: (1)、写出标号a的仪器名称。(2)、从A、B、C中选择一个实验室制取二氧化碳的发生装置(填字母序号),此装置的优点是 , 发生反应的化学方程式为。(3)、D为测定空气中氧气体积分数的实验装置,实验中红磷燃烧的现象是;实验完毕打开止水夹,发现进入集气瓶中水的体积明显小于集气瓶中气体体积的五分之一,可能的原因是(写出一点即可)。28. 依据下图所示实验回答问题。
(1)、写出标号a的仪器名称。(2)、从A、B、C中选择一个实验室制取二氧化碳的发生装置(填字母序号),此装置的优点是 , 发生反应的化学方程式为。(3)、D为测定空气中氧气体积分数的实验装置,实验中红磷燃烧的现象是;实验完毕打开止水夹,发现进入集气瓶中水的体积明显小于集气瓶中气体体积的五分之一,可能的原因是(写出一点即可)。28. 依据下图所示实验回答问题。 (1)、A实验中观察到的现象是。(2)、B实验用玻璃棒引流的目的是。(3)、C中热水的作用是。对比铜片上的白磷和红磷,得出的结论是。29. 某“暖宝宝”取暖贴的透气无纺布袋内装有铁粉、活性炭、氯化钠、水等物质,兴趣小组同学对此展开探究。(1)、【活动一】用铁钉探究铁的锈蚀
(1)、A实验中观察到的现象是。(2)、B实验用玻璃棒引流的目的是。(3)、C中热水的作用是。对比铜片上的白磷和红磷,得出的结论是。29. 某“暖宝宝”取暖贴的透气无纺布袋内装有铁粉、活性炭、氯化钠、水等物质,兴趣小组同学对此展开探究。(1)、【活动一】用铁钉探究铁的锈蚀某同学用相同的铁钉探究铁生锈与哪些因素有关,设计了下图所示的实验。

该实验中,能形成对比的一组实验是(填字母)
(2)、该实验中将蒸馏水煮沸的目的是。(3)、经过一周的观察,试管B和试管C中的铁钉无明显变化,试管A中的铁钉明显锈蚀,说明铁锈是铁与发生化学反应生成的。(4)、【活动二】用“暖宝宝”中的物质探究铁的锈蚀用无纺布袋装入干燥的铁粉、活性炭和氯化钠,分别放在锥形瓶底部,进行下图所示的实验。

图1所示实验,锥形瓶在短时间内发烫,冷却至室温,打开弹簧夹,观察到 , 打开无纺布袋,黑色粉末有部分变成色,图2和图3所示实验均无明显现象。(5)、与【活动一】所示实验相比较,图1所示实验可在短时间内完成,除了铁粉的因素外,你对活性炭与氯化钠作用的合理猜测是(写出1点即可)。(6)、【活动三】用“暖宝宝”测定空气里氧气的含量利用【活动二】中图1所示实验,测定空气里氧气的含量。
①实验时,需要获得的数据有锥形瓶内空气的体积、;实验时需要注意的事项是(写出1点即可)。
②与用红磷测定空气里氧气的含量的实验相比,实验利用“暖宝宝”测定空气里氧气的含量的优点是(写出1条即可)。
30. A、B、C、D为初中化学常见物质,它们都含有同一种元素,B是相对分子质量最小的氧化物,D的固体俗称干冰。它们之间的转化关系如图所示(“→”表示某一种物质经一步反应可转化为另一种物质)。 (1)、A的化学式为。(2)、写出D的一种用途。(3)、A→C反应的化学方程式为 , 该反应属于反应。31. 阅读下面科普短文。
(1)、A的化学式为。(2)、写出D的一种用途。(3)、A→C反应的化学方程式为 , 该反应属于反应。31. 阅读下面科普短文。为应对CO2等温室气体引起的气候变化问题,世界各国以全球协约的方式减排温室气体,我国提出碳达峰和碳中和目标。碳达峰指的是在某一时间,CO2的排放量达到历史最高值,之后逐步回落;碳中和指的是通过植树造林、节能减排、碳捕集与封存等形式,抵消生产生活中CO2的排放量,从而达到CO2相对“零排放”。我国目标是争取2030年前达到碳达峰,2060年实现碳中和。现阶段我国的能源结构以化石燃料为主,其燃烧释放出大量的CO2.实现碳中和的路径之一为降低化石能源在消费能源中的比例,提高可再生、非化石能源比例。路径之二为捕集、利用和封存CO2 , 如利用废气中的CO2 , 制取甲醇(CH3OH),反应的微观示意图如图1所示。在实际生产中,CH3OH的产率除受浓度、温度、压强等因素影响外,还受催化剂CuO质量分数的影响(如图2所示)。

我国科学家们撰文提出“液态阳光”概念,即将太阳能转化为可稳定存储并且可输出的燃料,实现燃料零碳化。随着科学技术的发展,今后的世界,每天的阳光将为我们提供取之不尽、用之不竭的热、电,还有可再生燃料!
依据文章内容回答下列问题。
(1)、我国碳达峰的目标是。(2)、化石燃料包括煤、、天然气。(3)、化石燃料的过度使用会加剧的环境问题是。(4)、在日常生活中,你如何践行“碳中和”理念(写一条)。(5)、根据图1,写出CO2制取甲醇的化学方程式:。(6)、由图2可得到的结论是。(7)、下列说法正确的是____(填序号)。A、碳达峰、碳中和中的“碳”指的是碳单质 B、控制化石燃料的使用可减少碳排放 C、碳中和指的是没有碳排放 D、“液态阳光”将实现燃料零碳化三、计算题
-
32. 工业上用1000t含氧化铁80%的赤铁矿,理论上可炼出含杂质4%的生铁的质量是多少?(要求用化学方程式计算,最后结果精确到0.1t)