江西省赣州市石城县2023-2024学年九年级上学期期末质量检测化学试题
试卷更新日期:2024-02-22 类型:期末考试
一、单项选择题(本大题包括10小题,每小题有四个选项,其中只有-一个选项符合题意,请将符合题意的选项代号填涂在答题卡的相应位置上。1-5每小题1分,6-10每小题2分,共15分)
-
1. 2023年10月8日杭州亚运会胜利闭幕。下列情景与化学变化有关的是( )A、五星红旗缓缓升起 B、零碳甲醇点燃亚运主火炬 C、人浪营造海潮图形 D、会场探照灯通电绚丽夺目2. 规范的实验操作是科学探究的基本要求,下列实验操作正确的是( )A、闻气体气味
 B、倾倒液体
B、倾倒液体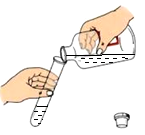 C、滴加液体
C、滴加液体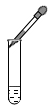 D、加入块状固体
D、加入块状固体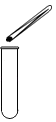 3. 下列做法与“文明阜宁”在行动这一主题不相符合的是( )A、减少燃煤使用 B、回收废旧金属 C、野外焚烧垃圾 D、大力植树造林4. 常温下为液态的金属是( )A、汞 B、金 C、银 D、铝5. 2023年12月27日9时08分,杭昌高铁黄昌段首趟G4012次列车从南昌东站缓缓启动,驶向黄山北站。这标志着杭昌高铁黄昌段正式开通运营,我省成为全国首个市市通时速350公里高铁的省份,高铁车厢内禁止吸烟须张贴的标志是( )A、
3. 下列做法与“文明阜宁”在行动这一主题不相符合的是( )A、减少燃煤使用 B、回收废旧金属 C、野外焚烧垃圾 D、大力植树造林4. 常温下为液态的金属是( )A、汞 B、金 C、银 D、铝5. 2023年12月27日9时08分,杭昌高铁黄昌段首趟G4012次列车从南昌东站缓缓启动,驶向黄山北站。这标志着杭昌高铁黄昌段正式开通运营,我省成为全国首个市市通时速350公里高铁的省份,高铁车厢内禁止吸烟须张贴的标志是( )A、 B、
B、 C、
C、 D、
D、 6. 现有X、Y、Z三种金属,常温下只有X能和稀硫酸反应,把Y、Z两种金属分别放入硝酸银溶液中,只有Y表面有银白色物质析出。三种金属的活动性顺序为( )A、Y>X>Z B、Y>Z>X C、X>Y>Z D、X>Z>Y7. 铕是一种稀土元素,铕在元素周期表中的信息如图所示。下列叙述错误的是( )
6. 现有X、Y、Z三种金属,常温下只有X能和稀硫酸反应,把Y、Z两种金属分别放入硝酸银溶液中,只有Y表面有银白色物质析出。三种金属的活动性顺序为( )A、Y>X>Z B、Y>Z>X C、X>Y>Z D、X>Z>Y7. 铕是一种稀土元素,铕在元素周期表中的信息如图所示。下列叙述错误的是( ) A、铕是一种金属元素 B、铕原子中的质子数为63 C、铕的相对原子质量为152.0g D、稀土资源应合理利用和保护8. 物质的性质决定其用途。下列物质的性质与用途对应关系不正确的是( )A、干冰升华吸热,可用于人工降雨 B、一氧化碳具有氧化性,可用于冶炼金属 C、金刚石硬度大,可用于裁玻璃 D、氮气化学性质不活泼,可用作食品防腐的保护气9. 证据推理是化学学科核心素养的重要内容,下列合理的是( )A、燃烧一定放热,所以放热的反应一定是燃烧 B、分子可以构成物质,所以物质都由分子构成 C、化合反应的生成物只有一种,所以只有一种生成物的反应一定是化合反应 D、含有一种元素的纯净物是单质,所以单质中只含有一种元素10. 下列实验过程与图像的对应关系正确的是( )A、加热高锰酸钾固体至质量不再减轻
A、铕是一种金属元素 B、铕原子中的质子数为63 C、铕的相对原子质量为152.0g D、稀土资源应合理利用和保护8. 物质的性质决定其用途。下列物质的性质与用途对应关系不正确的是( )A、干冰升华吸热,可用于人工降雨 B、一氧化碳具有氧化性,可用于冶炼金属 C、金刚石硬度大,可用于裁玻璃 D、氮气化学性质不活泼,可用作食品防腐的保护气9. 证据推理是化学学科核心素养的重要内容,下列合理的是( )A、燃烧一定放热,所以放热的反应一定是燃烧 B、分子可以构成物质,所以物质都由分子构成 C、化合反应的生成物只有一种,所以只有一种生成物的反应一定是化合反应 D、含有一种元素的纯净物是单质,所以单质中只含有一种元素10. 下列实验过程与图像的对应关系正确的是( )A、加热高锰酸钾固体至质量不再减轻 B、等质量、等浓度的过氧化氢溶液制取氧气
B、等质量、等浓度的过氧化氢溶液制取氧气  C、高温加热氧化铜和碳的混合物
C、高温加热氧化铜和碳的混合物  D、一定质量的石灰石中不断加入稀盐酸
D、一定质量的石灰石中不断加入稀盐酸 
二、选择填充题(本大题包括3小题,先在A、B、C中选择一个正确选项的代号填涂在答题卡的相应位置上,然后在D处补充一个符合题意的答案。每小题2分,其中选择1分,填充1分,共6分)
-
11. 下列变化中,属于缓慢氧化的是
A 电灯发光 B 木炭燃烧 C 食物腐烂 D .
12. 2023年4月29日《科技日报》报道“我国科学家实现二氧化碳到葡萄糖和油脂的人工合成”,合成过程中的一个反应微观示意图如图,有关说法正确的是。
A.反应前后分子的种类一定改变 B.反应前后共有三种氧化物
C.丙物质由8个原子构成 D.反应中甲和丁的分子个数比是
13. 下列实验方法能达到实验目的的是。选项
实验目的
实验方法
A
实验室鉴别食盐水和蔗糖水
尝味道
B
区分氧化铜粉末和炭粉
观察颜色
C
除去井水中的色素和异味
加入活性炭
D
除去氯化亚铁溶液中少量氯化铜
三、填空与说明题(包括4小题,共23分)
-
14. 2023年1月4日《江西省义务教育新课程实施办法》出台,规定一至九年级开设《美丽江西》课程。请回答下列问题:(1)、春天婺源赏油菜:从微观角度分析,在远处就能闻到油菜花的香味的原因是。(2)、夏天庐山望瀑布:检验瀑布水是否是硬水的方法是 , 生活中庐山瀑布水经过 , 既可以消毒,又可以将水软化。(3)、深秋赣南品脐橙:赣南脐橙名扬四海,被称之为“中华名果”。脐橙中含丰富的营养物质,如每100克脐橙中维生素C的质量是15毫克,成人每人每天所需维生素C的质量约为60毫克,假设某人一天所需的维生素C一半从脐橙中获得,则此人每天至少食用脐橙的质量为克;脐橙中含丰富水分,标出水中氢元素的化合价。(4)、冬天宜春泡温泉:温泉富含硒,这里的“硒”是指(选填“元素”、“原子”、“离子”或“分子”)。15. 叩问天穹,化学助力。(1)、万户飞天:明代万户飞天时用黑火药(含有硫、木炭和硝酸钾)作火箭燃料。黑火药属于(填“混合物”或“纯净物”)。(2)、卫星发射:1970年我国首颗人造卫星“东方红一号”成功入轨。制造人造卫星常用到钛合金,工业制取钛()的一种方法: , 式中x为。(3)、载人航天:2003年“神舟五号”载人飞船成功发射。运载火箭的燃料之一偏二甲肼()中氢、氮元素的质量比为。(4)、探月探火:近日“祝融号”火星车发现火星低纬度地区存在液态水,为星际移民的能源供给提供了可能。利用太阳能电池电解水制氢气的化学方程式为。16. 工业上以空气、水等自然资源为原料合成碳酸氢铵的工艺流程图如图所示:
 (1)、步骤1是利用各成分的不同,通过冷却、加压、蒸馏将其分离。(2)、实验室中完成步骤④,玻璃棒作用是。(3)、步骤②涉及的化学反应基本类型为。(4)、写出合成碳酸氢铵NH4HCO3的化学方程式。17. 实验是化学学习的一个重要途径,结合下列实验装置回答问题:
(1)、步骤1是利用各成分的不同,通过冷却、加压、蒸馏将其分离。(2)、实验室中完成步骤④,玻璃棒作用是。(3)、步骤②涉及的化学反应基本类型为。(4)、写出合成碳酸氢铵NH4HCO3的化学方程式。17. 实验是化学学习的一个重要途径,结合下列实验装置回答问题: (1)、实验1中观察到白磷燃烧,活塞先向右滑动后又向左滑动,最终大约停留在刻度处(底部塞子所占体积忽略不计),此实验中沸水的作用是。(2)、实验2(填“能”或“不能”)直接用于验证质量守恒定律。(3)、实验3甲中发生反应的化学方程式为。一段时间后乙中的液体变为红色,然后停止通入CO2 , 加热乙中的液体,观察到的现象是。
(1)、实验1中观察到白磷燃烧,活塞先向右滑动后又向左滑动,最终大约停留在刻度处(底部塞子所占体积忽略不计),此实验中沸水的作用是。(2)、实验2(填“能”或“不能”)直接用于验证质量守恒定律。(3)、实验3甲中发生反应的化学方程式为。一段时间后乙中的液体变为红色,然后停止通入CO2 , 加热乙中的液体,观察到的现象是。四、实验与探究题(本大题包括2小题,共16分)
-
18. 如图是氧气和二氧化碳的实验室制取与性质的有关实验示意图。
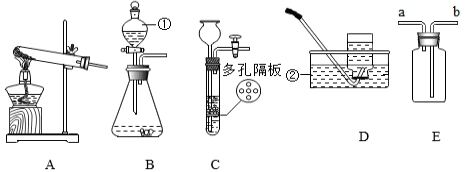 (1)、仪器名称:②。(2)、用氯酸钾和二氧化锰制取较纯净的O2 , 可选用发生装置A和收集装置(选填序号)组合,反应的化学方程式为。加热药品前使试管均匀受热的具体操作是。(3)、实验室可用装置B或C制CO2 , C装置相对于B的优点有。E中盛放澄清石灰水试剂可检验CO2气体,气体应从(选填“a”或“b”)端通入。19. 《梦溪笔谈》中有关于湿法炼铜的描述,表明我国很早就开始利用硫酸铜。兴趣小组的同学开展了有关硫酸铜项目研究。(1)、项目一:硫酸铜的性质
(1)、仪器名称:②。(2)、用氯酸钾和二氧化锰制取较纯净的O2 , 可选用发生装置A和收集装置(选填序号)组合,反应的化学方程式为。加热药品前使试管均匀受热的具体操作是。(3)、实验室可用装置B或C制CO2 , C装置相对于B的优点有。E中盛放澄清石灰水试剂可检验CO2气体,气体应从(选填“a”或“b”)端通入。19. 《梦溪笔谈》中有关于湿法炼铜的描述,表明我国很早就开始利用硫酸铜。兴趣小组的同学开展了有关硫酸铜项目研究。(1)、项目一:硫酸铜的性质
硫酸铜是一种白色固体粉末,描述的是硫酸铜的(填“物理”或“化学”)性质。(2)、将一根打磨过的铁丝插入盛有硫酸铜溶液的试管中,反应一段时间后观察到的实验现象是 , 且溶液由蓝色逐渐变为浅绿色。(3)、项目二:硫酸铜的用途农业上用硫酸铜、生石灰加水混合配制常用的杀菌剂波尔多液,但不能用铁制容器配制,原因是(用化学方程式解释)。
(4)、项目三:硫酸铜的制备【查阅资料】制备硫酸铜的一种方案:Cu+H2O2+H2SO4=CuSO4+2H2O。
【进行实验】将反应物装入烧杯中,观察到如下现象:开始时有少量气泡,后来反应剧烈产生大量气泡,放出热量,溶液呈蓝色,该溶液即为硫酸铜溶液。
【提出疑问】实验中为什么有气体生成?同学们进行了如下探究。
项目四:实验异常现象探究
【查阅资料】制备硫酸铜过程中,H2O2发生了分解反应,生成的气体是
【提出问题】什么因素加快了H2O2分解?
【猜想与假设】
猜想一:生成的CuSO4;
猜想二:温度升高;
猜想三:。
(5)、【实验探究】
【实验分析】
实验观察到的现象:实验一产生气泡;实验二无明显现象;实验三产生气泡;实验四快速产生气泡,对比实验一和实验二可以得出的结论是。为了验证温度升高能加快H2O2的分解,甲同学的方案是实验二和实验三对比;乙同学的方案是实验一和实验四对比。你认为同学的方案更严谨,理由是。
【实验结论】猜想三正确。
五、综合计算题(本大题包括1小题,共10分)
-
20. 黄铜可用于制造子弹壳,已知组成某弹壳的黄铜中只含有锌和铜,现将20g该弹壳剪碎后放入烧杯中,再向烧杯中加入过量稀硫酸至完全反应。测得反应过程中生成的氢气质量与反应时间关系如图所示。
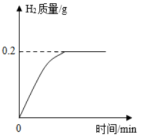
请回答:
(1)、实验过程中将弹壳剪碎的目的是。(2)、判断稀硫酸与黄铜完全反应的现象是 , 完全反应后烧杯中含有的阳离子是(填离子符号)。(3)、兴趣小组的同学为了充分利用资源,将反应后的物质过滤,回收其中的金属物质。过滤中需要用到的下列玻璃仪器有____。A、量筒 B、烧杯 C、长颈漏斗 D、铁架台(4)、计算该弹壳中铜的质量分数。(写出计算过程)