江苏省南京市玄武区2023-2024学年九年级上学期期末化学试题
试卷更新日期:2024-02-20 类型:期末考试
一、选择题
-
1. 下列变化中,属于化学变化的是A、玻璃破碎 B、铁钉生锈 C、石蜡熔化 D、干冰升华2. 下列金属中,熔点最高的是A、铜 B、钨 C、汞 D、铝3. 把少量下列物质分别放入水中,充分搅拌,能得到溶液的是A、蔗糖 B、碘粒 C、汽油 D、面粉4. 下列物质由分子构成的是( )A、汞 B、水 C、金刚石 D、氯化钠5. 下列物质加入一定量的水中,能使液体温度明显降低的是( )A、硝酸铵 B、氢氧化钠 C、生石灰 D、氯化钠6. 下列化学用语表达正确的是A、氦气一He2 B、2个氮分子一2N C、3个氧原子一O3 D、1个镁离子一Mg2+7. 下列图示实验操作中,正确的是A、读取液体体积
 B、称量固体
B、称量固体 C、过滤
C、过滤 D、取少量液体
D、取少量液体 8. 从环境保护的角度考虑,下列做法合理的是A、植树造林 B、露天焚烧垃圾 C、深埋废旧电池 D、排放未处理的废气9. 氮化镓是制造芯片的材料之一,图1是镓元素(元素符号为:Ga)的原子结构示意图,图2是元素周期表的一部分。下列说法不正确的是
8. 从环境保护的角度考虑,下列做法合理的是A、植树造林 B、露天焚烧垃圾 C、深埋废旧电池 D、排放未处理的废气9. 氮化镓是制造芯片的材料之一,图1是镓元素(元素符号为:Ga)的原子结构示意图,图2是元素周期表的一部分。下列说法不正确的是图1
 图2
图2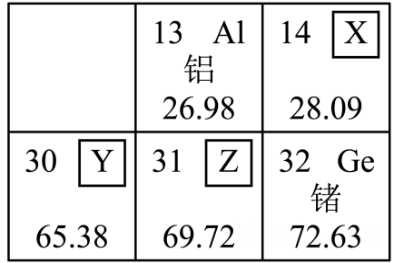 A、图1中,m=3 B、图2中,Z为Ga C、锗原子中有5个电子层 D、Ga与Al的最外层电子数相同10. 下列关于燃烧与灭火的说法中,不正确的是
A、图1中,m=3 B、图2中,Z为Ga C、锗原子中有5个电子层 D、Ga与Al的最外层电子数相同10. 下列关于燃烧与灭火的说法中,不正确的是 A、发生森林火灾时,开辟隔离带的灭火原理是移走可燃物 B、由图a中的现象可知,金属镁引起的火灾不可以用二氧化碳灭火 C、将大块煤粉碎后再燃烧,其目的是增大煤与氧气的接触面积使其充分燃烧 D、图b中火柴头朝上时更容易燃烧,是因为散逸的热量会加热火柴梗,提高温度11. 茶叶中含有茶黄素(C29H24O12),下列说法不正确的是A、茶黄素由三种元素组成 B、茶黄素的相对分子质量为574 C、茶黄素中碳元素、氢元素、氧元素的质量比为29:2:16 D、一个茶黄素分子由29个碳原子、24个氢原子、12个氧原子构成12. 下列解释不合理的是A、品红在水中扩散,说明分子在不断运动 B、将氧气压缩贮存于钢瓶中,说明分子之间有间隔 C、水受热变为水蒸气,说明分子的大小随温度的升高而增大 D、一滴水中有1.67×1021个水分子,说明分子的质量和体积都很小13. 下列除杂方法正确的是
A、发生森林火灾时,开辟隔离带的灭火原理是移走可燃物 B、由图a中的现象可知,金属镁引起的火灾不可以用二氧化碳灭火 C、将大块煤粉碎后再燃烧,其目的是增大煤与氧气的接触面积使其充分燃烧 D、图b中火柴头朝上时更容易燃烧,是因为散逸的热量会加热火柴梗,提高温度11. 茶叶中含有茶黄素(C29H24O12),下列说法不正确的是A、茶黄素由三种元素组成 B、茶黄素的相对分子质量为574 C、茶黄素中碳元素、氢元素、氧元素的质量比为29:2:16 D、一个茶黄素分子由29个碳原子、24个氢原子、12个氧原子构成12. 下列解释不合理的是A、品红在水中扩散,说明分子在不断运动 B、将氧气压缩贮存于钢瓶中,说明分子之间有间隔 C、水受热变为水蒸气,说明分子的大小随温度的升高而增大 D、一滴水中有1.67×1021个水分子,说明分子的质量和体积都很小13. 下列除杂方法正确的是选项
物质
杂质
除杂方法
A
N2
O2
将气体缓缓地通过灼热的碳粉
B
FeCl2溶液
CuCl2
往溶液中加入足量镁粉,搅拌,过滤
C
CO2
CO
将气体点燃
D
Ca(OH)2溶液
CaCO3
将混合物过滤
A、A B、B C、C D、D14. 下图的实验操作或方法能达到实验目的的是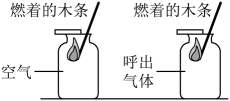


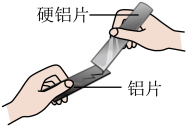
A.比较空气与呼出气体中CO2含量的多少
B.利用碳酸钠与盐酸的反应验证质量守恒定律
C.利用蒸馏水、植物油、干燥剂等探究铁生锈的条件
D.比较合金和纯金属的硬度
A、A B、B C、C D、D15. 用如下图所示的装置测定铁的氧化物的组成。实验前,测得硬质玻璃管及管内固体药品(铁的氧化物FexOy)的总质量为65.8g,其中硬质玻璃管的质量为60g:打开弹簧夹K,通入CO并加热:当铁的氧化物全部转化为铁单质后,测得硬质玻璃管及管内固体的总质量为64.2g,则该铁的氧化物FexOy , 化学式为 A、FeO B、Fe2O3 C、Fe3O4 D、Fe4O5
A、FeO B、Fe2O3 C、Fe3O4 D、Fe4O5二、填空题
-
16. 如图是硫元素的价类图。请回答下列问题:
 (1)、(填字母)点对应的物质是H2SO4。(2)、写出图中C、E点对应物质的化学式、;(各写一个)(3)、写出A点对应的物质转化为B点对应的物质的化学方程式。17. “氧循环”、“碳循环”是自然界存在的两大重要循环。请回答相关问题:
(1)、(填字母)点对应的物质是H2SO4。(2)、写出图中C、E点对应物质的化学式、;(各写一个)(3)、写出A点对应的物质转化为B点对应的物质的化学方程式。17. “氧循环”、“碳循环”是自然界存在的两大重要循环。请回答相关问题: (1)、化石燃料主要包括煤、和天然气;天然气的主要成分甲烷属于(填序号)。
(1)、化石燃料主要包括煤、和天然气;天然气的主要成分甲烷属于(填序号)。A.可燃物 B.单质 C.化合物 D.温室气体
(2)、图1中能吸收二氧化碳的途径有(填序号),为了控制途径①中二氧化碳的排放量,可使用清洁能源氢气,氢气燃烧的化学方程式是。(3)、科学家们利用Ni基双金属催化剂在一定条件下将二氧化碳和甲烷进行反应得到两种气体燃料,反应过程如图2所示,请写出该反应的化学方程式。(4)、工业上,煅烧石灰石可制得生石灰和二氧化碳,如果要制取8.8t二氧化碳,需要含碳酸钙80%的石灰石(杂质不参加反应)的质量是多少?(请在答题纸上写出计算过程)。三、综合题
-
18. 海水是重要的自然资源,回答下列问题。


【资科】海水中含有较多的氯化钠、氯化镁、氯化钙等可溶性物质。
(1)、小组同学用图1所示的自制净水器对海水样品进行净化,其中活性炭的作用是。(2)、经上述自制净水器净化后的水为(选填“硬水”或“软水”),请设计实验验证之,并完成实验报告。实验步骤
实验现象
实验结论
。
。
。
(3)、采用膜分离技术可将净化后的海水进行淡化,如图2所示。通过对淡化膜右侧的海水加压,水分子透过淡化膜进入左侧淡水池,而海水中的各种离子不能透过淡化膜,从而得到淡水。对加压后右侧海水组成的变化进行分析,正确的说法是____(填序号)。A、溶质质量减少 B、溶剂质量减少 C、溶液质量减少(4)、海水中某些元素组成的物质的溶解度曲线如图3所示。
①t2℃时,从硝酸钾(含少量硒酸镉)的饱和溶液中获取较纯净的硝酸钾晶体可以采用的方法是。
②在溶液质量不变的情况下,将接近饱和的硒酸镉溶液变为饱和溶液的方法为。
③t3℃时,将硝酸钾和氯化钠的饱和溶液蒸发等质量的水,再恢复到t3℃,析出晶体较多的是物质(填化学式)
④将t3℃时等质量的三种物质的饱和溶液分别降温到t1℃,对所得溶液的分析正确的是。
A.t1℃物质的溶解度:c>a =b B.溶剂质量:c>a>b
C.溶液质量:c>b>a D.溶质质量:a=b>c
19. 金属在人类发展的历史长河中起着非常重要的作用。(1)、用如图所示的实验来验证铁、铜、银的金属活动性强弱,两试管中加入的溶液为同一种物质的溶液,写出铁丝和该物质发生反应的化学方程式。 (2)、硫酸铁铵【NH4Fe(SO4)2】是一种重要的化合物。在实验室中利用废铁屑来制备硫酸铁铵的流程如下:
(2)、硫酸铁铵【NH4Fe(SO4)2】是一种重要的化合物。在实验室中利用废铁屑来制备硫酸铁铵的流程如下:
回答下列问题:
①步骤1中发生反应的化学方程式是。经检验,废渣是片状石墨,它与金刚石的物理性质有很大差异,原因是。
②完成步骤I中的反应:2 FeSO4+ H2O2+= Fe2(SO4)3+2H2O。
③步骤I中发生的反应属于(填基本反应类型)。
(3)、下列能有效保护金属资源的是____(填字母)。A、防止金属腐蚀 B、回收利用废旧金属 C、合理有效地开采矿物 D、寻找金属的代用品20. A~K是初中化学常见的物质,分别由H、C、O、Al、Cl、Ca、Cu中的一种或几种元素组成。其中A、B、D、K为单质,其余均为化合物;其中在空气中A表面会生成一层致密的氧化膜,阻止其进一步的氧化:B、D、G在常温下为气体:J是由两种元素组成且两种元素的质量比为1:4,图中“—”表示两端的物质间能发生化学反应:“→”表示物质间存在转化关系:部分反应物、生成物或反应条件已略去。
 (1)、写出化学式:C;E。(2)、写出J→F反应的化学方程式。(3)、写出G和H反应的化学方程式。
(1)、写出化学式:C;E。(2)、写出J→F反应的化学方程式。(3)、写出G和H反应的化学方程式。四、实验探究题
-
21. 某兴趣小组同学进行二氧化碳气体的制取及相关性质的探究。(1)、【实验探究1】探究二氧化碳的制取。
写出实验室用石灰石与稀盐酸反应制取二氧化碳的化学方程式。(2)、使用下列装置能实现“随开随用,随关随停”的是。(填序号) (3)、【实验探究2】探究二氧化碳与澄清石灰水反应。
(3)、【实验探究2】探究二氧化碳与澄清石灰水反应。组装好实验装置(如图1所示),并检查装置的气密性,瓶中充满二氧化碳,实验时先迅速注入注射器中澄清石灰水,后注入注射器中稀盐酸实验过程中采集到数据如图2所示。

分析CD段压强增大的原因是。
(4)、图表中压强始终没有达到0kPa,可能的原因是。(5)、【实验探究3】探究二氧化碳与氢氧化钠的反应:查阅资料:
①氢氧化钠与氢氧化钙有相似的化学性质,也能与二氧化碳反应,生成碳酸钠和水:该反应的化学方程式为。碳酸钠易溶于水。
②通常情况下1体积水大约能溶解1体积二氧化碳。
(6)、进行实验:组装好实验装置(如图3所示),并检查装置的气密性。
先关闭K,从a处缓缓通入600mL二氧化碳,观察到现象;然后打开K,再次缓缓通入二氧化碳,观察到现象,可说明二氧化碳能与氢氧化钠反应。
得出结论:二氧化碳能与氢氧化钠反应。
反思评价:在实验室里,检验二氧化碳一般用澄清石灰水,吸收二氧化碳一般用氢氧化钠溶液。