江苏省南京市鼓楼区2023-2024学年九年级上学期期末化学试题
试卷更新日期:2024-02-20 类型:期末考试
一、选择题
-
1. 化学用语“K”不能表示A、物质 B、元素 C、原子 D、分子2. 决定元素种类的是A、电子层数 B、最外层电子数 C、质子数 D、中子数3. 下列图示实验中发生化学变化的是A、
 B、
B、 C、
C、 D、
D、 4. 下列说法正确的是A、天然存在最硬的物质一一金刚石 B、熔点最低的金属一一银 C、空气中体积分数最大的气体一一氧气 D、地壳中含量最高的金属元素一一铁5. 下列溶液中,溶剂不是水的是A、稀盐酸 B、澄清石灰水 C、碘酒溶液 D、蔗糖溶液6. 性质决定用途,用途反映性质。下列说法中不正确的是A、氮气化学性质不活泼,可用作保护气 B、洗涤剂能溶解油污,可用于清洗餐具 C、活性炭有吸附性,可用作冰箱除味剂 D、钛合金与人体具有很好的“相容性”,可用于制造人造骨7. 北宋的沈括在《梦溪笔谈》中首次提出了“石油”的概念:“鹿郭、延境内有石油,旧说‘高奴县出脂水’,即此也。…然(通‘燃’)之如麻,但烟甚浓,所沾帷幕皆黑。…盖石油之多,生于地中无穷,不若松木有时而竭。…”下列关于石油的说法不正确的是A、石油是一种化工产品 B、石油是不可再生资源 C、石油是一种混合物 D、石油燃烧产生炭黑,说明石油含有碳元素8. 下列叙述不正确的是A、淬火后的钢针能弯曲 B、煮沸可用于生活中降低水的硬度 C、硫酸铜溶液可作过氧化氢分解的催化剂 D、二氧化碳灭火器可用于扑灭图书档案的失火9. 天气闷热时,水中的含氧量降低,养鱼池里的鱼总是接近水面游动。下列有关说法正确的是A、氧气在水中的溶解度随温度的升高而减小 B、氧气在水中的溶解度随压强的增大而减小 C、水中的含氧量降低,这里的“氧”指的是氧元素 D、利用水泵把养鱼池中的水喷向空中,可增大氧气在水中的溶解度10. 化合物C22H12的分子结构如图所示。下列关于该化合物的说法中,正确的是
4. 下列说法正确的是A、天然存在最硬的物质一一金刚石 B、熔点最低的金属一一银 C、空气中体积分数最大的气体一一氧气 D、地壳中含量最高的金属元素一一铁5. 下列溶液中,溶剂不是水的是A、稀盐酸 B、澄清石灰水 C、碘酒溶液 D、蔗糖溶液6. 性质决定用途,用途反映性质。下列说法中不正确的是A、氮气化学性质不活泼,可用作保护气 B、洗涤剂能溶解油污,可用于清洗餐具 C、活性炭有吸附性,可用作冰箱除味剂 D、钛合金与人体具有很好的“相容性”,可用于制造人造骨7. 北宋的沈括在《梦溪笔谈》中首次提出了“石油”的概念:“鹿郭、延境内有石油,旧说‘高奴县出脂水’,即此也。…然(通‘燃’)之如麻,但烟甚浓,所沾帷幕皆黑。…盖石油之多,生于地中无穷,不若松木有时而竭。…”下列关于石油的说法不正确的是A、石油是一种化工产品 B、石油是不可再生资源 C、石油是一种混合物 D、石油燃烧产生炭黑,说明石油含有碳元素8. 下列叙述不正确的是A、淬火后的钢针能弯曲 B、煮沸可用于生活中降低水的硬度 C、硫酸铜溶液可作过氧化氢分解的催化剂 D、二氧化碳灭火器可用于扑灭图书档案的失火9. 天气闷热时,水中的含氧量降低,养鱼池里的鱼总是接近水面游动。下列有关说法正确的是A、氧气在水中的溶解度随温度的升高而减小 B、氧气在水中的溶解度随压强的增大而减小 C、水中的含氧量降低,这里的“氧”指的是氧元素 D、利用水泵把养鱼池中的水喷向空中,可增大氧气在水中的溶解度10. 化合物C22H12的分子结构如图所示。下列关于该化合物的说法中,正确的是 A、C22H12的相对分子质量为276g B、C22H12中碳、氢元素质量比为11:6 C、一个C22H12分子中含有6个H2 D、C22H12与CH4分子构成不同,化学性质存在差异11. 根据图示,下列有关“实验室制取气体”的叙述不正确的是
A、C22H12的相对分子质量为276g B、C22H12中碳、氢元素质量比为11:6 C、一个C22H12分子中含有6个H2 D、C22H12与CH4分子构成不同,化学性质存在差异11. 根据图示,下列有关“实验室制取气体”的叙述不正确的是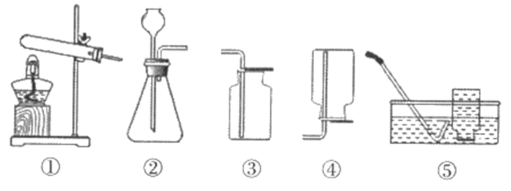 A、实验室中选择装置①制O2的反应属于分解反应 B、实验室制H2、O2、CO2均可选择装置② C、O2和CO2均可选择装置③收集 D、选择装置②制气,可控制反应的发生和停止12. 逻辑推理是学习化学常用的思维方法。下列推理正确的是A、置换反应有单质和化合物生成,所以有单质和化合物生成的反应一定是置换反应 B、单质只含一种元素,所以由一种元素组成的纯净物一定是单质 C、溶液具有均一性和稳定性,所以具有均一性和稳定性的液体一定是溶液 D、化学反应伴随着能量的变化,所以有能量变化的一定是化学反应13. 除去下列物质中混有的少量杂质(括号内为杂质),拟定的实验方案不可行的是A、Cu粉(Fe)一加入足量稀盐酸,过滤、洗涤、干燥 B、CO2气体(O2)一通过炽热的炭层 C、CaO固体(CaCO3)一高温煅烧至固体质量不再减少 D、CuO固体(C)一在氧气流中灼烧14. 下列图像表示的对应关系不正确的是
A、实验室中选择装置①制O2的反应属于分解反应 B、实验室制H2、O2、CO2均可选择装置② C、O2和CO2均可选择装置③收集 D、选择装置②制气,可控制反应的发生和停止12. 逻辑推理是学习化学常用的思维方法。下列推理正确的是A、置换反应有单质和化合物生成,所以有单质和化合物生成的反应一定是置换反应 B、单质只含一种元素,所以由一种元素组成的纯净物一定是单质 C、溶液具有均一性和稳定性,所以具有均一性和稳定性的液体一定是溶液 D、化学反应伴随着能量的变化,所以有能量变化的一定是化学反应13. 除去下列物质中混有的少量杂质(括号内为杂质),拟定的实验方案不可行的是A、Cu粉(Fe)一加入足量稀盐酸,过滤、洗涤、干燥 B、CO2气体(O2)一通过炽热的炭层 C、CaO固体(CaCO3)一高温煅烧至固体质量不再减少 D、CuO固体(C)一在氧气流中灼烧14. 下列图像表示的对应关系不正确的是 A、图①:室温下,分别将生石灰和硝酸铵固体放入水中 B、图②:向一定质量的硝酸银溶液中不断加入铜粉 C、图③:加热一定质量的高锰酸钾固体 D、图④:保持温度不变,向接近饱和的硝酸钾溶液中不断加入硝酸钾固体15. 工业上用NO生产HNO3过程中的物质转化关系如图所示。下列有关说法正确的是
A、图①:室温下,分别将生石灰和硝酸铵固体放入水中 B、图②:向一定质量的硝酸银溶液中不断加入铜粉 C、图③:加热一定质量的高锰酸钾固体 D、图④:保持温度不变,向接近饱和的硝酸钾溶液中不断加入硝酸钾固体15. 工业上用NO生产HNO3过程中的物质转化关系如图所示。下列有关说法正确的是 A、转化过程中,只有氮元素的化合价发生变化 B、反应①中,参加反应的NO与O2的分子数目之比为1:2 C、反应②中,生成的HNO3和NO的质量之比为21:5 D、理论上,每生产63kgHNO3需消耗48kgO2
A、转化过程中,只有氮元素的化合价发生变化 B、反应①中,参加反应的NO与O2的分子数目之比为1:2 C、反应②中,生成的HNO3和NO的质量之比为21:5 D、理论上,每生产63kgHNO3需消耗48kgO2二、非选择题
-
16. 随着经济的发展,能源与环境成为人们关注的焦点。(1)、煤、石油和等化石燃料的燃烧都会产生CO2。若大气中CO2的含量不断上升,会导致增强,全球气候变暖。(2)、煤燃烧时排放出二氧化硫、二氧化氮等污染物,会形成酸雨,请写出二氧化硫的化学式并标出其中各元素的化合价。(3)、在汽油中加入适量乙醇(C2H5OH)作为汽车燃料,可在一定程度上减少汽车尾气的污染。乙醇在空气中完全燃烧的化学方程式为。(4)、氢气是一种理想的清洁、高能燃料,氢气在空气中燃烧的化学方程式为。近年来,我国科研人员在制氢研究方面取得突破。如图是一种以甲烷和二氧化碳为原料制氢反应的微观示意图。

请根据图示写出该反应的化学方程式。
17. 海洋是地球上最大的储水库,蕴藏着丰富的化学资源。(1)、如图是利用海水提取粗盐的过程。
根据海水晒盐的原理,下列说法中不正确的是____(填序号)。
A、海水进入贮水池,海水的成分基本不变 B、在蒸发池中,海水中氯化钠的质量逐渐增加 C、析出晶体后的母液是氯化钠的不饱和溶液(2)、配制50g溶质质量分数为10%的氯化钠溶液。①本实验的操作步骤顺序为(填序号)。
a.称量及量取 b.计算 c.溶解 d.装瓶贴标签
②所需氯化钠固体的质量为g。
(3)、用50g质量分数为10%的氧化钠溶液,配制质量分数为5%的氯化钠溶液,需要加水mL(水的密度可近似看做1g/cm3)。若其他操作均正确,量取水时仰视读数,所配溶液的质量分数5%(填“>”、“<”或“=”)。(4)、KCl和NaCl的溶解度曲线如图所示,试回答下列问题:
①t2℃时,将30gKCl固体加入50g水中,充分搅拌后,所得溶液中溶质与溶液的质量比为(最简整数比)。
②将t2℃时等质量的KCl和NaCl的饱和溶液,分别降温至t1℃。所得溶液的质量:前者后者(填“>”、“<”或“=”)。
三、实验探究题
-
18. 控制变量是学习化学的一种科学方法。(1)、用如图1所示实验验证“可燃物燃烧的条件”(白磷和红磷的着火点分别为40℃、240℃)。

①热水的作用是提供热量和。
②由图1实验中的现象,可知燃烧需要温度达到可燃物的着火点。
(2)、用如图2所示实验探究CO2的性质。
①纸花2不变色,纸花3变红,说明二氧化碳(填一条化学性质)。
②纸花3先变红,纸花1后变红,说明二氧化碳(填一条物理性质)。
(3)、用如图3所示实验探究“铁制品锈蚀的条件”。
①实验所用蒸馏水需经煮沸并迅速冷却。煮沸的目的是。
②通过对比甲,乙、丙试管中的现象,说明铁生锈的主要条件是铁与直接接触。
(4)、探究影响H2O2分解速率的因素。分别取5mLH2O2溶液进行实验,测定产生相同体积O2所需时间,实验结果记录如表:
实验序号
H2O2溶液的溶质质量分数/%
温度/C
MnO2粉末用量/g
反应时间/s
a
30
35
0
t1
b
30
55
0
t2
c
5
20
0.1
3
d
15
20
0.1
1
①根据实验a、b中t1t2(填“>”、“=”或“<”)可知:其他条件相同时,温度越高,H2O2分解速率越快。
②能证明H2O2分解速率与H2O2溶液的溶质质量分数有关的实验是(填实验序号)。
四、综合题
-
19. 2023年5月天舟6号货运飞船成功发射,航天员在空间站进行了与多孔铜、镁合金等金属材料相关的实验。(1)、铜能拉成丝,说明铜具有良好的____(填序号)。A、导电性 B、导热性 C、延展性(2)、镁合金的硬度一般比纯镁的硬度(填“大”或“小”)。(3)、设计实验证明镁的金属活动性比铜强,并完成实验报告。
实验步骤
实验现象
实验结论及解释
将用砂纸打磨过的镁条插入中,过一会儿取出,观察
结论:镁的金属活动性比铜强;发生反应的化学方程式为
(4)、将一定质量的镁加入足量稀盐酸中,充分反应后共得到0.6g氢气。请计算参加反应的镁的质量。(利用化学方程式计算,写出完整计算过程。)20. 如图中的A~H表示初中化学常见的物质,且分别由H、C、O、Cl、Ca、Fe、Cu中的一种或几种元素组成,其中D、F、G、H由一种元素组成,A、C、E由两种元素组成,B由三种元素组成,E是最常用的溶剂。图中“一”表示两端的物质间能发生化学反应;“→”表示物质间存在转化关系;反应条件、部分反应物和生成物已略去。 (1)、写出E的化学式:。(2)、写出A和B反应的化学方程式。(3)、写出H和F反应的化学方程式。(4)、写出D→G反应的化学方程式。21. 乙二酸(H2C2O4)俗称草酸,常温下为固体,是生产、生活中常用的漂白剂。加热时,草酸发生分解反应,兴趣小组围绕草酸分解产物开展如下探究。
(1)、写出E的化学式:。(2)、写出A和B反应的化学方程式。(3)、写出H和F反应的化学方程式。(4)、写出D→G反应的化学方程式。21. 乙二酸(H2C2O4)俗称草酸,常温下为固体,是生产、生活中常用的漂白剂。加热时,草酸发生分解反应,兴趣小组围绕草酸分解产物开展如下探究。【查阅资料】①CO与氯化钯(PdCl2)溶液反应生成黑色沉淀,可用于检验CO,反应原理可用化学方程式表示为:PdCl2+CO+H2O=Pd↓+CO2+2HCl;
②浓硫酸可吸水,氢氧化钠溶液可吸收CO2。
(1)、【活动一】探究草酸分解的产物。
兴趣小组设计了如图所示两套实验方案,实验中均观察到PdCl2溶液中出现黑色沉淀和澄清石灰水变浑浊的现象,由此得出“草酸分解产物中有CO和CO2”的结论。你认为方案(填“I”或“II”)不合理,理由是。 (2)、写出澄清石灰水变浑浊的化学方程式。(3)、加热时,草酸(H2C2O4)发生分解反应,生成三种氧化物,生成物的分子个数比为1:1:1,写出该反应的化学方程式。(4)、【活动二】利用草酸分解产物中的CO测定物质的组成。
(2)、写出澄清石灰水变浑浊的化学方程式。(3)、加热时,草酸(H2C2O4)发生分解反应,生成三种氧化物,生成物的分子个数比为1:1:1,写出该反应的化学方程式。(4)、【活动二】利用草酸分解产物中的CO测定物质的组成。兴趣小组设计实验测定某只含铁、氧两种元素的固体样品中铁、氧原子个数比,实验装置如图所示(假设每步反应均完全):

用文字描述装置C中发生反应的原理。
(5)、进行实验并记录实验数据如表所示:计算该固体样品中铁、氧原子的个数比为(最简整数比)。装置
D和E
反应前质量
492.4g
反应后质量
505.6g
(6)、若缺少装置A,利用上述方法测得结果将(填“偏大”、“偏小”或“无影响”,下同);若缺少装置E,测得结果将。
-