重庆市渝北区2023-2024学年九年级上学期期末质量监测化学试题
试卷更新日期:2024-02-20 类型:期末考试
一、选择题
-
1. 《联合国气候变化框架公约》第28届大会以“团结、行动、落实”为主题。下列理念不符合的是A、低碳技术 B、能源转型 C、燃煤发电 D、生态发展2. 渝北剪纸是重庆市第六批市级非物质文化遗产项目。下列工艺过程有化学变化的是A、油灯熏制 B、图案绘制 C、剪刀雕刻 D、剪纸装裱3. 因精确测定铟元素的原子量数据而被国际标准采纳的中国“两院”院士是A、袁隆平 B、张青莲 C、屠呦呦 D、杨振宁4. 规范操作是实验成功的保障。下列实验操作正确的是A、倾倒液体
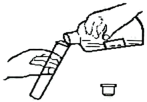 B、滴加液体
B、滴加液体 C、量取液体
C、量取液体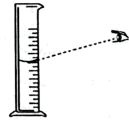 D、过滤液体
D、过滤液体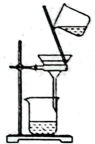 5. 当火灾发生初期,人们迅速将灭火毯覆盖在可燃物上就达到灭火目的,其灭火的原理A、隔绝可燃物 B、降低可燃物的着火点 C、隔绝空气 D、降低温度至可燃物着火点以下6. 下列化学用语中数字“2”所表示的含义理解正确的是A、O2——氧气中有2个氧原子 B、Ca2+——钙元素的化合价为+2价 C、2H ———2个氢元素 D、2NO ——2个一氧化氮分子7. 下列物质的性质与用途,对应关系错误的是A、金刚石硬度大——用于切割大理石 B、氮气的化学性质不活泼——用于霓虹灯 C、石墨具有导电性——用来做电极 D、生石灰与水反应放热——可作发热剂8. 归纳与总结是提炼化学观念的基本方法。下列选项正确的是
5. 当火灾发生初期,人们迅速将灭火毯覆盖在可燃物上就达到灭火目的,其灭火的原理A、隔绝可燃物 B、降低可燃物的着火点 C、隔绝空气 D、降低温度至可燃物着火点以下6. 下列化学用语中数字“2”所表示的含义理解正确的是A、O2——氧气中有2个氧原子 B、Ca2+——钙元素的化合价为+2价 C、2H ———2个氢元素 D、2NO ——2个一氧化氮分子7. 下列物质的性质与用途,对应关系错误的是A、金刚石硬度大——用于切割大理石 B、氮气的化学性质不活泼——用于霓虹灯 C、石墨具有导电性——用来做电极 D、生石灰与水反应放热——可作发热剂8. 归纳与总结是提炼化学观念的基本方法。下列选项正确的是选项
归纳与总结
化学知识
A
化学与概念
①倡导低“碳”生活,这里的“碳”指碳单质
②食用加“碘”食盐,这里的“碘”指碘元素
B
化学与安全
①在煤炉上放一盆水不能防止一氧化碳中毒
②室内起火,立即开窗通风
C
化学与计量
①地壳中含量最多的金属元素:铝
②空气中含量最多的物质:氧气
D
化学与分类
①冰水混合物、干冰、液态氧属于纯净物
②煤、石油、天然气属于化石能源,不可再生
A、A B、B C、C D、D9. 鱼腥草素 是鱼腥草(别名“折耳根”)的主要抗菌成分,对流感杆菌、结核杆菌等有一定抑制作用。常用于慢性气管炎、小儿肺炎等疾病治疗。下列有关鱼腥草素的说法正确的是A、鱼腥草素属于氧化物 B、鱼腥草素由12个碳原子、22个氢原子和2个氧原子构成 C、鱼腥草素分子是由 三种元素组成的 D、鱼腥草素中碳元素的质量分数大于氢元素的质量分数10. 逻辑推理是一种重要的化学科学思维,下列推理正确的是A、化合物中含有多种元素,则含有多种元素的纯净物是化合物 B、燃烧都伴有发光、放热现象,则有发光、放热现象的一定是燃烧 C、单质是由同种元素组成的纯净物,则由同种元素组成的物质一定是单质 D、离子都是带电的粒子,则带电的粒子一定都是离子11. 《天工开物》记载了火井制盐:西川有火井……以长竹剖开去节合缝漆布,一头插入井底,其上曲接,以口紧对釜脐。注卤水釜中,只见火意烘烘,水即滚沸。以下说法不严谨的是A、“火意烘烘”说明反应放热 B、“釜”相当于玻璃烧杯 C、“火井”中可能蕴含天然气 D、“长竹”相当于玻璃导气管12. 日本核污水含有如钻、铀等多种放射性元素,钻元素的相关信息如下图所示,下列说法中错误的是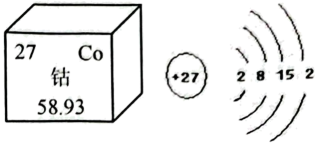 A、钴的原子序数为27 B、钴原子易形成阳离子 C、钴元素位于元素周期表第四周期 D、钴原子的相对原子质量为13. 铝热焊技术常用于钢轨焊接,其反应原理为:。该反应中作还原剂的是A、 B、 C、 D、14. 中国空间站的生命保障系统中,宇航员呼出的二氧化碳的后续反应微观示意图如下,下列说法错误的是
A、钴的原子序数为27 B、钴原子易形成阳离子 C、钴元素位于元素周期表第四周期 D、钴原子的相对原子质量为13. 铝热焊技术常用于钢轨焊接,其反应原理为:。该反应中作还原剂的是A、 B、 C、 D、14. 中国空间站的生命保障系统中,宇航员呼出的二氧化碳的后续反应微观示意图如下,下列说法错误的是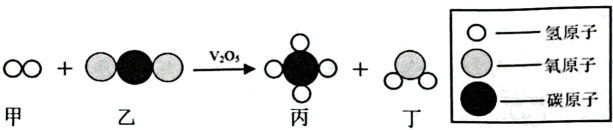 A、丙是由分子构成的物质 B、反应前后化学性质不变 C、反应前后分子的数目不变 D、反应前后原子的种类不变15. 正确设计实验方案是化学实验成功的保证。下列实验方案合理的是
A、丙是由分子构成的物质 B、反应前后化学性质不变 C、反应前后分子的数目不变 D、反应前后原子的种类不变15. 正确设计实验方案是化学实验成功的保证。下列实验方案合理的是选项
实验目的
实验方案
A
比较黄铜和铜的硬度
将两种金属相互刻画
B
检验酒精中含有碳元素
在空气中点燃,在火焰上方罩一个冷而干燥的烧杯
C
除去 溶液中的
加入适量的锌粉,过滤
D
除去中混有的少量
将混合气体点燃
A、A B、B C、C D、D16. 实验室用红磷燃烧来测定空气中氧气的含量,从塞紧橡胶塞到打开弹簧夹前,测得集气瓶中各物理量随时间变化的图像如下,其中图像能正确反应对应过程的有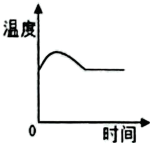
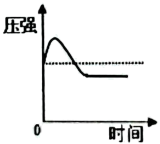
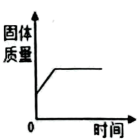

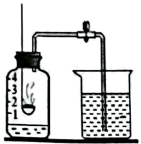 A、4个 B、3个 C、2个 D、1个
A、4个 B、3个 C、2个 D、1个二、填空题
-
17. 海洋中含有80多种化学元素,蕴藏着丰富的化学资源。(1)、海水中含量最多的元素的符号为。(2)、二氧化碳的过量排放会导致海洋酸化,标出二氧化碳中碳元素的化合价。(3)、氯化镁会让海水呈现苦味,氯化镁的化学式为。(4)、碳酸钙(CaCO3)为海底珊瑚的主要成分,其中阴离子的符号为。18. 水是生态之基、生产之要、生命之源。
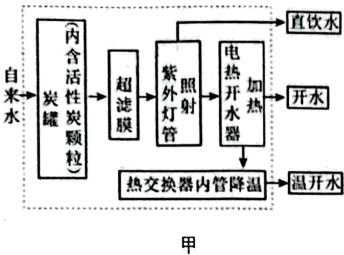

 (1)、目前许多学校安装了直饮水机,其主要工作流程如图。
(1)、目前许多学校安装了直饮水机,其主要工作流程如图。①甲图中紫外灯管照射的作用是。向所得的开水中加入少量肥皂水,充分振荡后观察到的现象是。
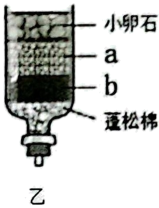
②已知粒径:小卵石石英砂>活性炭,乙图中活性炭应放置在(选填“a”或“b”)层。正确放置后,用此装置充分净化少量山泉水,理论上可得到的“水”是。
A.无泥沙的水 B.无颜色、无气味的水 C.不含钙镁离子的水
(2)、保护环境从我做起。下列做法利于环境保护的是____(填字母)。A、实验室含酸废水未经处理直接倒入铁质下水道 B、生活污水未经处理直接排放 C、收集家里废旧金属至回收站,再利用19. 2023年5月,神舟十六号载人航天飞船成功发射。我国已实现空间站氧气资源再生。国际空间站曾用高压氧气瓶、固体燃料氧气发生器(又称“氧烛”)等方法供氧。 (1)、氧气可被加压储存,说明分子间有。(2)、电解水供氧,在外接电源的(填“正”或“负”)极端收集。(3)、如图“氧烛”模型中产氧药块主要成分为氯酸钠 和金属粉末。 与 性质相似。写出它在催化剂并加热条件下反应的化学方程式。金属粉末发生氧化反应会(“放出”或“吸收”)热量,促进 反应,保证放氧自动完成。20. 第19届亚洲运动会在杭州开幕。开幕式上数实融合点燃主火炬的一幕令人印象深刻。
(1)、氧气可被加压储存,说明分子间有。(2)、电解水供氧,在外接电源的(填“正”或“负”)极端收集。(3)、如图“氧烛”模型中产氧药块主要成分为氯酸钠 和金属粉末。 与 性质相似。写出它在催化剂并加热条件下反应的化学方程式。金属粉末发生氧化反应会(“放出”或“吸收”)热量,促进 反应,保证放氧自动完成。20. 第19届亚洲运动会在杭州开幕。开幕式上数实融合点燃主火炬的一幕令人印象深刻。
 (1)、①“薪火”火炬炬身金属为铝合金,该材料不具有性能为。
(1)、①“薪火”火炬炬身金属为铝合金,该材料不具有性能为。A.质轻 B.硬度大 C.熔点低
②铝具有良好的抗腐蚀性的原因(用化学方程式表示)。
(2)、①火炬整体庄重大气、造型和配色优雅。铝金属表面先后经历多道工序,其中包含盐酸腐蚀雕刻。其发生反应的化学方程式为。②设计可行的实验方案验证铝、铜的金属活动性强弱。现有药品:铝丝、铜丝、硫酸铜溶液和稀硫酸。(金属均已打磨,且大小形状相同)
实验操作
实验现象
实验结论
铝的金属活动性比铜强
(3)、①火炬使用的一种液体燃料——“零碳甲醇” , 它的燃烧产物没有硫氧化物和氮氧化物,因此被誉为“绿色燃料”。化学方程式 , 的化学式为。②下列不属于新能源的是(填字母)。
A.石油 B.潮汐能 C.地热能
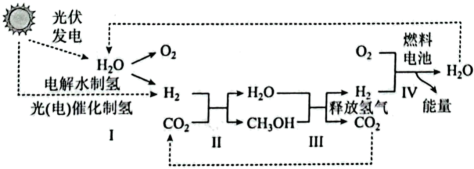
(4)、围绕“绿色、智能、节俭、文明”办赛理念。科研团队利用催化剂 实现 、高效催化 加氢制备“零碳甲醇”的工艺。如图所示①下列有关说法正确的是(填字母)。
A.电解水可以证实水是由氢、氧元素组成
B.燃煤脱硫有利于实现“碳中和”
C.积极鼓励植树造林,降低空气中 含量
②工艺生产过程中反应Ⅱ的化学方程式为。
③理论上反应Ⅰ消耗的 中氢元素质量(填“>” “”或“”)反应 生成的甲醇中氢元素质量。
21. 硅是现代信息技术的基础材料,高纯硅可制芯片。用石英砂(主要成分 )制备高纯硅的模拟工艺如下,回答下列问题。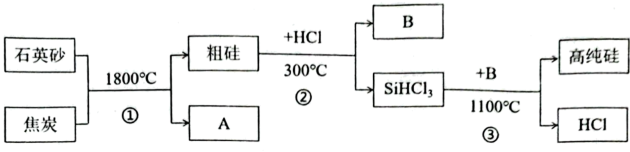
已知:Ⅰ.粗硅、高纯硅主要成分均是单质硅。
是可燃气体,B是密度小于空气的单质。
(1)、①反应前需要粉碎处理,是为了增大接触面积,使。(2)、物质 A是 , 上述流程中可以循环利用的物质是(填一种)。(3)、请写出步骤②的化学方程式。三、实验题
-
22. 实验是化学的学科属性。
 (1)、结合下图回答问题。
(1)、结合下图回答问题。①写出仪器甲的名称。
②小明用装置 A制备氧气,该反应的化学方程式为 , 若用 作为收集装置,则验满的方法是。
③实验室制备二氧化碳的化学方程式为 , 应选择发生装置;若用 C装置检验二氧化碳,将生成的气体从管口(选填“ ”或“b”)通入。实验室若用 装置制取氧气,则发生反应的化学方程式为。
(2)、图 是用“碎碎冰”软塑料管自制的气体发生装置,利用该装置也可以制取 气体,药品加入完毕后(药品量如图 ),为了使反应发生,接下来的操作是。(3)、如图所示,某小组收集了三瓶 气体(集气瓶体积大小相同),分别加入 体积的试剂。甲、乙立即塞紧瓶塞,丙敞口,均振荡一会儿(水的挥发忽略不计),乙中微观示意图如图。
则表示甲图的是(填下图中的字母,下同),表示丙图的是。此时,甲,乙、丙中气体压强由大到小的顺序是。
A、
 B、
B、 C、
C、 23. 下图是现行初中化学教材中的几个常见实验,请回答问题。
23. 下图是现行初中化学教材中的几个常见实验,请回答问题。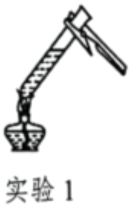
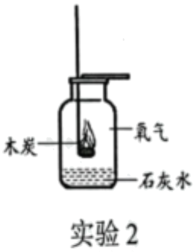
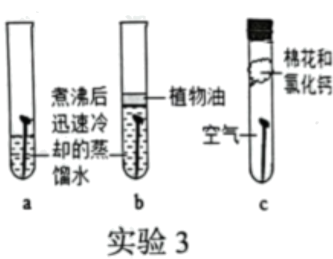 (1)、实验1中试管内液体过多,液体不应超过试管容积的。(2)、实验2中可观察到和石灰水变浑浊的现象,写出石灰水变浑浊的化学方程式。(3)、实验3运用控制变量思维探究铁钉生锈的条件。对比 说明铁生锈需要的物质是;对比a、c说明铁生锈需要的物质是。24. 是初中化学常见气体,实验室常用制备。
(1)、实验1中试管内液体过多,液体不应超过试管容积的。(2)、实验2中可观察到和石灰水变浑浊的现象,写出石灰水变浑浊的化学方程式。(3)、实验3运用控制变量思维探究铁钉生锈的条件。对比 说明铁生锈需要的物质是;对比a、c说明铁生锈需要的物质是。24. 是初中化学常见气体,实验室常用制备。某同学为了探究 的还原性,设计如下图所示的实验。
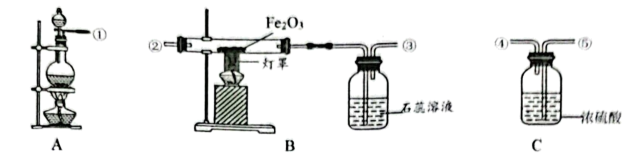
根据所学知识回答下列问题。
已知:是被逐步被还原的,铁元素的化合价逐渐降低,最后为0价。
(1)、装置烧瓶中的反应,浓硫酸起作脱水、吸水和作用,为了保证实验的安全和成功,上图中各装置连接顺序(以气流方向)为(用数字表示)。(2)、随着反应进行,装置可观察到红色粉末变黑和的现象。(3)、为了探究反应后 装置中黑色粉末的成分,他补充了如下探究:
【查阅资料】 铁的氧化物主要有 (黑色)、(红棕色)、(黑色);很不稳定,极易与氧气反应生成其他氧化物;
【资料分析】
由资料推知,黑色固体的成分中(填“有”或“没有”) 。
(4)、【猜测成分】① ② ③和【综合】取少许粉末加入稀硫酸,粉末逐渐溶解且有气泡产生,则猜测不成立。为了进一步探究黑色产物成分,请你从定量角度设计实验方案,简述为。
四、计算题