2024中考一轮总复习 第31课时 生活中常见的盐
试卷更新日期:2024-02-18 类型:一轮复习
一、选择题
-
1. 下列物质按酸、碱、盐的顺序排列的是( )。A、Mg(OH)2、CuSO4、H2CO3 B、HNO3、KOH、NaCl C、CaCO3、NaOH、H3PO4 D、H2SO4、KNO3、NaOH2. 在发酵面团中加入含下列某种物质的溶液揉和,既能除去面团中的酸,又能使蒸出的馒头疏松多孔。这种物质是( )A、Na2CO3 B、Ca(OH)2 C、CaO D、NaCl3. 食盐、食醋、纯碱等均为家庭厨房中常用的物质,利用这些物质你能完成的实验是( )
①除去热水瓶中的水垢②鉴别食盐和纯碱③检验鸡蛋壳能否溶于酸.
A、①② B、①③ C、① D、①②③4. 下列各种盐中属于不溶于水但能溶于酸的( )A、氯化钡 B、碳酸钙 C、硫酸钡 D、硝酸银5. 下列说法不正确的是( )A、冬季向公路上的积雪撒盐,可以加速冰雪的融化 B、块状碳酸钙可做补钙剂 C、硝酸铵溶于水制成的冰袋可以给发烧病人降温 D、厨房洗涤剂有溶解油污的作用6. 下列做法不会导致中毒的是( )A、用氯化钠配制生理盐水 B、用工业用盐亚硝酸钠烹调食物 C、用工业酒精配制白酒 D、用胆矾对饮用井水消毒、杀菌7. 根据复分解反应发生的条件判断,下列不能发生复分解反应的是( )A、 AgNO3与AlCl3 B、HNO3与K2 CO3 C、Cu(OH)2与HNO3 D、MgCl2与ZnSO48. 分别将下列各组物质,同时加到水中,一定有沉淀生成的是( )A、FeCl3 , KOH,稀盐酸 B、Na2CO3 , 稀H2SO4 , KNO3 C、AgNO3 , NaCl,稀HNO3 D、CuSO4 , MgCl2 , 稀盐酸9. 用括号内的物质不能区分的一组是()A、NaCl、NaOH、NH4NO3三种固体 (水) B、K2CO3、Na2SO4、BaCl2三种溶液 (稀硫酸) C、铁粉、碳粉、氧化铜粉末 (稀盐酸) D、CaCl2、Ba(OH)2、HNO3三种溶液 (K2CO3溶液)10. 能在同一溶液中大量共存,且溶液为无色透明的一组物质是( )
A、FeCl3 , CuSO4 , NaCl B、BaCl2、Na2SO4、NaOH C、CaCl2、NaNO3、AgNO3 D、K2SO4、NaNO3、NH4Cl11. 下列实验操作中(括号内为待检验物质或杂质),不能达到实验目的的是( )选项
物质
目的
主要实验操作
A
CaCO3(CaCl2)粉末
除杂
加入足量的稀盐酸,过滤
B
SO2 和CO2
鉴别
将气体通入紫红色高锰酸钾溶液,观察现象
C
C(Fe)粉末
检验
取样,滴入适量稀硫酸
D
NaCl、FeCl3的混合溶液
分离
溶解、加过量NaOH溶液、过滤、洗涤、分别向滤渣和滤液中滴加适量稀盐酸
A、A B、B C、C D、D12. 已知常温下许多盐的水溶液(如硫酸钠)呈中性。现有硫酸与CuSO4的混合溶液,向其中逐渐加入过量的下列某种物质X,溶液的pH随加入物质X的量的变化关系如图所示,则X可能是( ) A、氯化钡溶液 B、烧碱溶液 C、稀盐酸 D、碳酸钙
A、氯化钡溶液 B、烧碱溶液 C、稀盐酸 D、碳酸钙二、填空题
-
13. 下列物质组合能发生复分解反应的有。(填序号)
①K2CO3+CaCl2
②H2SO4+KCl
③CuO+HCl
④Fe+CuSO4
⑤CO2+NaOH
⑥K2SO4+BaCl2
⑦BaCO3+NaOH
14. 松花蛋又名皮蛋,微山湖出产的松花蛋因色味具佳享誉齐鲁.松花蛋的制作工艺一般是用水将灰料[主要是生石灰(CaO)、纯碱(Na2CO3)、食盐(NaCl)等]调成糊状,涂于新鲜鸭蛋,密封保存一段时间后,即可得到松花蛋.请根据以上信息回答:①松花蛋腌制中共发生个化学反应,写出其中属于化合反应的化学反应化学方程式: .
②剥除松花蛋外边灰料后,常常发现蛋壳上有一些坚硬的不溶于水的白色斑点,这斑点的主要成分是 , 写出这种成分与盐酸反应的化学方程式: .
③食用劣质松花蛋时往往有涩味,食用时如何除去涩味?可以加 .
④取制松花蛋的糊状物放入水中充分溶解后过滤得滤液甲,则滤液甲中一定含 , 可能含 .
15. 如何设计实验证明氢氧化钠溶液的变质程度?(请写出操作、现象、结论)操作
可能出现现象
结论
② 取适量液体,加入足量的氯化钡溶液,振荡
②静置操作①后的液体,取上层的清夜,滴加几滴酚酞溶液,振荡
①没有出现浑浊
②酚酞溶液变红
①②
部分变质
①②
由此小明联想到实验室里的一些药品必须密封保存.实验室中必须密封保存的药品可分为以下几类:
①药品能与空气中的成分发生反应,如澄清的石灰水;
②药品具有挥发性,如;
③ , 如浓硫酸.
16. 无土栽培是利用营养液栽培作物的一种方法.现有一种无色的营养液,可能由KNO3、Ca(NO3)2、K2CO3、KCl中的一种或几种物质组成,为探究其成分,某同学设计并完成了如图所示的实验.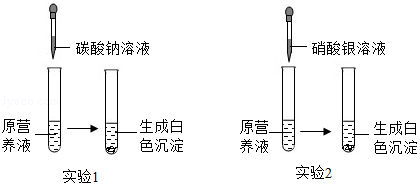
根据以上实验,请你进行有关推断.
①由实验1可确定原营养液中一定没有的物质是;
②根据实验1、实验2推测原营养液的组成可能有种情况;
③若测得原营养液中K+和Cl﹣的数目之比为3:1,则原营养液的组成中的溶质 .
三、综合题
-
17. 海水的综合利用流程图如下:
 (1)、(一)利用海水制取精盐
(1)、(一)利用海水制取精盐海水在阳光与风力作用下逐渐析出粗盐,该步骤类似于实验室的 结晶。
(2)、粗盐晶体中常常含有泥沙、CaCl2、MgSO4杂质,一系列步骤包含溶解、加入化学试剂、过滤、用稀盐酸调节pH值至7,然后再蒸发结晶。其中加入的化学试剂必须过量其目的主要是 。此时用 除去CaCl2 , 用除去MgSO4。(3)、除去CaCl2、MgSO4从合理安排的角度来讲它们被除去的先后顺序为 。A、先除CaCl2后除MgSO4 B、先除MgSO4后除CaCl2(4)、用稀盐酸调节pH等于7的目的是除去过量的杂质,所发生的化学反应基本类型是 。A、中和反应 B、置换反应 C、复分解反应(5)、(二)镁的生产工业中用石灰乳与母液反应得到Mg(OH)2一般不用澄清的石灰水,其原因是 。
(6)、步骤③中通过观察到 现象证明稀HCl过量。(7)、电解熔融的氯化镁可以得到金属镁,此过程的反应方程式为 。四、推断题
-
18. 如图表示物质间转化关系(反应条件和部分产物已略)。常温下A、C是由相同元素组成的无色液体,且A具有消毒杀菌作用:D、I、J均为无色气体,其中I能使澄清的石灰水变浑浊;K为红棕色粉末。请回答下列问题:
 (1)、反应①中B物质的作用是。(2)、图中标出的反应①到⑦中是化合反应的是(填序号)。(3)、在图中标出的12种物质中,单质有种。(4)、反应③中的现象是。(5)、⑤是反应(填“放热”或者“吸热”)(6)、写出反应⑥的化学方程式。
(1)、反应①中B物质的作用是。(2)、图中标出的反应①到⑦中是化合反应的是(填序号)。(3)、在图中标出的12种物质中,单质有种。(4)、反应③中的现象是。(5)、⑤是反应(填“放热”或者“吸热”)(6)、写出反应⑥的化学方程式。五、实验探究题
-
19. 某化学兴趣小组同学发现实验台上整齐摆放的药品中(见下图),有一试剂瓶的标签破损。

[提出问题]这瓶试剂的成分是什么?
(1)、[讨论]根据受损标签及实验室药品分类摆放的原则,这瓶试剂不可能是 。(填字母序号)A、酸 B、碱 C、盐(2)、[猜想]①可能是NaOH溶液;②可能是Na2CO3溶液;③可能是(任写一种)溶液。(3)、[设计并实验]小明用洁净干燥的玻璃棒蘸取该溶液滴到湿润的pH试纸上,测得pH=10,他判断这是一种碱性溶液。对他的操作方法、测量结果及结论的评价,正确的是 。(填字母序号)
A、方法正确,结果正确,且结论正确 B、方法不正确,结果偏小,但结论正确 C、方法不正确,结果偏大,结论不正确 D、方法正确,结果正确,但结论不正确(4)、小明认为它是氢氧化钠溶液,小俊认为它是碳酸钠溶液。要进一步确定它的成分,小俊认为只需选择上图已有的试剂就能把它鉴别出来。他们又进行了如下实验:操作步骤
实验现象
结论及化学方程式
取样放入试管中,
猜想②正确,相关的化学方程式为
-
-