2024中考一轮总复习 第24课时 金属资源的利用与保护
试卷更新日期:2024-02-18 类型:一轮复习
一、选择题
-
1. “绿水青山就是金山银山”,垃圾分类处理有利于生态文明建设。废弃物中,易拉罐属于( )A、可回收物 B、餐厨垃圾 C、有害垃圾 D、其它垃圾2. 下列物品中,由金属材料制成的是( )A、纯棉毛巾 B、铁制剪刀 C、橡胶导管 D、陶瓷坩埚3. 地壳中含量最多的非金属元素和金属元素组成化合物的化学式是( )A、 B、 C、 D、4. 下列有关金属材料的说法错误的是( )A、在潮湿的空气中铁易生绣 B、金属的回收利用是保护金属资源的有效途径之一 C、铁和金的化学性质都很稳定,都有很好的抗腐蚀性 D、高炉炼铁的原理是在高温条件下,用一氧化碳把铁从铁矿石里还原出来5. 下列有关对自行车的做法不合理的是( )A、车架表面喷涂油漆 B、钢圈表面镀防护金属 C、露天放置,日晒雨淋 D、链条表面涂机油6. 下列关于铁的冶炼的说法错误的是( )。A、把铁矿石、焦炭和石灰石一起加入高炉 B、石灰石的主要作用是将矿石中的二氧化硅转变成炉渣 C、生铁的含碳量为2%~4.3%,钢的含碳量为0.03%~2% D、在反应过程中,Fe2O3作还原剂,被氧化7. 下列有关资源、能源的叙述正确的是( )A、海洋是巨大的资源宝库,其中含有80多种物质 B、目前,世界上已有90%以上的铁和50%以上的金得到了回收利用 C、废旧金属的回收利用,可节约金属资源,减少对环境的污染 D、金属资源广泛存在于地壳中,人类每年从自然界中提取最多的金属是铝8. 为了探究铁的锈蚀,同学们设计并完成了如图的家庭小实验,表明实验取得成功的现象是红墨水液面( )
 A、两端持平 B、左高右低 C、左低右高 D、无法判断9. 关于金属,下列说法中,错误的是( )A、中国古代的湿法炼铜,原理是:Fe+CuSO4=FeSO4+Cu B、常见铁容器不能用来盛放酸溶液,会被腐蚀 C、自行车的车架,可以通过涂油层来防止其生锈 D、家里的菜刀,成分基本都是钢,属于铁合金10. 某化学兴趣小组探究铁生锈实验,取一块废旧铁丝网,将铁丝网剪成几小片,用稀盐酸除去铁锈后,放入锥形瓶中、在锥形瓶中加入3~4mL浓食盐水,塞紧带导管的单孔塞后,将导管的另一端伸入滴有红墨水的水中,下列说法中错误的是( )
A、两端持平 B、左高右低 C、左低右高 D、无法判断9. 关于金属,下列说法中,错误的是( )A、中国古代的湿法炼铜,原理是:Fe+CuSO4=FeSO4+Cu B、常见铁容器不能用来盛放酸溶液,会被腐蚀 C、自行车的车架,可以通过涂油层来防止其生锈 D、家里的菜刀,成分基本都是钢,属于铁合金10. 某化学兴趣小组探究铁生锈实验,取一块废旧铁丝网,将铁丝网剪成几小片,用稀盐酸除去铁锈后,放入锥形瓶中、在锥形瓶中加入3~4mL浓食盐水,塞紧带导管的单孔塞后,将导管的另一端伸入滴有红墨水的水中,下列说法中错误的是( )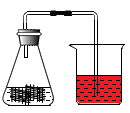 A、浓食盐水的作用是加快铁丝网生锈 B、水中滴加红墨水,便于观察实验现象 C、实验过程中,烧杯中的导管口会冒气泡 D、一段时间后,铁丝表面出现红棕色物质11. 下图是探究铁钉锈蚀条件的4个实验,一段时间后观察现象。下列说法错误的是( )
A、浓食盐水的作用是加快铁丝网生锈 B、水中滴加红墨水,便于观察实验现象 C、实验过程中,烧杯中的导管口会冒气泡 D、一段时间后,铁丝表面出现红棕色物质11. 下图是探究铁钉锈蚀条件的4个实验,一段时间后观察现象。下列说法错误的是( )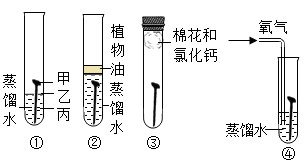 A、①中甲、乙、丙三处比较,生锈最明显的地方是甲 B、①②对比说明铁生锈需要空气,①③对比说明铁生锈需要水 C、③中附着在棉花上的氯化钙的作用是作干燥剂 D、四个实验中,生锈最快的是④中的铁钉12. 小明将未经砂纸打磨的铝条放入盛有稀盐酸的密闭容器中,用压强传感器测得容器内压强和反应时间的变化曲线如图所示,下列分析正确的是()
A、①中甲、乙、丙三处比较,生锈最明显的地方是甲 B、①②对比说明铁生锈需要空气,①③对比说明铁生锈需要水 C、③中附着在棉花上的氯化钙的作用是作干燥剂 D、四个实验中,生锈最快的是④中的铁钉12. 小明将未经砂纸打磨的铝条放入盛有稀盐酸的密闭容器中,用压强传感器测得容器内压强和反应时间的变化曲线如图所示,下列分析正确的是()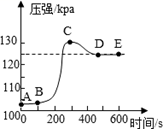 A、AB段表示铝与盐酸反应 B、CD段压强变化的主要影响因素是温度 C、C点生成的氢气质量大于D点 D、D点处反应刚好结束
A、AB段表示铝与盐酸反应 B、CD段压强变化的主要影响因素是温度 C、C点生成的氢气质量大于D点 D、D点处反应刚好结束二、填空题
-
13. 为了防治月饼变质,通常在月饼的包装中放入一小袋的“防腐剂”,这种“防腐剂”的是铁粉.试分析这种防腐剂防止月饼变质的化学原理 .14. 地球上金属资源广泛地存在于和中,除少数很不活泼的金属、等有单质形式存在外,其余都以化合物形式存在,如铁、铜等,它们主要存在于矿石中,而把矿石冶炼成金属则是一个复杂的过程.如工厂用赤铁矿炼铁,其反应设备是 , 原料是 , 试写出反应设备中由下往上的化学方程式:、 , .15. 保护金属资源的途径有:①防止;②废旧金属的;③有计划、合理地开采金属;④寻找金属的 .16. 国庆佳节家人团聚,丰盛的家宴自然少不了鱼.炖鱼后锅内会残留较多的油渍,可以加入洗涤剂清洗,是利用洗涤剂具有作用,家用铁锅多为生铁,用完后擦洗不净常会生锈,铁锈主要成分的化学式为;在铁锅表面加膜不仅起到不粘锅,而且还能防止锅内表面生锈,其防锈原理是;家宴自然也少不了同学们爱喝的可乐,当打开可乐时常会有液体溢出的现象,是因为可乐中溶有二氧化碳气体,打开瓶盖后减小,减小,气体逸出将可乐带出.
 17. 生活中处处有化学.铁锅是厨房中常用的炊具,请用所学的化学知识填空.
17. 生活中处处有化学.铁锅是厨房中常用的炊具,请用所学的化学知识填空.①铁锅作炊具主要是利用铁的性.
②铁锅手柄上使用的塑料应具有性(填“热塑”或“热固”).
③使用铁锅有利于人体健康,主要是因为 .
④请你说出一个厨房中防止铁锅生锈的方法 .
 18. 食品包装学问大
18. 食品包装学问大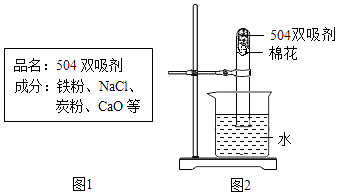
①我区特产﹣﹣嘶马羊耳采用真空包装,延长了食品的保质期,原理是;
②如图1所示是“504双吸剂”的标签,请问答下列问题:
a.其中至少含有种单质;
b.为测定此双吸剂的使用效果,取足量双吸剂做了如图2所示的实验,一段时间后,进入试管中水的体积21%(填“>”、“<”或“=”),理由是;
c.部分失效的双吸剂中,有红棕色固体,其主要是(填化学式);
d.此双吸剂中,NaCl的作用可能是 .
三、综合题
-
19. 我国劳动人民早在春秋战国时期就已经懂得钢铁冶炼,铁也是生活中使用最为广泛的金属,目前我国钢铁产量已经位居世界第一.下面是一组有关铁的问题,请你用所学化学知识加以回答:(1)、铁是地壳中含量第位的元素;(2)、铁可以拉成铁丝,压成铁片,这是利用了铁的性;在公路上行驶的油罐车尾部经常有一条铁链拖在地面上,这是利用了铁的性;家里铁制炊具要有木柄或塑料柄,这是因为铁有很好的性;(3)、焊接钢管时,经常用硫酸铜溶液在钢管表面画交叉线,然后根据出现的红线对准焊接,用化学方程式表示反应原理 .(4)、颗粒大小达到纳米级的单质铁具有很强的反应活性,俗称纳米铁.在高温环境下,用H2和FeCl2反应,可以生成纳米铁和一种易溶于水显强酸性的气体,写出该反应的化学方程式 , 纳米铁粉在空气中受撞击时会燃烧,生成一种黑色固体,写出该反应的化学方程式 . 请你写出纳米铁和稀盐酸反应的化学反应方程式 .20. 化学新材料的应用,使人们的生活质量不断提高,如图是不同年代常用的水管
 (1)、图示水管中,含有的金属元素是 ,(2)、铸铁管容易生锈,工业上常用稀盐酸来除铁锈(Fe2O3),该反应的化学方程式是 . 请你提出一种防止铁制品腐蚀的方法: .(3)、由水管所用材料的变迁,你得到的启示是 .21. 请你参与某学习小组的探究活动,并回答相关问题:
(1)、图示水管中,含有的金属元素是 ,(2)、铸铁管容易生锈,工业上常用稀盐酸来除铁锈(Fe2O3),该反应的化学方程式是 . 请你提出一种防止铁制品腐蚀的方法: .(3)、由水管所用材料的变迁,你得到的启示是 .21. 请你参与某学习小组的探究活动,并回答相关问题:[发现问题]王馨悦同学发现盛水的铁锅在与水面接触的部位最易生锈;程后乐同学发现自己的铜制眼框表面出现了绿色的铜锈;顾浩宇同学发现苹果切开不久,果肉上会产生一层咖啡色物质,好象生了“锈”一般.
[提出问题]这三种物质“生锈”的原因是什么?
[收集证据]回忆已有知识:铁生锈的实质是铁与发生反应.
[查阅有关资料]“铜锈”主要成分是Cu2(OH)2CO3(俗称铜绿);苹果“生锈”是果肉里的物质(酚和酶)与空气中的氧气发生了一系列的反应,生成咖啡色的物质.碱石灰能吸水与二氧化碳.
[实验探究]将四小块铜片分别按下图所示放置较长时间,观察现象如下:
实验装置

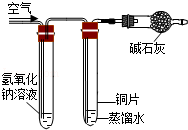

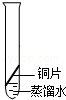
实验现象
铜片不生锈
铜片不生锈
铜片不生锈
铜片生锈且水面附近锈蚀最严重
由实验可知,铜生锈是铜与水、、等物质共同作用的结果.这个反应的化学方程式
为属反应.
[得出结论]三位同学认为这些物质“生锈”除了可能与水有关外,还可能都与(填物质名称)有关.
[反思与应用]利用所得结论填空:写出一种防止铁或铜等金属制品生锈的具体方法;请你提出一条延长食品保质期的建议 .
四、实验探究题
-
22. 如图是一氧化碳还原氧化铁实验装置图,回答下列问题:
 (1)、①C装置中反应的化学方程式为;尾气处理的目的是 .
(1)、①C装置中反应的化学方程式为;尾气处理的目的是 .②关于该实验的说法正确的是(填字母)
A.装置B处玻璃管内黑色粉末变红
B.实验结束后,应先熄灭B处的酒精喷灯
C.B处玻璃管内反应铁元素化合价升高
③实验结束后,若要确定B装置玻璃管里固体生成铁,请设计合理的实验方案
实验步骤
现象
结论
说明生成铁
(2)、每年因腐蚀而浪费掉的金属材料数量惊人,铁栅栏常采取的防锈措施是 , 除防止金属腐蚀外,保护金属资源的有效途径还有(答一点即可)(3)、工业炼铁会产生二氧化硫,烟气脱硫工艺不仅能消除二氧化硫,还能将其转化为硫酸钙(CaSO4)等产品,实现“变废为宝”.反应的化学方程式为:2CaCO3+O2+2SO2═2CaSO4+2CO2 , 现用1.25t含碳酸钙80%的石灰石吸收烟气中的二氧化硫.试求可吸收二氧化硫的质量.23. 兔首和鼠首均为青铜器(铜、锡合金)如图所示,某些铜器表面呈绿色,这是铜器长期曝露在空气中生了铜渍。为了弄清“铜绿”的组成和铜生成“铜绿”的条件,某化学实验小组进行了如下探究: (1)、【查阅资料】了解到这层绣渍的化学成分是碱式碳酸铜[Cu2(OH)2CO3]俗称“铜绿”。它受热会分解生成三种氧化物。“铜绿”分解的化学方程式为。(2)、【猜想与假设】经仔细了解了水龙头的使用环境后,据“铜绿”的组成和查阅的资料判断,铜绿可能是铜与氧气及、共同作用而生成的。(3)、【设计与实验】借鉴课本“铁制品锈蚀条件”的探究实验,小刚设计了“铜片锈蚀条件的探究”实验,实验如下图所示(所用铜片洁净、光亮,试管内的为图片)
(1)、【查阅资料】了解到这层绣渍的化学成分是碱式碳酸铜[Cu2(OH)2CO3]俗称“铜绿”。它受热会分解生成三种氧化物。“铜绿”分解的化学方程式为。(2)、【猜想与假设】经仔细了解了水龙头的使用环境后,据“铜绿”的组成和查阅的资料判断,铜绿可能是铜与氧气及、共同作用而生成的。(3)、【设计与实验】借鉴课本“铁制品锈蚀条件”的探究实验,小刚设计了“铜片锈蚀条件的探究”实验,实验如下图所示(所用铜片洁净、光亮,试管内的为图片)
实验较长时间后,发现试管中铜片最先生锈(填写试管字母编号)。
(4)、【评价与改进】小明认为小刚设计的实验还不够完善,要得出正确的结论,还要补充一个实验。你认为要补充的一个实验是(用图表示亦可):。(5)、【拓展与应用】小红从不同地点收集到两个铜器(一个是纯铜做的,一个是青铜做的)中,纯铜器的铜绿比青铜器的少,他据此分析认为青铜比纯铜易锈蚀。小红的分析是否全面?请你说明理由:24. 某金属冶炼厂的管道烟泥中含有某些金属,随机取样对烟泥进行分析.由下表中的数据可知,在烟泥中含有的铜、锌以及能造成污染的硫.因此从效益和环保角度出发应考虑把铜、锌回收利用,并对硫进行适当的处理.
编号
Cu
Zn
S
1
10.3%
5.0%
1.2%
2
11.5%
4.9%
1.8%
3
12.4%
10.3%
0.9%
[设计方案]
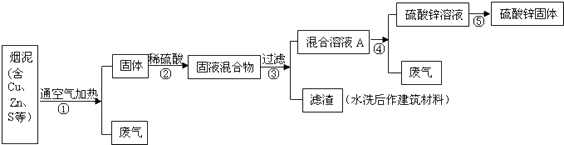 (1)、步骤①②中含铜元素的物质发生反应的化学方程式:
(1)、步骤①②中含铜元素的物质发生反应的化学方程式:①、②
(2)、写出本方案中处理废气的方法(用化学方程式表示): .(3)、步骤⑤中所用的操作方法是: .(4)、在步骤④中,可选用试剂从混合溶液A中得到铜.五、计算题
-
25. 某炼铁厂用赤铁矿石冶炼生铁.若要炼出1120t含铁95%的生铁,需要含氧化铁80%的赤铁矿石多少吨?(Fe2O3+3CO 2Fe+3CO2)