2024中考一轮总复习 第15课时 化学方程式
试卷更新日期:2024-02-18 类型:一轮复习
一、选择题
-
1. 如图是四位同学正在讨论某一化学方程式表示的意义,他们所描述的化学方程式是()
 A、 B、 C、 D、2. 化学方程式 配平后a、b、c、d的数值为( )A、1、2、1、2 B、2、5、2、4 C、4、5、2、4 D、1、3、1、23. 下列化学方程式的书写和对应的基本反应类型都正确的是( )A、化合反应 B、分解反应 C、置换反应 D、氧化反应4. 下列有关叙述和对应的化学方程式所属基本反应类型都正确的是( )A、溶洞的形成:化合反应 B、工业上用石灰石制取熟石灰:分解反应 C、氢氧化镁治疗胃酸过多:中和反应 D、纯碱制烧碱复分解反应5. 下列应用和相应的原理(用化学方程式表示)及基本反应类型都正确的是( )A、金属铝放罝在空气中形成氧化膜 4Al + 3O2 =2Al2O3 氧化反应 B、用氢氧化铝治疗胃酸过多症 Al(OH)3 +3HCl=AlCl3 +H2O 复分解反应 C、比较铜和银的活动性强弱 Cu +2AgCl = CuCl2 +2Ag 置换反应 D、用盐酸除铁锈 Fe2O3 +6HCl=2FeCl3 +3H2O 复分解反应6. 下列反应的化学方程式书写正确的是()A、炼铁时用一氧化碳还原氧化铁:
A、 B、 C、 D、2. 化学方程式 配平后a、b、c、d的数值为( )A、1、2、1、2 B、2、5、2、4 C、4、5、2、4 D、1、3、1、23. 下列化学方程式的书写和对应的基本反应类型都正确的是( )A、化合反应 B、分解反应 C、置换反应 D、氧化反应4. 下列有关叙述和对应的化学方程式所属基本反应类型都正确的是( )A、溶洞的形成:化合反应 B、工业上用石灰石制取熟石灰:分解反应 C、氢氧化镁治疗胃酸过多:中和反应 D、纯碱制烧碱复分解反应5. 下列应用和相应的原理(用化学方程式表示)及基本反应类型都正确的是( )A、金属铝放罝在空气中形成氧化膜 4Al + 3O2 =2Al2O3 氧化反应 B、用氢氧化铝治疗胃酸过多症 Al(OH)3 +3HCl=AlCl3 +H2O 复分解反应 C、比较铜和银的活动性强弱 Cu +2AgCl = CuCl2 +2Ag 置换反应 D、用盐酸除铁锈 Fe2O3 +6HCl=2FeCl3 +3H2O 复分解反应6. 下列反应的化学方程式书写正确的是()A、炼铁时用一氧化碳还原氧化铁: B、镁在空气中燃烧:
B、镁在空气中燃烧: 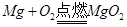 C、铁放入盐酸中反应:
C、铁放入盐酸中反应: 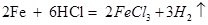 D、实验室制取二氧化碳:
D、实验室制取二氧化碳:  7. 下列有关叙述和对应的化学方程式均正确的是 ( )A、用含氢氧化镁的药物治疗胃酸过多症
7. 下列有关叙述和对应的化学方程式均正确的是 ( )A、用含氢氧化镁的药物治疗胃酸过多症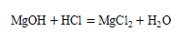 B、正常雨水显酸
B、正常雨水显酸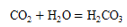 C、比较铜和银的金属活动性
C、比较铜和银的金属活动性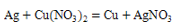 D、乙醇燃烧
D、乙醇燃烧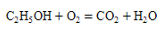 8. 下列指定反应的化学方程式正确的是( )A、实验室用双氧水制氧气: B、碳酸氢铵受热分解: C、铁丝和稀盐酸反应: D、电解饱和食盐水:9. 中国将采取更加有力的措施努力争取2060年前实现碳中和。一种CO2的“捕捉”和转化过程如下:在高压时将烟道气中CO2溶于甲醇(CH3OH)中,得到二氧化碳的甲醇溶液;用“捕捉”到的二氧化碳与氢气在一定条件下生产甲醇,同时生成水。下列说法错误的是( )A、整个过程有助于减少温室气体排放 B、二氧化碳中碳元素的化合价为+4 C、转化过程中的“一定条件”可能需要合适的催化剂 D、转化过程中发生反应的化学方程式为
8. 下列指定反应的化学方程式正确的是( )A、实验室用双氧水制氧气: B、碳酸氢铵受热分解: C、铁丝和稀盐酸反应: D、电解饱和食盐水:9. 中国将采取更加有力的措施努力争取2060年前实现碳中和。一种CO2的“捕捉”和转化过程如下:在高压时将烟道气中CO2溶于甲醇(CH3OH)中,得到二氧化碳的甲醇溶液;用“捕捉”到的二氧化碳与氢气在一定条件下生产甲醇,同时生成水。下列说法错误的是( )A、整个过程有助于减少温室气体排放 B、二氧化碳中碳元素的化合价为+4 C、转化过程中的“一定条件”可能需要合适的催化剂 D、转化过程中发生反应的化学方程式为二、填空题
-
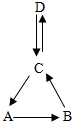
10. 天然气的主要成分完全燃烧的化学方程式为;氢气作为最理想的新能源的优点是(答出一条即可)。11. 学校运动会上短跑项目“发令枪”里的火药成分为KClO3 , MnO2和红磷,当扣动扳机时,①撞针撞击火药,产生热量使KClO3分解产生O2;②并引燃红磷产生白烟,试分别写这两步反应的化学方程式。(1)、;基本反应类型是。(2)、;基本反应类型是。12. “天宫课堂”第一课于2021年12月9日正式开启,王亚平老师展示了如何在太空中饮用再生水。获取再生水的首选方法是收集航天员的尿液和其他废水通过方法制得纯水并加以利用;第二种方法是通过“萨巴蒂尔”反应,即在催化剂存在的条件下,使二氧化碳和氢气转化为甲烷和水,该反应的化学方程式为。13. A、B、C三种物质均含有人体中含量最多的金属元素,D可作气体肥料,它们的转化关系如图(部分物质和反应条件已略去),A的相对分子质量为56,A与水化合得B.则A→B的化学方程式为;C→A的化学反应类型属于;D→C的化学方程式为。
 14. 书写下列反应的文字表达式或化学方程式。(1)、生成有刺激性气味气体的反应 ;(2)、有二氧化碳生成的化合反应;(3)、有黑色固体生成的化合反应;(4)、有水生成的分解反应;(5)、在空气中燃烧发出耀眼白光的反应 。15. 写出下列反应的化学方程式,并在括号里注明反应的基本类型.(1)、过氧化氢与二氧化锰混合制氧气 , 反应;(2)、铁丝在氧气中燃烧 , 反应;(3)、铜丝浸入硝酸银溶液中;(4)、镁在二氧化碳中燃烧生成氧化镁和炭黑。16. 氮化镓(GaN)充电器有体积小、效率高、更安全等优势。
14. 书写下列反应的文字表达式或化学方程式。(1)、生成有刺激性气味气体的反应 ;(2)、有二氧化碳生成的化合反应;(3)、有黑色固体生成的化合反应;(4)、有水生成的分解反应;(5)、在空气中燃烧发出耀眼白光的反应 。15. 写出下列反应的化学方程式,并在括号里注明反应的基本类型.(1)、过氧化氢与二氧化锰混合制氧气 , 反应;(2)、铁丝在氧气中燃烧 , 反应;(3)、铜丝浸入硝酸银溶液中;(4)、镁在二氧化碳中燃烧生成氧化镁和炭黑。16. 氮化镓(GaN)充电器有体积小、效率高、更安全等优势。①氮化镓(GaN)在1050℃下会分解为金属镓(Ga)和氮气(N2),氮气是由组成的,由构成的,N2中2的意义是。氮气是一种化学性质不活泼的气体,一般可以作。常温下,氮气会很慢地与氢气反应,反应过程可用下图表示,请补全下图:

(
 表示氮原子,
表示氮原子,  表示氢原子)请书写产物
表示氢原子)请书写产物  的化学式。
的化学式。②液态金属镓可以用做高温温度计,这是由它的决定的(选填“物理性质”或“化学性质”)。金属镓(Ga)还能与足量稀硫酸(H2SO4)反应生成H2 , 参与反应的Ga与生成物H2的关系如下表所示,请填写下表。
Ga物质的量
0.25
0.67
1
H2物质的量
0.75
2.01
根据以上数据,请书写金属镓(Ga)与足量稀硫酸(H2SO4)反应生成H2的化学方程式。
三、综合题
-
17. 我国在南海试采可燃冰(主要含有甲烷水合物)获得成功。这一成果对促进能源安全保障、优化结构都具有重大意义。请回答下列问题:(1)、甲烷在空气中燃烧的化学方程式为。(2)、可燃冰燃烧主要是将化学能转化为能。(3)、甲烷不充分燃烧会生成、二氧化碳和水:要使其充分燃烧,你的做法是。(4)、可燃冰 (填“属于”或“不属于”)新能源:目前人们正在利用和开发的新能源还有(填一种即可)。18. 硅(Si)是一种重要的半导体材料,应用范围很广。三氯甲硅烷(SiHCl3)还原法是当前制备高纯硅的主要方法,生产过程如图所示:
 (1)、硅属于(填“金属”或“非金属”)元素:(2)、写出上述流程中一种氧化物的化学式。(3)、上述流程中①、④反应的化学方程式为;。①和④反应中、都具有还原性。(4)、如果还原SiHCl3过程中混入O2 , 可能引起的后果是。(5)、该流程中可以循环利用的物质的化学式是。
(1)、硅属于(填“金属”或“非金属”)元素:(2)、写出上述流程中一种氧化物的化学式。(3)、上述流程中①、④反应的化学方程式为;。①和④反应中、都具有还原性。(4)、如果还原SiHCl3过程中混入O2 , 可能引起的后果是。(5)、该流程中可以循环利用的物质的化学式是。