2024中考一轮总复习 第14课时 质量守恒定律
试卷更新日期:2024-02-18 类型:一轮复习
一、选择题
-
1. 已知亚硝酸钠(NaNO2)外观与食盐很相似,有咸味,误食会使人中毒。亚硝酸钠易分解,放出有刺激性气味的气体,你认为此气体可能是( )A、O2 B、N2 C、SO2 D、NO22. “洁厕灵”与“漂白剂”不能混用,两者若混合易产生一种有毒气体X。反应原理为:NaClO+2HCl=NaCl+X↑+H2O,则X的化学式为( )A、Cl2 B、ClO2 C、HClO D、HClO33. 在化学反应前后,肯定不会发生变化的是( )
①原子的数目 ②分子的数目 ③元素的种类 ④物质的质量总和 ⑤物质的种类 ⑥物质的体积
A、②④⑤ B、①③④ C、①③④⑥ D、①③⑥4. 下列对质量守恒定律的理解,正确的是( )A、将5g铁和5g铜混合后。物质的总质量为10g,遵守质量守恒定律 B、5g硫和5g氧气恰好完全反应,生成物二氧化硫为10g C、化学反应前后分子的总数一定不会发生变化 D、镁条燃烧后质量增加,不遵循质量守恒定律5. 利用天平及下列物品(必要时还可用燃着的酒精灯),能够直接用于验证质量守恒定律的是( )A、 B、
B、 C、
C、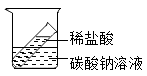 D、
D、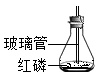 6. 氯化氢转化为氯气的技术是科学家研究的热点之一,下图是该反应的微观示意图(其中:
6. 氯化氢转化为氯气的技术是科学家研究的热点之一,下图是该反应的微观示意图(其中: 表示氢原子,
表示氢原子, 表示氧原子,
表示氧原子, 表示氯原子),下列说法正确的是( )
表示氯原子),下列说法正确的是( )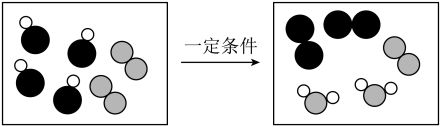 A、该反应属于化合反应 B、生成物有两种 C、反应物的分子个数比是2∶1 D、反应前后氯元素化合价没有改变7. 下列关于化学反应 2X+Y=2Z 的叙述,错误的是A、Z一定是化合物 B、若a g X与 b g Y 充分反应,生成 Z 的质量可能为(a+b)g C、若X和Y的相对分子质量分别为 m 和 n,则 Z 的相对分子质量为 m+n D、在反应中X、Y、Z 三种物质的粒子数目比为 2∶1∶28. 某密闭容器内有X、Y、Z、W四种物质,在一定条件反应一段时间,测得各物质的质量如下表,下列说法正确的是( )
A、该反应属于化合反应 B、生成物有两种 C、反应物的分子个数比是2∶1 D、反应前后氯元素化合价没有改变7. 下列关于化学反应 2X+Y=2Z 的叙述,错误的是A、Z一定是化合物 B、若a g X与 b g Y 充分反应,生成 Z 的质量可能为(a+b)g C、若X和Y的相对分子质量分别为 m 和 n,则 Z 的相对分子质量为 m+n D、在反应中X、Y、Z 三种物质的粒子数目比为 2∶1∶28. 某密闭容器内有X、Y、Z、W四种物质,在一定条件反应一段时间,测得各物质的质量如下表,下列说法正确的是( )物质
X
Y
Z
W
反应前质量/g
20
1
10
2
反应一段时间后质量/g
11
5
15
待测
A、W一定是催化剂 B、X一定是化合物 C、该反应可能不是分解反应 D、该反应中Y、Z变化的质量比为1:39. 根据如下微观示意图分析,下列结论正确的是( ) A、该反应属于置换反应 B、该反应前后各元素化合价不变 C、该反应生成的丙与丁的质量比为27∶44 D、参加反应的甲与乙的分子个数比为1∶110. 密闭容器中只有甲、乙、丁三种物质,在一定条件下发生了一个化学反应,容器中丙质量随甲、乙、丁的质量变化情况如图所示。下列说法错误的是( )
A、该反应属于置换反应 B、该反应前后各元素化合价不变 C、该反应生成的丙与丁的质量比为27∶44 D、参加反应的甲与乙的分子个数比为1∶110. 密闭容器中只有甲、乙、丁三种物质,在一定条件下发生了一个化学反应,容器中丙质量随甲、乙、丁的质量变化情况如图所示。下列说法错误的是( ) A、丁可能是该反应的催化剂 B、a=8 C、乙、丙的相对分子质量之比为2:3 D、当甲为5g时,容器中乙和丁的质量之比为2:111. 下列实验中,固体质量变化与下图相符合的是( )
A、丁可能是该反应的催化剂 B、a=8 C、乙、丙的相对分子质量之比为2:3 D、当甲为5g时,容器中乙和丁的质量之比为2:111. 下列实验中,固体质量变化与下图相符合的是( ) A、硫在盛有氧气的集气瓶中燃烧 B、铁丝在盛有氧气的集气瓶中燃烧 C、一定量的镁条在氧气中充分燃烧 D、向盛有氢氧化钠溶液的试管中逐滴加入硫酸铜溶液12. 我国化学家研究出一种新型催化剂,在太阳光照射下实现了水的高效分解。该反应过程的微观示意图如图。下列说法错误的是( )
A、硫在盛有氧气的集气瓶中燃烧 B、铁丝在盛有氧气的集气瓶中燃烧 C、一定量的镁条在氧气中充分燃烧 D、向盛有氢氧化钠溶液的试管中逐滴加入硫酸铜溶液12. 我国化学家研究出一种新型催化剂,在太阳光照射下实现了水的高效分解。该反应过程的微观示意图如图。下列说法错误的是( )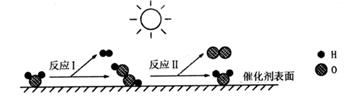 A、
A、 表示的物质属于氧化物
B、反应Ⅰ的化学方程式为2H2O H2O2+H2↑
C、反应Ⅱ中,反应前后原子的种类和数目均不变
D、该成果对氢能源的推广应用有重要的实践意义
表示的物质属于氧化物
B、反应Ⅰ的化学方程式为2H2O H2O2+H2↑
C、反应Ⅱ中,反应前后原子的种类和数目均不变
D、该成果对氢能源的推广应用有重要的实践意义
二、填空题
-
13. 在潜水艇中常用过氧化钠(Na2O2)来吸收人体呼出的二氧化碳气体,其反应的化学方程式为:2Na2O2+2CO2=2Na2CO3+X,则X的化学式为。反应前后氧元素共表现出种化合价。Na2CO3中的阴离子为(写出离子符号)。14. 在化学反应3X+4Y=2Z中,已知X和Z的相对分子质量分别是32和102,则Y的相对分子质量为。15. Vc泡腾片,可增强机体抵抗力,某品牌维C泡腾片主要成分如图所示。将其溶于水,有许多气泡产生。实验产生的气泡中不可能含有N2 , 是因为;把纯净的维生素C(C6H8O6)在一定质量的氧气中充分燃烧,生成了CO、CO2和H2O,测得生成物的总质量为30.4g,其中水的质量为7.2g,则参加反应的氧气质量为g。
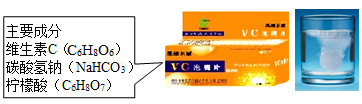 16. “天宫课堂”给我们留下了深刻的印象。(1)、“太空教师”王亚平将少量蓝色色素注入水球,水球很快全变为蓝色,在这个过程中分子的种类(选填“改变”或“不变”)。(2)、将泡腾片放入水球中,产生很多气泡,这是因为泡腾片中的柠檬酸(C6H8O7)和碳酸氢钠(NaHCO3)在水中发生了如下反应:C6H8O7+3NaHCO3═C6H5O7Na3+3H2O+3X↑,其中X的化学式是;碳酸氢钠中含有碳酸氢根离子,写出其离子符号:。(3)、空间站内的“人造空气”与地球上的空气成分相似,含有78%的氮气、21%的(填化学式)和0.7%的二氧化碳等气体。(4)、水的净化再利用是天宫资源利用最大化的重要措施。如图所示的“生命吸管”是一种便携式户外净水装置,下列说法错误的是___________(填字母)。
16. “天宫课堂”给我们留下了深刻的印象。(1)、“太空教师”王亚平将少量蓝色色素注入水球,水球很快全变为蓝色,在这个过程中分子的种类(选填“改变”或“不变”)。(2)、将泡腾片放入水球中,产生很多气泡,这是因为泡腾片中的柠檬酸(C6H8O7)和碳酸氢钠(NaHCO3)在水中发生了如下反应:C6H8O7+3NaHCO3═C6H5O7Na3+3H2O+3X↑,其中X的化学式是;碳酸氢钠中含有碳酸氢根离子,写出其离子符号:。(3)、空间站内的“人造空气”与地球上的空气成分相似,含有78%的氮气、21%的(填化学式)和0.7%的二氧化碳等气体。(4)、水的净化再利用是天宫资源利用最大化的重要措施。如图所示的“生命吸管”是一种便携式户外净水装置,下列说法错误的是___________(填字母)。 A、超滤膜可以过滤大部分颗粒杂质,降低浑浊度 B、椰壳活性炭可以吸附色素和异味,提升口感 C、抗菌颗粒可以杀灭细菌 D、通过“生命吸管”可以得到纯净的水
A、超滤膜可以过滤大部分颗粒杂质,降低浑浊度 B、椰壳活性炭可以吸附色素和异味,提升口感 C、抗菌颗粒可以杀灭细菌 D、通过“生命吸管”可以得到纯净的水三、综合题
-
17. 如图是某化学反应的微观示意图。请结合图示回答下列问题:
 (1)、该反应属于反应(填基本反应类型)。(2)、在该反应的化学方程式中,A、B的化学计量数之比为。(3)、产物C、D中,属于单质的是 , 说出你从微观判断的理由。18. 请沿用科学家认识事物的方式认识“空气”。(1)、从分类角度:空气属于(填“混合物”或“纯净物”)。(2)、从微观角度:用“○”表示氮原子,用“”表示氧原子。
(1)、该反应属于反应(填基本反应类型)。(2)、在该反应的化学方程式中,A、B的化学计量数之比为。(3)、产物C、D中,属于单质的是 , 说出你从微观判断的理由。18. 请沿用科学家认识事物的方式认识“空气”。(1)、从分类角度:空气属于(填“混合物”或“纯净物”)。(2)、从微观角度:用“○”表示氮原子,用“”表示氧原子。①用“
 ”可表示的微粒是(填名称)。
”可表示的微粒是(填名称)。②同温同压下,气体的体积比等于分子数目比。若空气中其他成分忽略不计,下图中可表示空气微观模型的是(填字母标号)。
 (3)、从变化角度:已知:常压下,氮气沸点―196℃,氧气沸点--183℃。将燃着的木条置于盛满液态空气(模拟分离液态空气条件)的烧杯口,观察到的现象是。该烧杯放置一段时间后,液态物质剩余约1/10体积,其主要成分是(4)、从应用角度:利用空气制取氮肥的流程下图所示。
(3)、从变化角度:已知:常压下,氮气沸点―196℃,氧气沸点--183℃。将燃着的木条置于盛满液态空气(模拟分离液态空气条件)的烧杯口,观察到的现象是。该烧杯放置一段时间后,液态物质剩余约1/10体积,其主要成分是(4)、从应用角度:利用空气制取氮肥的流程下图所示。
①Ⅰ中参加反应的单质甲为
②Ⅱ中反应的化学方程式为
③物质所含元素化合价发生变化的反应称为氧化还原反应,反应Ⅱ(填“属于”或“不属于”)氧化还原反应。
(5)、从环保角度,下列保护空气措施不合理的有_____(填序号)。A、工厂通过加高烟囱直接排放废气 B、推广使用乙醇汽油代替普通汽油 C、提倡步行、骑自行车等“低碳”出行方式四、实验探究题
-
19. 2021年12月9日下午,小明观看完“天宫第一课”后,对王亚平老师的泡腾片实验非常感兴趣,想起自己在补充维生素C时也用过泡腾片,于是把一颗维生素C泡腾片药片丢入水中,发现药片表面产生大量的气泡。出于好奇他开展了如下探究:
【查阅资料】维C泡腾片是一种较新的药物剂型,主要成分有:维C(C6H8O6)、碳酸氢钠(NaHCO3)、柠檬酸(C6H8O7)。维C泡腾片利用柠檬酸和碳酸氢钠反应做泡腾崩解剂、置入水中,即刻发生泡腾反应,生成大量的气体,状如沸腾,故名泡腾片。
【提出猜想】假设产生的气体可能是CO2、N2、O2
(1)、小明认真思考后认为产生的气体不可能是N2 , 因为。(2)、【进行实验】小明将气体通入中,观察到现象,证明该气体是CO2。
(3)、【反思评价】为了验证该反应是否遵循质量守恒定律,小明设计了如图所示的实验,实验前托盘天平的指针指向中间,反应结束后发现天平的指针偏 , 其原因是。由此他得出凡是有气体参与或生成的化学反应,在验证质量守恒时,反应装置应该在容器内进行。

小明继续查阅资料,得知:泡腾片在消毒剂上也有广泛的应用,其中二氧化氯泡腾片是其中一种消毒泡腾片。
(4)、二氧化氯的化学式为 , 其中氯元素的化合价为。(5)、我国研制出制取二氧化氯的新方法,其反应的微观过程如下图所示。(其中 表示氯原子,
表示氯原子, 表示钠原子,
表示钠原子, 表示氧原子)请在丙方框虚线框内把微粒示意图补充完整。
表示氧原子)请在丙方框虚线框内把微粒示意图补充完整。 20. 质量守恒定律是自然界的基本定律之一,化学兴趣小组以“探究质量守恒定律”为主题开展实验探究。
20. 质量守恒定律是自然界的基本定律之一,化学兴趣小组以“探究质量守恒定律”为主题开展实验探究。【提出问题】化学反应前后各物质的质量总和是否相等?
【猜想与假设】猜想1:不相等;猜想2:相等。
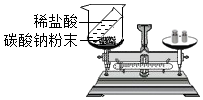
【资料信息】碳酸钠与稀盐酸反应的化学方程式:Na2CO3+2HCl═2NaCl+H2O+CO2↑。
(1)、【实验探究】甲、乙两组同学用托盘天平分别称量反应前后装置的质量。甲组
乙组
实验方案
实验现象
有气泡产生,天平指针向右偏转
瓶内 , 天平指针没有偏转
实验结论
猜想1正确
猜想2正确,反应的化学方程式:
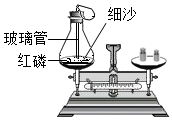
(2)、【反思评价】两个实验,得出了相反的结论。请讨论分析甲组中导致指针向右偏转的原因是。(3)、【得出结论】同学们经过讨论分析,得出猜想二正确。最终得出结论:的各物质的质量总和等于反应后生成的各物质的质量总和。(4)、【解释应用】请从微观角度解释质量守恒定律:。(5)、【总结交流】通过以上实验,小组同学总结出:验证质量守恒定律时,若反应有气体生成时,应在中进行。(6)、【拓展延伸】小华同学设计了如图实验来验证质量守恒定律,小刚同学认为该实验设计是不正确的,原因是
