广东省深圳市光明区2023-2024学年高一上学期期末考试化学试题
试卷更新日期:2024-02-01 类型:期末考试
一、选择题:本题共20小题,每小题3分,共60分。在每小题给出的四个选项中,只有一个选项符合题目的要求。
-
1. 文化岭南,古韵悠长。下列西汉南越王博物馆馆藏珍宝中,主要由合金材料制成的是( )




A.青铜双耳酒器
B.漆木双面彩绘屏风
C.透雕龙凤重环玉佩
D.广彩瓷咖啡杯
A、A B、B C、C D、D2. 我国古代四大发明对人类文明作出了重大贡献。下列有关四大发明的应用,涉及到氧化还原反应的是( )A、造纸术—文字书写 B、火药—矿山爆破 C、印刷术—书籍出版 D、指南针—海上导航3. 近年我国在科技领域不断取得新成就。下列说法正确的是( )A、“长征系列”火箭所用的燃料中,为氧化性气体 B、“深海一号”开采深海的天然气可作清洁燃料,实现零碳排放 C、“华龙一号”核反应堆所用铀棒中含有的与互为同位素 D、火星全球影像彩图显示了火星表土颜色,表土中赤铁矿主要成分为FeO4. 分类是认识元素及其化合物的方法之一。下列有关物质分类的说法,正确的是( )A、纯净物:盐酸、酒精 B、电解质:碳酸钠、食盐水 C、强酸:次氯酸、硫酸 D、碱性氧化物:氧化铁、氧化钠5. 化学与生活密切相关。下列说法不正确的是( )A、代替氯气用于自来水消毒 B、纯碱常用作胃药 C、不锈钢可用于制餐具 D、放射性同位素可用于诊断和治疗疾病6. 下列化学用语表达正确的是( )A、的结构模型为 B、的结构示意图:
B、的结构示意图: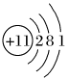 C、的结构式为
D、的电子式为
C、的结构式为
D、的电子式为 7. 实验室配制100mL0.1mol/LNaCl溶液时,下列有关操作正确的是( )A、
7. 实验室配制100mL0.1mol/LNaCl溶液时,下列有关操作正确的是( )A、 B、
B、 C、
C、 D、
D、 8. 当光束通过下列物质时,能观察到丁达尔效应的是( )A、云、雾 B、乙醇 C、硫酸铜溶液 D、澄清石灰水9. 下列物质中,含共价键的离子化合物是( )A、 B、 C、 D、10. 化学实验中,安全意识是重要的科学素养。下列实验操作不正确的是( )A、实验室制备氯气时,在通风橱中进行 B、金属钠着火时,用干燥的沙土覆盖 C、戴护目镜观察氢气在氯气中燃烧 D、实验后剩余的金属钠可丢入水槽中11. 下列劳动项目与所述的化学知识没有关联的是( )
8. 当光束通过下列物质时,能观察到丁达尔效应的是( )A、云、雾 B、乙醇 C、硫酸铜溶液 D、澄清石灰水9. 下列物质中,含共价键的离子化合物是( )A、 B、 C、 D、10. 化学实验中,安全意识是重要的科学素养。下列实验操作不正确的是( )A、实验室制备氯气时,在通风橱中进行 B、金属钠着火时,用干燥的沙土覆盖 C、戴护目镜观察氢气在氯气中燃烧 D、实验后剩余的金属钠可丢入水槽中11. 下列劳动项目与所述的化学知识没有关联的是( )选项
劳动项目
化学知识
A
锅炉工人用醋酸除水垢(主要含)
能与醋酸反应
B
工人用溶液作腐蚀液去除覆铜板上不需要的铜
金属铁的还原性比金属铜强
C
面包师用小苏打粉作膨松剂烘培糕点
受热易分解放出
D
保洁员用含NaClO的消毒液对公共场所消毒
NaClO有强氧化性
A、A B、B C、C D、D12. 在无色溶液中能大量共存的一组离子是( )A、 B、 C、 D、13. 下列离子方程式书写正确的是( )A、氢氧化钡溶液与硫酸铜溶液混合: B、盐酸中加入铝粉: C、氧化铝与氢氧化钠溶液混合: D、氯化亚铁溶液中滴加氨水:14. 下列有关性质的比较,不能用元素周期律解释的是( )A、非金属性: B、还原性: C、碱性: D、酸性:15. 钛和钛的合金被誉为“21世纪最有发展前景的金属材料”,它们具有很多优良的性能,如熔点高、密度小、耐压且强度高、不易腐蚀、易于加工,尤其是钛合金与人体器官具有很好的“生物相容性”。根据它们的主要性能,下列用途不切实际的是( )A、用来制造人造骨 B、用于制造潜水艇外壳 C、用于制造高端自行车车架 D、用来作保险丝16. 下表各选项中甲组两种物质,用乙组试剂进行检验,不能达到目的的是( )选项
甲组(被检物质)
乙组(检验试剂)
A
铝片和铁片
NaOH溶液
B
溶液和NaCl溶液
溶液和稀硝酸
C
KBr溶液和KI溶液
淀粉溶液
D
溶液和溶液
NaOH溶液
A、A B、B C、C D、D17. 侯德榜制碱法第一步制备的反应原理是设为阿伏加德罗常数的值,下列叙述正确的是( )A、含有的原子数目为 B、含有离子数目为 C、58.5gNaCl含有NaCl分子数目为 D、常温常压下,含有的原子数目为18. 部分含铁物质的分类与相应铁元素的化合价关系如图所示。下列说法不正确的是( ) A、在高温下,a与水蒸气可发生置换反应 B、b分别与水、盐酸反应对应生成e、f C、e在潮湿的空气中容易被氧化生成d D、一定条件下,f与g可以相互转化19. a~f六种短周期主族元素在周期表的位置如下表所示,其中a原子最外层电子数是4。下列叙述正确的是( )
A、在高温下,a与水蒸气可发生置换反应 B、b分别与水、盐酸反应对应生成e、f C、e在潮湿的空气中容易被氧化生成d D、一定条件下,f与g可以相互转化19. a~f六种短周期主族元素在周期表的位置如下表所示,其中a原子最外层电子数是4。下列叙述正确的是( )a
b
c
d
e
f
A、原子半径大小: B、气态氢化物的稳定性: C、e的氧化物能分别与d、f的最高价氧化物对应水化物发生反应 D、将d的单质加入到e的盐溶液中,能发生置换反应得到e的单质20. 氮化铝(AlN)广泛应用于电子、陶瓷等工业领域。在一定条件下,AlN可通过反应合成。对于该反应,下列叙述不正确的是( )A、AlN中氮元素的化合价为-3 B、C是还原剂,是氧化剂 C、由上述反应可得,C的还原性比AlN强 D、理论上,当有6mol电子发生转移,可生成1molAlN二、非选择题:本题共4个小题,共40分。
-
21. 某研究性学习小组在实验室制取纯净的氯气,设计实验装置如图所示。

回答下列问题:
(1)、写出A中发生反应的化学方程式是 , 该反应体现了浓盐酸的酸性和性。(2)、B中饱和食盐水的作用是。(3)、E中NaOH溶液的作用是除去剩余氯气,防止污染空气。写出该反应的离子方程式。(4)、该组同学将新制的饱和氯水慢慢滴入含有酚酞的NaOH溶液中,当滴到一定量时,红色褪去。①预测红色褪去的原因:甲同学认为可能是氯水中的酸与NaOH发生中和反应所致,乙同学认为可能是氯水中(填化学式)的强氧化性所致。
②设计实验证明红色褪色的原因:取褪色后的溶液于试管中,加入 , 若观察到 , 证明同学的观点是正确。
22. 某硫酸厂用硫铁矿焙烧后的烧渣(主要成分为、、 , 不考虑其他杂质)制备绿矾粗产品的流程如下:
已知是酸性氧化物。
回答下列问题:
(1)、流程中两次“操作”的名称是。(2)、“还原”步骤中溶液由黄色变浅绿色,写出溶液变浅绿色的离子方程式。(3)、“调pH至5-6”步骤中,写出生成的离子方程式。(4)、鉴别滤液a中金属阳离子的实验方案如下,按要求填空:操作
现象
结论或离子方程式
步骤1:取少量滤液a进行①(填实验名称)。
火焰呈②。
滤液a中含有。
步骤2:另取少量滤液a于试管中,依次滴入③(填化学式)溶液和氯水。
溶液先无红色,后变红色。
滤液a中含有 , 不含。写出该过程中属于氧化还原反应的离子方程式④。
23. 元素周期律是指导我们学习元素及其化合物知识的重要工具。已知氧族元素(不含Po)的部分知识如下表所示。氧族元素
O(氧)
S(硫)
Se(硒)
Te(碲)
核电荷数
8
16
34
52
单质熔点/℃
-218.4
113
450
单质沸点/℃
-183
444.6
685
1390
主要化合价
-2
-2,+4,+6
-2,+4,+6
回答下列问题:
(1)、硫元素位于元素周期表的第三周期族,的电子式为。(2)、依据元素周期律和表中知识,预测单质硒的熔点范围可能大于℃,小于℃,硒元素的主要化合价有。(3)、硫的非金属性比氧、(填“强”或“弱”),因此,氢硫酸溶液在空气中长期露置易变质出现浑浊,写出该反应的化学方程式为。(4)、将少量通入下列溶液中能发生化学反应,从物质类别和硫元素的价态推断反应产物,并在横线上写出产物中含硫物质的化学式:①NaOH溶液 , ②新制的氯水。
24. 不同类别物质间的转化关系是认识元素及其化合物的线索之一,某学习小组绘制了五种含钠元素物质间的转化关系图。
回答下列问题:
(1)、转化关系图中X的类别是碱,写出反应②的化学方程式。(2)、发生反应⑤和⑥分别需要的试剂是 , , 从氧化剂和还原剂角度分析,反应⑤中的作用是 , 写出的一种用途。(3)、小组同学为验证和酸反应是分步进行的,设计实验方案并进行了实验:向盛有溶液的试管中滴加稀盐酸,开始无气泡产生,滴加一定量盐酸后产生气泡。有关实验现象对应的离子方程式分别为 , 。(4)、现有27.4g含和混合物的样品,向其中加入足量稀硫酸,充分反应后,共产生(标准状况),则样品中的质量为g。