广东省汕头市潮南区2023-2024学年九年级上学期1月期末化学试题
试卷更新日期:2024-02-01 类型:期末考试
一、选择题(每小题只有一个选项符合题意)
-
1. 下列变化属于化学变化的是:( )A、汽油挥发 B、石油分馏 C、光合作用 D、干冰升华2. 下列图标表示“国家节水标志”的是:( )A、
 B、
B、 C、
C、 D、
D、 3. 下列物质属于混合物的是:( )A、水银 B、一氧化碳 C、高锰酸钾 D、稀有气体4. 下列化学用语书写正确的是:( )A、两个铁离子:2Fe2+ B、两个氮分子:2N2 C、氖气:Ne2 D、氧化镁中镁元素的化合价:5. 下列基本实验操作正确的是:( )A、
3. 下列物质属于混合物的是:( )A、水银 B、一氧化碳 C、高锰酸钾 D、稀有气体4. 下列化学用语书写正确的是:( )A、两个铁离子:2Fe2+ B、两个氮分子:2N2 C、氖气:Ne2 D、氧化镁中镁元素的化合价:5. 下列基本实验操作正确的是:( )A、 B、
B、 C、
C、 D、
D、 6. 下列物质的性质和用途的对应关系错误的是:( )A、氮气具有稳定性,可作保护气 B、氧气能够供给呼吸,可用于气割、气焊 C、木炭具有还原性,可用于冶炼金属 D、镁燃烧发出耀眼的白光,可制作闪光弹7. 氮化镓充电器体积小、效率高,可满足电子产品快速充电的需求。如图为镓元素的相关信息,以下说法正确的是:( )
6. 下列物质的性质和用途的对应关系错误的是:( )A、氮气具有稳定性,可作保护气 B、氧气能够供给呼吸,可用于气割、气焊 C、木炭具有还原性,可用于冶炼金属 D、镁燃烧发出耀眼的白光,可制作闪光弹7. 氮化镓充电器体积小、效率高,可满足电子产品快速充电的需求。如图为镓元素的相关信息,以下说法正确的是:( ) A、镓属于金属元素,图中x=8 B、镓原子的中子数为31 C、镓的相对原子质量为69.72g D、镓原子在化学反应中易失去电子8. 对下列事实的解释错误的是:( )A、湿衣服在夏天比冬天易晾干——温度越高,分子运动越快 B、氩气被压缩到钢瓶里——分子间间隔变小 C、水结成冰——分子停止运动 D、金刚石硬,石墨软——碳原子的排列方式不同9. 乙硫醇(化学式为C2H6S)易挥发,有蒜臭味,人对该气味极其敏感,下列有关乙硫醇的说法错误的是:( )A、乙硫醇的相对分子质量为62 B、在管道煤气中添加微量乙硫醇,目的是及时发现煤气泄漏 C、乙硫醇中C、H、S三种元素的质量比是2∶6∶1 D、硫元素的质量分数是10. 酒精灯是实验室常用的热源。下列说法错误的是:( )A、酒精灯燃烧时,酒精燃烧而棉线灯芯不燃烧,原因是棉线没有与氧气接触 B、将酒精灯灯芯拨松可使火焰变旺,原因是增大可燃物与空气的接触面积 C、熄灭酒精灯时用灯帽盖灭火焰,原因是将可燃物撤离燃烧区,隔离火源 D、酒精灯火焰上方放一块白瓷板,白瓷板变黑,原因是酒精发生不完全燃烧11. H2S是一种生命体系信号分子,其燃烧的化学方程式为 , 则X是:( )A、SO2 B、SO3 C、O2 D、H212. 模型建构是化学学习的重要思想,下列模型正确的是:( )A、原子结构
A、镓属于金属元素,图中x=8 B、镓原子的中子数为31 C、镓的相对原子质量为69.72g D、镓原子在化学反应中易失去电子8. 对下列事实的解释错误的是:( )A、湿衣服在夏天比冬天易晾干——温度越高,分子运动越快 B、氩气被压缩到钢瓶里——分子间间隔变小 C、水结成冰——分子停止运动 D、金刚石硬,石墨软——碳原子的排列方式不同9. 乙硫醇(化学式为C2H6S)易挥发,有蒜臭味,人对该气味极其敏感,下列有关乙硫醇的说法错误的是:( )A、乙硫醇的相对分子质量为62 B、在管道煤气中添加微量乙硫醇,目的是及时发现煤气泄漏 C、乙硫醇中C、H、S三种元素的质量比是2∶6∶1 D、硫元素的质量分数是10. 酒精灯是实验室常用的热源。下列说法错误的是:( )A、酒精灯燃烧时,酒精燃烧而棉线灯芯不燃烧,原因是棉线没有与氧气接触 B、将酒精灯灯芯拨松可使火焰变旺,原因是增大可燃物与空气的接触面积 C、熄灭酒精灯时用灯帽盖灭火焰,原因是将可燃物撤离燃烧区,隔离火源 D、酒精灯火焰上方放一块白瓷板,白瓷板变黑,原因是酒精发生不完全燃烧11. H2S是一种生命体系信号分子,其燃烧的化学方程式为 , 则X是:( )A、SO2 B、SO3 C、O2 D、H212. 模型建构是化学学习的重要思想,下列模型正确的是:( )A、原子结构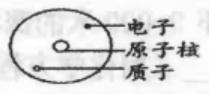 B、C60分子结构
B、C60分子结构 C、地壳中元素含量
C、地壳中元素含量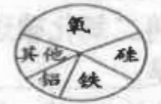 D、氯元素化合价
D、氯元素化合价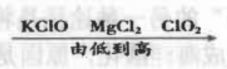 13. 下列实验设计能达到目的的是:( )A、检验集气瓶中O2是否集满:伸入燃着的木条 B、鉴别MnO2和碳粉:观察颜色 C、除去CaO中的少量CaCO3:加水溶解后过滤 D、除去CO2中的少量O2:将气体通入灼热的铜网14. 下列实验方案不能达到相应目的的是:( )A、探究CO2是否溶于水
13. 下列实验设计能达到目的的是:( )A、检验集气瓶中O2是否集满:伸入燃着的木条 B、鉴别MnO2和碳粉:观察颜色 C、除去CaO中的少量CaCO3:加水溶解后过滤 D、除去CO2中的少量O2:将气体通入灼热的铜网14. 下列实验方案不能达到相应目的的是:( )A、探究CO2是否溶于水 
B、测定空气中O2的含量
B、测定空气中O2的含量 
C、验证质量守恒定律
C、验证质量守恒定律 
D、比较不同物质的着火点
D、比较不同物质的着火点 
15. 某化学小组将一定浓度的稀盐酸、稀硫酸分别加入装有等质量CaCO3粉末的容器中,相同条件下测得二者产生的CO2体积(V)与反应时间(t)的关系如图。下列判断错误的是:( )
15. 某化学小组将一定浓度的稀盐酸、稀硫酸分别加入装有等质量CaCO3粉末的容器中,相同条件下测得二者产生的CO2体积(V)与反应时间(t)的关系如图。下列判断错误的是:( ) A、0~300s内,两个容器中酸的浓度均越来越小 B、0~100s内,反应Ⅰ、Ⅱ生成CO2的速率均先慢后快 C、反应Ⅱ中0~100s内产生的CO2比100~200s内少5amL D、实验室可用一定浓度的稀硫酸与CaCO3粉末制取CO2
A、0~300s内,两个容器中酸的浓度均越来越小 B、0~100s内,反应Ⅰ、Ⅱ生成CO2的速率均先慢后快 C、反应Ⅱ中0~100s内产生的CO2比100~200s内少5amL D、实验室可用一定浓度的稀硫酸与CaCO3粉末制取CO2二、非选择题(本题包括6小题)
-
16. 水与人类的生活和生产密切相关。(1)、节约用水,防止水污染应成为我们的自觉行为。下列叙述正确的是____(填字母)。A、为了节约用水,用工业废水直接浇灌农田 B、水的天然循环能实现水的重新分配,不需兴建水利工程 C、将生活用水、地表雨水分类处理,可减少污染,保护水资源(2)、日常生活中常用的方法除去硬水中过多的(填离子符号)和Ca2+来得到软水。(3)、图甲是水电解实验示意图。
甲
 乙
乙
①实验中,试管a中产生的气体为(填名称)。
②写出该反应的化学方程式。
(4)、有的同学利用所学的知识将浑浊的水用简易净水器(如图丙所示)进行净化,其中小卵石、石英砂的作用是。17. 能源是支撑经济和社会发展的源动力和物质基础,而生态环境是经济和社会可持续发展的根本支撑。(1)、化石燃料主要包括煤、石油和。化石燃料的燃烧是二氧化碳排放的主要因素,二氧化碳过量排放会引起的环境问题是。(2)、二氧化碳甲醇化助力我国更早实现“碳中和”,反应的微观示意图如图。
①请把图中反应物的微观示意图补画完整。
②实现“碳中和”的另一种途径是将二氧化碳送入海面以下3000米的深海里进行封存,但此举可能会造成海洋酸化,原因是(用化学方程式表示)。
(3)、“绿色化学”的特点之一是“零排放”。若二氧化碳和氢气反应只生成一种产物就能实现“零排放”,该产物是____(填序号)。A、甲酸(CH2O2) B、乙醇(C2H6O) C、乙酸(C2H4O2)(4)、氢能是未来最理想的能源,从环保角度分析,氢能的优点是。18. 气体的制取与性质实验是初中化学实验的重要内容。(1)、Ⅰ.气体的制取实验
图1
图1中仪器①的名称为。 (2)、实验室加热高锰酸钾制取氧气的化学方程式为 , 选择并组装发生和收集装置,正确的连接顺序为(填接口处字母)。(3)、装置B、C都可以作为实验室制取二氧化碳和氢气的发生装置,与装置C相比,装置B的优点是。(4)、Ⅱ.气体的性质实验
(2)、实验室加热高锰酸钾制取氧气的化学方程式为 , 选择并组装发生和收集装置,正确的连接顺序为(填接口处字母)。(3)、装置B、C都可以作为实验室制取二氧化碳和氢气的发生装置,与装置C相比,装置B的优点是。(4)、Ⅱ.气体的性质实验图2
 图3
图3 图4
图4
木炭燃烧实验(如图2)。加热后的木炭在空气中红热,在氧气中剧烈燃烧,(填实验现象),放出热量。燃烧现象不同的原因是。
(5)、二氧化碳性质实验(如图3)。当观察到短蜡烛熄灭时,关闭K,片刻后长蜡烛熄灭。从二氧化碳性质的角度分析原因:。(6)、氢气性质实验(如图4)。用排水法收集到一瓶氢气,倒置于铁架台上,将一根点燃的蜡烛缓慢插入瓶中,瓶口有一团火焰,插入瓶中后蜡烛熄灭了。上述实验及操作能说明的是____(多选,填序号)。A、氢气能支持燃烧 B、氢气具有可燃性 C、氢气的密度比空气小 D、氢气难溶于水19.(1)、兴趣小组发现实验室一片久置的铜片表面附着有一层绿色固体,查阅资料得知绿色固体是铜绿 , 甲同学从铜片上刮下一些铜绿进行如下探究,请完成下表:实验装置
实验现象
实验结论

试管内壁有水雾
铜绿加热后产生
铜绿加热后生成氧化铜
气球胀大
乙同学对气球胀大的原因产生兴趣,于是进行了如下探究。
【作出猜想】猜想Ⅰ:试管内的空气受热膨胀;
猜想Ⅱ:铜绿加热后生成CO2;
猜想Ⅲ:铜绿加热后生成CO;
猜想Ⅳ:铜绿加热后生成CO2和CO。
(2)、【实验与分析】熄灭酒精灯并冷却至室温后,气球仍然胀大没有变瘪,证明猜想(填序号)不成立。(3)、乙同学用下图装置进行实验,发现A中 , 说明铜绿加热后生成二氧化碳,此现象的反应的化学方程式是 , B处玻璃管内没有明显现象,说明猜想不成立。 (4)、【实验结论】猜想成立。(5)、【反思】根据铜绿的化学式可知,铜绿是铜与空气中的氧气、水和共同作用形成的。(6)、丙同学认为乙同学的实验中省略A处集气瓶也能得到相同的结论,请描述与结论相对应的实验现象:。20. 我国的北斗卫星导航系统标志是北斗星和司南的结合。(1)、我国“长三乙”火箭将第55颗北斗卫星送入预定轨道,完成了北斗卫星导航系统的组网。该火箭的推进剂是液氢和液氧,二者发生的反应属于反应(填基本反应类型)。(2)、“司南之杓,投之于地,其柢指南”中“杓”的主要成分是Fe3O4 , 其中铁元素的质量分数为(结果精确到0.1%)。(3)、如图“北斗七星”代表7种初中化学常见的物质,“—”表示相邻的物质间能发生反应,“→”表示能一步实现的物质转化方向。已知A、C的元素组成相同且常温下均为液体,D可作食品干燥剂,F是农业生产中常用的气体肥料。
(4)、【实验结论】猜想成立。(5)、【反思】根据铜绿的化学式可知,铜绿是铜与空气中的氧气、水和共同作用形成的。(6)、丙同学认为乙同学的实验中省略A处集气瓶也能得到相同的结论,请描述与结论相对应的实验现象:。20. 我国的北斗卫星导航系统标志是北斗星和司南的结合。(1)、我国“长三乙”火箭将第55颗北斗卫星送入预定轨道,完成了北斗卫星导航系统的组网。该火箭的推进剂是液氢和液氧,二者发生的反应属于反应(填基本反应类型)。(2)、“司南之杓,投之于地,其柢指南”中“杓”的主要成分是Fe3O4 , 其中铁元素的质量分数为(结果精确到0.1%)。(3)、如图“北斗七星”代表7种初中化学常见的物质,“—”表示相邻的物质间能发生反应,“→”表示能一步实现的物质转化方向。已知A、C的元素组成相同且常温下均为液体,D可作食品干燥剂,F是农业生产中常用的气体肥料。
①写出A的名称:。
②B在空气中的体积分数约为。“铁丝在氧气中燃烧实验”中C的作用是。
③写出D→E的化学方程式:。
④写出F的另一种用途:。若G能与血红蛋白结合导致人体中毒,则其化学式为。
21. 石灰石是一种常见的矿石,其制得的产品应用十分广泛。实验室将10.0g石灰石样品高温煅烧,对样品进行分析,实验数据记录如表(杂质不参与反应)。反应时间/min
1
2
3
4
剩余固体质量/g
8.6
7.3
6.7
6.7
(1)、完全反应后生成二氧化碳的质量是g。(2)、该石灰石样品中碳酸钙的质量分数是多少?(3)、以石灰石为原料制得的“石头纸”是一种介于纸张和塑料之间的新型材料,与传统纸张相比,“石头纸”的优点是。