广东省阳江市2023-2024学年九年级上学期期末监测化学试题
试卷更新日期:2024-01-31 类型:期末考试
一、选择题
-
1. 中华文化源远流长。下列词语蕴含化学变化的是A、蜡炬成灰 B、水落石出 C、清风徐来 D、愚公移山2. 下列化学用语书写正确的是A、锰元素:MN B、60个碳原子:C60 C、3个三氧化硫分子:3SO3 D、氧化铁:FeO3. 同学们在实验室里进行与水有关的实验时,所涉及的操作或方法正确的是A、活性炭净化水
 B、量取水
B、量取水 C、检验生成水
C、检验生成水 D、加热水
D、加热水 4. 每年5月12日是我国“防灾减灾日”。以下有关处理火灾现场方法错误的是A、无法逃生时,应退回室内,关闭门窗,向门窗浇水,并发出求救信号 B、身上着火时不可乱跑,要就地打滚使火熄灭 C、炒菜时油锅着火,立即盖上锅盖 D、电线由于老化短路而起火可用水灭火5. 李兰娟院士的研究团队发现:达芦那韦(化学式C27H37N3O7S)能显著抑制新冠肺炎病毒复制。下列说法正确的是( )A、从分类上看:达芦那韦属于混合物 B、从质量上看:达芦那韦中碳、氢、氧三种元素的质量比为27:37:7 C、从微观上看:每个达芦那韦分子由74个原子构成 D、从宏观上看:达芦那韦是由碳、氢、氮、氧、硫五种元素组成6. 根据如图所示信息判断,下列有关说法错误的是
4. 每年5月12日是我国“防灾减灾日”。以下有关处理火灾现场方法错误的是A、无法逃生时,应退回室内,关闭门窗,向门窗浇水,并发出求救信号 B、身上着火时不可乱跑,要就地打滚使火熄灭 C、炒菜时油锅着火,立即盖上锅盖 D、电线由于老化短路而起火可用水灭火5. 李兰娟院士的研究团队发现:达芦那韦(化学式C27H37N3O7S)能显著抑制新冠肺炎病毒复制。下列说法正确的是( )A、从分类上看:达芦那韦属于混合物 B、从质量上看:达芦那韦中碳、氢、氧三种元素的质量比为27:37:7 C、从微观上看:每个达芦那韦分子由74个原子构成 D、从宏观上看:达芦那韦是由碳、氢、氮、氧、硫五种元素组成6. 根据如图所示信息判断,下列有关说法错误的是 A、镁是金属元素 B、镁的相对原子质量是24.31g C、②对应的粒子在反应中易得到电子 D、①②对应的元素可组成MgO7. 下列实验设计不能达到实验目的的是
A、镁是金属元素 B、镁的相对原子质量是24.31g C、②对应的粒子在反应中易得到电子 D、①②对应的元素可组成MgO7. 下列实验设计不能达到实验目的的是实验
设计




实验
目的
探究人呼出的气体与空气中二氧化碳含量的多少
探究同一种物质在不同溶剂中的溶解性不同
探究燃烧的条件之一是需要可燃物
探究氧气的浓度是影响硫燃烧剧烈程度的因素
A、A B、B C、C D、D8. 下面药品最适宜应用在实验室中制取二氧化碳的是A、鸡蛋壳碎和稀醋酸 B、大理石颗粒和稀盐酸 C、大理石颗粒和稀硫酸 D、碳酸钠粉末和盐酸9. 下列有关CO2的用途,说法错误的是A、供给呼吸 B、生产汽水 C、气体肥料 D、灭火10. 如图为验证CO2的性质的实验装置,下列说法错误的是 A、实验中,观察到塑料瓶内下层纸花变红色,而上层纸花不变色 B、观察到短蜡烛熄灭后,关闭K,片刻后长蜡烛熄灭,说明二氧化碳的密度比空气大 C、此实验装置既能验证二氧化碳的物理性质,也能验证二氧化碳的化学性质 D、实验后向去顶部的塑料瓶中注入澄清石灰水,振荡,观察到石灰水变浑浊,说明蜡烛燃烧生成二氧化碳11. 如图为我国“十三五”期间能源消费结构占比统计图。下列说法不正确的是
A、实验中,观察到塑料瓶内下层纸花变红色,而上层纸花不变色 B、观察到短蜡烛熄灭后,关闭K,片刻后长蜡烛熄灭,说明二氧化碳的密度比空气大 C、此实验装置既能验证二氧化碳的物理性质,也能验证二氧化碳的化学性质 D、实验后向去顶部的塑料瓶中注入澄清石灰水,振荡,观察到石灰水变浑浊,说明蜡烛燃烧生成二氧化碳11. 如图为我国“十三五”期间能源消费结构占比统计图。下列说法不正确的是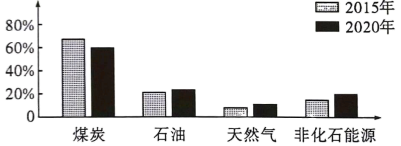 A、煤炭、石油、天然气是不可再生能源,非化石能源有风能、太阳能等 B、煤炭消费占比下降,能源消费结构向清洁低碳转变 C、煤炭燃烧产生的CO2会造成酸雨,对环境影响大 D、氢气是清洁的高能燃料,液氢已被应用于航天等领域12. “催化转化器”可以将汽车尾气中的有毒气体一氧化碳和一氧化氮转变为无毒气体,其反应的微观示意图如图所示。下列有关该反应的说法不正确的是
A、煤炭、石油、天然气是不可再生能源,非化石能源有风能、太阳能等 B、煤炭消费占比下降,能源消费结构向清洁低碳转变 C、煤炭燃烧产生的CO2会造成酸雨,对环境影响大 D、氢气是清洁的高能燃料,液氢已被应用于航天等领域12. “催化转化器”可以将汽车尾气中的有毒气体一氧化碳和一氧化氮转变为无毒气体,其反应的微观示意图如图所示。下列有关该反应的说法不正确的是 A、该反应可以减少汽车尾气污染 B、参加反应的两种物质的分子个数比为2:3 C、生成物中
A、该反应可以减少汽车尾气污染 B、参加反应的两种物质的分子个数比为2:3 C、生成物中 和
和 的质量比是7:22
D、
的质量比是7:22
D、 和
和 化学性质不同的原因是二者的分子构成不同
13. 除去下列各组物质中的杂质,所用试剂和方法均正确的是
化学性质不同的原因是二者的分子构成不同
13. 除去下列各组物质中的杂质,所用试剂和方法均正确的是选项
物质
杂质
除杂质所用试剂和方法
A
CO2
CO
通过灼热的CuO
B
FeCl2溶液
CuCl2溶液
加入过量锌粉,过滤
C
Fe
Cu
加入足量硫酸铜溶液,过滤
D
CaO
CaCO3
加入足量水,过滤
A、A B、B C、C D、D14. 10℃时,将甲、乙两种可溶性固体各3g分别放入盛有10mL水的试管中,图1是两种物质的溶解情况,图2是两种物质的溶解度曲线图。下列对甲、乙两物质的判断,正确的是 A、甲物质对应的溶解度曲线为b B、10℃时,甲、乙两物质的溶液都是饱和溶液 C、甲中混有少量乙,可用蒸发结晶法分离提纯甲 D、温度升高至25℃时,图1试管内所得甲、乙两物质的溶液都是不饱和溶液15. 如图所示,“—”表示物质可以发生反应,“→”表示物质可以转化,下列说法正确的是
A、甲物质对应的溶解度曲线为b B、10℃时,甲、乙两物质的溶液都是饱和溶液 C、甲中混有少量乙,可用蒸发结晶法分离提纯甲 D、温度升高至25℃时,图1试管内所得甲、乙两物质的溶液都是不饱和溶液15. 如图所示,“—”表示物质可以发生反应,“→”表示物质可以转化,下列说法正确的是 A、①的现象是有气泡产生 B、②中转化前后碳元素的化合价不变 C、③可用于工业炼铁,属于置换反应 D、隔绝氧气或者水可以防止④的发生
A、①的现象是有气泡产生 B、②中转化前后碳元素的化合价不变 C、③可用于工业炼铁,属于置换反应 D、隔绝氧气或者水可以防止④的发生二、非选择题
-
16. 中华优秀传统文化涉及很多化学知识、原理与应用。
 (1)、《天工开物》介绍了酒曲的制作工艺,使用淀粉类作物加入酒曲发酵酿酒的过程属于(填“剧烈氧化”或“缓慢氧化”)。(2)、西汉铜缸灯(如图1)出土时表面有铜绿,可用稀盐酸擦去,有关反应的化学方程式为Cu2(OH)2CO3+4HCl=2+3H2O+CO2↑。铜缸灯灯罩可自由开合,以调节进风量的大小。当有大量黑烟产生时,应(填“扩大”或“减小”)进风口。(3)、化学能拓展绘画表现形式。如图2,在未着色的葡萄画旁边放置盛有浓氨水的烧杯,一段时间后,“葡萄”变红了。从微观视角分析,“葡萄”变红的原因是。(4)、长期放置的油画因生成黑色的PbS而色彩变暗。用H2O2修复油画时,生成白色的PbSO4和一种常见的氧化物,反应的化学方程式为。(5)、《吕氏春秋》记载“金柔锡柔,合两柔则刚(即坚硬)”(注:金指铜单质,锡指锡单质)。这句话说明铜锡合金具有的特性是。17. 向海洋进军——LNG船:航行在大洋上的巨轮中,有一种我国自主研发、制造难度堪比航母的巨轮,它就是LNG液化天然气运输船,被喻为世界造船业“皇冠上的明珠”。
(1)、《天工开物》介绍了酒曲的制作工艺,使用淀粉类作物加入酒曲发酵酿酒的过程属于(填“剧烈氧化”或“缓慢氧化”)。(2)、西汉铜缸灯(如图1)出土时表面有铜绿,可用稀盐酸擦去,有关反应的化学方程式为Cu2(OH)2CO3+4HCl=2+3H2O+CO2↑。铜缸灯灯罩可自由开合,以调节进风量的大小。当有大量黑烟产生时,应(填“扩大”或“减小”)进风口。(3)、化学能拓展绘画表现形式。如图2,在未着色的葡萄画旁边放置盛有浓氨水的烧杯,一段时间后,“葡萄”变红了。从微观视角分析,“葡萄”变红的原因是。(4)、长期放置的油画因生成黑色的PbS而色彩变暗。用H2O2修复油画时,生成白色的PbSO4和一种常见的氧化物,反应的化学方程式为。(5)、《吕氏春秋》记载“金柔锡柔,合两柔则刚(即坚硬)”(注:金指铜单质,锡指锡单质)。这句话说明铜锡合金具有的特性是。17. 向海洋进军——LNG船:航行在大洋上的巨轮中,有一种我国自主研发、制造难度堪比航母的巨轮,它就是LNG液化天然气运输船,被喻为世界造船业“皇冠上的明珠”。天然气装载时,应该在-163℃环境下将其变为液态。而液化后的体积是气态的 , 大大提高了运输效率。一般17万立方米的运输船装载的液态天然气经汽化后形成的容量,可满足2418万人一个月的使用量,是一种“海上超级冷冻车”。
装载这类货物的运货系统所用钢板,含镍量达到36%,称为殷瓦钢。它非常薄,只有0.7mm,在-196℃之内,其收缩量膨胀系数非常低。它在空气中对温度的要求非常高,如在施工过程中沾上汗水,24小时内就会被锈穿,使得钢板报废。殷瓦钢还在制造精密仪器、仪表零部件中有着广泛的应用。

依据上文,回答下列问题。
(1)、殷瓦钢的主要成分为 , 属于(填“非金属”或“金属”)材料。(2)、殷瓦钢具有的性质是(写一条)。(3)、下列关于殷瓦钢的说法不正确的是(多选,填字母)。a.殷瓦钢是纯净物 b.殷瓦钢的硬度比铁小
c.殷瓦钢的熔点比镍低 d.殷瓦钢中各成分均不与稀盐酸反应
(4)、天然气燃烧时发生反应的化学方程式为。(5)、LNG船可通过降温加压使天然气液化后再运输的原因是。18. 实验室制取O2(1)、ⅰ、图1中仪器①的名称是。
ⅱ、写出实验室用氯酸钾、二氧化锰混合制取氧气的化学方程式: , 所选用的发生装置为图1中的(填编号)。如果选用丙装置收集生成的氧气,那么气体应由(填“A”或“B”)端进。
ⅲ、下列是加热高锰酸钾制取并收集氧气的部分操作示意图,其中正确的是(填字母)。
a.检查装置的气密性
 b.出现气泡立即收集
b.出现气泡立即收集
c.收集满后移出集气瓶
 d.结束后先停止加热
d.结束后先停止加热 (2)、对食盐水的组成进行探究
(2)、对食盐水的组成进行探究ⅰ、食盐溶解在水中,是以(填化学符号)形式分散在水中,形成无色透明溶液。
ⅱ、探究水的组成:如图2为自制电解水实验装置,结束时,注射器Ⅰ、Ⅱ中活塞分别停留在mL、12mL刻度线处。拔出注射器、检验所得气体。电解水的化学方程式为 , 由此可知水是由氢元素、氧元素组成的。
 19. 中央电视台举办的“3·15”晚会曾曝出某品牌金饰品掺假的事件,引起同学们的好奇。某化学兴趣小组在老师的指导下对几种常见金属饰品进行了以下相关的探究活动。
19. 中央电视台举办的“3·15”晚会曾曝出某品牌金饰品掺假的事件,引起同学们的好奇。某化学兴趣小组在老师的指导下对几种常见金属饰品进行了以下相关的探究活动。【查阅资料】
①假黄金通常含黄铜(Cu-Zn合金)。
②假铂金或假银饰品通常含金属钯(Pd),钯是航空、航天等高科技领域以及汽车制造业不可缺少的关键材料,呈银白色,有金属光泽,可作饰品。
【提出问题】①怎样鉴别真假黄金? ②怎样确定钯的金属活动性?
【实验药品】钯(Pd)、铂(Pt)、稀盐酸(HCI)、硝酸银(AgNO3)溶液和氯化钯(PdCl2)溶液。
【实验探究】
(1)、鉴别黄金样品的真假实验步骤
实验现象
分析与结论
取少量黄金样品于试
管中,滴加
黄金样品表面
有气泡产生
此样品为(填“真”或“假”)
黄金,反应的化学方程式为。
(2)、探究钯的金属活动性实验步骤
实验现象
分析与结论
①将钯浸入硝酸银溶液中一段时间
无明显现象
金属活动性:PdAg
(填 “>”或“<")
②将铂浸入溶液中一段时间
金属活动性:Pd>Pt
结合实验步骤①和步骤②,初步得出钯、银、铂的金属活动性由强到弱的顺序为(用化学式表示)。
(3)、【拓展应用】小组同学在鉴别黄金样品的真假时,除了选上述方法外,还可以取少量黄金样品于试管中,滴加 , 观察现象,也可得到相同的结论。
(4)、银、铂、钯都属于贵重金属,其回收具有重要的现实意义,请写出其中一点:。20. 锌精矿(主要成分为ZnS,含少量铜元素)是生产金属锌的主要原料,用锌精矿石火法炼锌的工艺流程如图所示。 (1)、沸腾炉的炉气若直接排放会引起酸雨,这是因为其中含有 , 它产生的原因是。(2)、焦炭进入还原炉前需粉碎处理,这样做的目的是 , 焦炭与氧化铜反应的化学方程式为。(3)、冷凝器中锌蒸气变为固体锌的微观实质是锌原子间的间隔。(4)、相同质量的下列化合物中,含锌质量最多的是(填字母)。
(1)、沸腾炉的炉气若直接排放会引起酸雨,这是因为其中含有 , 它产生的原因是。(2)、焦炭进入还原炉前需粉碎处理,这样做的目的是 , 焦炭与氧化铜反应的化学方程式为。(3)、冷凝器中锌蒸气变为固体锌的微观实质是锌原子间的间隔。(4)、相同质量的下列化合物中,含锌质量最多的是(填字母)。a.ZnS b.ZnO c.ZnCO3 d.Zn(OH)2
21. 利用数据传感器可以形象地比较过氧化氢溶液在有无催化剂条件下分解速率的不同及测过氧化氢溶液的浓度。小芳利用图1的装置测得瓶内气压如图2所示。 (1)、二氧化锰作为催化剂,在化学反应前后本身的质量和都没有发生变化,反应后可通过、洗涤、烘干等操作分离出来再利用。(2)、由图分析可知,曲线(填“①”或“②”)能表示甲瓶反应情况。(3)、甲瓶完全反应后最终生成1.6g氧气,已知此过氧化氢溶液的密度为1g/cm3 , 请计算30mL该过氧化氢溶液中的溶质质量分数。(写出计算过程,结果精确到0.1%)(4)、图2中的①和②两条线最终重合的原因是。
(1)、二氧化锰作为催化剂,在化学反应前后本身的质量和都没有发生变化,反应后可通过、洗涤、烘干等操作分离出来再利用。(2)、由图分析可知,曲线(填“①”或“②”)能表示甲瓶反应情况。(3)、甲瓶完全反应后最终生成1.6g氧气,已知此过氧化氢溶液的密度为1g/cm3 , 请计算30mL该过氧化氢溶液中的溶质质量分数。(写出计算过程,结果精确到0.1%)(4)、图2中的①和②两条线最终重合的原因是。