广东省广州市海珠区2023-2024学年九年级上学期期末化学试题
试卷更新日期:2024-01-31 类型:期末考试
一、选择题
-
1. 下列属于化学变化的是A、用石墨为原料合成金刚石 B、用铜片制成铜壶 C、用彩纸剪出精美的作品 D、用活性炭脱去色素制白糖2. 下列对实验现象的描述正确的是A、木炭在氧气中剧烈燃烧,生成黑色固体 B、在空气中加热铜丝,黑色固体变成红色 C、向氢氧化钠溶液中滴加硫酸铜溶液,产生蓝色沉淀 D、将带火星木条伸入5%过氧化氢溶液中,木条复燃3. 在生产、运输、使用和贮存化学药品时,应注意安全。汽油运输车须张贴的标志是( )A、

B、
B、
C、
C、
D、
D、
4. 下列物质中,属于氧化物的是A、ZnSO4 B、O3 C、HgO D、Al(NO3)35. 下列化学用语与含义相符的是A、3Ne——3个氖元素 B、2——2个亚铁离子 C、I2——2个碘原子 D、NaBr——溴化钠6. 下列说法中,正确的是A、氢元素与氧元素的本质区别是相对原子质量不同 B、与元素化学性质关系最密切的是其原子的最外层电子数 C、氯化钠是由氯化钠离子构成的 D、原子中,由于核电荷数等于质子数,所以原子不显电性7. 下列实验操作正确的是A、读出量筒中液体的体积
4. 下列物质中,属于氧化物的是A、ZnSO4 B、O3 C、HgO D、Al(NO3)35. 下列化学用语与含义相符的是A、3Ne——3个氖元素 B、2——2个亚铁离子 C、I2——2个碘原子 D、NaBr——溴化钠6. 下列说法中,正确的是A、氢元素与氧元素的本质区别是相对原子质量不同 B、与元素化学性质关系最密切的是其原子的最外层电子数 C、氯化钠是由氯化钠离子构成的 D、原子中,由于核电荷数等于质子数,所以原子不显电性7. 下列实验操作正确的是A、读出量筒中液体的体积 B、用燃着的酒精灯点燃酒精灯
B、用燃着的酒精灯点燃酒精灯 C、取液后的胶头滴管平放在桌面
C、取液后的胶头滴管平放在桌面 D、将混合液倒入过滤器过滤
D、将混合液倒入过滤器过滤 8. 下列物质鉴别的实验方案中,不可行的是
8. 下列物质鉴别的实验方案中,不可行的是选项
实验目的
实验设计
A
鉴别CO与H2
分别点燃,观察火焰颜色
B
鉴别食醋和蒸馏水
通过闻气味鉴别
C
鉴别硫酸铜溶液和稀硫酸
观察颜色
D
鉴别CO2和CO
通过澄清石灰水
A、A B、B C、C D、D9. 如图是一氧化碳与氧化铜反应的装置,下列说法错误的是 A、一氧化碳的还原性可用于冶炼金属 B、A处观察到的有气体生成 C、B处石灰水变浑浊,说明有二氧化碳生成 D、C处酒精灯的作用是点燃一氧化碳,防止污染空气10. 高氯酸(HClO4)可用于人造金刚石提纯,其中Cl的化合价为A、-1 B、+3 C、+5 D、+711. 硒元素是动物体必需营养元素和植物有益的营养元素。硒在元素周期表中的信息及原子结构示意图如图所示。下列关于硒元素的说法错误的是( )
A、一氧化碳的还原性可用于冶炼金属 B、A处观察到的有气体生成 C、B处石灰水变浑浊,说明有二氧化碳生成 D、C处酒精灯的作用是点燃一氧化碳,防止污染空气10. 高氯酸(HClO4)可用于人造金刚石提纯,其中Cl的化合价为A、-1 B、+3 C、+5 D、+711. 硒元素是动物体必需营养元素和植物有益的营养元素。硒在元素周期表中的信息及原子结构示意图如图所示。下列关于硒元素的说法错误的是( )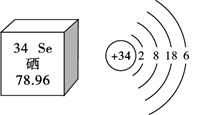 A、硒的原子序数为34 B、硒的相对原子质量是78.96 C、硒在化学反应中容易失去电子 D、硒化氢的化学式是H2Se12. 空气是多种气体的混合物,下列生产生活中用到的气体来自空气的是A、新能源汽车中使用的氢气 B、填充气球用到的氦气 C、炼铁用到的一氧化碳 D、做饭用到的天然气13. 广州北部水厂平用了先进的超滤膜净水技术,超滤膜能有效去除水中的悬浮物、藻类、细菌等不溶性杂质。下列说法错误的是A、经过超滤膜后的水不是纯净水 B、活性炭可除去水中异味 C、超滤膜可降低水的硬度 D、加入明矾能促进水中悬浮杂质沉降14. 氢化钠NaH可在野外用作生氢剂,其中氢元素为-1价。NaH用作生氢剂时的化学反应原理为:NaH+H2O=X+H2↑,关于此反应的说法错误的是A、X的化学式为NaOH B、反应前后物质状态发生变化 C、反应前后有氢元素化合价发生变化 D、反应前后元素种类发生变化15. 液氢、煤油(含C、H元素)、液氧可用作神舟飞船运载火箭的推进剂,下列说法不正确的是A、火箭发射时仅靠空气不足以使燃料充分燃烧 B、液氢和煤油完全燃烧的反应都是化合反应 C、液氢是高能燃料且燃烧后的产物无污染 D、飞船进入轨道后主要利用太阳能维持工作16. 下列关于碳和碳的氧化物的说法,正确的是A、空气中的二氧化碳是造成酸雨的主要物质 B、用碳素墨水书写具有保存价值的档案,因为碳常温下化学性质稳定 C、金刚石、石墨、C60物理性质不同是因为其碳原子的结构不同 D、空气中CO2体积分数达到10%,会导致人呼吸停止,因此,二氧化碳有毒性17. 下列化学方程式中,书写正确的是A、3Fe+2O2Fe2O3 B、2C+O22CO C、H2+Cl22HCl↑ D、Zn+2H2SO4=Zn(SO4)2+H2↑18. 下列关于能源的说法,正确的是A、酒精是一种常见的不可再生能源 B、石油是一种重要的化工产品,主要含碳、氢元素 C、工业上常把煤块粉碎后使其充分燃烧,其目的是减少煤的浪费 D、人类利用的能源都是通过化学反应获得的19. 下列说法正确的是A、蜡烛燃烧后质量减小,说明质量守恒定律不是普遍规律 B、6g氢气和30g氧气反应,可生成36g水 C、根据化学方程式,可知道化学反应的快慢 D、根据化学方程式可以获得参与反应的各物质的微粒个数比20. 下列实验中,根据实验现象可得到相应结论的是
A、硒的原子序数为34 B、硒的相对原子质量是78.96 C、硒在化学反应中容易失去电子 D、硒化氢的化学式是H2Se12. 空气是多种气体的混合物,下列生产生活中用到的气体来自空气的是A、新能源汽车中使用的氢气 B、填充气球用到的氦气 C、炼铁用到的一氧化碳 D、做饭用到的天然气13. 广州北部水厂平用了先进的超滤膜净水技术,超滤膜能有效去除水中的悬浮物、藻类、细菌等不溶性杂质。下列说法错误的是A、经过超滤膜后的水不是纯净水 B、活性炭可除去水中异味 C、超滤膜可降低水的硬度 D、加入明矾能促进水中悬浮杂质沉降14. 氢化钠NaH可在野外用作生氢剂,其中氢元素为-1价。NaH用作生氢剂时的化学反应原理为:NaH+H2O=X+H2↑,关于此反应的说法错误的是A、X的化学式为NaOH B、反应前后物质状态发生变化 C、反应前后有氢元素化合价发生变化 D、反应前后元素种类发生变化15. 液氢、煤油(含C、H元素)、液氧可用作神舟飞船运载火箭的推进剂,下列说法不正确的是A、火箭发射时仅靠空气不足以使燃料充分燃烧 B、液氢和煤油完全燃烧的反应都是化合反应 C、液氢是高能燃料且燃烧后的产物无污染 D、飞船进入轨道后主要利用太阳能维持工作16. 下列关于碳和碳的氧化物的说法,正确的是A、空气中的二氧化碳是造成酸雨的主要物质 B、用碳素墨水书写具有保存价值的档案,因为碳常温下化学性质稳定 C、金刚石、石墨、C60物理性质不同是因为其碳原子的结构不同 D、空气中CO2体积分数达到10%,会导致人呼吸停止,因此,二氧化碳有毒性17. 下列化学方程式中,书写正确的是A、3Fe+2O2Fe2O3 B、2C+O22CO C、H2+Cl22HCl↑ D、Zn+2H2SO4=Zn(SO4)2+H2↑18. 下列关于能源的说法,正确的是A、酒精是一种常见的不可再生能源 B、石油是一种重要的化工产品,主要含碳、氢元素 C、工业上常把煤块粉碎后使其充分燃烧,其目的是减少煤的浪费 D、人类利用的能源都是通过化学反应获得的19. 下列说法正确的是A、蜡烛燃烧后质量减小,说明质量守恒定律不是普遍规律 B、6g氢气和30g氧气反应,可生成36g水 C、根据化学方程式,可知道化学反应的快慢 D、根据化学方程式可以获得参与反应的各物质的微粒个数比20. 下列实验中,根据实验现象可得到相应结论的是 A、实验①:进行粉尘爆炸实验,鼓入空气后罐内发生爆炸,说明面粉具有可燃性 B、实验②:向鸡蛋壳中加入醋酸产生气泡,气体使澄清石灰水变浑浊,说明鸡蛋壳中含有钙元素 C、实验③:检查装置气密性时导管口有气泡冒出,说明装置内气体分子的大小发生变化 D、实验④:用向下排空气法收集甲烷,说明甲烷的密度比空气大
A、实验①:进行粉尘爆炸实验,鼓入空气后罐内发生爆炸,说明面粉具有可燃性 B、实验②:向鸡蛋壳中加入醋酸产生气泡,气体使澄清石灰水变浑浊,说明鸡蛋壳中含有钙元素 C、实验③:检查装置气密性时导管口有气泡冒出,说明装置内气体分子的大小发生变化 D、实验④:用向下排空气法收集甲烷,说明甲烷的密度比空气大二、填空题
-
21. 用化学用语表示。(1)、2个钠原子。(2)、钙离子。(3)、氢氧化镁。(4)、氯化铁中铁的化合价。22. 在A、B、C、D、E、F六种物质中,C被誉为生命之源,A、D都是单质,在一定的条件下它们存在如下的转化关系:
①A+B→Cu+C②D+B→Cu+E③F→CaO+E
请回答:
(1)、写出有关物质的化学式:C;F。(2)、写出反应②、③的化学方程式:反应②:;反应③:。
23. 人类的生活和工农业生产都离不开水。(1)、如图是自来水厂净水过程示意图。
我国古人也使用了相关的净水方法。
①《茶经·四之器》记载了人们用一种铜制成的“水囊”工具去除饮用水中的难溶性物质,其原理和上述的池相同。
②采用明矾净水最早见于《天工开物》一书,其原理和上述的池相同。
(2)、进行过滤操作时:①需用到的玻璃仪器有玻璃棒、烧杯、。
②过滤操作中要注意“一贴二低三靠”,“一贴”是指用少量水润湿滤纸并使滤纸与漏斗壁之间不要有气泡,原因是。
(3)、日常生活中,既可降低水的硬度,又可杀菌的方法是。(4)、水曾经被认为是一种不可再分的物质,经过不断探索和实验,揭开了水的组成奥秘,下列说法正确的是____。(填标号)A、电解水的反应属于分解反应 B、只能通过电解水实验,才能证明水是由氢、氧两种元素组成的 C、通过电解水实验,说明水分子中含有氢分子和氧分子 D、找到合适的催化剂就能利用太阳光将水分解生产H224. 对宏观现象进行微观分析,是学习化学的重要思路和方法。(1)、从宏观角度看,氨气(NH3)是由组成;从微观角度看,构成氨气的粒子是。(2)、硫粉在空气中燃烧产生火焰,在氧气中燃烧产生火焰,从微观角度分析,硫在氧气中燃烧更剧烈的原因是。(3)、燃油汽车发动机排出的气体中含有CO和NO等,安装催化转化器可减少这些有害气体的排放。CO和NO在经过催化转化器时相互反应,示意图如图。
生成物“
 ”是(写化学式),两种生成物的分子个数比为。25. 习近平主席提出我国力争在2060年前实现碳中和。碳中和是指二氧化碳的排放量等于吸收量。(1)、化石燃料包括煤、天然气和。(2)、天然气主要成分是甲烷,甲烷燃烧的化学方程式为。(3)、埋于海底,可能替代化石燃料的新能源是。(4)、大气中的二氧化碳主要是靠植物的光合作用进行吸收。石灰水也能吸收二氧化碳并生成白色沉淀,该反应的化学方程式为;已知二氧化碳可发生下述反应:CaCO3+CO2+H2O=Ca(HCO3)2 , 且Ca(HCO3)2能溶于水,预测继续通入二氧化碳现象为。
”是(写化学式),两种生成物的分子个数比为。25. 习近平主席提出我国力争在2060年前实现碳中和。碳中和是指二氧化碳的排放量等于吸收量。(1)、化石燃料包括煤、天然气和。(2)、天然气主要成分是甲烷,甲烷燃烧的化学方程式为。(3)、埋于海底,可能替代化石燃料的新能源是。(4)、大气中的二氧化碳主要是靠植物的光合作用进行吸收。石灰水也能吸收二氧化碳并生成白色沉淀,该反应的化学方程式为;已知二氧化碳可发生下述反应:CaCO3+CO2+H2O=Ca(HCO3)2 , 且Ca(HCO3)2能溶于水,预测继续通入二氧化碳现象为。三、计算题
-
26. N(NO2)3是科学家发现的一种新型火箭燃料。请计算:(1)、N(NO2)3中,氮、氧两种元素的质量比是。(2)、N(NO2)3中,氮元素的质量分数是(计算结果精确到0.1%)(3)、kgN(NO2)3中含有28kg氮元素。27. 如图为电解水实验。
 (1)、a处产生的物质为。(填化学式)(2)、a、b两处气体的分子个数比为。(3)、a、b两处气体的质量比为。(4)、a、b两处气体的密度比约为。
(1)、a处产生的物质为。(填化学式)(2)、a、b两处气体的分子个数比为。(3)、a、b两处气体的质量比为。(4)、a、b两处气体的密度比约为。已知:气体的密度(p)=
四、实验与探究
-
28. 以下是实验室制取气体的部分仪器和装置。
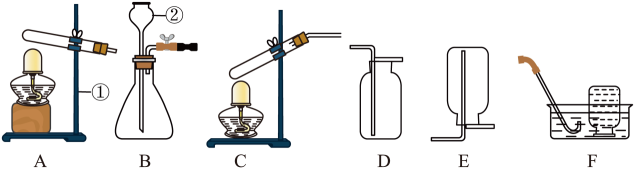 (1)、仪器①、②的名称是:① , ②。(2)、用高锰酸钾制取氧气,装置A需要改动的是 , 如用F装置收集氧气,当观察到时,再把导管口伸入盛满水的集气瓶里。(3)、检查装置B的气密性,按图连接好装置,用弹簧夹夹紧胶管,再向长颈漏斗中加水至形成一段水柱,静止,若观察到 , 说明气密性良好。(4)、小明想用同一套装置分别制取O2和CO2 , 应选用发生装置和收集装置的组合是(填标号)。其中,实验制取CO2的化学方程式为。(5)、制备CO的原理是:HCOOHCO↑+H2O(HCOOH在常温下为液态),如图可用于制备CO的发生装置是(填标号)。29. 利用CO2解决全球能源和环境问题的最有前途的方案之一。用光能和光催化剂,可将CO2和水蒸气转化为CH4和O2 , 紫外光照射时,在不间光催化剂(I,II,III)作用下,CH4产量随光照时间的变化如图所示。
(1)、仪器①、②的名称是:① , ②。(2)、用高锰酸钾制取氧气,装置A需要改动的是 , 如用F装置收集氧气,当观察到时,再把导管口伸入盛满水的集气瓶里。(3)、检查装置B的气密性,按图连接好装置,用弹簧夹夹紧胶管,再向长颈漏斗中加水至形成一段水柱,静止,若观察到 , 说明气密性良好。(4)、小明想用同一套装置分别制取O2和CO2 , 应选用发生装置和收集装置的组合是(填标号)。其中,实验制取CO2的化学方程式为。(5)、制备CO的原理是:HCOOHCO↑+H2O(HCOOH在常温下为液态),如图可用于制备CO的发生装置是(填标号)。29. 利用CO2解决全球能源和环境问题的最有前途的方案之一。用光能和光催化剂,可将CO2和水蒸气转化为CH4和O2 , 紫外光照射时,在不间光催化剂(I,II,III)作用下,CH4产量随光照时间的变化如图所示。 (1)、请写出该反应的化学反应方程式。(2)、根据图像分析,CH4的产量受到因素的影响。(3)、反应开始后的12小时内,在第种(填“I”“II”“III”)光催化剂的作用下,收集的CH4最多。30. 懂得燃烧条件和灭火原理,对于防范火灾和自救至关重要。(1)、用棉花分别蘸酒精和水,放到酒精灯火焰上加热片刻,观察现象。该实验可说明燃烧的条件之一是。(2)、用如图所示实验探究燃烧的条件。
(1)、请写出该反应的化学反应方程式。(2)、根据图像分析,CH4的产量受到因素的影响。(3)、反应开始后的12小时内,在第种(填“I”“II”“III”)光催化剂的作用下,收集的CH4最多。30. 懂得燃烧条件和灭火原理,对于防范火灾和自救至关重要。(1)、用棉花分别蘸酒精和水,放到酒精灯火焰上加热片刻,观察现象。该实验可说明燃烧的条件之一是。(2)、用如图所示实验探究燃烧的条件。已知:白磷的着火点是40℃、红磷的着火点是240℃。
I
II
III
IV




白磷不燃烧
白磷不燃烧
白磷不燃烧
白磷燃烧
请回答:
①获得“可燃物燃烧需要氧气(或空气)”这一结论的实验是。(填标号)
②对比实验III、IV说明燃烧的条件之一是。
③白磷保存在水中,以防。
④本实验用红磷替代白磷,(填“能”或“不能”)得到相同的实验结论,原因是。
⑤查阅资料:五氧化二磷与热水反应生成磷酸(H3PO4),请写出该反应的化学方程式。
(3)、炒菜时油锅着火,灭火的方法是。31. 小明同学看到了两瓶不同的碳酸饮料A和B,它们的标签如表:饮料A
饮料B
配料
水、果葡糖浆、白砂糖、食品添加剂(二氧化碳、柠檬酸、柠檬酸钠、苯甲酸钠)、食用香精
水、食品添加剂(二氧化碳、柠檬酸、柠檬酸钠、苯甲酸钠、阿斯巴甜、安赛蜜、蔗糖素)、食用香精
营养成分表
蛋白质0g/100mL
蛋白质0g/100mL
脂肪0g/100mL
脂肪0g/100mL
碳水化合物11.0g/100mL
碳水化合物0g/100mL
钠19mg/100mL
钠21mg/100mL
能量
191kJ/100mL
0kJ/100mL
小明利用这两瓶饮料进行了以下的实验探究:
实验用品:饮料A、饮料B、注射器、紫色石蕊试液、干燥的紫色石蕊试纸(用紫色石蕊试液染成后晾干制成)、试管若干
(1)、振荡两瓶饮料时均产生大量的气泡,该现象的化学方程式为。用注射器抽取饮料产生的气体,通入澄清石灰水,澄清石灰水变浑浊。(2)、分别取少量饮料A和饮料B于试管中,滴加紫色石蕊试液,试液变为红色,得出结论:碳酸能使紫色石蕊试液变红。你认为该结论是否正确,请说明理由:。(3)、用注射器抽取饮料产生的气体,通入紫色石蕊试液中,溶液变为红色。小明猜想使紫色石蕊变色的因素有三种:
①水能使紫色石蕊变色;
②。
③二氧化碳和水反应生成的碳酸能使紫色石蕊变色。
通过分析,因为 , 所以排除假设①。
设计实验验证猜想②和猜想③。
实验操作
实验现象
实验结论
1.用注射器抽取饮料产生的气体,通入装有干燥的紫色石蕊试纸的试管中
则猜想②不成立
2.用注射器抽取饮料产生的气体,
紫色石蕊试纸变红
结合操作1结论,猜想③成立。
(4)、根据观察两瓶饮料的标签,你觉得能产生能量的物质是。