沪教版初中化学九年级下册 7.2 常见的酸和碱 同步分层训练培优题(第2课时)
试卷更新日期:2024-01-30 类型:同步测试
一、单项选择题
-
1. 在室温下将少量氧化钙加入到一定量的饱和氢氧化钙溶液中,搅拌并恢复到室温。图像中x代表时间,则y代表的是( )
 A、溶液的质量 B、溶质的溶解度 C、溶质的质量 D、溶质的质量分数2. 推理是学习化学的一种方法。以下推理正确的是( )A、碱溶液显碱性,则显碱性的溶液一定是碱溶液 B、pH<7 的溶液呈酸性,则pH<7的雨水是酸雨 C、由金属离子和酸根离子构成的化合物是盐,所以盐中一定含有金属元素 D、复分解反应只是两种化合物相互交换成分,则复分解反应一定没有元素化合价的改变3. 开展如图实验探究,下列说法错误的是( )
A、溶液的质量 B、溶质的溶解度 C、溶质的质量 D、溶质的质量分数2. 推理是学习化学的一种方法。以下推理正确的是( )A、碱溶液显碱性,则显碱性的溶液一定是碱溶液 B、pH<7 的溶液呈酸性,则pH<7的雨水是酸雨 C、由金属离子和酸根离子构成的化合物是盐,所以盐中一定含有金属元素 D、复分解反应只是两种化合物相互交换成分,则复分解反应一定没有元素化合价的改变3. 开展如图实验探究,下列说法错误的是( )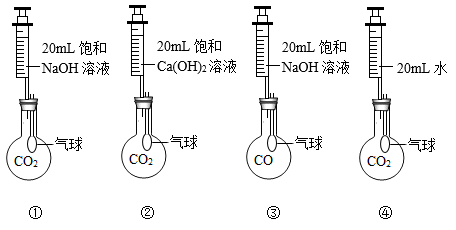 A、对比①②可探究:饱和NaOH溶液对CO2的吸收效果更好 B、对比①③可探究:CO不与NaOH反应 C、对比①④可探究:CO2能与NaOH反应 D、对比②④可探究:CO2能与水反应4. 化学与生活息息相关。日常生活中的下列说法或做法不正确的是( )A、浓硫酸不慎沾在皮肤上,先用大量水冲洗,再涂上3%—5%的烧碱溶液 B、氢氧化钠可作炉具清洁剂 C、被蚊虫叮咬后可涂抹肥皂水来消除痛痒 D、用熟石灰改良酸性土壤5. 盐酸与氢氧化钠溶液反应时溶液pH的变化如下图。下列说法正确的是( )
A、对比①②可探究:饱和NaOH溶液对CO2的吸收效果更好 B、对比①③可探究:CO不与NaOH反应 C、对比①④可探究:CO2能与NaOH反应 D、对比②④可探究:CO2能与水反应4. 化学与生活息息相关。日常生活中的下列说法或做法不正确的是( )A、浓硫酸不慎沾在皮肤上,先用大量水冲洗,再涂上3%—5%的烧碱溶液 B、氢氧化钠可作炉具清洁剂 C、被蚊虫叮咬后可涂抹肥皂水来消除痛痒 D、用熟石灰改良酸性土壤5. 盐酸与氢氧化钠溶液反应时溶液pH的变化如下图。下列说法正确的是( )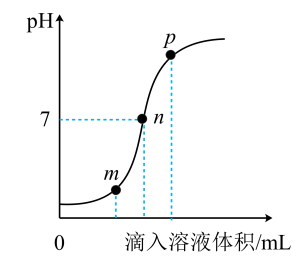 A、点所示溶液中的溶质为 B、、点所示溶液中加酚酞溶液显红色 C、该图所对应操作是将盐酸滴入氢氧化钠溶液中 D、该反应的本质是溶液中的与反应生成水6. 某实验探究小组用pH传感器探究稀盐酸和氢氧化钠溶液的反应过程,实验操作和测定结果如图所示。下列叙述中正确的是( )
A、点所示溶液中的溶质为 B、、点所示溶液中加酚酞溶液显红色 C、该图所对应操作是将盐酸滴入氢氧化钠溶液中 D、该反应的本质是溶液中的与反应生成水6. 某实验探究小组用pH传感器探究稀盐酸和氢氧化钠溶液的反应过程,实验操作和测定结果如图所示。下列叙述中正确的是( )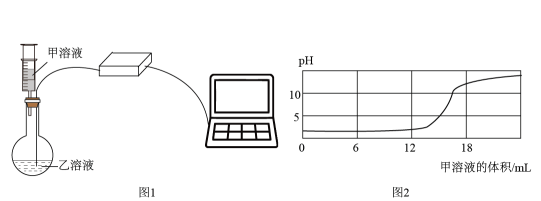
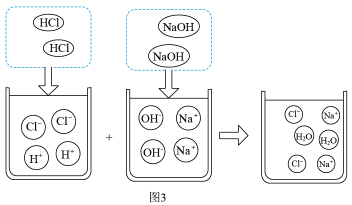 A、图1使用注射器加入甲溶液,主要是为了精确地计量液体体积 B、依据图2给定结果,圆底烧瓶内加入的乙溶液为NaOH溶液 C、结合图3分析,加入甲溶液6mL时,烧瓶中的溶液只有Na+、Cl- D、加入甲溶液12mL后,将所得溶液蒸干,得到固体只含NaCl7. 若用100g8%的盐酸和100g8%的氢氧化钾溶液反应,则反应后溶液的pH( )A、大于7 B、小于7 C、等于7 D、无法确定8. 向氢氧化钠溶液中加入一定量的稀硫酸充分反应。取少量反应后的溶液进行下列实验,能证明二者恰好完全反应的是( )A、滴入几滴酚酞溶液,溶液变红色 B、滴入适量CuCl2溶液,无沉淀生成 C、滴入适量BaCl2溶液和稀硝酸,观察到有白色沉淀 D、测得混合液中Na+与的个数比为2:19. 下列实际应用中,利用中和反应原理的是( )
A、图1使用注射器加入甲溶液,主要是为了精确地计量液体体积 B、依据图2给定结果,圆底烧瓶内加入的乙溶液为NaOH溶液 C、结合图3分析,加入甲溶液6mL时,烧瓶中的溶液只有Na+、Cl- D、加入甲溶液12mL后,将所得溶液蒸干,得到固体只含NaCl7. 若用100g8%的盐酸和100g8%的氢氧化钾溶液反应,则反应后溶液的pH( )A、大于7 B、小于7 C、等于7 D、无法确定8. 向氢氧化钠溶液中加入一定量的稀硫酸充分反应。取少量反应后的溶液进行下列实验,能证明二者恰好完全反应的是( )A、滴入几滴酚酞溶液,溶液变红色 B、滴入适量CuCl2溶液,无沉淀生成 C、滴入适量BaCl2溶液和稀硝酸,观察到有白色沉淀 D、测得混合液中Na+与的个数比为2:19. 下列实际应用中,利用中和反应原理的是( )①用氢氧化钠溶液洗涤石油中残余的硫酸②用含氢氧化铝的药物治疗胃酸过多
③用熟石灰改良酸性土壤
④将稀氨水(含有、OH-)涂抹在蚊虫叮咬处(分泌出蚁酸)能止痒
A、①②③④ B、仅①②③ C、仅②③④ D、仅①③④10. 如图所示,滴管中吸入某种液体,平底烧瓶中盛有另一种物质,挤压滴管滴入液体,一段时间后气球明显鼓起。下列选项不符合题意的是( )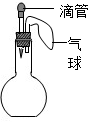
选项
滴管内物质
平底烧瓶内物质
A
稀盐酸
锌粒
B
氢氧化钙溶液
二氧化碳气体
C
浓硫酸
水
D
碳酸钠溶液
稀硫酸
A、A B、B C、C D、D11. 某同学对化学知识的归纳正确的是 ( )A、饱和溶液析出晶体后溶质质量分数一定减小 B、同种元素组成的物质一定是单质 C、生成盐和水的反应一定是复分解反应 D、碱溶液和盐溶液发生反应后,所得溶液的质量一定减小12. 反应可用于钢铁除锈。下列说法正确的是( )A、X的化学式为FeCl2 B、该反应属于复分解反应 C、使用NaOH溶液亦可去除铁锈 D、去除铁锈后所得废液可以直接排放13. 下列实验不能达到实验目的的是( )A、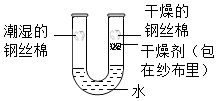 实验探究铁锈蚀是否与水有关
B、
实验探究铁锈蚀是否与水有关
B、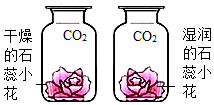 实验探究二氧化碳是否与水发生反应
C、
实验探究二氧化碳是否与水发生反应
C、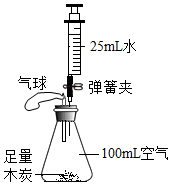 实验测定空气中氧气的含量
D、
实验测定空气中氧气的含量
D、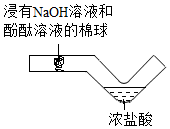 实验探究氢氧化钠与盐酸能否发生反应
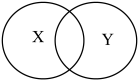
14. 下列概念之间存在图所示关系的是( )
实验探究氢氧化钠与盐酸能否发生反应
14. 下列概念之间存在图所示关系的是( )选项
A
B
C
D
概念
X
单质
氧化反应
碱溶液
中和反应
Y
化合物
化合反应
碱性溶液
分解反应
 A、A B、B C、C D、D15. 类比推理在化学学习和科学研究中有重要意义,下列类比推理正确的是( )A、氢氧化钠可以中和盐酸,因此用氢氧化钠治疗胃酸过多 B、中和反应生成盐和水,因此有盐和水生成的反应一定是中和反应. C、酸能使紫色石蕊溶液变红,因此使石蕊溶液变红的就一定是酸性溶液 D、溶液具有均一性、稳定性,因此具有均一、稳定性的液体一定是溶液
A、A B、B C、C D、D15. 类比推理在化学学习和科学研究中有重要意义,下列类比推理正确的是( )A、氢氧化钠可以中和盐酸,因此用氢氧化钠治疗胃酸过多 B、中和反应生成盐和水,因此有盐和水生成的反应一定是中和反应. C、酸能使紫色石蕊溶液变红,因此使石蕊溶液变红的就一定是酸性溶液 D、溶液具有均一性、稳定性,因此具有均一、稳定性的液体一定是溶液二、综合题
-
16. 某化学兴趣小组在学习盐酸与氢氧化钠的反应后,分别结合自己在实验室中所做的实验,各从不同方面对其进行图像描述。图1是反应过程中溶液的酸碱度变化图,图2是微观粒子结合过程的示意图。
图1
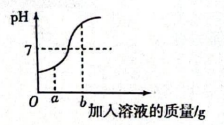 图2
图2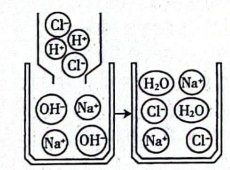
根据图1的曲线变化,回答下列问题:
(1)、该变化对应的实验操作是将滴加到另一种溶液中;(2)、当滴入溶液的质量为ag时,溶液中的溶质为(填化学式);(3)、当溶液的pH=7时,溶液中的主要离子是(填离子符号);(4)、当加入溶液的质量为bg时,向所得溶液中滴加紫色石蕊溶液,溶液呈色。(5)、【结论】从反应前后离子的种类看,有些离子参与了反应,有些离子只是旁观者,该反应中参与反应的离子是。17. 根据下列实验装置图,回答有关问题.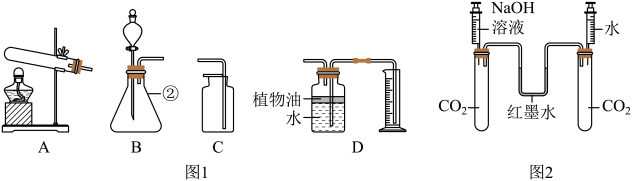 (1)、写出仪器①的名称 .(2)、用相同装置分别制取氧气和二氧化碳,应选用图1中的(填字母)作发生装置,其中制取氧气的化学方程式为 , 用D装置收集二氧化碳的优点是(任写一点).(3)、按图2进行实验,将注射器中相同体积的NaOH溶液和水同时注入试管中,观察到现象,说明二氧化碳和氢氧化钠发生了反应.18. 甲、乙分别是稀盐酸和NaOH溶液中的某一种,如图表示向甲中加入乙时,溶液pH的变化曲线。回答问题:
(1)、写出仪器①的名称 .(2)、用相同装置分别制取氧气和二氧化碳,应选用图1中的(填字母)作发生装置,其中制取氧气的化学方程式为 , 用D装置收集二氧化碳的优点是(任写一点).(3)、按图2进行实验,将注射器中相同体积的NaOH溶液和水同时注入试管中,观察到现象,说明二氧化碳和氢氧化钠发生了反应.18. 甲、乙分别是稀盐酸和NaOH溶液中的某一种,如图表示向甲中加入乙时,溶液pH的变化曲线。回答问题: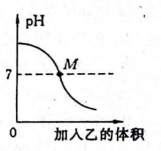 (1)、甲是。(2)、用pH试纸测甲溶液的pH时,测试结果比实际值偏低,可能的原因是。
(1)、甲是。(2)、用pH试纸测甲溶液的pH时,测试结果比实际值偏低,可能的原因是。三、实验探究题
-
19. 学习酸碱中和反应时,同学们发现稀盐酸与氢氧化钠溶液混合在一起无明显现象。学习小组的同学们对其产生探究兴趣,于是他们分别从不同的角度探究酸碱中和反应。
 (1)、【探究一】通过能量变化的角度,证明酸碱发生中和反应。
(1)、【探究一】通过能量变化的角度,证明酸碱发生中和反应。毛毛同学将固体氢氧化钠放入装有稀硫酸的试管中并振荡,试管壁发烫,于是他得出酸碱中和反应是放热反应的结论。牛牛同学认为毛毛同学推理不合理,理由是。
(2)、牛牛同学为了验证毛毛同学的结论,将实验加以改进:将稀硫酸慢慢滴入装有氢氧化钠溶液的烧杯中,用温度计测出氢氧化钠溶液温度随加入稀硫酸质量的变化如图①所示:①由图知,稀硫酸与氢氧化钠溶液发生的反应是(填“放热”或“吸热”)反应。
②从A到B过程中,烧杯中溶液pH逐渐 , 到达C时溶液中溶质有。
(3)、 【探究二】通过溶液酸碱性变化的角度,证明酸碱发生中和反应。娇娇同学利用图②实验进行反应,证明碱与酸发生反应的现象是。
(4)、明明同学观察到实验过程中有气泡产生,他认为氢氧化钠溶液已经变质,请你分析变质的原因(用化学方程式表示)。(5)、【探究三】通过证明有新物质生成的角度,证明酸碱发生中和反应。为验证中和反应有水生成,萌萌同学在老师的指导下,查阅了相关资料,进行如图所示的三个实验。
已知:①变色硅胶吸水后由蓝色变为红色。
②无水醋酸与氢氧化钠反应生成醋酸钠和水。
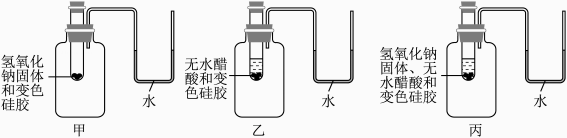
证明无水醋酸与氢氧化钠反应有水生成的现象是。
(6)、实验过程中,观察到丙的U形管内液面。(7)、 【探究四】从微观角度认识酸碱中和反应的本质。下图是氢氧化钠溶液与稀盐酸反应的微观示意图,请你补充完整。
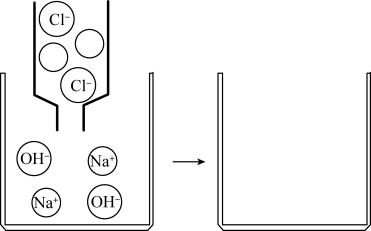
四、计算题
-
20. 氢氧化钠是一种重要的工业原料,同时也是实验室中常用的一种化学药品。(1)、制取少量氢氧化钠可以用如图所示的流程:

①上述步骤②的基本反应类型是 反应(填“化合”、“分解”、“置换”或“复分解”之一)。
②写出步骤③发生反应的化学方程式 。
③氢氧化钠有很强的腐蚀性,如果不小心沾到皮肤上,要立即用大量的水冲洗 ,然后涂上 (填选项序号之一)。
A.稀硫酸
B.3%﹣5%的碳酸氢钠溶液
C.硼酸溶液
D.石灰水
(2)、在一烧杯中盛有20gNa2CO3和NaCl组成的固体混合物,加100g水完全溶解,制成不饱和溶液。向其中逐渐滴加溶质质量分数为10%的稀盐酸 ,放出气体的总质量与所滴入稀盐酸的质量关系曲线如图所示:请根据题意回答问题: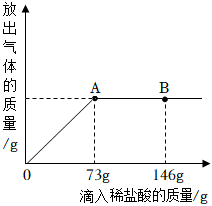
①当滴加稀盐酸至图中B点时,烧杯中溶液里的溶质有 。
②当滴加了73g稀盐酸时(即A点时),烧杯中为不饱和溶液,试通过计算求所得氯化钠溶液的质量。
-