浙江省嘉兴市平湖市六校联考2023-2024学年九年级上学期科学11月期中试卷
试卷更新日期:2024-01-29 类型:期中考试
一、选择题(本大题共15小题,每题2分,共30分,每小题只有一个选项是正确的,不选、多选、错选均不给分)
-
1. 下列变化中,属于化学变化的是( )A、铁丝弯折 B、钢铁熔化 C、钢铁生锈 D、铁球下落2. 在测定土壤酸碱性的实验中,下列操作规范的是( )A、装入土样粉末
 B、滴加蒸馏水
B、滴加蒸馏水 C、上下振荡浸出液
C、上下振荡浸出液 D、测定酸碱性
D、测定酸碱性 3. 紫甘蓝是大众爱吃的蔬菜,含有丰富的花青素,花青素遇酸性溶液变红色,遇碱性溶液变蓝色,在凉拌紫甘蓝丝时,观察到菜丝变成红色,可能是加入了下列哪种调味品( )A、食盐 B、味精 C、食醋 D、香油4. 小明家的芹菜茎秆细弱,他应施加的化肥是( )A、KOH B、Ca3(PO4)2 C、K2CO3 D、CO(NH2)25. 创造了10909m深潜新纪录的“奋斗者号”载人潜水器的外壳是由钛合金制造。钛合金属于( )A、金属材料 B、无机非金属材料 C、合成材料 D、有机物6. 为比较Fe、Cu、Ag之间的活动性强弱,某同学在实验室分别准备用如下几组物质进行实验,你认为不可行的是( )A、Fe、Ag、CuSO4溶液 B、Cu、Ag、FeSO4溶液 C、Fe、Cu、稀盐酸、AgNO3溶液 D、Cu、FeSO4溶液、AgNO3溶液7. 酸碱反应的应用十分广泛。下列实例不属于酸碱之间的反应的是( )A、金属表面锈蚀后,可用稀盐酸进行清洗 B、胃酸分泌过多的病人遵医嘱服用含有氢氧化铝的药物以缓解胃酸 C、蚊虫叮咬人的皮肤分泌出蚁酸,如果涂含碱的药水就可减轻痛痒 D、土壤酸化后加入熟石灰改良8. 现有锌、氧化铜、硫酸钡和石灰石四种固体,为了区分它们,小阳参照二歧分类检索表制作了一个物质检索表,如表所示。下列叙述错误的是( )
3. 紫甘蓝是大众爱吃的蔬菜,含有丰富的花青素,花青素遇酸性溶液变红色,遇碱性溶液变蓝色,在凉拌紫甘蓝丝时,观察到菜丝变成红色,可能是加入了下列哪种调味品( )A、食盐 B、味精 C、食醋 D、香油4. 小明家的芹菜茎秆细弱,他应施加的化肥是( )A、KOH B、Ca3(PO4)2 C、K2CO3 D、CO(NH2)25. 创造了10909m深潜新纪录的“奋斗者号”载人潜水器的外壳是由钛合金制造。钛合金属于( )A、金属材料 B、无机非金属材料 C、合成材料 D、有机物6. 为比较Fe、Cu、Ag之间的活动性强弱,某同学在实验室分别准备用如下几组物质进行实验,你认为不可行的是( )A、Fe、Ag、CuSO4溶液 B、Cu、Ag、FeSO4溶液 C、Fe、Cu、稀盐酸、AgNO3溶液 D、Cu、FeSO4溶液、AgNO3溶液7. 酸碱反应的应用十分广泛。下列实例不属于酸碱之间的反应的是( )A、金属表面锈蚀后,可用稀盐酸进行清洗 B、胃酸分泌过多的病人遵医嘱服用含有氢氧化铝的药物以缓解胃酸 C、蚊虫叮咬人的皮肤分泌出蚁酸,如果涂含碱的药水就可减轻痛痒 D、土壤酸化后加入熟石灰改良8. 现有锌、氧化铜、硫酸钡和石灰石四种固体,为了区分它们,小阳参照二歧分类检索表制作了一个物质检索表,如表所示。下列叙述错误的是( ) A、甲表示的是石灰石 B、乙表示的是锌 C、表中“ ”应该表示为“黑色固体” D、也可根据是否含有氧元素对丙、丁分类9. 铕(Eu)是非常活泼的金属,能与冷水反应,应保存在氢气中。铕与水反应的化学方程式为:Eu+2H2O=Eu(OH)2+H2↑。该反应属于( )A、化合反应 B、分解反应 C、置换反应 D、复分解反应10. 下列物质的分类正确的是( )A、活泼金属:镁、铝、铜 B、单质:氧气、臭氧、液氧 C、氧化物:水、氧化铁、熟石灰 D、混合物:纯碱、石油、钢11. 智能百叶窗的叶片上贴有太阳能板,在光照时发电,给电动机供电以调节百叶窗的开合。该过程中发生的能量转换是( )A、电能→机械能→光能 B、光能→机械能→电能 C、光能→电能→机械能 D、机械能→电能→光能12. 下列有关如图所示四幅图的观点中(不计摩擦),分析错误的是( )
A、甲表示的是石灰石 B、乙表示的是锌 C、表中“ ”应该表示为“黑色固体” D、也可根据是否含有氧元素对丙、丁分类9. 铕(Eu)是非常活泼的金属,能与冷水反应,应保存在氢气中。铕与水反应的化学方程式为:Eu+2H2O=Eu(OH)2+H2↑。该反应属于( )A、化合反应 B、分解反应 C、置换反应 D、复分解反应10. 下列物质的分类正确的是( )A、活泼金属:镁、铝、铜 B、单质:氧气、臭氧、液氧 C、氧化物:水、氧化铁、熟石灰 D、混合物:纯碱、石油、钢11. 智能百叶窗的叶片上贴有太阳能板,在光照时发电,给电动机供电以调节百叶窗的开合。该过程中发生的能量转换是( )A、电能→机械能→光能 B、光能→机械能→电能 C、光能→电能→机械能 D、机械能→电能→光能12. 下列有关如图所示四幅图的观点中(不计摩擦),分析错误的是( ) A、图甲中,起跳离开地面后,人只受到重力的作用 B、图乙中,在下降过程中,滚摆的动能逐渐减小 C、图丙中,卫星在近地点的速度最大 D、图丁中,小球运动到③位置时速度不为零13. 推理是一重要的思想方法,下列推理合理的是( )A、H2在空气中点燃要验纯,所以在空气中点燃可燃性气体前都要验纯 B、CO2与NaOH反应生成盐和水,所以能与碱反应生成盐和水的一定是氧化物 C、单质均由同种元素组成,所以由同种元素组成的物质都是单质 D、碱的溶液使无色酚酞变红,所以能使无色酚酞变红的一定是碱的溶液14. 除去下列物质中的少量杂质,所选试剂或操作方法不合理的是( )
A、图甲中,起跳离开地面后,人只受到重力的作用 B、图乙中,在下降过程中,滚摆的动能逐渐减小 C、图丙中,卫星在近地点的速度最大 D、图丁中,小球运动到③位置时速度不为零13. 推理是一重要的思想方法,下列推理合理的是( )A、H2在空气中点燃要验纯,所以在空气中点燃可燃性气体前都要验纯 B、CO2与NaOH反应生成盐和水,所以能与碱反应生成盐和水的一定是氧化物 C、单质均由同种元素组成,所以由同种元素组成的物质都是单质 D、碱的溶液使无色酚酞变红,所以能使无色酚酞变红的一定是碱的溶液14. 除去下列物质中的少量杂质,所选试剂或操作方法不合理的是( )选项
物质
杂质
除杂试剂或操作方法
A
N2
O2
通过灼热的铜网
B
KCl固体
MnO2
溶解、过滤、蒸发结晶
C
NaOH溶液
Na2CO3
滴加适量的BaCl2溶液后过滤
D
Cu
Fe
用磁铁吸引
A、A B、B C、C D、D15. 几千年前,人类就用木炭作为还原剂进行金属冶炼 。木炭在高温条件下还原氧化铜所生成的“气体产物”可能是:①一氧化碳,②二氧化碳,③一氧化碳和二氧化碳的混合物。某学习小组为此用如图装置对木炭在高温条件下还原氧化铜所生成的“气体产物”进行探究。关于该实验的说法正确的( )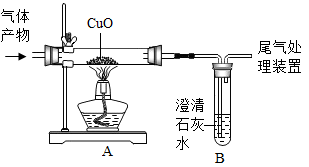 A、观察到试管中的黑色物质变红色,则“气体产物”一定是①一氧化碳 B、观察到澄清石灰水变浑浊,则“气体产物”中一定有②二氧化碳 C、要证明是否存在二氧化碳,不需要在原装置前再连接一个装澄清石灰水的洗气瓶 D、该实验不能确定“气体产物”是一氧化碳,或二氧化碳,或二者的混合物
A、观察到试管中的黑色物质变红色,则“气体产物”一定是①一氧化碳 B、观察到澄清石灰水变浑浊,则“气体产物”中一定有②二氧化碳 C、要证明是否存在二氧化碳,不需要在原装置前再连接一个装澄清石灰水的洗气瓶 D、该实验不能确定“气体产物”是一氧化碳,或二氧化碳,或二者的混合物二、填空题(本大题共有9小题,每空格1分,共20分)
-
16. 2019年11月1日,浙江省开始在全省范围稳步推进垃圾分类管理,将生活垃圾分为图所示的四类。
 (1)、以下四种物品中属于垃圾分类中可回收物的是____;A、破碗瓷片 B、过期药物 C、废旧报 D、枯枝落叶(2)、废电池属于“有害垃圾”,主要是因为废电池里含有大量的汞、镉、锰、铅等重金属(选填“元素”或“单质”)。(3)、沼气发电时,能量转化形式是转化为电能。17. 每逢中秋佳节,赏月吃月饼是中国人的传统。科学兴趣小组对某月饼包装盒中的“脱氧剂”又称“双吸剂”很好奇,他们观察到“脱氧剂”外包装标注的主要成分是铁粉。打开发现这包“脱氧剂”发现已变成了红棕色,而铁粉是黑色的,说明这包“脱氧剂”已变质。(1)、黑色的铁粉变成了红棕色是因为铁与共同作用生成了氧化铁的缘故;(2)、要检验这包“脱氧剂”是否完全变质失效,下列所选试剂或方法正确的____。A、氢氧化钠溶液 B、稀盐酸 C、用磁铁吸引18. 归纳总结是学习科学的重要方法,小明同学用图甲总结了NaOH的四条化学性质(即NaOH与四类物质能够发生化学变化)。
(1)、以下四种物品中属于垃圾分类中可回收物的是____;A、破碗瓷片 B、过期药物 C、废旧报 D、枯枝落叶(2)、废电池属于“有害垃圾”,主要是因为废电池里含有大量的汞、镉、锰、铅等重金属(选填“元素”或“单质”)。(3)、沼气发电时,能量转化形式是转化为电能。17. 每逢中秋佳节,赏月吃月饼是中国人的传统。科学兴趣小组对某月饼包装盒中的“脱氧剂”又称“双吸剂”很好奇,他们观察到“脱氧剂”外包装标注的主要成分是铁粉。打开发现这包“脱氧剂”发现已变成了红棕色,而铁粉是黑色的,说明这包“脱氧剂”已变质。(1)、黑色的铁粉变成了红棕色是因为铁与共同作用生成了氧化铁的缘故;(2)、要检验这包“脱氧剂”是否完全变质失效,下列所选试剂或方法正确的____。A、氢氧化钠溶液 B、稀盐酸 C、用磁铁吸引18. 归纳总结是学习科学的重要方法,小明同学用图甲总结了NaOH的四条化学性质(即NaOH与四类物质能够发生化学变化)。 (1)、为了验证反应①,小明将无色酚酞试液滴入NaOH溶液中,溶液变成色。(2)、依据反应②说明NaOH必须密封保存,否则在空气中会变质,其化学方程式为。(3)、为了验证反应④能够发生,你选择的物质是____(填序号)。A、Na2CO3 B、HCl C、CuSO4 D、NaCl19. 建立宏观、微观和符号之间的联系是学习化学的重要方法.请按要求填空。(1)、碳酸钠是一种重要的化工原料,其化学式为;(2)、恩施被誉为世界硒都,具有丰富的硒资源.硒(Se)是人生命中必需的微量元素在周期表中与硫同族、化学性质相似.A、B、C、D表示4种物质,它们的微观示意图如图:
(1)、为了验证反应①,小明将无色酚酞试液滴入NaOH溶液中,溶液变成色。(2)、依据反应②说明NaOH必须密封保存,否则在空气中会变质,其化学方程式为。(3)、为了验证反应④能够发生,你选择的物质是____(填序号)。A、Na2CO3 B、HCl C、CuSO4 D、NaCl19. 建立宏观、微观和符号之间的联系是学习化学的重要方法.请按要求填空。(1)、碳酸钠是一种重要的化工原料,其化学式为;(2)、恩施被誉为世界硒都,具有丰富的硒资源.硒(Se)是人生命中必需的微量元素在周期表中与硫同族、化学性质相似.A、B、C、D表示4种物质,它们的微观示意图如图:
物质A((H2Se)和B在点燃条件下反应生成C和D两种物质,反应的化学方程式是
20. 小莉是一个爱探究的孩子,到实验室做了一个实验:她先将少量鸡蛋壳装入气球,再把气球套在盛有稀盐酸的锥形瓶瓶口,然后把气球中的鸡蛋壳加入锥形瓶中(装置的气密性良好,鸡蛋壳主要成分与大理石主要成分相同),实验过程现象如图。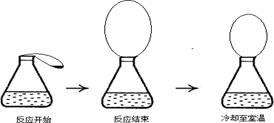 (1)、请写出鸡蛋壳中的主要成分与稀盐酸反应的化学方程式:;(2)、从实验过程可以看出,反应结束时气球膨胀程度最大,冷却到室温时气球体积又变小一些,说明鸡蛋壳中的主要成分与稀盐酸反应时还会(填实验现象)。21. 木板OAB各处的粗糙程度均相同,其中OA部分是斜面,AB部分水平放置,小球从O点由静止释放后加速滚下,先经过A点,最后停在B点处(不计空气阻力),小球在O、A、B三个点的位置上:
(1)、请写出鸡蛋壳中的主要成分与稀盐酸反应的化学方程式:;(2)、从实验过程可以看出,反应结束时气球膨胀程度最大,冷却到室温时气球体积又变小一些,说明鸡蛋壳中的主要成分与稀盐酸反应时还会(填实验现象)。21. 木板OAB各处的粗糙程度均相同,其中OA部分是斜面,AB部分水平放置,小球从O点由静止释放后加速滚下,先经过A点,最后停在B点处(不计空气阻力),小球在O、A、B三个点的位置上: (1)、动能最大的位置是点;(2)、机械能最大的位置点。22. 有一包白色粉末,可能是由硫酸铜、氯化钠、碳酸钠中的一种或几种组成。为检验其中的成分,按以下流程进行实验:
(1)、动能最大的位置是点;(2)、机械能最大的位置点。22. 有一包白色粉末,可能是由硫酸铜、氯化钠、碳酸钠中的一种或几种组成。为检验其中的成分,按以下流程进行实验: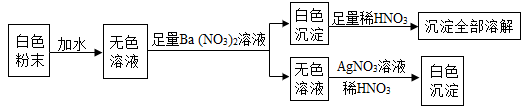 (1)、根据实验现象,白色粉末中一定有。(2)、实验中不能用BaCl2 溶液代替 Ba(NO3)2 溶液的理由是。23. 有一种纳米材料添加剂,由铝粉、氧化铝粉末、铜粉中的一种或几种组成,为探究该添加剂的成分,科学学习小组进行了下列实验,请回答实验中的相关问题:(1)、取适量添加剂于试管中,加入足量稀盐酸,产生大量气泡并有红色固体残留,该现象说明添加剂中一定含有;(2)、另取适量添加剂于另一试管中,加入一定量的硝酸银溶液,充分反应,过滤,得到滤渣和蓝色溶液。则蓝色溶液中一定含有的溶质是。24. 对知识的及时整理与归纳是学习科学的重要方法。某同学在学习了硫酸的化学性质后,初步归纳出稀硫酸与其它物质相互反应的关系,如图所示(“一”表示相连的两种物质能发生反应,五个圈中的物质属于不同的类别)。
(1)、根据实验现象,白色粉末中一定有。(2)、实验中不能用BaCl2 溶液代替 Ba(NO3)2 溶液的理由是。23. 有一种纳米材料添加剂,由铝粉、氧化铝粉末、铜粉中的一种或几种组成,为探究该添加剂的成分,科学学习小组进行了下列实验,请回答实验中的相关问题:(1)、取适量添加剂于试管中,加入足量稀盐酸,产生大量气泡并有红色固体残留,该现象说明添加剂中一定含有;(2)、另取适量添加剂于另一试管中,加入一定量的硝酸银溶液,充分反应,过滤,得到滤渣和蓝色溶液。则蓝色溶液中一定含有的溶质是。24. 对知识的及时整理与归纳是学习科学的重要方法。某同学在学习了硫酸的化学性质后,初步归纳出稀硫酸与其它物质相互反应的关系,如图所示(“一”表示相连的两种物质能发生反应,五个圈中的物质属于不同的类别)。 (1)、已知X是金属单质,则X可以是。(填一种即可)(2)、请写出稀硫酸与Y反应的一个化学方程式。
(1)、已知X是金属单质,则X可以是。(填一种即可)(2)、请写出稀硫酸与Y反应的一个化学方程式。三、实验探究题(本题有3小题,共10空格,每空格2分,共20分)
-
25. 我国不少地方有端午吃“灰水粽”的习俗,所谓“灰水粽”是指用草木灰的浸出液(“灰水”)俗称浸泡糯米做成的粽子,这种粽子清香软糯,小乐对制作“灰水粽”的草木灰展开了如下探究:

【查阅资料】①糯米中加入食用碱可起到中和微生物生成的酸、软化食物纤维等作用。②草木灰中富含钾盐,主要成分是K2CO3 , 还含有少量K2SO4和KCl。
【实验探究】检验草木灰的成分,并测定草木灰中K2CO3的质量分数。
(1)、取适量草木灰于烧杯中,加足量水浸泡,过滤得到草木灰的浸出液;取少量浸出液于试管中,滴加几滴酚酞试液,观察到酚酞试液变成红色,则说明草木灰的浸出液 , 可起到食用碱的作用。(2)、为了检验草木灰的浸出液中存在Cl- , 小乐先往浸出液中加入足量的Ba(NO3)2溶液后过滤,这样操作的目的是。(3)、小海用图示装置(图中夹持仪器已略去)测定草木灰中K2CO3 , 的质量分数,实验中通过测定装置质量的增加量来计算K2CO3的质量(草木灰中其他成分不与稀盐酸产生气体),实验过程中需持续缓缓通入空气,如果不往装置中持续缓慢通入空气,会导致测量结果偏小,其原因是。26. 小明取一包某食品包装袋内的“脱氧剂”,查阅资料发现其成分除铁粉外,可能含有碳粉、Na2CO3、NaCl、Fe2O3等。为确定其成分,进行了如下实验: (1)、过滤操作中除了需带铁圈的铁架台、滤纸、玻璃棒外,还需要用到的仪器有。(2)、写出用 pH试纸测定滤液pH的方法。(3)、试剂X的名称是。(4)、由实验可知,该包“脱氧剂”一定含有的物质是。27. 某同学在观看台球比赛时发现:有时运动的白球去撞击一个静止的球后,白球会立即静止在碰撞时的位置,而被撞的球似乎接替了白球,沿白球原来的运动方向,以几乎相同的速度向前运动。该同学想:白球碰撞后立即静止,被撞的球是以白球撞前相同大小的速度运动出去的吗?通过了解和初步实验,他发现只有当体积和质量均相同的两球,而且球心在同一直线上相碰时,才可能出现上述现象。为进一步探究,他设计了下述实验方案,将一个两端翘起、中间水平的轨道固定在水平桌面上,取两个相同的台球A、B,将B球静置于轨道的水平部分,A球置于轨道左端斜面上某处,测出该点到水平桌面的高度h1 , 如图所示,释放A球,撞击后,A球静止,B球向前运动并冲上轨道右端斜面能到达的最高点,测出该点的高度h2。通过比较h2与h1的大小关系即可作出判断。
(1)、过滤操作中除了需带铁圈的铁架台、滤纸、玻璃棒外,还需要用到的仪器有。(2)、写出用 pH试纸测定滤液pH的方法。(3)、试剂X的名称是。(4)、由实验可知,该包“脱氧剂”一定含有的物质是。27. 某同学在观看台球比赛时发现:有时运动的白球去撞击一个静止的球后,白球会立即静止在碰撞时的位置,而被撞的球似乎接替了白球,沿白球原来的运动方向,以几乎相同的速度向前运动。该同学想:白球碰撞后立即静止,被撞的球是以白球撞前相同大小的速度运动出去的吗?通过了解和初步实验,他发现只有当体积和质量均相同的两球,而且球心在同一直线上相碰时,才可能出现上述现象。为进一步探究,他设计了下述实验方案,将一个两端翘起、中间水平的轨道固定在水平桌面上,取两个相同的台球A、B,将B球静置于轨道的水平部分,A球置于轨道左端斜面上某处,测出该点到水平桌面的高度h1 , 如图所示,释放A球,撞击后,A球静止,B球向前运动并冲上轨道右端斜面能到达的最高点,测出该点的高度h2。通过比较h2与h1的大小关系即可作出判断。 (1)、B球由静止变为运动是因为B球在碰撞中获得了能。(2)、vA表示碰撞前瞬间A球运动速度,vB表示B球被撞后开始运动的速度。若h2=h1 , 则vBvA(选填“>”、“=”或“<”)。(3)、实际实验中,测出的h2总小干h1 , 若导致这一现象的原因轨道不光滑,那么在阻力不可避免的情况下,你认为该同学的设计是否还有价值?说出你的理由。
(1)、B球由静止变为运动是因为B球在碰撞中获得了能。(2)、vA表示碰撞前瞬间A球运动速度,vB表示B球被撞后开始运动的速度。若h2=h1 , 则vBvA(选填“>”、“=”或“<”)。(3)、实际实验中,测出的h2总小干h1 , 若导致这一现象的原因轨道不光滑,那么在阻力不可避免的情况下,你认为该同学的设计是否还有价值?说出你的理由。四、分析与计算(本题有4小题,28题4分,29题10分,30、31题各8分;共30分)
-
28. 氢气被视为未来理想的能源,科学家对氢的研究从未停歇。氢能源的广泛使用需解决制氢、储氢等问题。
 (1)、图1、图2分别为全球制氢原料占比和主流制氢方法的经济性对比图。
(1)、图1、图2分别为全球制氢原料占比和主流制氢方法的经济性对比图。①由图象可知:目前氢气的主要来源是(填“天然气和煤”、“醇类”或“水”)。
②电解水制氢需要消耗大量电能,下列获取电能的方式中,一定存在碳排放的是。
A.水力发电 B.太阳能发电 C.燃煤发电
(2)、氢气的储存有以下两种方式。①方法一:将氢气直接加压储存在由某种镁铝合金制造的储氢罐中备用。从物质分类的角度来看,镁铝合金属于(填“纯净物”或“混合物”);
②方法二:先通过Mg2Cu与氢气反应,将氢气转化为MgH2暂时“储存”起来,此为储氢反应(如图3):需要使用氢气时,可通过释氢反应实现:MgH2+2HCl=MgCl2+2H2↑。请写出储氢反应的化学方程式。
29. 人类的生产生活离不开金属。(1)、下列铜制品的用途中,利用金属导电性的是。 (2)、某兴趣小组为了测定铜钱(铜锌合金)中铜的质量分数,取多枚铜钱放入烧杯中,另取80克稀硫酸,分四次等质量加入,每次均充分反应,实验数据记录如下表。
(2)、某兴趣小组为了测定铜钱(铜锌合金)中铜的质量分数,取多枚铜钱放入烧杯中,另取80克稀硫酸,分四次等质量加入,每次均充分反应,实验数据记录如下表。实验次数
1
2
3
4
稀硫酸的用量/克
20
20
20
20
剩余固体的质量/克
20.0
17.4
14.8
13.8
分析上述数据,请回答下列问题:
①第4次实验结束后溶液的pH ▲ 7(填“>”、“=”或“<”)。
②计算铜钱中铜的质量分数(计算结果精确到0.1%)。
③计算参加反应的稀硫酸中的溶质质量(计算结果保留一位小数)。
30.某校化学兴趣小组用一瓶含有少量氯化钠的硫酸钠固体样品,进行如图所示的实验.

请根据以上信息计算(结果保留到小数点后两位):
(1)、反应生成沉淀的质量为 .(2)、样品中氯化钠的质量.(3)、滤液中溶质的质量分数.31. 钢铁工业是一个国家的支柱产业之一,某同学采集了一些生铁样品(含杂质,杂质不溶于水,不与稀硫酸反应)采用如下左图所示装置进行分析。分别称得锥形瓶与棉花的质量为44.1g,生铁样品的质量为9.0g。在锥形瓶中加入足量稀硫酸后,立即开始记录电子天平的示数,记录数据如下右图。
请认真分析数据,回答下列问题:
(1)、小军数据处理的图象中正确的是 (2)、计算样品中铁的质量分数;(3)、计算反应后所得溶液中硫酸亚铁的质量分数。
(2)、计算样品中铁的质量分数;(3)、计算反应后所得溶液中硫酸亚铁的质量分数。